文档内容
九年级化学试卷
可能用到的相对原子质量:H-1 C-12 O-16 Fe-56
一、选择题(共20分)
1. 属于稀有气体的是
A. H B. He C. HO D. HO
2 2 2 2
2. 属于复合肥的是
A. KNO B. NH Cl C. Ca(NO ) D. Ca(HPO )
3 4 3 2 2 4 2
3. 一些物质的pH范围如下,其中呈碱性的是
A. 柠檬汁(2~3) B. 酱油(4~5) C. 护发素(5~6) D. 洗发水(8~9)
4. 下列物质的用途中,利用其化学性质的是
A. 银用作镜子 B. 干冰用作制冷剂
C. 一氧化碳用作冶炼金属 D. 金刚石用于切割玻璃
5. 与氧气互为同素异形体的是
A. 过氧化氢 B. 液氧 C. 空气 D. 臭氧
的
6. 下列物质在空气中大量燃烧后,会造成酸雨 是
A. 硫粉 B. 碳块 C. 镁带 D. 铁丝
7. 在水的净化过程中,可用于杀菌消毒的物质是
A. 活性炭 B. 明矾 C. 氯气 D. 氯化氢
8. 水结冰的过程中体积变大,关于该过程中的说法正确的是
A. 水分子由运动变为静止 B. 水分子间距变大
C. 水分子的质量变小 D. 水分子的体积变大
9. 化学变化中一定会发生变化的
A. 分子的种类 B. 分子的个数
C. 原子的种类 D. 原子的个数
的
10. 下列物质 分类正确的是
A. HCO 属于一元酸 B. Cu(OH) 属于难溶性碱
2 3 2
C. NaHCO 属于正盐 D. NaCl属于含氧酸盐
3
的
11. 对于实验现象描述正确 是
A. 打开浓盐酸的瓶塞,瓶口上方出现白烟
B. 将二氧化碳通入紫色石蕊试液后,溶液由紫色变为蓝色C. 木炭还原氧化铜实验中,红色固体变黑
D. 无水硫酸铜上滴几滴水,白色固体变为蓝色
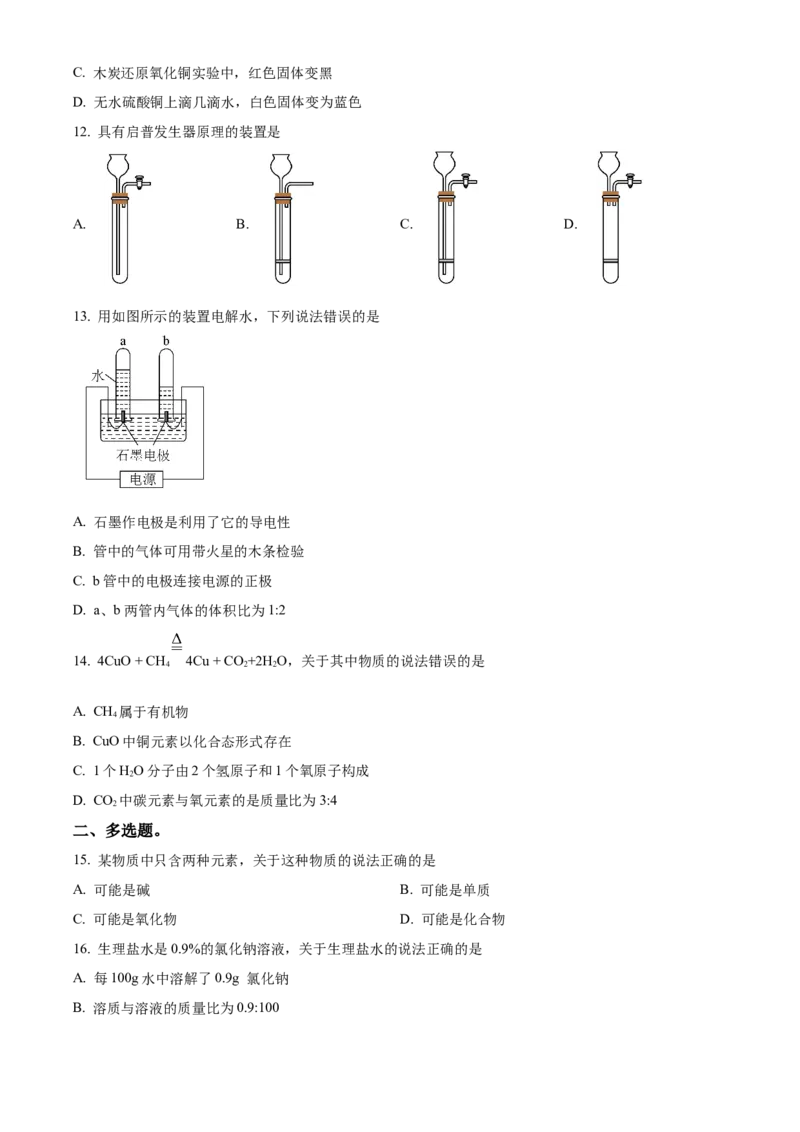
12. 具有启普发生器原理的装置是
A. B. C. D.
13. 用如图所示的装置电解水,下列说法错误的是
A. 石墨作电极是利用了它的导电性
B. 管中的气体可用带火星的木条检验
C. b管中的电极连接电源的正极
D. a、b两管内气体的体积比为1:2
14. 4CuO + CH 4Cu + CO +2H O,关于其中物质的说法错误的是
4 2 2
A. CH 属于有机物
4
B. CuO中铜元素以化合态形式存在
C. 1个HO分子由2个氢原子和1个氧原子构成
2
D. CO 中碳元素与氧元素的是质量比为3:4
2
二、多选题。
15. 某物质中只含两种元素,关于这种物质的说法正确的是
A. 可能是碱 B. 可能是单质
C. 可能是氧化物 D. 可能是化合物
16. 生理盐水是0.9%的氯化钠溶液,关于生理盐水的说法正确的是
A. 每100g水中溶解了0.9g 氯化钠
B. 溶质与溶液的质量比为0.9:100C. 氯化钠的溶解度为0.9g/100g水
D. 加入0.1g氯化钠完全溶解后得到1%的氯化钠溶液
17. 用如图装置验证质量守恒定律。反应前称得质量为m,引燃白磷,冷却后称得质量为m。下列说法正
1 2
确的是
A. 实验中白磷一定要过量
B. 实验过程中气球膨胀不会影响实验结果
C. 若装置气密性良好,则 m=m
1 2
D. 反应生成PO 的质量一定等于装置中白磷和氧气的质量和
2 5
三、简答题(共30分)
18. 中药芒硝的主要成分是NaSO ·10H O,具有清火消肿之功效。
2 4 2
(1)芒硝属于______(选填“混合物”或“纯净物”)。
(2)NaSO ·10H O中硫元素的化合价为______。1 mol Na SO ·10H O中含水分子_____个。
2 4 2 2 4 2
(3)向NaSO 溶液中滴加BaCl 溶液,发生反应的化学方程式为_______,观察到的现象是______。
2 4 2
(4)鉴别NaSO 溶液和KSO 溶液时,用铂丝蘸取样品溶液,在火焰上灼烧,通过蓝色钴玻璃片观察到
2 4 2 4
_______,则该样品是KSO 溶液。
2 4
的
19. 铁、锌和铝是生活中常用 金属,这些金属在空气中与氧气、二氧化碳和水等物质作用,都会生
锈,但锈蚀的程度不同。
(1)铁因在空气中生成疏松的铁锈而会严重锈蚀,铁锈的主要成分是______(填化学式)。
(2)锌的金属活动性比铁______(选填“活泼”或“不活泼”),理应更容易锈蚀,但由于在锌的表面
会生成一层致密的碱式碳酸锌,而不易进一步锈蚀。生成碱式碳酸锌的反应原理为
2Zn+O +CO +H O=Zn (OH) CO,该反应属于_______。(填基本反应类型)
2 2 2 2 2 3
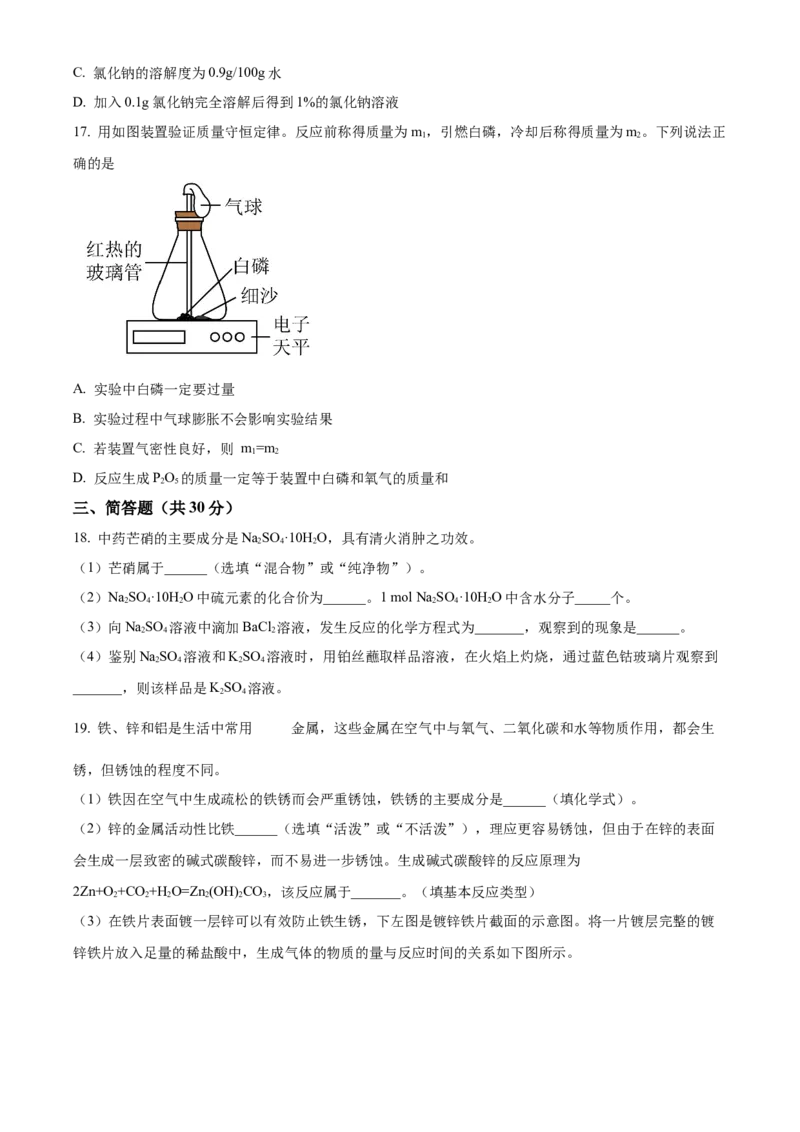
(3)在铁片表面镀一层锌可以有效防止铁生锈,下左图是镀锌铁片截面的示意图。将一片镀层完整的镀
锌铁片放入足量的稀盐酸中,生成气体的物质的量与反应时间的关系如下图所示。①oa段是碱式碳酸锌与盐酸反应,化学方程为Zn(OH) CO+4HCl=2X+3HO+CO↑,其中X的化学式为
2 2 3 2 2
_______。若要检验该反应生成的气体可以用______。(填试剂的名称)
②写出bc段发生反应的化学方程式__________。
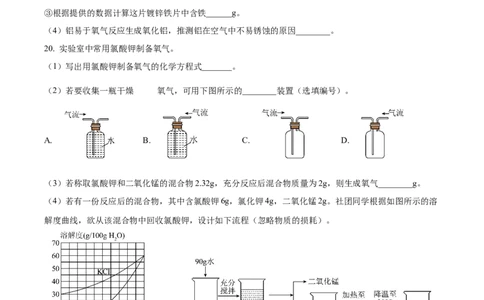
③根据提供的数据计算这片镀锌铁片中含铁______g。
(4)铝易于氧气反应生成氧化铝,推测铝在空气中不易锈蚀的原因________。
20. 实验室中常用氯酸钾制备氧气。
(1)写出用氯酸钾制备氧气的化学方程式_______。
的
(2)若要收集一瓶干燥 氧气,可用下图所示的________装置(选填编号)。
A. B. C. D.
(3)若称取氯酸钾和二氧化锰的混合物2.32g,充分反应后混合物质量为2g,则生成氧气________g。
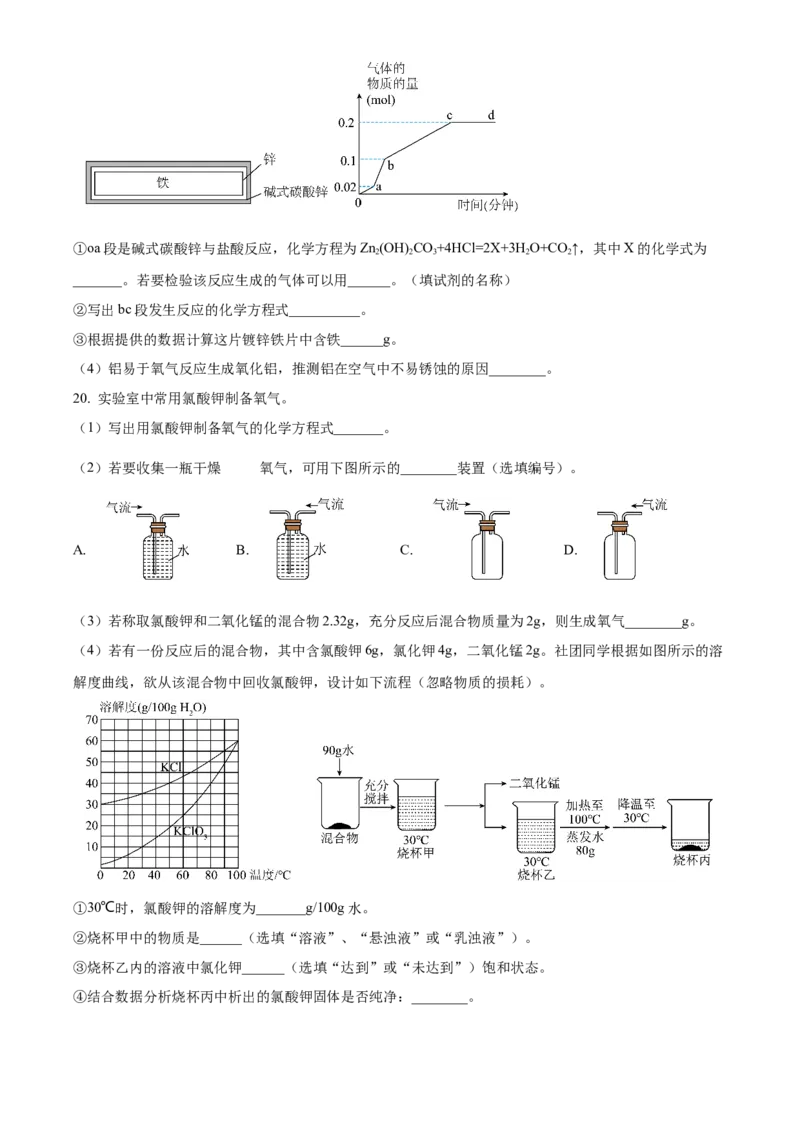
(4)若有一份反应后的混合物,其中含氯酸钾6g,氯化钾4g,二氧化锰2g。社团同学根据如图所示的溶
解度曲线,欲从该混合物中回收氯酸钾,设计如下流程(忽略物质的损耗)。
①30℃时,氯酸钾的溶解度为_______g/100g水。
②烧杯甲中的物质是______(选填“溶液”、“悬浊液”或“乳浊液”)。
③烧杯乙内的溶液中氯化钾______(选填“达到”或“未达到”)饱和状态。
④结合数据分析烧杯丙中析出的氯酸钾固体是否纯净:________。21. 我国拥有丰富的煤炭资源。利用煤炭与水制备氢气的反应原理为反应1:C+H O CO+H;反应
2 2
2:CO+HO CO+H ,将上述反应原理设计为生产流程如下图所示:
2 2 2
(1)相比直接燃烧煤炭,用氢气做燃料的优点是__________。(只需写出一条)
(2)步骤ii中发生反应的化学方程式为__________。
(3)设计实验证明溶液1中含有NaOH。
操作 现象 结论
①取少量溶液1于试管中,加入过量的_____,充分振荡后静置。 产生白色沉淀
溶液1中
含有
②吸取上述试管中的上层清液,置于另一支试管,加入酚酞试液,振荡。 ____ NaOH
(4)工业上每吨生石灰的价格约为260元,每吨氢氧化钠的价格约为2000元左右。步骤iii中的操作是
____。设计步骤iii的目的是_____。
(5)若步骤i中加入水蒸气的量不足,除了会造成氢气产量减少,还会造成什么后果? ______只需写出一
条)