文档内容
2022 学年度第二学期初三练习卷
化学学科
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Mg-24 Ca-40
一、选择题(本大题共25小题,共30分。1~20题均只有一个正确选项,21~25题每题均有
1~2个正确选项)
1. 属于金属元素的是
A. Fe B. H C. Cl D. P
2. 属于化学变化的是
A. 海水晒盐 B. 冰块融化 C. 干冰升华 D. 钢铁生锈
3. 空气中含量最多的气体是
A. 氮气
B. 氧气
.
C 氦气
D. 二氧化碳
4. 三氧化二铋(BiO)可作防火纸,其中铋元素的化合价是
2 3
A. +2 B. +3 C. +4 D. +5
5. 物质中含有原子团的是
A. HNO B. CaCl C. MgO D. HO
3 2 2 2
6. 物质的化学式与名称对应正确的是
A. 氯化氨:NH Cl B. 硝酸钙:Ca(NO )
4 3 2
C. 氢氧化铁:Fe(OH) D. 碳酸钠:NaCO
2 3
7. 关于氢氧化钠的说法错误的是
A. 化学式:NaOH B. 颜色:白色
C. 类别:碱 D. 用途:中和土壤酸性
8. 化学用语的表述正确的是
A. 汞元素:hg B. 2个氧原子:O
2
C. 二氧化氮:No D. +2价的钙元素:
2
9. 属于溶液的是
A. 汽水 B. 豆浆 C. 米粥 D. 牛奶
第1页/共11页
学科网(北京)股份有限公司10. 根据化学方程式S+O SO ,无法获得的信息是
2 2
A. 反应前后反应物和生成物的种类 B. 反应物与生成物的质量比
C. 化学反应速率的快慢程度 D. 反应发生所需要的条件
11. 下列不能与稀盐酸反应的物质是
A. Cu B. NaOH C. AgNO D. MgO
3
12. 自来水生产中,能起到杀菌消毒作用的过程是
A. 加入明矾 B. 沉降过滤
C. 通入氯气 D. 加压供水
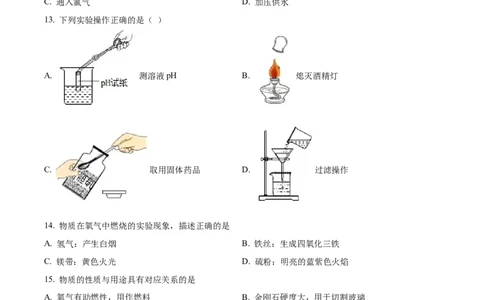
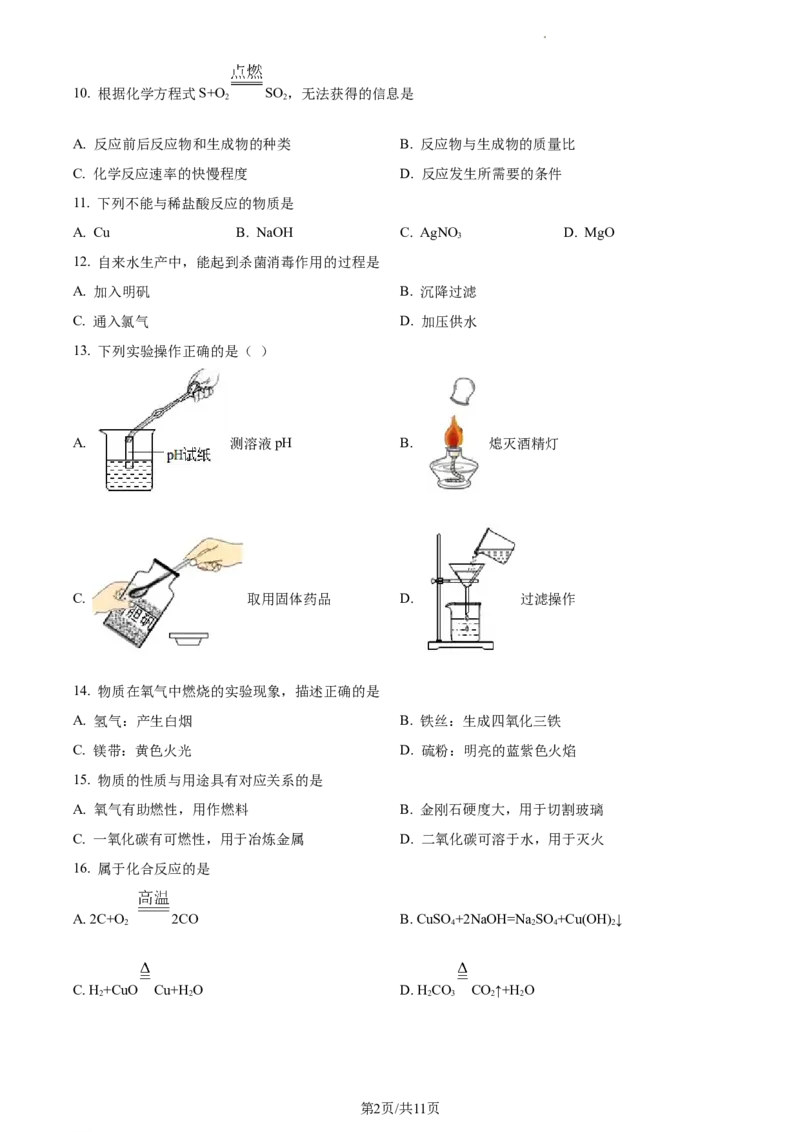
13. 下列实验操作正确的是( )
A. 测溶液pH B. 熄灭酒精灯
C. 取用固体药品 D. 过滤操作
14. 物质在氧气中燃烧的实验现象,描述正确的是
A. 氢气:产生白烟 B. 铁丝:生成四氧化三铁
C. 镁带:黄色火光 D. 硫粉:明亮的蓝紫色火焰
15. 物质的性质与用途具有对应关系的是
A. 氧气有助燃性,用作燃料 B. 金刚石硬度大,用于切割玻璃
C. 一氧化碳有可燃性,用于冶炼金属 D. 二氧化碳可溶于水,用于灭火
16. 属于化合反应的是
A. 2C+O 2CO B. CuSO +2NaOH=Na SO +Cu(OH) ↓
2 4 2 4 2
C. H+CuO Cu+H O D. H CO CO↑+H O
2 2 2 3 2 2
第2页/共11页
学科网(北京)股份有限公司17. 燃烧前常将汽油(含C H 等)喷成雾状,可以
8 18
A. 减少O 消耗量 B. 增大汽油与空气的接触面
2
C. 减少CO 生成量 D. 使C H 等分子变得更小
2 8 18
18. 除去下列物质中所含的少量杂质,所用方法正确的是
选项 物质(括号内为杂质) 除杂方法
A CO(CO) 点燃气体
2
B KNO(NaCl) 溶解,蒸发结晶,过滤
3
C CaCl 溶液(HCl) 加入碳酸钙固体(足量),过滤
2
D Fe(Fe O) 加入稀盐酸(足量),过滤
2 3
A. A B. B C. C D. D
19. 用对比实验探究碱的性质,下列说法错误的是
A. 软塑料瓶变瘪的程度为A>B>C
B. 只有对比B、C瓶变瘪的程度才可证明CO 能与氢氧化钙反应
2
C. 饱和氢氧化钠溶液能吸收二氧化碳的量比饱和石灰水一定多
D. 可溶性碱能与酸性氧化物反应
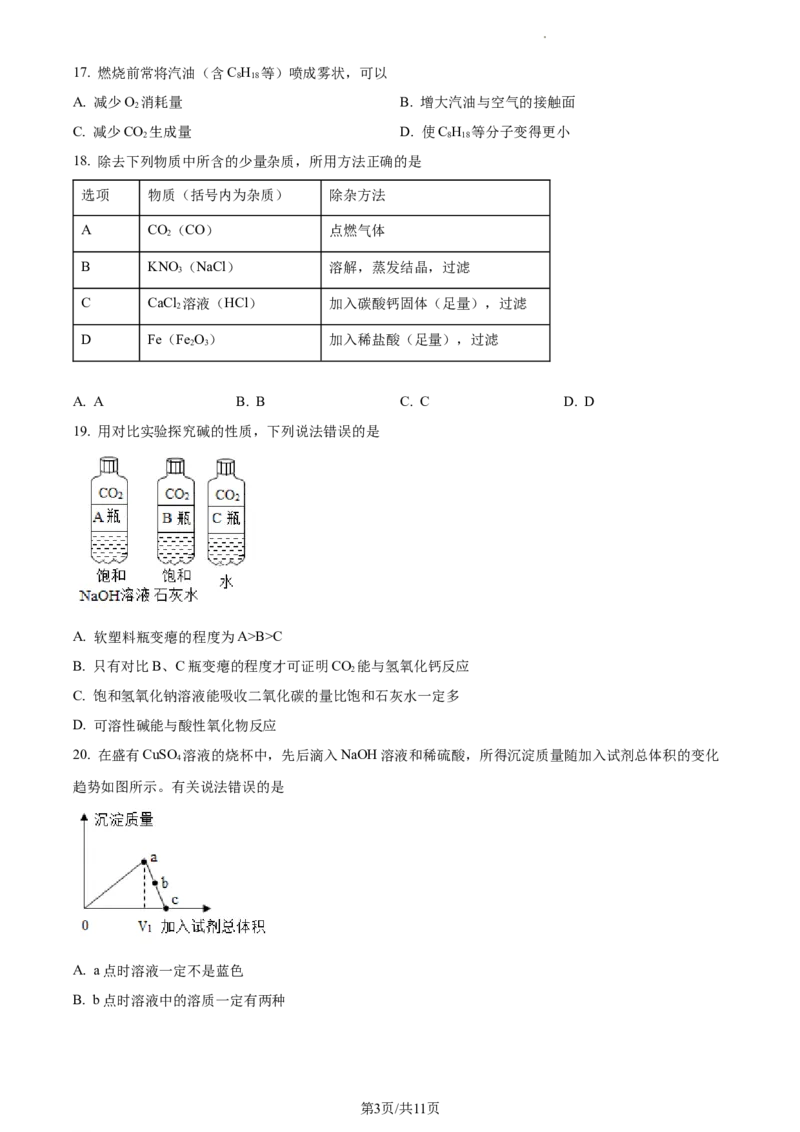
20. 在盛有CuSO 溶液的烧杯中,先后滴入NaOH溶液和稀硫酸,所得沉淀质量随加入试剂总体积的变化
4
趋势如图所示。有关说法错误的是
A. a点时溶液一定不是蓝色
B. b点时溶液中的溶质一定有两种
第3页/共11页
学科网(北京)股份有限公司C. c点时溶液中CuSO 的量与最初烧杯中CuSO 的量一样多
4 4
D. 加入试剂总体积为V 时,溶液中一定不存在NaOH
1
21. 有关溶液的说法,正确的是
A. 溶质一定是固体 B. 降温一定使溶液浓度减小
C. 溶液一定是混合物 D. 稀溶液一定是不饱和溶液
22. 关于“单质”的理解正确的是
A. 一定是纯净物 B. 同种元素组成的物质一定是单质
C. 不可能存在于混合物中 D. 只含一种元素,且以游离态存在
的
23. 关于分子、原子 叙述错误的是
A. 分子可以分成原子 B. 分子的质量比原子的质量大
C. 分子是化学变化中的最小微粒 D. 分子和原子都可以构成物质
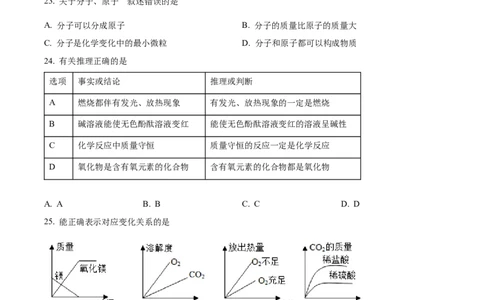
24. 有关推理正确的是
选项 事实或结论 推理或判断
A 燃烧都伴有发光、放热现象 有发光、放热现象的一定是燃烧
B 碱溶液能使无色酚酞溶液变红 能使无色酚酞溶液变红的溶液呈碱性
C 化学反应中质量守恒 质量守恒的反应一定是化学反应
D 氧化物是含有氧元素的化合物 含有氧元素的化合物都是氧化物
A. A B. B C. C D. D
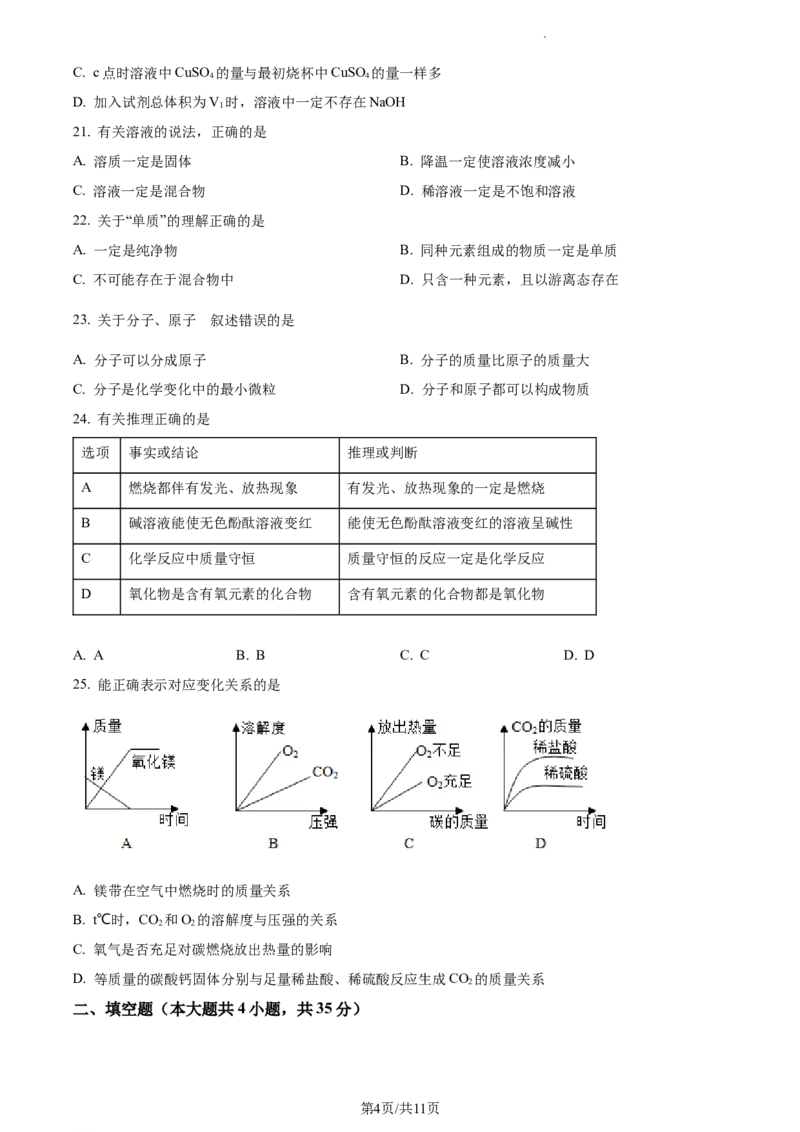
25. 能正确表示对应变化关系的是
A. 镁带在空气中燃烧时的质量关系
B. t℃时,CO 和O 的溶解度与压强的关系
2 2
C. 氧气是否充足对碳燃烧放出热量的影响
D. 等质量的碳酸钙固体分别与足量稀盐酸、稀硫酸反应生成CO 的质量关系
2
二、填空题(本大题共4小题,共35分)
第4页/共11页
学科网(北京)股份有限公司26. 神舟十四号载人飞船的安全返回,标志着我国的航天科技水平已处于世界领先地位。
(1)发射时,选用偏二甲肼(C HN)和四氧化二氮(NO)组成双元动力推进剂。
2 8 2 2 4
Ⅰ.偏二甲肼(C HN)由_______种元素组成,碳、氢、氮元素质量比_______。
2 8 2
Ⅱ.偏二甲肼在一定条件下与四氧化二氮反应的化学方程式:C HN+ 2N O 4X + 2CO + 3N ,其
2 8 2 2 4 2 2
中X的化学式是_______。
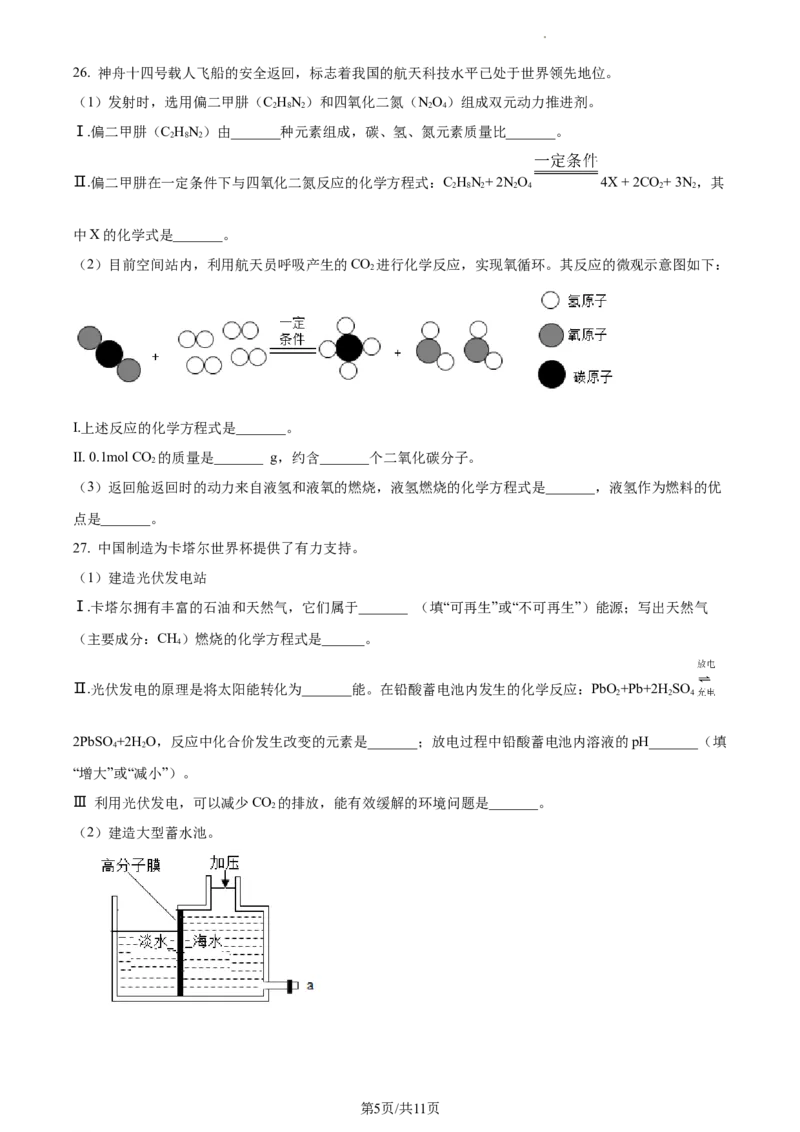
(2)目前空间站内,利用航天员呼吸产生的CO 进行化学反应,实现氧循环。其反应的微观示意图如下:
2
I.上述反应的化学方程式是_______。
II. 0.1mol CO 的质量是_______ g,约含_______个二氧化碳分子。
2
(3)返回舱返回时的动力来自液氢和液氧的燃烧,液氢燃烧的化学方程式是_______,液氢作为燃料的优
点是_______。
27. 中国制造为卡塔尔世界杯提供了有力支持。
(1)建造光伏发电站 。
Ⅰ.卡塔尔拥有丰富的石油和天然气,它们属于_______ (填“可再生”或“不可再生”)能源;写出天然气
(主要成分:CH)燃烧的化学方程式是______。
4
Ⅱ.光伏发电的原理是将太阳能转化为_______能。在铅酸蓄电池内发生的化学反应:PbO +Pb+2H SO
2 2 4
2PbSO +2H O,反应中化合价发生改变的元素是_______;放电过程中铅酸蓄电池内溶液的pH_______(填
4 2
“增大”或“减小”)。
Ⅲ 利用光伏发电,可以减少CO 的排放,能有效缓解的环境问题是_______。
2
(2)建造大型蓄水池。
第5页/共11页
学科网(北京)股份有限公司I.卡塔尔的生活用水主要来自于海水淡化,海水属于_______(填“纯净物”或“混合物”)。
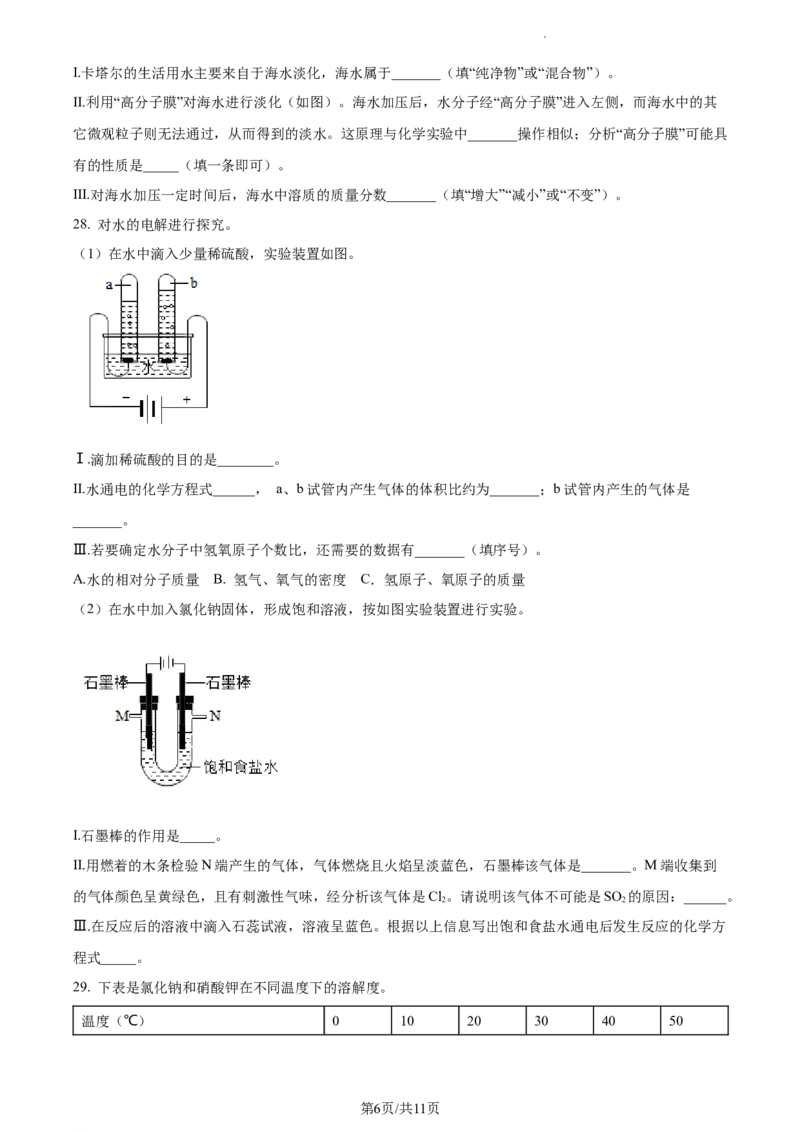
II.利用“高分子膜”对海水进行淡化(如图)。海水加压后,水分子经“高分子膜”进入左侧,而海水中的其
它微观粒子则无法通过,从而得到的淡水。这原理与化学实验中_______操作相似;分析“高分子膜”可能具
有的性质是_____(填一条即可)。
III.对海水加压一定时间后,海水中溶质的质量分数_______(填“增大”“减小”或“不变”)。
28. 对水的电解进行探究。
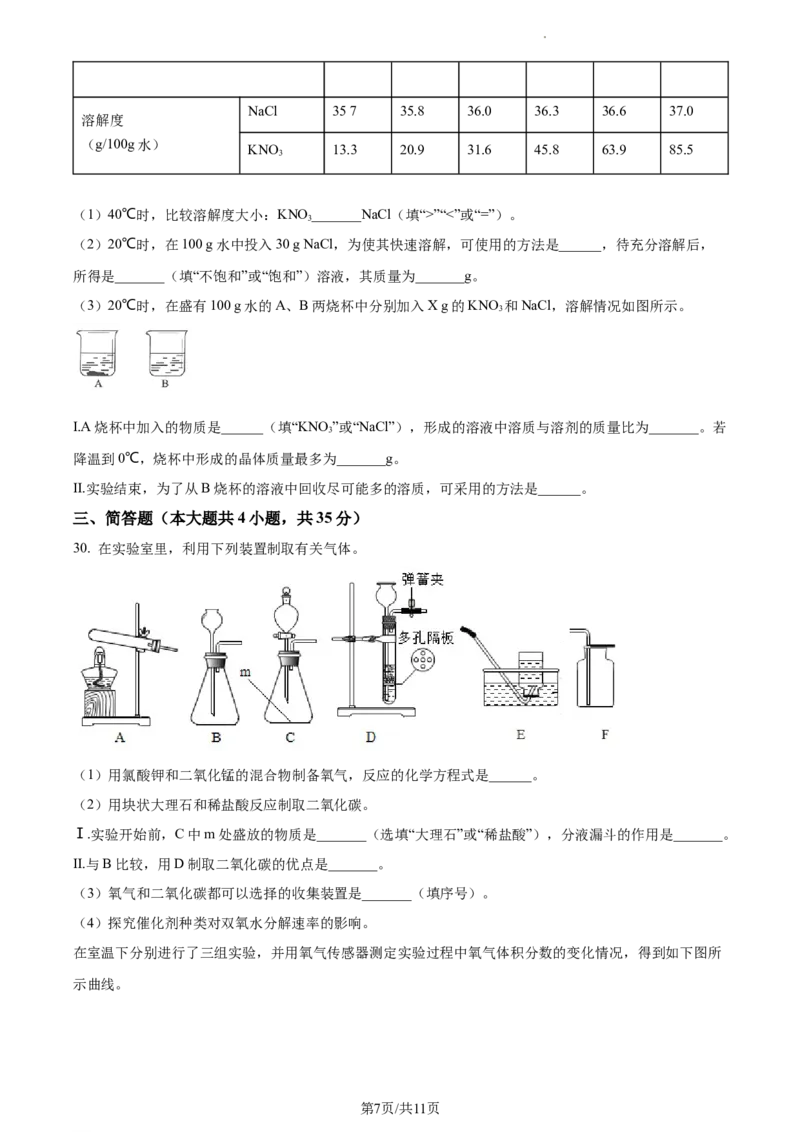
(1)在水中滴入少量稀硫酸,实验装置如图。
Ⅰ.滴加稀硫酸的目的是________。
II.水通电的化学方程式______, a、b试管内产生气体的体积比约为_______;b试管内产生的气体是
_______。
Ⅲ.若要确定水分子中氢氧原子个数比,还需要的数据有_______(填序号)。
A.水的相对分子质量 B. 氢气、氧气的密度 C.氢原子、氧原子的质量
(2)在水中加入氯化钠固体,形成饱和溶液,按如图实验装置进行实验。
I.石墨棒的作用是_____。
II.用燃着的木条检验N端产生的气体,气体燃烧且火焰呈淡蓝色,石墨棒该气体是_______。M端收集到
的气体颜色呈黄绿色,且有刺激性气味,经分析该气体是Cl。请说明该气体不可能是SO 的原因:______。
2 2
Ⅲ.在反应后的溶液中滴入石蕊试液,溶液呈蓝色。根据以上信息写出饱和食盐水通电后发生反应的化学方
程式_____。
29. 下表是氯化钠和硝酸钾在不同温度下的溶解度。
温度(℃) 0 10 20 30 40 50
第6页/共11页
学科网(北京)股份有限公司.
NaCl 357 35.8 36.0 36.3 36.6 37.0
溶解度
(g/100g水)
KNO 13.3 20.9 31.6 45.8 63.9 85.5
3
(1)40℃时,比较溶解度大小:KNO_______NaCl(填“>”“<”或“=”)。
3
(2)20℃时,在100 g水中投入30 g NaCl,为使其快速溶解,可使用的方法是______,待充分溶解后,
所得是_______(填“不饱和”或“饱和”)溶液,其质量为_______g。
(3)20℃时,在盛有100 g水的A、B两烧杯中分别加入X g的KNO 和NaCl,溶解情况如图所示。
3
I.A烧杯中加入的物质是______(填“KNO”或“NaCl”),形成的溶液中溶质与溶剂的质量比为_______。若
3
降温到0℃,烧杯中形成的晶体质量最多为_______g。
II.实验结束,为了从B烧杯的溶液中回收尽可能多的溶质,可采用的方法是______。
三、简答题(本大题共4小题,共35分)
30. 在实验室里,利用下列装置制取有关气体。
(1)用氯酸钾和二氧化锰的混合物制备氧气,反应的化学方程式是______。
(2)用块状大理石和稀盐酸反应制取二氧化碳。
Ⅰ.实验开始前,C中m处盛放的物质是_______(选填“大理石”或“稀盐酸”),分液漏斗的作用是_______。
II.与B比较,用D制取二氧化碳的优点是_______。
(3)氧气和二氧化碳都可以选择的收集装置是_______(填序号)。
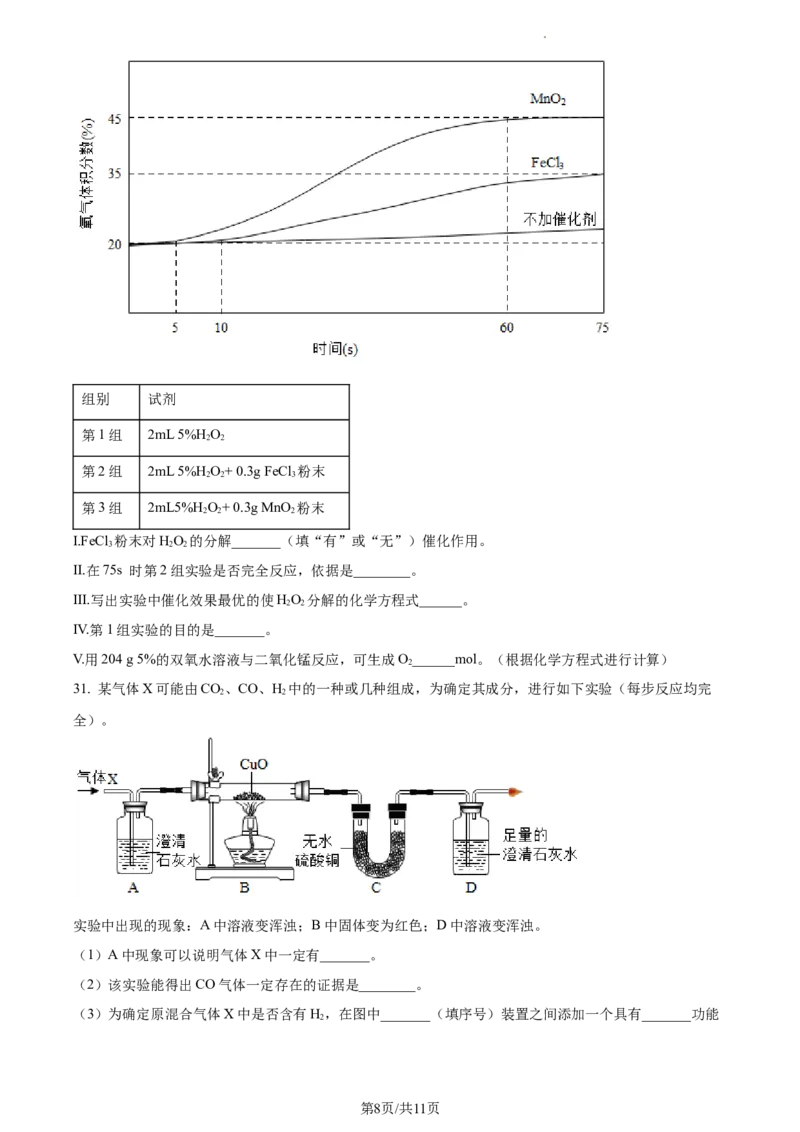
(4)探究催化剂种类对双氧水分解速率的影响。
在室温下分别进行了三组实验,并用氧气传感器测定实验过程中氧气体积分数的变化情况,得到如下图所
示曲线。
第7页/共11页
学科网(北京)股份有限公司组别 试剂
第1组 2mL 5%HO
2 2
第2组 2mL 5%HO+ 0.3g FeCl 粉末
2 2 3
第3组 2mL5%H O+ 0.3g MnO 粉末
2 2 2
I.FeCl 粉末对HO 的分解_______(填“有”或“无”)催化作用。
3 2 2
II.在75s 时第2组实验是否完全反应,依据是________。
III.写出实验中催化效果最优的使HO 分解的化学方程式______。
2 2
IV.第1组实验的目的是_______。
V.用204 g 5%的双氧水溶液与二氧化锰反应,可生成O______mol。(根据化学方程式进行计算)
2
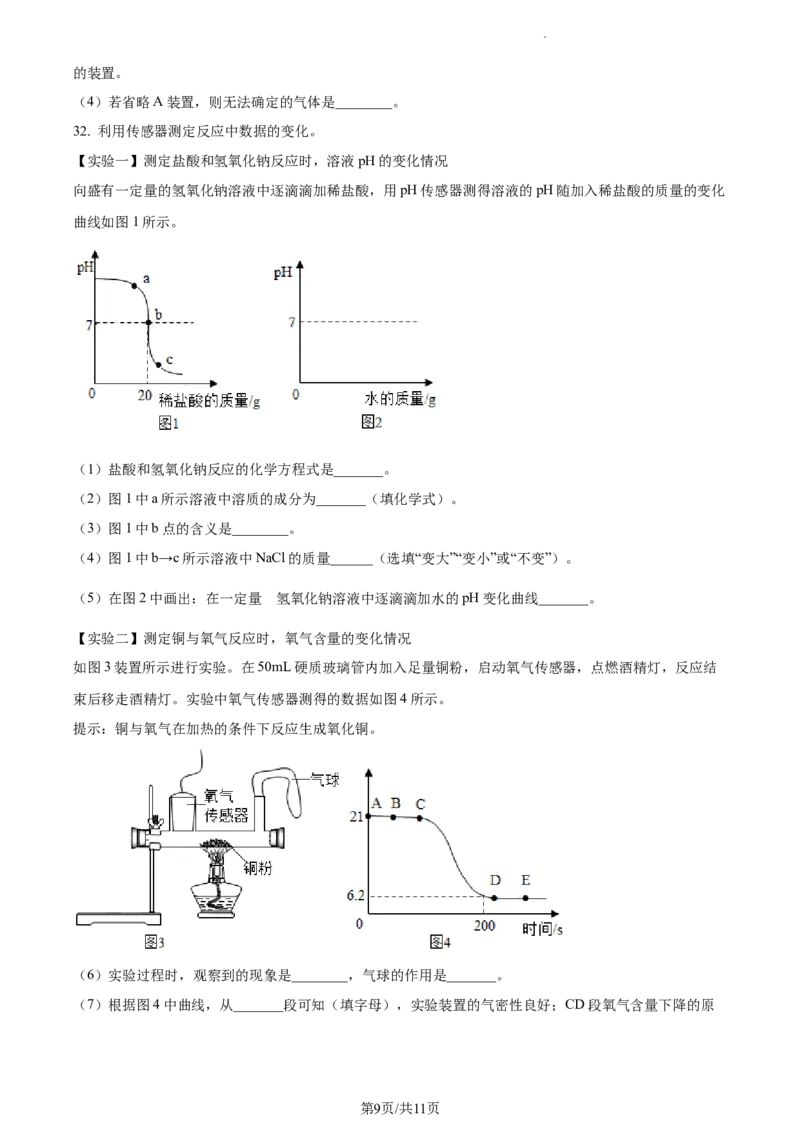
31. 某气体X可能由CO、CO、H 中的一种或几种组成,为确定其成分,进行如下实验(每步反应均完
2 2
全)。
实验中出现的现象:A中溶液变浑浊;B中固体变为红色;D中溶液变浑浊。
(1)A中现象可以说明气体X中一定有_______。
(2)该实验能得出CO气体一定存在的证据是________。
(3)为确定原混合气体X中是否含有H,在图中_______(填序号)装置之间添加一个具有_______功能
2
第8页/共11页
学科网(北京)股份有限公司的装置。
(4)若省略A装置,则无法确定的气体是________。
32. 利用传感器测定反应中数据的变化。
【实验一】测定盐酸和氢氧化钠反应时,溶液pH的变化情况
向盛有一定量的氢氧化钠溶液中逐滴滴加稀盐酸,用pH传感器测得溶液的pH随加入稀盐酸的质量的变化
曲线如图1所示。
(1)盐酸和氢氧化钠反应的化学方程式是_______。
(2)图1中a所示溶液中溶质的成分为_______(填化学式)。
(3)图1中b点的含义是________。
(4)图1中b→c所示溶液中NaCl的质量______(选填“变大”“变小”或“不变”)。
的
(5)在图2中画出:在一定量 氢氧化钠溶液中逐滴滴加水的pH变化曲线_______。
【实验二】测定铜与氧气反应时,氧气含量的变化情况
如图3装置所示进行实验。在50mL硬质玻璃管内加入足量铜粉,启动氧气传感器,点燃酒精灯,反应结
束后移走酒精灯。实验中氧气传感器测得的数据如图4所示。
提示:铜与氧气在加热的条件下反应生成氧化铜。
(6)实验过程时,观察到的现象是________,气球的作用是_______。
(7)根据图4中曲线,从_______段可知(填字母),实验装置的气密性良好;CD段氧气含量下降的原
第9页/共11页
学科网(北京)股份有限公司因是______。
(8)DE段装置内气压_______(填“变大”、“变小”或“不变”)。
(9)实验结束后,为回收固体中的铜粉,进行的实验操作是________。
33. 探究石灰石高温煅烧后的固体成分。
(1)将石灰石高温煅烧一段时间,反应的化学方程式是_______。
(2)对煅烧后的固体成分进行如下实验:
实验操作 现象 结论
步骤一:取煅烧后的固体于试管中, 加水振 试管壁发烫,且在试管底部有
荡 白色不溶物
步骤二:取上层清液于另一试管中,滴入酚 上层清液中一定含有氢
________
酞试液 氧化钙
步骤三:取部分底部白色不溶物于第三支试 白色不溶物中一定含有
有气泡产生
管中,滴加_______ _______
(3)结论:煅烧后固体的成分是________。
(4)反思:若不进行步骤二是否也可以获得相同的实验结论,请说明原因:________。
第10页/共11页
学科网(北京)股份有限公司第11页/共11页
学科网(北京)股份有限公司