文档内容
化学部分
可能用到的相对原子质量:H-1 C-12 O-16 C1-35.5 Fe-56
一、选择题(共20分)
1-14每题均只有一个正确选项
1. 铝元素的符号是
.
A Cl B. AL C. Al D. Ag
2. 《天工开物》中记载的下列过程主要涉及化学变化的是
A. 棉纱织布 B. 海水晒盐 C. 伐木制舟 D. 五谷酿酒
3. 空气中体积分数约为21%的是
A. N B. O C. CO D. 水蒸气
2 2 2
4. 属于氧化物的是
A. HSO B. MgO C. Mg(OH) D. Mg(NO)
2 4 2 3 2
5. 古代皇帝“朱笔御批”的原料主要成分是HgS,其中Hg的化合价为+2,则S的化合价是
A. -1 B. -2 C. +1 D. +2
6. 属于钾肥的是
A. KCl B. CO(NH) C. NH Cl D. Ca (PO )
2 2 4 3 4 2
7. 在足量水中能形成溶液的是
A. 植物油 B. 碳酸钙 C. 硝酸钠 D. 氢氧化铜
8. 焰色反应呈黄色的是
A. NaCl B. Cu(NO ) C. KNO D. CaCl
3 2 3 2
的
9. 以下是室温下不同溶液 pH,其中碱性最强的是
A. pH=3 B. pH=7 C. pH=10 D. pH=13
的
10. 互为同素异形体 是
A. 氧气和液氧 B. 水和双氧水
C. 冰和干冰 D. 红磷和白磷
11. 物质的俗名与化学式对应的是
A. 胆矾CuSO B. 烧碱NaOH
4
C. 干冰HO D. 食盐HCl
2
12. 掌握一定的化学知识可有效保障安全,下列做法正确的是
A. 电器着火用水扑灭 B. 霉变的食物洗净后食用C. 油锅起火用锅盖盖灭 D. 高层发生火灾乘电梯逃生
13. 对实验现象描述正确的是
A. 碳还原氧化铜时,观察到固体由红色变黑色
B. 氢氧化钠溶液中滴加稀盐酸,溶液由红色变为无色
C. 打开盛有浓盐酸的试剂瓶的瓶盖,瓶口上方出现白烟
D. 硫在空气中燃烧,火焰呈淡蓝色,产生具有刺激性气味的气体
14. 关于分子和原子的说法,正确的是
A. 分子可分,原子不可再分 B. 分子的质量比原子的质量大
C. 相同原子可以构成不同分子 D. 化学反应前后,分子和原子的种类保持不变
15-17每题有1-2个正确选项
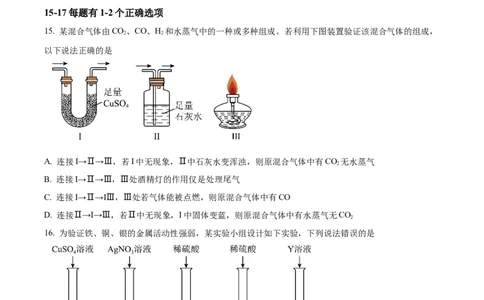
15. 某混合气体由CO、CO、H 和水蒸气中的一种或多种组成。若利用下图装置验证该混合气体的组成,
2 2
以下说法正确的是
A. 连接I→Ⅱ→Ⅲ,若I中无现象,Ⅱ中石灰水变浑浊,则原混合气体中有CO 无水蒸气
2
B. 连接I→Ⅱ→Ⅲ,Ⅲ处酒精灯的作用仅是处理尾气
C. 连接I→Ⅱ→IⅢ,Ⅲ处若气体能被点燃,则原混合气体中有CO
D. 连接Ⅱ→I→Ⅲ,若Ⅱ中无现象,I中固体变蓝,则原混合气体中有水蒸气无CO
2
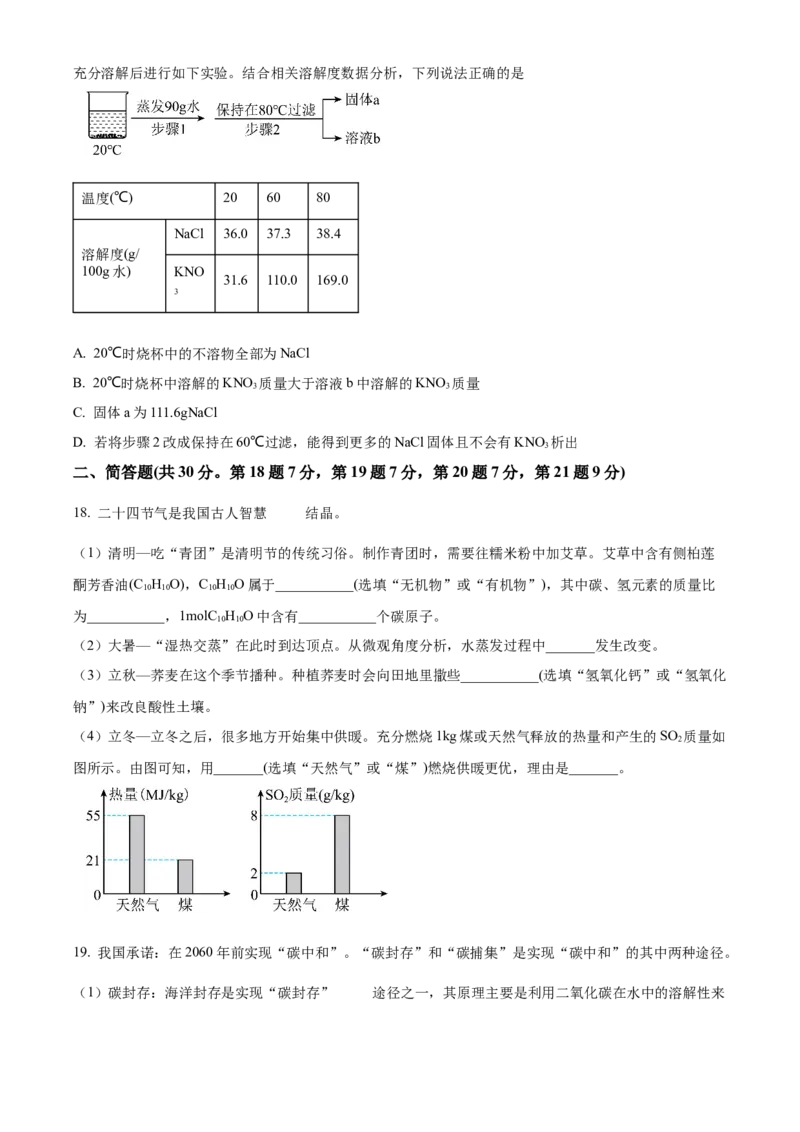
16. 为验证铁、铜、银的金属活动性强弱,某实验小组设计如下实验,下列说法错误的是
A. 通过实验①②,能验证金属活动性:Fe>Cu>Ag
B. 通过实验①④,能验证三种金属中Fe的活动性最强
C. 通过实验②③,能验证三种金属中Ag的活动性最弱
D. 若试管⑤中X为Cu,Y溶液为稀硫酸,通过实验②③⑤能验证金属活动:Fe>Cu>Ag
17. 现有一份由150gNaCl和10gKNO 组成的混合物。为提纯氯化钠,实验小组将该混合物放入100g水中,
3充分溶解后进行如下实验。结合相关溶解度数据分析,下列说法正确的是
温度(℃) 20 60 80
NaCl 36.0 37.3 38.4
溶解度(g/
100g水) KNO
31.6 110.0 169.0
3
A. 20℃时烧杯中的不溶物全部为NaCl
B. 20℃时烧杯中溶解的KNO 质量大于溶液b中溶解的KNO 质量
3 3
C. 固体a为111.6gNaCl
D. 若将步骤2改成保持在60℃过滤,能得到更多的NaCl固体且不会有KNO 析出
3
二、简答题(共30分。第18题7分,第19题7分,第20题7分,第21题9分)
的
18. 二十四节气是我国古人智慧 结晶。
(1)清明—吃“青团”是清明节的传统习俗。制作青团时,需要往糯米粉中加艾草。艾草中含有侧柏莲
酮芳香油(C H O),C H O属于___________(选填“无机物”或“有机物”),其中碳、氢元素的质量比
10 10 10 10
为___________,1molC H O中含有___________个碳原子。
10 10
(2)大暑—“湿热交蒸”在此时到达顶点。从微观角度分析,水蒸发过程中_______发生改变。
(3)立秋—荞麦在这个季节播种。种植荞麦时会向田地里撒些___________(选填“氢氧化钙”或“氢氧化
钠”)来改良酸性土壤。
(4)立冬—立冬之后,很多地方开始集中供暖。充分燃烧1kg煤或天然气释放的热量和产生的SO 质量如
2
图所示。由图可知,用_______(选填“天然气”或“煤”)燃烧供暖更优,理由是_______。
19. 我国承诺:在2060年前实现“碳中和”。“碳封存”和“碳捕集”是实现“碳中和”的其中两种途径。
的
(1)碳封存:海洋封存是实现“碳封存” 途径之一,其原理主要是利用二氧化碳在水中的溶解性来吸收CO。海洋封存会导致海水酸化,其原因为___________(用化学方程式表示)。
2
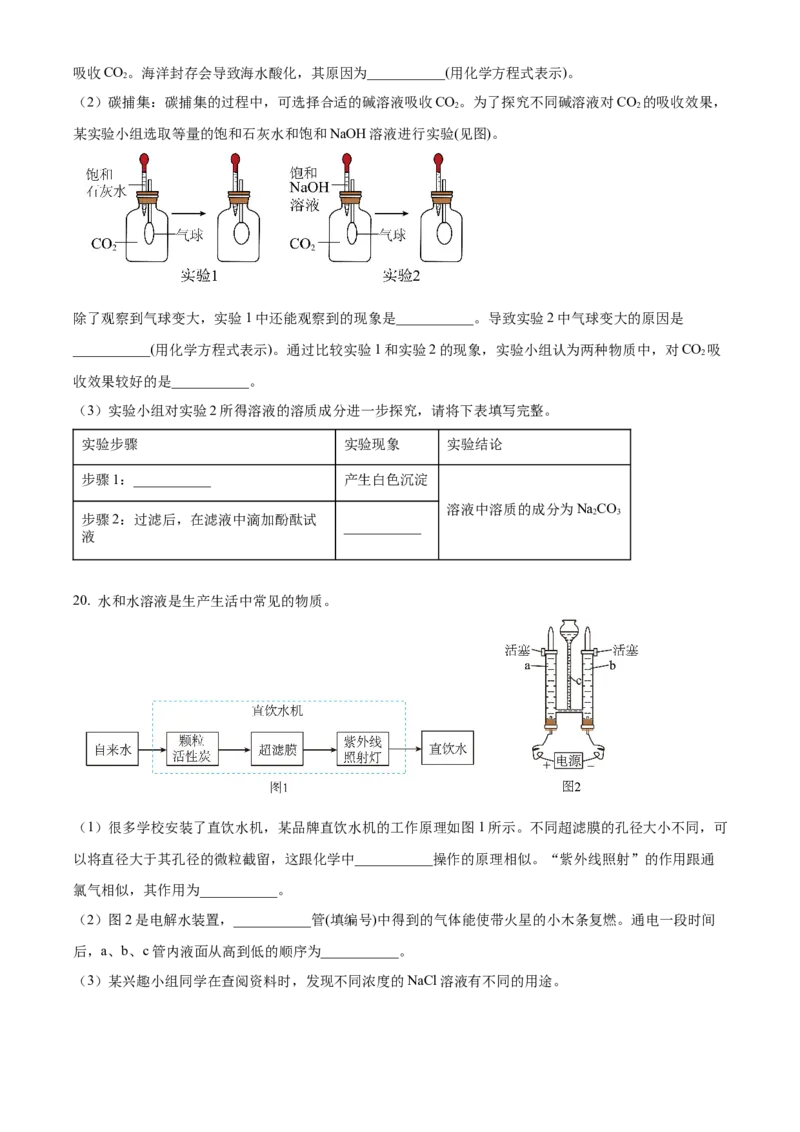
(2)碳捕集:碳捕集的过程中,可选择合适的碱溶液吸收CO。为了探究不同碱溶液对CO 的吸收效果,
2 2
某实验小组选取等量的饱和石灰水和饱和NaOH溶液进行实验(见图)。
除了观察到气球变大,实验1中还能观察到的现象是___________。导致实验2中气球变大的原因是
___________(用化学方程式表示)。通过比较实验1和实验2的现象,实验小组认为两种物质中,对CO 吸
2
收效果较好的是___________。
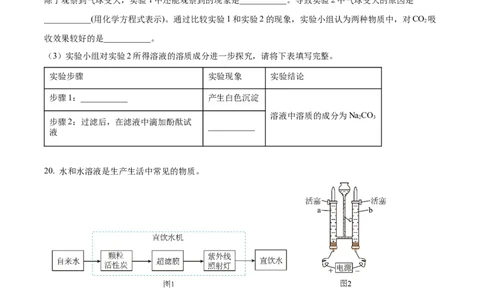
(3)实验小组对实验2所得溶液的溶质成分进一步探究,请将下表填写完整。
实验步骤 实验现象 实验结论
步骤1:___________ 产生白色沉淀
溶液中溶质的成分为NaCO
2 3
步骤2:过滤后,在滤液中滴加酚酞试
___________
液
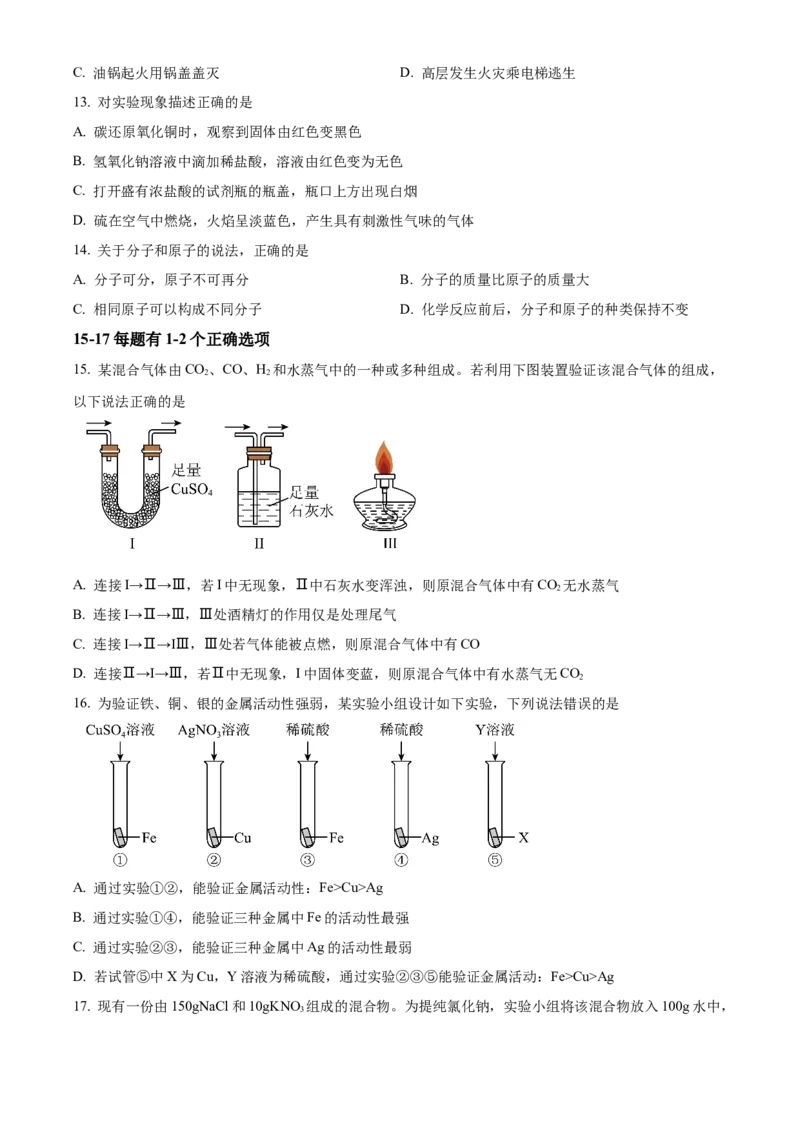
20. 水和水溶液是生产生活中常见的物质。
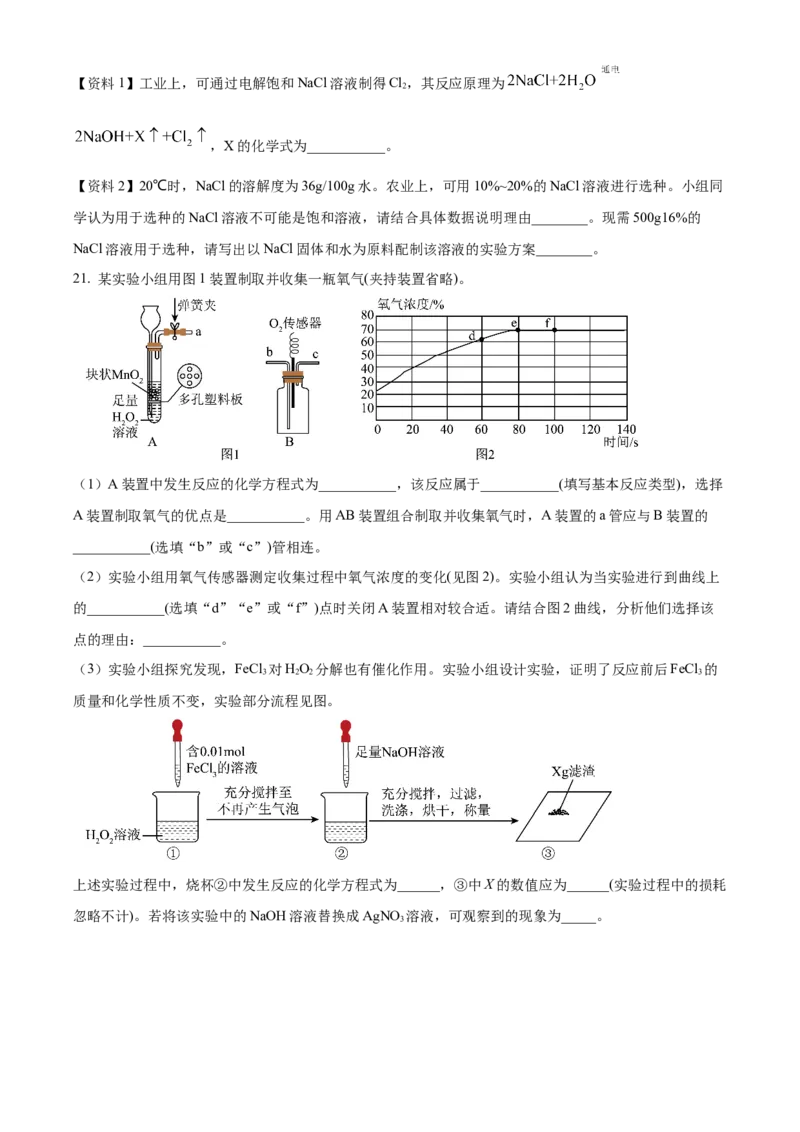
(1)很多学校安装了直饮水机,某品牌直饮水机的工作原理如图1所示。不同超滤膜的孔径大小不同,可
以将直径大于其孔径的微粒截留,这跟化学中___________操作的原理相似。“紫外线照射”的作用跟通
氯气相似,其作用为___________。
(2)图2是电解水装置,___________管(填编号)中得到的气体能使带火星的小木条复燃。通电一段时间
后,a、b、c管内液面从高到低的顺序为___________。
(3)某兴趣小组同学在查阅资料时,发现不同浓度的NaCl溶液有不同的用途。【资料1】工业上,可通过电解饱和NaCl溶液制得Cl,其反应原理为
2
,X的化学式为___________。
【资料2】20℃时,NaCl的溶解度为36g/100g水。农业上,可用10%~20%的NaCl溶液进行选种。小组同
学认为用于选种的NaCl溶液不可能是饱和溶液,请结合具体数据说明理由________。现需500g16%的
NaCl溶液用于选种,请写出以NaCl固体和水为原料配制该溶液的实验方案________。
21. 某实验小组用图1装置制取并收集一瓶氧气(夹持装置省略)。
(1)A装置中发生反应的化学方程式为___________,该反应属于___________(填写基本反应类型),选择
A装置制取氧气的优点是___________。用AB装置组合制取并收集氧气时,A装置的a管应与B装置的
___________(选填“b”或“c”)管相连。
(2)实验小组用氧气传感器测定收集过程中氧气浓度的变化(见图2)。实验小组认为当实验进行到曲线上
的___________(选填“d”“e”或“f”)点时关闭A装置相对较合适。请结合图2曲线,分析他们选择该
点的理由:___________。
(3)实验小组探究发现,FeCl 对HO 分解也有催化作用。实验小组设计实验,证明了反应前后FeCl 的
3 2 2 3
质量和化学性质不变,实验部分流程见图。
上述实验过程中,烧杯②中发生反应的化学方程式为______,③中X的数值应为______(实验过程中的损耗
忽略不计)。若将该实验中的NaOH溶液替换成AgNO 溶液,可观察到的现象为_____。
3