文档内容
上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
2022 学年第二学期期中
高三年级化学学科等级考质量监测试卷
考生注意:
1.本试卷满分100分,考试时间60分钟。
2.本试卷设试卷和答题纸两部分,试卷包括试题与答题要求;所有答案必须涂或写在答题纸
上;做在试卷上一律不得分。
3.答题前,考生务必在答题纸上用钢笔或圆珠笔在答题纸正面清楚地填写姓名、准考证号。
4.答题纸与试卷在试题编号上是一一对应的,答题时应特别注意,不能错位。
相对原子质量:O-16 C-12 H-1 N-14 Cl-35.5 Si-28 N-14 Cu-64 S-32
一、选择题(共40分,每小题2分。每小题只有一个正确答案)
1. 下列属于新能源的是
A. 煤 B. 石油 C. 太阳能 D. 天然气
2. 关于生铁和钢的区别正确的是
A. 生铁属于纯净物,钢属于混合物 B. 生铁比钢的含碳量更高
C. 生铁比钢弹性更好 D. 生铁属于铁-碳合金,钢也 是合金但不含碳
3. 关于NaO 的说法错误的是
2 2
A. 常温下是淡黄色固体 B. 只含有离子键
C. 熔融状态下能导电 D. 具有强氧化性的原因和氧元素有关
4. 以下表示氦原子结构的化学用语中,对电子运动状态描述最详尽的是
A. :He B. C. D.
5. 实验室海带提碘的实验中不涉及的操作是
A. 灼烧 B. 溶解 C. 过滤 D. 蒸发
6. 下列反应中生成物总能量高于反应物总能量的是
A. 碳酸钙受热分解 B. 甲烷燃烧
C. 铝粉与氧化铁粉末反应 D. 铁粉与硫粉反应
7. 在下列变化 ①工业固氮,②大气固氮,③碳铵分解,按氮元素被氧化、被还原、既不被氧化又不被还
原的顺序排列,正确的是
A. ②①③ B. ③②① C. ①②③ D. ③①②
第 1 页 共 8 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
8. 下列关于工业生产的叙述错误的是
A. 氯碱工业的产品主要是氯气、氢气和氢氧化钠及相关物质
B. 合成氨工业中反应难以发生的原因和氮气的结构有关
C. 硫酸工业中二氧化硫的转化选择475℃是因为高温有利于平衡向产物方向移动
D. 纯碱工业使用联合制碱法可提高钠和氯的利用率
9. 下列变化规律正确的是
A. HCl、HBr、HI热稳定性由弱到强
B. HCO、HClO、CHCOOH的酸性由弱到强
2 3 3
C. 物质的量浓度相等的NaCl、MgCl 、AlCl 三种溶液的pH值由小到大
2 3
D. 等物质的量的乙烷、乙烯、乙炔充分燃烧,所耗用氧气的量由多到少
10. 标准状况下,向100mL氢硫酸溶液中通入二氧化硫气体,溶液pH先增大后减小,当通入SO 112mL时
2
溶液pH最大,则原氢硫酸溶液的物质的量浓度为_____mol·L-1。
A. 0.1 B. 0.05 C. 0.01 D. 0.005
11. 下列有关物质性质的描述不符合事实的是
A. 有机物不导电 B. 金刚石是自然界最硬的物质
C. 可用作食品防腐剂 D. N0可用于某些疾病的治疗
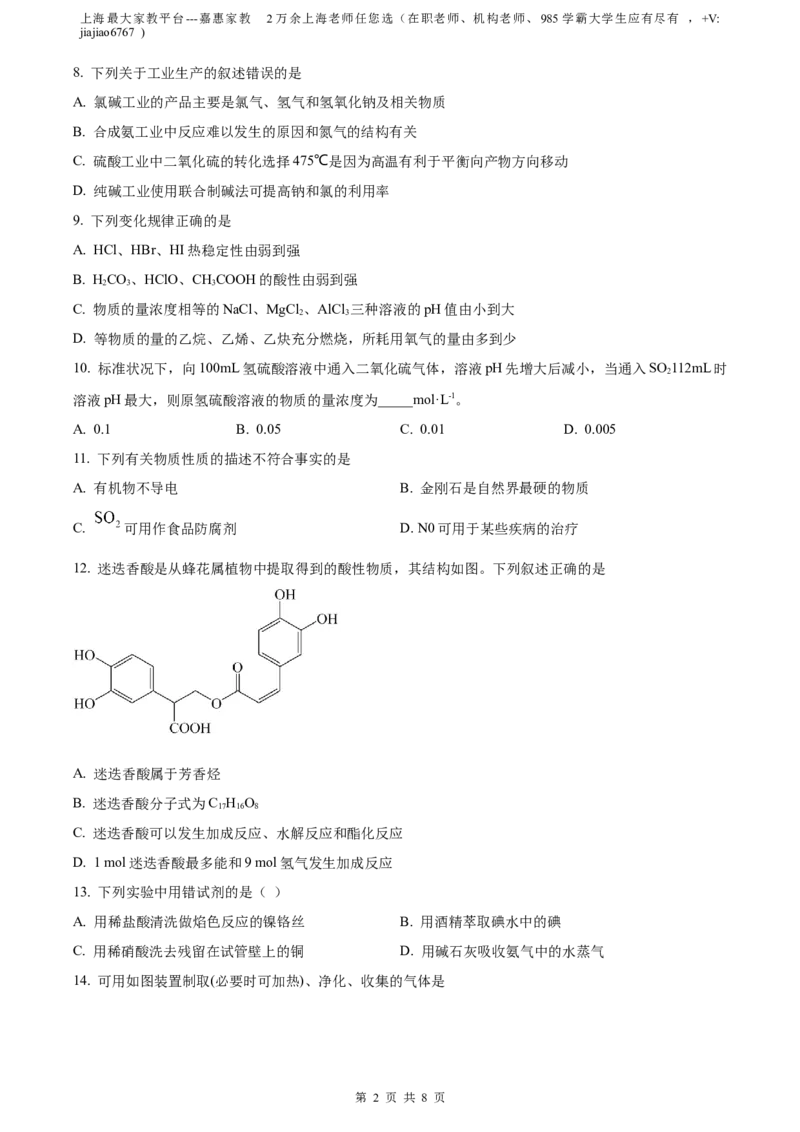
12. 迷迭香酸是从蜂花属植物中提取得到的酸性物质,其结构如图。下列叙述正确的是
A. 迷迭香酸属于芳香烃
B. 迷迭香酸分子式为C H O
17 16 8
C. 迷迭香酸可以发生加成反应、水解反应和酯化反应
D. 1 mol迷迭香酸最多能和9 mol氢气发生加成反应
13. 下列实验中用错试剂的是( )
A. 用稀盐酸清洗做焰色反应的镍铬丝 B. 用酒精萃取碘水中的碘
C. 用稀硝酸洗去残留在试管壁上的铜 D. 用碱石灰吸收氨气中的水蒸气
14. 可用如图装置制取(必要时可加热)、净化、收集的气体是
第 2 页 共 8 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
A. 铜和稀硝酸制一氧化氮
B. 氯化钠与浓硫酸制氯化氢
.
C 锌和稀硫酸制氢气
D. 碳化钙与饱和食盐水制乙炔
15. 下列实验基本操作错误的是
A. 测定未知NaOH溶液浓度时,酸式滴定管需用标准酸液润洗2~3次
B. 硫酸铜结晶水含量测定时,需用小火缓慢加热,防止晶体飞溅
C. 滴定时,左手控制活塞,右手握持锥形瓶,边滴边振荡,眼睛注视滴定管中的液面
D. 配制0.1 mol·L-1 HSO 溶液时,将浓HSO 沿杯壁倒入加有水的烧杯中稀释
2 4 2 4
16. 下列物质的检验操作或试剂正确的是
A. 检验乙醛中的醛基,可以用银氨溶液小火加热得到银镜
B. 纸层析法检验试剂时,试样浸在展开剂中
C. 检验NaSO 是否变质,可以用BaCl 溶液
2 3 2
D. 检验FeSO 是否被氧化,使用硫氰化钾溶液
4
17. 1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯反应温度为115~125℃,反应装置如下图。
下列对该实验的描述错误的是
.
A 不能用水浴加热
B. 长玻璃管起冷凝回流作用
C. 提纯乙酸丁酯需要经过水、氢氧化钠溶液洗涤
D. 加入过量乙酸可以提高1-丁醇的转化率
18. 下列事实与解释不匹配的是
第 3 页 共 8 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
选项 事实 解释
A 在蔗糖中加入浓硫酸后出现发黑现象 浓硫酸具有脱水性
B 常温下,浓硝酸可以用铝罐贮存 铝与浓硝酸不反应
C 氯气通入碘化钾溶液中,溶液变为棕黄色 氯比碘活泼
D 氨水可使酚酞试剂变为红色 氨水显碱性
A. A B. B C. C D. D
19. 取一张用饱和NaCl溶液浸湿的pH试纸,两根铅笔芯作电极,接通直流电源,一段时间后,发现b电
极与试纸接触处出现一个双色同心圆,内圆为白色,外圆呈浅红色.则下列说法错误的是
A. a电极是阴极 B. b电极与电源的正极相连接
C. 电解过程中,水是氧化剂 D. a电极附近溶液的pH变小
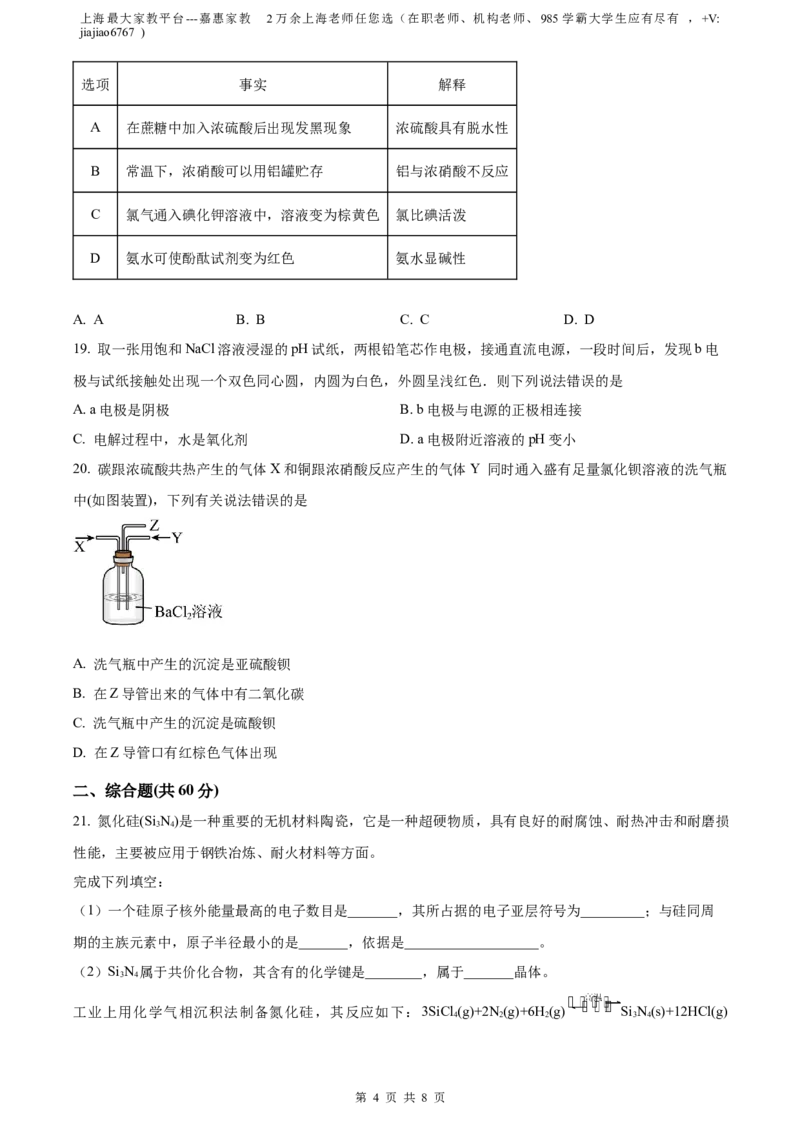
20. 碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y 同时通入盛有足量氯化钡溶液的洗气瓶
中(如图装置),下列有关说法错误的是
A. 洗气瓶中产生的沉淀是亚硫酸钡
B. 在Z导管出来的气体中有二氧化碳
C. 洗气瓶中产生的沉淀是硫酸钡
D. 在Z导管口有红棕色气体出现
二、综合题(共60分)
21. 氮化硅(Si N)是一种重要的无机材料陶瓷,它是一种超硬物质,具有良好的耐腐蚀、耐热冲击和耐磨损
3 4
性能,主要被应用于钢铁冶炼、耐火材料等方面。
完成下列填空:
(1)一个硅原子核外能量最高的电子数目是_______,其所占据的电子亚层符号为_________;与硅同周
期的主族元素中,原子半径最小的是_______,依据是___________________。
(2)Si N 属于共价化合物,其含有的化学键是________,属于_______晶体。
3 4
工业上用化学气相沉积法制备氮化硅,其反应如下:3SiCl (g)+2N(g)+6H(g) Si N(s)+12HCl(g)
4 2 2 3 4
第 4 页 共 8 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
+Q(Q>0)
(3)该反应的平衡常数表达式K=_____________________ 。
(4)在一定温度下进行上述反应,若反应容器的容积为2L,3min后达到平衡,测得固体的质量增加了
2.80g,则SiCl 的平均反应速率为________________ mol·L-1·min-1。
4
(5)上述反应达到平衡后,改变某一条件,下列说法正确的是________。
a.增加Si N 的量,平衡向左移动 b.减小HCl的量,平衡向左移动
3 4
c.增大压强,平衡常数K减小 d.降低温度,平衡常数K增大
(6)若平衡时H 和HCl的物质的量之比为 ,保持其他条件不变,升高温度后达到新的平衡时,H 和
2 2
HCl的物质的量之比_______ (填“>”、“<”或“=”) 。
的
22. 我们知道,电解质在溶液中 反应实质是离子之间的反应。通常,离子反应有两种情况,一种是没有
电子转移的,是离子互换反应;另一种是有电子转移的,属于氧化还原反应。
在溶液中发生的离子互换反应一般总是向离子浓度减小的方向进行。取 4mL1mol·L-1醋酸溶液在试管中,
逐滴滴入1mL1mol·L-1碳酸钠溶液。
(1)写出该反应的离子方程式______________。
随着碳酸钠溶液的滴加,溶液的pH___________(填“增大”、“减小”或“不变”)。
(2)这一离子互换反应 是否向离子浓度减小方向进行?请应用平衡移动原理进行说明。 ___________。
(3)当碳酸钠溶液全部滴加完后,测得该溶液显酸性,比较该溶液中除HO以外的微粒浓度大小(不考虑
2
CO 的溶解)_____________________。
2
氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:NO +4H++3e-
=NO+2HO。KMnO 、NaCO、Cu O、Fe (SO ) 四种物质中的一种物质能使上述还原过程发生。
2 4 2 3 2 2 4 3
(4)写出并配平该氧化还原反应的离子方程式,用单线桥法标出电子转移方向和数目。_________。
23. 用N-杂环卡其碱(NHC base)作为催化剂,可合成多环化合物。下面是一种多环化合物 H的合成路线(无
需考虑部分中间体的立体化学)。
第 5 页 共 8 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
已知: (-R表示烃基,其和苯环相连的碳上有氢原子)
完成下列填空:
(1)A中含氧官能团名称是______________;反应②涉及两步反应,已知第一步反应类型为加成反应,
第二步的反应类型为_________。
(2)检验C中“碳碳双键”的操作是___________________________________________。
(3)E的结构简式为_____________________。
(4)化合物X是C的同分异构体,可发生银镜反应,与酸性高锰酸钾溶液反应后可以得到对苯二甲酸(
),写出X的结构简式_______________________。
(5)参考上述信息,设计以甲苯和乙醛为原料,合成肉桂醛( )的合成路线(其他无机试
剂任选) _______________。(合成路线可表示为: )
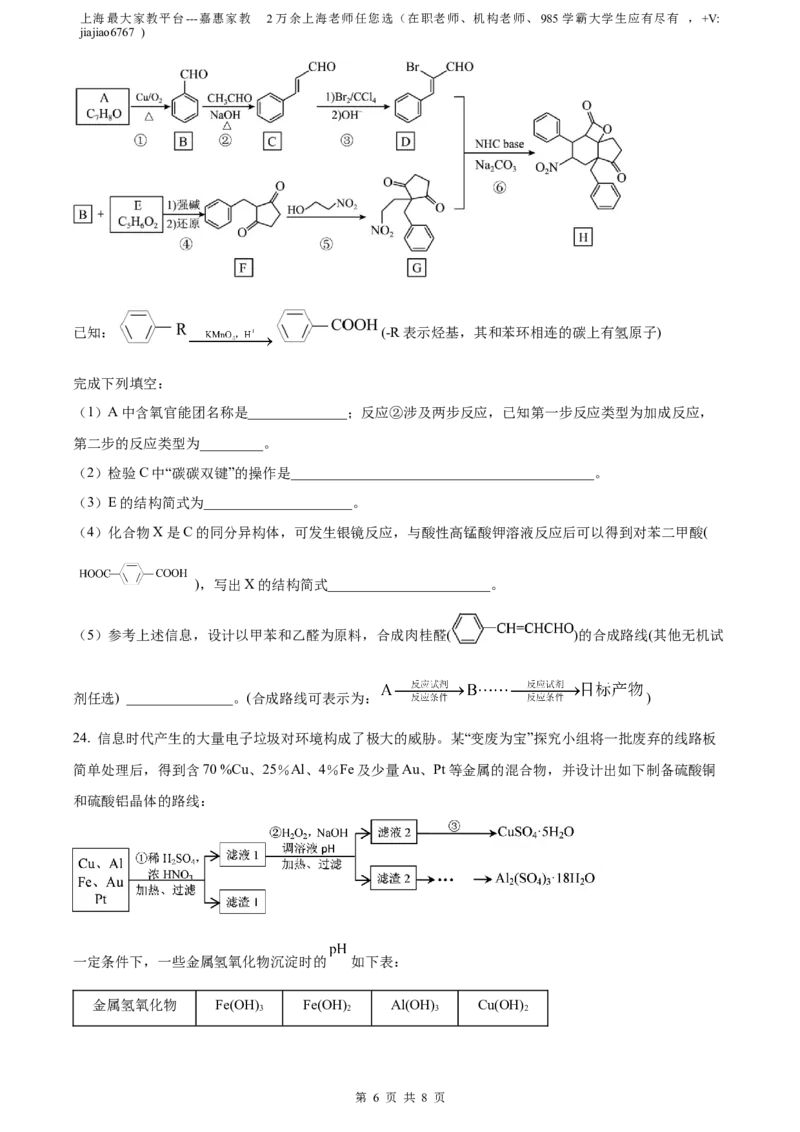
24. 信息时代产生的大量电子垃圾对环境构成了极大的威胁。某“变废为宝”探究小组将一批废弃的线路板
简单处理后,得到含70 %Cu、25%Al、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜
和硫酸铝晶体的路线:
一定条件下,一些金属氢氧化物沉淀时的 如下表:
金属氢氧化物 Fe(OH) Fe(OH) Al(OH) Cu(OH)
3 2 3 2
第 6 页 共 8 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
开始沉淀的pH 2.3 6.8 3.5 4.4
完全沉淀的pH 3.2 8.3 4.6 6.4
完成下列填空:
(1)写出第①步中Cu与酸反应生成NO的离子方程式________________;第②步中使用HO 做氧化剂的
2 2
优点是__________,NaOH调节溶液pH的目的是使____________生成沉淀。
(2)第③步的操作为:滤液2加热蒸发、_______、_______、乙醇洗涤、干燥,得到胆矾。
(3)由滤渣2制取Al (SO )·18H O ,探究小组设计了三种方案:
2 4 3 2
上述三种方案中,____方案不可行,原因是________;从原子利用率角度考虑,_____方案更合理。
(4)探究小组用滴定法测定CuSO ·5H O含量。取a g试样配成100 mL溶液,每次取20.00 mL,消除干扰
4 2
离子后,用c mol ·L-1 EDTA(H Y2-)标准溶液滴定至终点,平均消耗EDTA溶液b mL。滴定反应如下:Cu2+
2
+ H Y2-= CuY2- + 2H+
2
写出计算CuSO ·5H O质量分数的表达式ω= ________________________________ 。
4 2
下列操作会导致CuSO ·5H O含量的测定结果偏高的是_________。
4 2
a.未干燥锥形瓶 b.滴定终点时滴定管尖嘴中产生气泡 c.未除净可与EDTA反应的干扰离子
第 7 页 共 8 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
第 8 页 共 8 页