文档内容
上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
2023 年 3 月学业质量调研
高三化学
(满分100分,时间60分钟)
可能用到的相对原子质量:H-1 O-16 N-14 S-32
一、选择题(每小题2分,共40分,每小题只有一个正确选项)
1. 中华文明中有许多关于化学的记载,《吕氏春秋》中就有“金(即铜)柔锡柔,合两柔则刚”一说,下列关
于合金的说法正确的是
A. 熔点一般比原组成成分高 B. 硬度一般比原组成成分大
C. 密度比原组成成分都小 D. 合金中至少有两种金属
2. 中国企业承建的卡塔尔世界杯“大金碗”球场采用聚四氟乙烯材料构成屋面膜结构。下列说法不正确的是
A. 聚四氟乙烯中不存在碳碳双键 B. 合成聚四氟乙烯的单体是不饱和烃
的
C. 聚四氟乙烯是一种性质较稳定 物质 D. 聚四氟乙烯没有固定熔点
3. 下列化学用语只能用来表示一种微粒的是
A. C H B. C. 二氯乙烷 D.
3 8
4. 反应SiCl (g)+2H(g) Si(s)+4HCl(g)可用于“中国芯”原料高纯硅的制备。下列说法正确的是
4 2
A. SiCl 为极性分子 B. 反应中只有一种物质为电解质
4
C. 单晶硅为分子晶体 D. Si原子的结构示意图为
5. 下列元素的单质,工业上不需要用电解法制取的是
A. 镁 B. 铝 C. 溴 D. 氯
6. 下列分子中所有原子都处在同一平面上的是( )
A. B. C. D.
7. 下列消毒剂的有效成分属于盐的是
A. 84消毒液 B. 过氧乙酸溶液 C. 双氧水 D. 医用酒精
第 1 页 共 10 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
8. 下列变化需克服共价键的是
A. 金刚石熔化 B. 汞变成汞蒸气 C. 碘升华 D. 食盐溶于水
9. 下列判断正确的是
A. 稳定性:HS>HO B. 熔点:Na>Mg
2 2
C. 碱性:NaOH>Mg(OH) D. 酸性:HF>HCl
2
10. 下列试剂不能用来鉴别SO 和HS的是
2 2
A. 新制氯水 B. 品红溶液 C. 氢氧化钠溶液 D. 硫酸铜溶液
11. 下列物质分离(括号内为杂质)的方法错误的是
A. 溴苯(溴):KI溶液,分液 B. 乙烯(二氧化硫):氢氧化钠溶液,洗气
C. 硝基苯(苯):蒸馏 D. 乙酸乙酯(乙醇):饱和碳酸钠溶液,分液
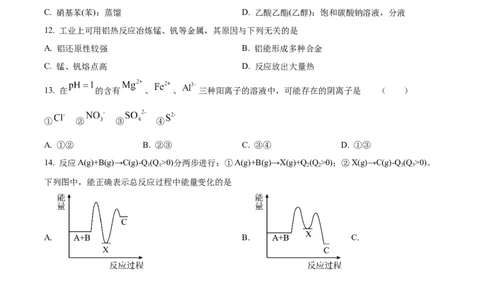
12. 工业上可用铝热反应冶炼锰、钒等金属,其原因与下列无关的是
A. 铝还原性较强 B. 铝能形成多种合金
C. 锰、钒熔点高 D. 反应放出大量热
13. 在 的含有 、 、 三种阳离子的溶液中,可能存在的阴离子是 ( )
① ② ③ ④
A. ①② B. ②③ C. ③④ D. ①③
14. 反应A(g)+B(g)→C(g)-Q (Q >0)分两步进行:①A(g)+B(g)→X(g)+Q (Q >0);②X(g)→C(g)-Q (Q >0)。
1 1 2 2 3 3
下列图中,能正确表示总反应过程中能量变化的是
A. B. C.
D.
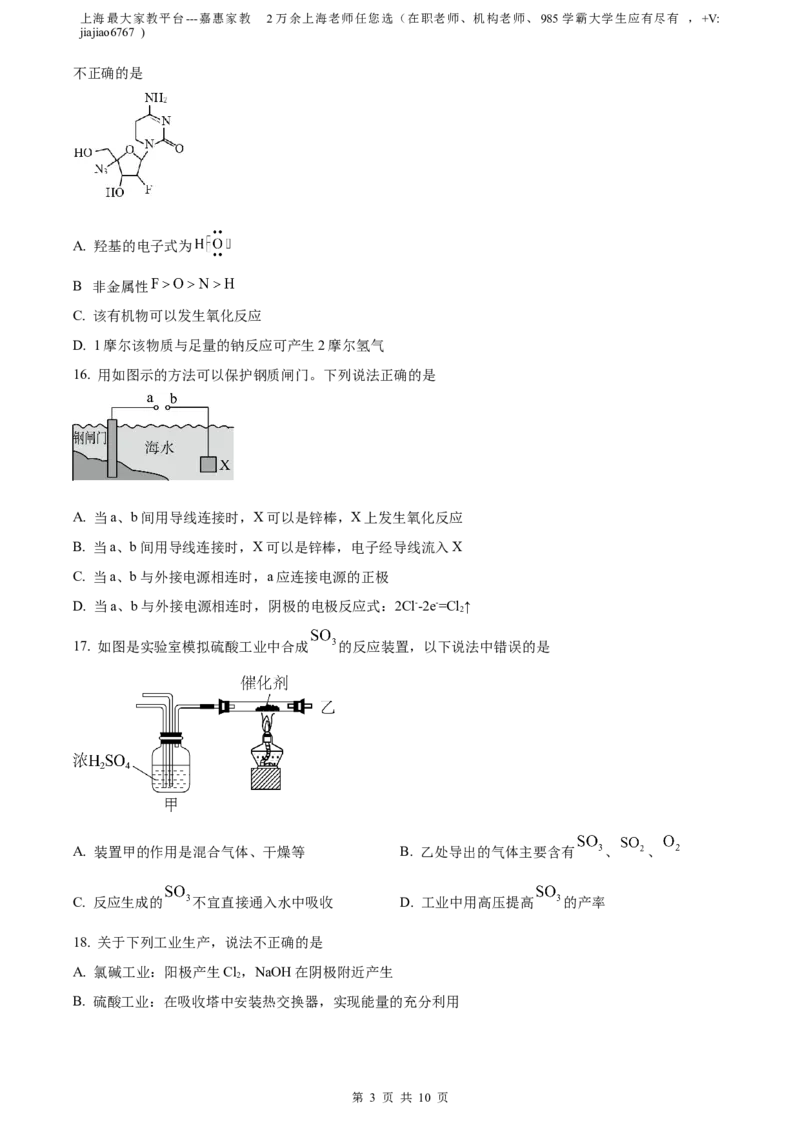
15. 2022年7月,我国首款治疗新冠肺炎的口服药阿兹夫定片获准上市,其有效成分结构如图,下列说法
第 2 页 共 10 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
不正确的是
A. 羟基的电子式为
.
B 非金属性
C. 该有机物可以发生氧化反应
D. 1摩尔该物质与足量的钠反应可产生2摩尔氢气
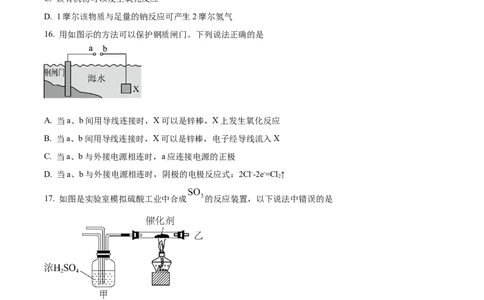
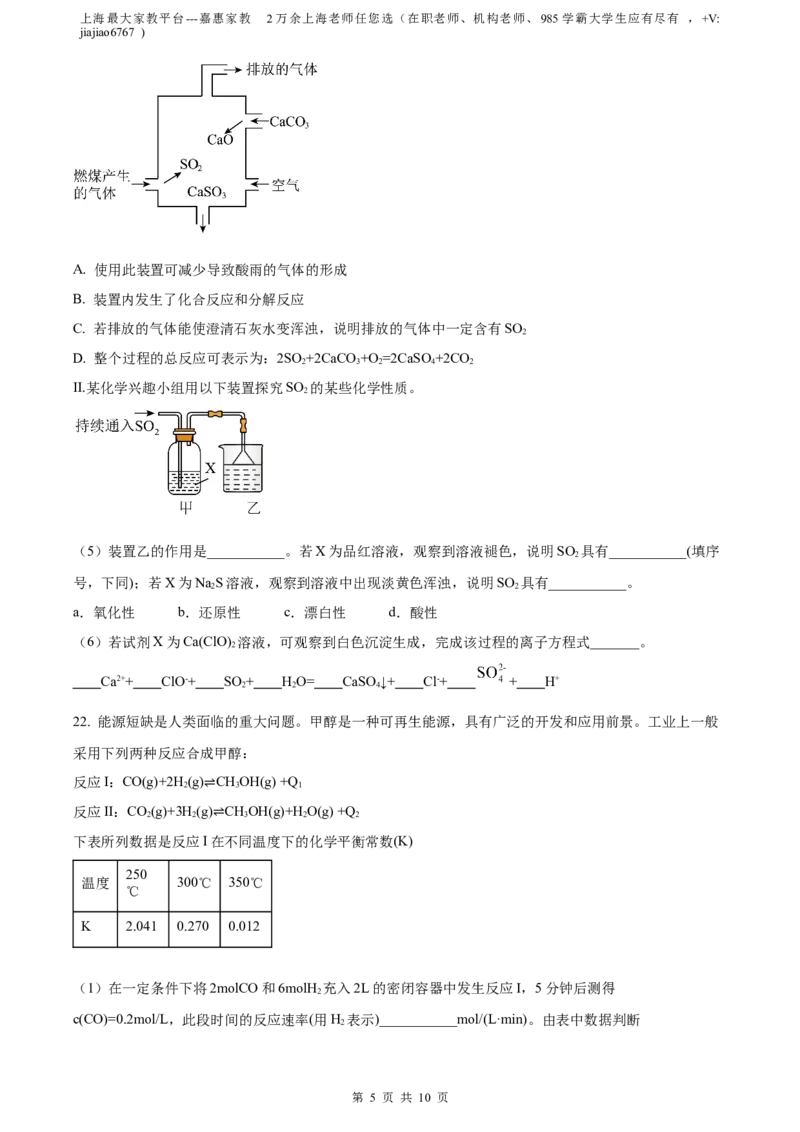
16. 用如图示的方法可以保护钢质闸门。下列说法正确的是
A. 当a、b间用导线连接时,X可以是锌棒,X上发生氧化反应
B. 当a、b间用导线连接时,X可以是锌棒,电子经导线流入X
C. 当a、b与外接电源相连时,a应连接电源的正极
D. 当a、b与外接电源相连时,阴极的电极反应式:2Cl--2e-=Cl↑
2
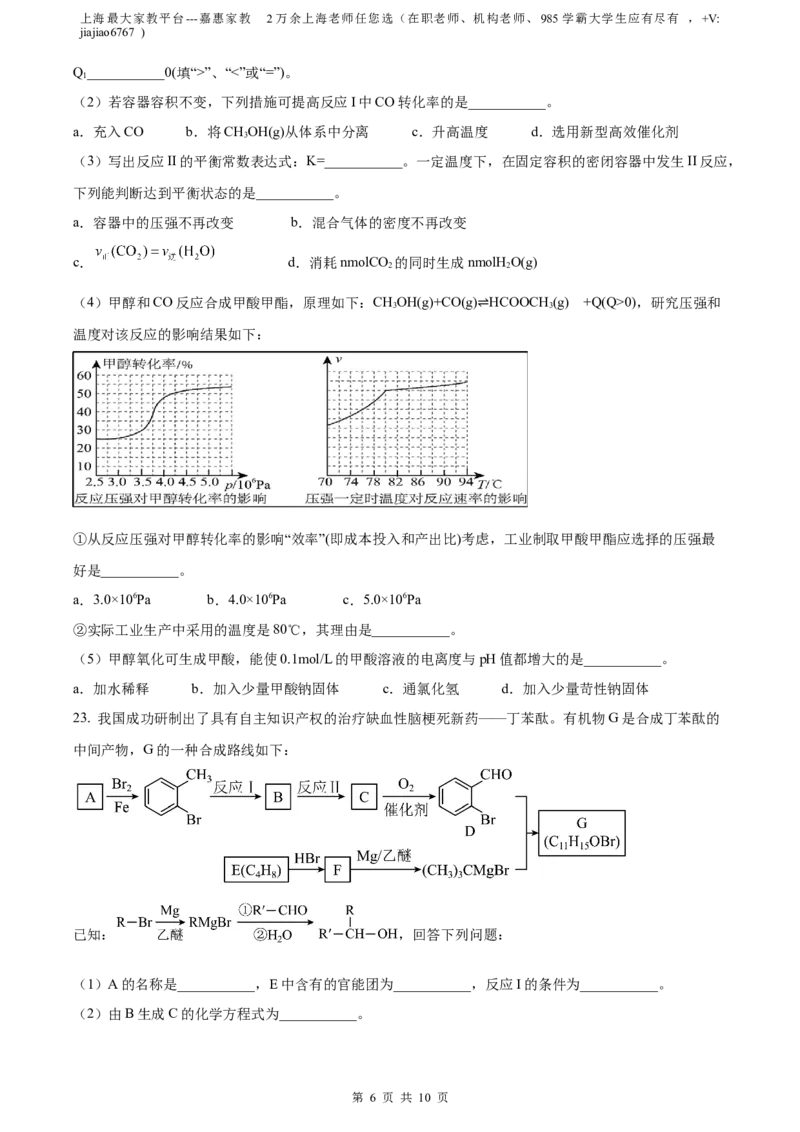
17. 如图是实验室模拟硫酸工业中合成 的反应装置,以下说法中错误的是
A. 装置甲的作用是混合气体、干燥等 B. 乙处导出的气体主要含有 、 、
C. 反应生成的 不宜直接通入水中吸收 D. 工业中用高压提高 的产率
18. 关于下列工业生产,说法不正确的是
A. 氯碱工业:阳极产生Cl,NaOH在阴极附近产生
2
B. 硫酸工业:在吸收塔中安装热交换器,实现能量的充分利用
第 3 页 共 10 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
C. 合成氨工业:利用氢气和氮气的循环来提高原料气的转化率
D. 纯碱工业:侯氏制碱法在分离出NaHCO 后的母液中加入食盐,促进NH Cl结晶
3 4
19. 密闭真空容器中放入BaO 固体,发生反应2BaO(s) 2BaO(s)+O(g) △H<0,并达到平衡状态Ⅰ;
2 2 2
保持温度不变,缩小容器体积,达到平衡状态Ⅱ;平衡状态Ⅰ与Ⅱ不同的是
A. 平衡常数 B. 反应速率 C. 氧气浓度 D. BaO的量
的
20. 室温下,在10mL浓度均为0.1mol/L 醋酸和盐酸混合液中,滴加0.1mol/L的NaOH溶液VmL,则下
列关系正确的是
A. V=0时:
B. V=10mL时:
C. V=20mL时:
D. 加入NaOH溶液至pH=7时, mL
二、综合题(共60分)
21. I.硫元素是动植物生长不可缺少的元素,广泛存在于自然界中。
(1)从图1中选择符合图2要求的X代表的物质:X___________。
(2)硫原子的最外层电子排布式为___________,其原子核外有___________种不同能量的电子。在周期
表中,与硫相邻的短周期元素的原子半径由大到小的顺序是___________。
(3)硫化氢溶液在空气中易变浑浊,说明S的非金属性比O___________(填“强”或“弱”),从原子结构的角
度解释其原因:___________。
的
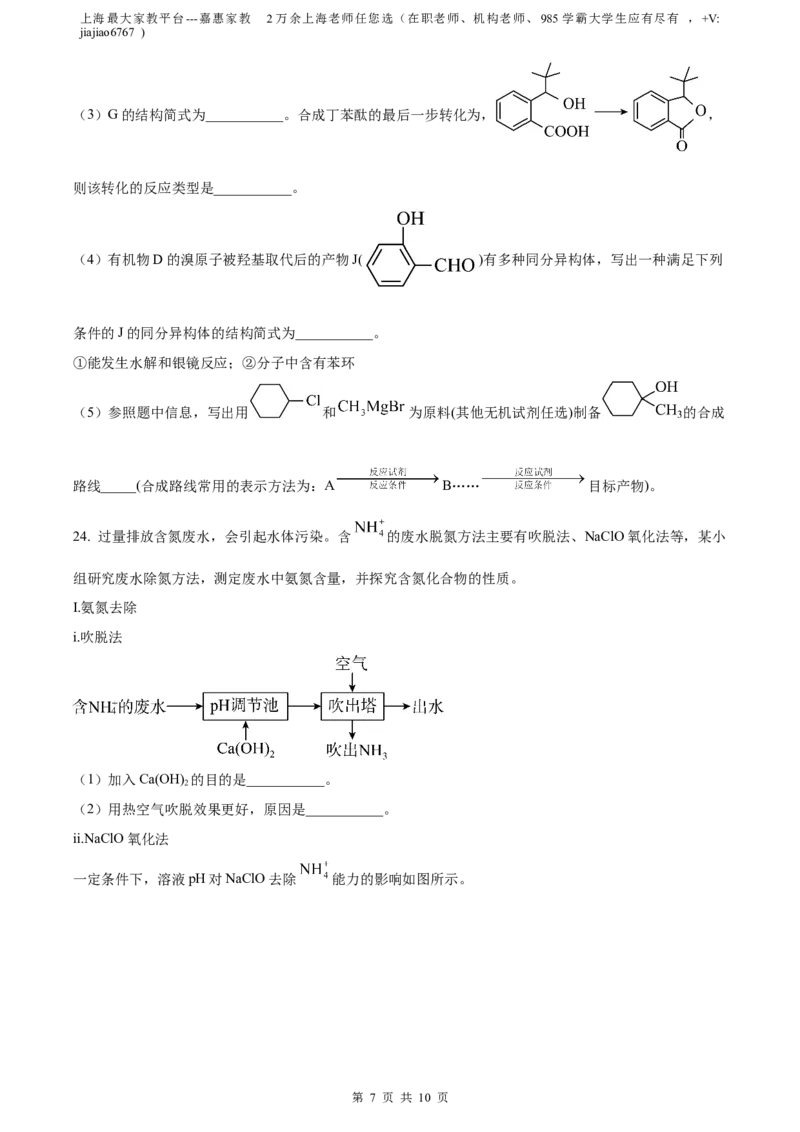
(4)下图是燃煤发电厂处理废气 装置示意图,下列说法不正确的是___________。
第 4 页 共 10 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
A. 使用此装置可减少导致酸雨的气体的形成
B. 装置内发生了化合反应和分解反应
C. 若排放的气体能使澄清石灰水变浑浊,说明排放的气体中一定含有SO
2
D. 整个过程的总反应可表示为:2SO +2CaCO +O =2CaSO +2CO
2 3 2 4 2
II.某化学兴趣小组用以下装置探究SO 的某些化学性质。
2
(5)装置乙的作用是___________。若X为品红溶液,观察到溶液褪色,说明SO 具有___________(填序
2
号,下同);若X为NaS溶液,观察到溶液中出现淡黄色浑浊,说明SO 具有___________。
2 2
a.氧化性 b.还原性 c.漂白性 d.酸性
(6)若试剂X为Ca(ClO) 溶液,可观察到白色沉淀生成,完成该过程的离子方程式_______。
2
Ca2++ ClO-+ SO + HO= CaSO↓+ Cl-+ + H+
2 2 4
22. 能源短缺是人类面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上一般
采用下列两种反应合成甲醇:
反应I:CO(g)+2H(g) CHOH(g) +Q
2 3 1
反应II:CO
2
(g)+3H
2
(g⇌) CH
3
OH(g)+H
2
O(g) +Q
2
下表所列数据是反应I在⇌不同温度下的化学平衡常数(K)
250
温度 300℃ 350℃
℃
K 2.041 0.270 0.012
(1)在一定条件下将2molCO和6molH 充入2L的密闭容器中发生反应I,5分钟后测得
2
c(CO)=0.2mol/L,此段时间的反应速率(用H 表示)___________mol/(L·min)。由表中数据判断
2
第 5 页 共 10 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
Q___________0(填“>”、“<”或“=”)。
1
(2)若容器容积不变,下列措施可提高反应I中CO转化率的是___________。
a.充入CO b.将CHOH(g)从体系中分离 c.升高温度 d.选用新型高效催化剂
3
(3)写出反应II的平衡常数表达式:K=___________。一定温度下,在固定容积的密闭容器中发生II反应,
下列能判断达到平衡状态的是___________。
a.容器中的压强不再改变 b.混合气体的密度不再改变
c. d.消耗nmolCO 的同时生成nmolH O(g)
2 2
(4)甲醇和CO反应合成甲酸甲酯,原理如下:CHOH(g)+CO(g) HCOOCH (g) +Q(Q>0),研究压强和
3 3
温度对该反应的影响结果如下: ⇌
①从反应压强对甲醇转化率的影响“效率”(即成本投入和产出比)考虑,工业制取甲酸甲酯应选择的压强最
好是___________。
a.3.0×106Pa b.4.0×106Pa c.5.0×106Pa
②实际工业生产中采用的温度是80℃,其理由是___________。
(5)甲醇氧化可生成甲酸,能使0.1mol/L的甲酸溶液的电离度与pH值都增大的是___________。
a.加水稀释 b.加入少量甲酸钠固体 c.通氯化氢 d.加入少量苛性钠固体
23. 我国成功研制出了具有自主知识产权的治疗缺血性脑梗死新药——丁苯酞。有机物G是合成丁苯酞的
中间产物,G的一种合成路线如下:
已知: ,回答下列问题:
(1)A的名称是___________,E中含有的官能团为___________,反应I的条件为___________。
(2)由B生成C的化学方程式为___________。
第 6 页 共 10 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
(3)G的结构简式为___________。合成丁苯酞的最后一步转化为, ,
则该转化的反应类型是___________。
(4)有机物D的溴原子被羟基取代后的产物J( )有多种同分异构体,写出一种满足下列
条件的J的同分异构体的结构简式为___________。
①能发生水解和银镜反应;②分子中含有苯环 。
(5)参照题中信息,写出用 和 为原料(其他无机试剂任选)制备 的合成
路线_____(合成路线常用的表示方法为:A B…… 目标产物)。
24. 过量排放含氮废水,会引起水体污染。含 的废水脱氮方法主要有吹脱法、NaClO氧化法等,某小
组研究废水除氮方法,测定废水中氨氮含量,并探究含氮化合物的性质。
I.氨氮去除
i.吹脱法
(1)加入Ca(OH) 的目的是___________。
2
(2)用热空气吹脱效果更好,原因是___________。
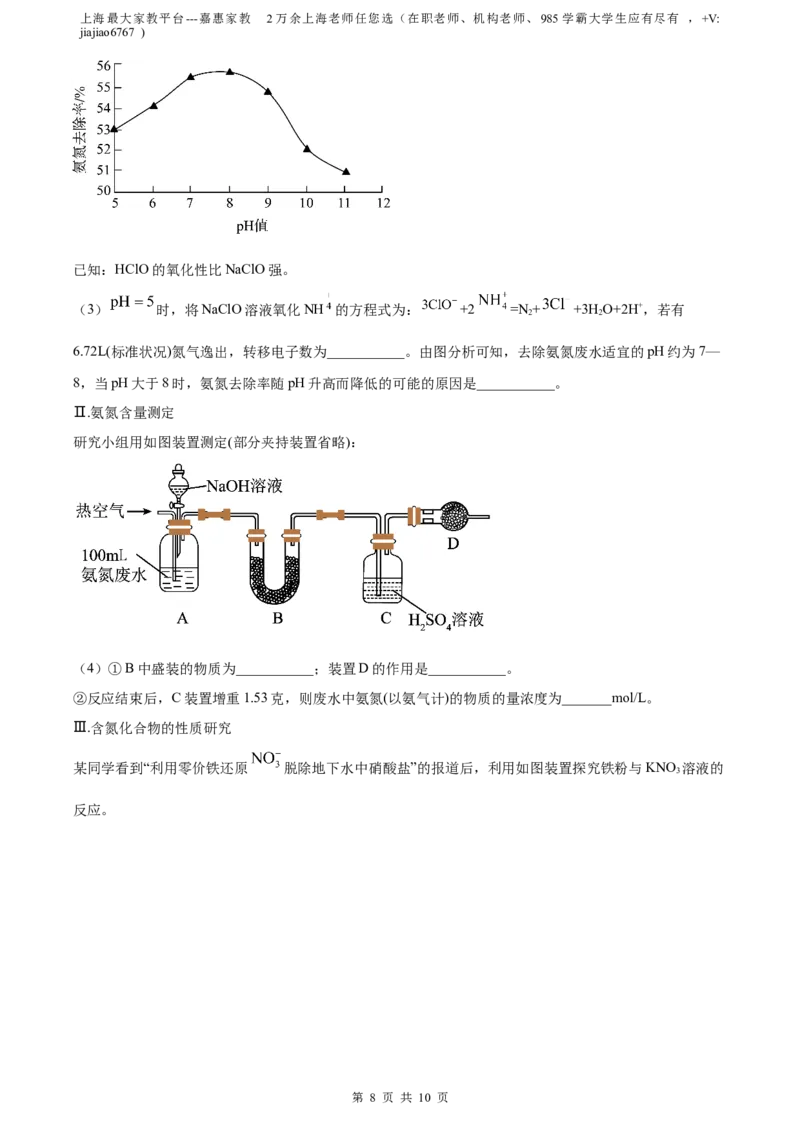
ii.NaClO氧化法
一定条件下,溶液pH对NaClO去除 能力的影响如图所示。
第 7 页 共 10 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
已知:HClO的氧化性比NaClO强。
(3) 时,将NaClO溶液氧化NH 的方程式为: +2 =N + +3H O+2H+,若有
2 2
6.72L(标准状况)氮气逸出,转移电子数为___________。由图分析可知,去除氨氮废水适宜的pH约为7—
8,当pH大于8时,氨氮去除率随pH升高而降低的可能的原因是___________。
Ⅱ.氨氮含量测定
研究小组用如图装置测定(部分夹持装置省略):
(4)①B中盛装的物质为___________;装置D的作用是___________。
②反应结束后,C装置增重1.53克,则废水中氨氮(以氨气计)的物质的量浓度为_______mol/L。
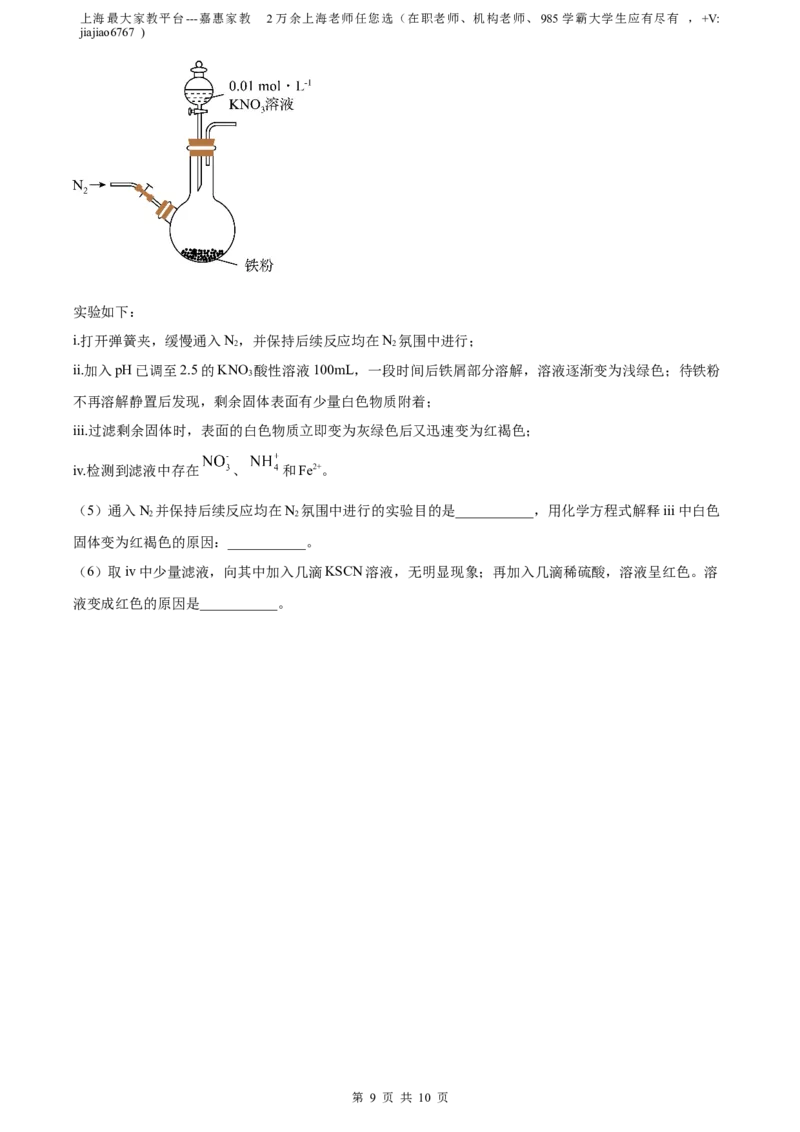
Ⅲ.含氮化合物的性质研究
某同学看到“利用零价铁还原 脱除地下水中硝酸盐”的报道后,利用如图装置探究铁粉与KNO 溶液的
3
反应。
第 8 页 共 10 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
实验如下:
i.打开弹簧夹,缓慢通入N,并保持后续反应均在N 氛围中进行;
2 2
ii.加入pH已调至2.5的KNO 酸性溶液100mL,一段时间后铁屑部分溶解,溶液逐渐变为浅绿色;待铁粉
3
不再溶解静置后发现,剩余固体表面有少量白色物质附着;
iii.过滤剩余固体时,表面的白色物质立即变为灰绿色后又迅速变为红褐色;
iv.检测到滤液中存在 、 和Fe2+。
(5)通入N 并保持后续反应均在N 氛围中进行的实验目的是___________,用化学方程式解释iii中白色
2 2
固体变为红褐色的原因:___________。
(6)取iv中少量滤液,向其中加入几滴KSCN溶液,无明显现象;再加入几滴稀硫酸,溶液呈红色。溶
液变成红色的原因是___________。
第 9 页 共 10 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
第 10 页 共 10 页