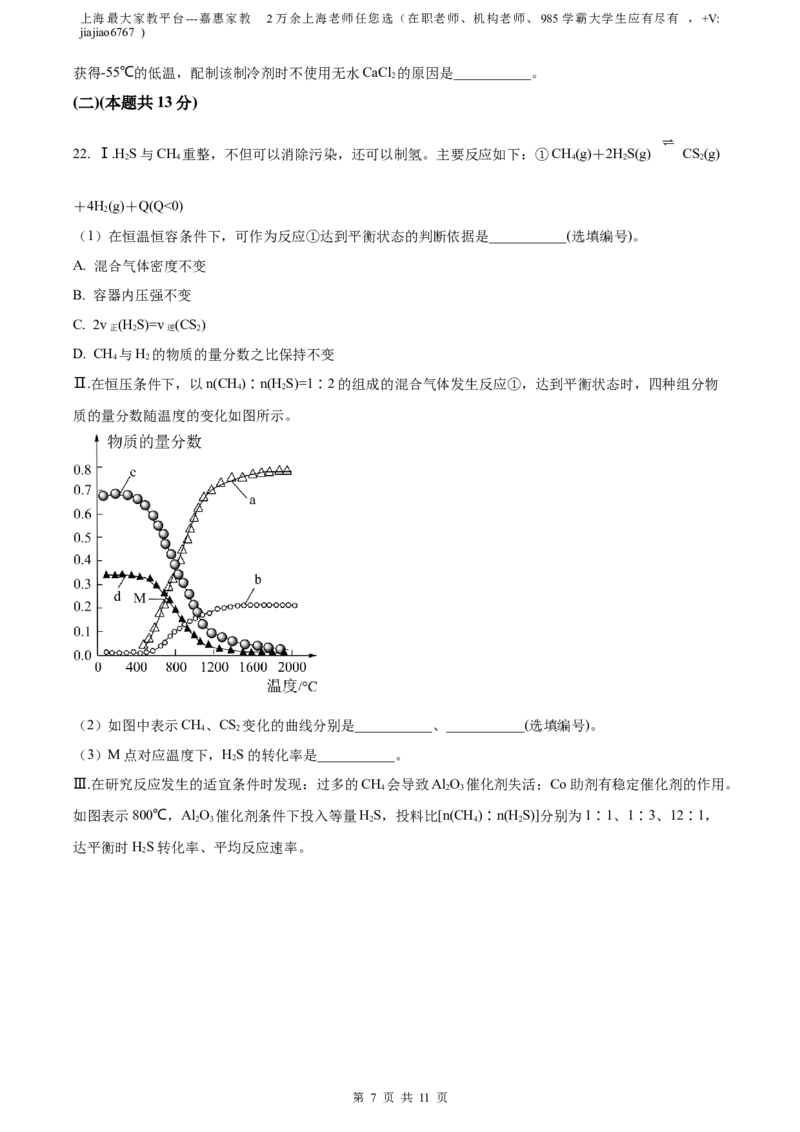文档内容
上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
上海市金山区 2022-2023 学年高三下学期二模测试
化学试题
考生注意:
1.考试时间60分钟,试卷满分100分。
2.答题前,务必在答题卡上填写座位号、学校和姓名。
3.本考试设试卷和答题纸两部分,所有答题必须做在答题纸上,做在试卷上一律不得分。
4.注意试题号与答题纸编号一一对应,不能错位。
相对原子质量:H-1 C-12 O-16 S-32 Cl-35.5 Zn-65 Ba-137
一、选择题(共40分,每小题2分。每小题只有一个正确答案)
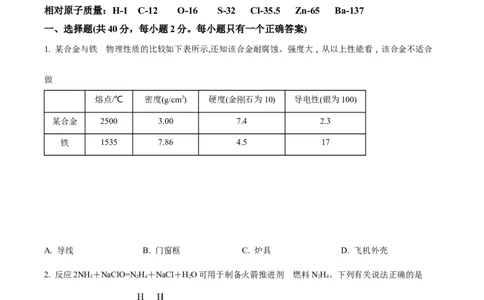
1. 某合金与铁 物的理性质的比较如下表所示,还知该合金耐腐蚀、强度大,从以上性能看,该合金不适合
做
熔点/℃ 密度(g/cm3) 硬度(金刚石为10) 导电性(银为100)
某合金 2500 3.00 7.4 2.3
铁 1535 7.86 4.5 17
A. 导线 B. 门窗框 C. 炉具 D. 飞机外壳
的
2. 反应2NH +NaClO=N H+NaCl+HO可用于制备火箭推进剂 燃料NH。下列有关说法正确的是
3 2 4 2 2 4
A. NH 的结构式: B. 中子数为8的氮原子:15N
2 4
C. O原子的最外层电子排布式:2s22p6 D. NaClO的电子式:
3. 下列物质在空气中久置会变质,变质过程不涉及氧化还原反应的物质是
A. Na B. NaO C. NaO D. NaSO
2 2 2 2 3
4. 在稀硫酸中加入铜粉,铜粉不溶解,再加入物质X后铜粉逐渐溶解,X可能是
第 1 页 共 11 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
A. HCl B. Fe (SO ) C. KS D. FeSO
2 4 3 2 4
5. 下列不能用键能解释的事实是
A. 晶体密度:SiO>CO B. 热稳定性:CH>SiH
2 2 4 4
C. 活泼性:乙烯>苯 D. 硬度:金刚石>晶体硅
6. 下列物质中,属于含非极性键的共价化合物是
A. CHOH B. NH Cl C. C H D. NaO
3 4 2 4 2 2
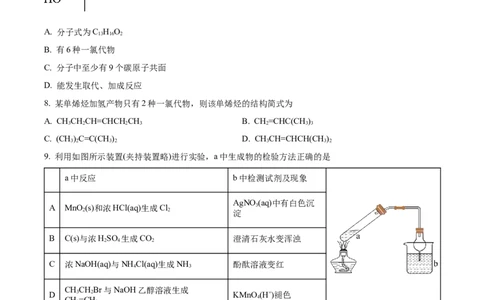
7. 布洛芬是一种解热镇痛药,结构简式如图所示。下列关于布洛芬的叙述正确的是
A. 分子式为C H O
13 16 2
B. 有6种一氯代物
C. 分子中至少有9个碳原子共面
D. 能发生取代、加成反应
8. 某单烯烃加氢产物只有2种一氯代物,则该单烯烃的结构简式为
A. CHCHCH=CHCH CH B. CH=CHC(CH )
3 2 2 3 2 3 3
C. (CH)C=C(CH ) D. CHCH=CHCH(CH )
3 2 3 2 3 3 2
9. 利用如图所示装置(夹持装置略)进行实验,a中生成物的检验方法正确的是
a中反应 b中检测试剂及现象
AgNO(aq)中有白色沉
A MnO (s)和浓HCl(aq)生成Cl 3
2 2 淀
B C(s)与浓HSO 生成CO 澄清石灰水变浑浊
2 4 2
C 浓NaOH(aq)与NH Cl(aq)生成NH 酚酞溶液变红
4 3
CHCHBr与NaOH乙醇溶液生成
D 3 2 KMnO (H+)褪色
CH=CH 4
2 2
A. A B. B C. C D. D
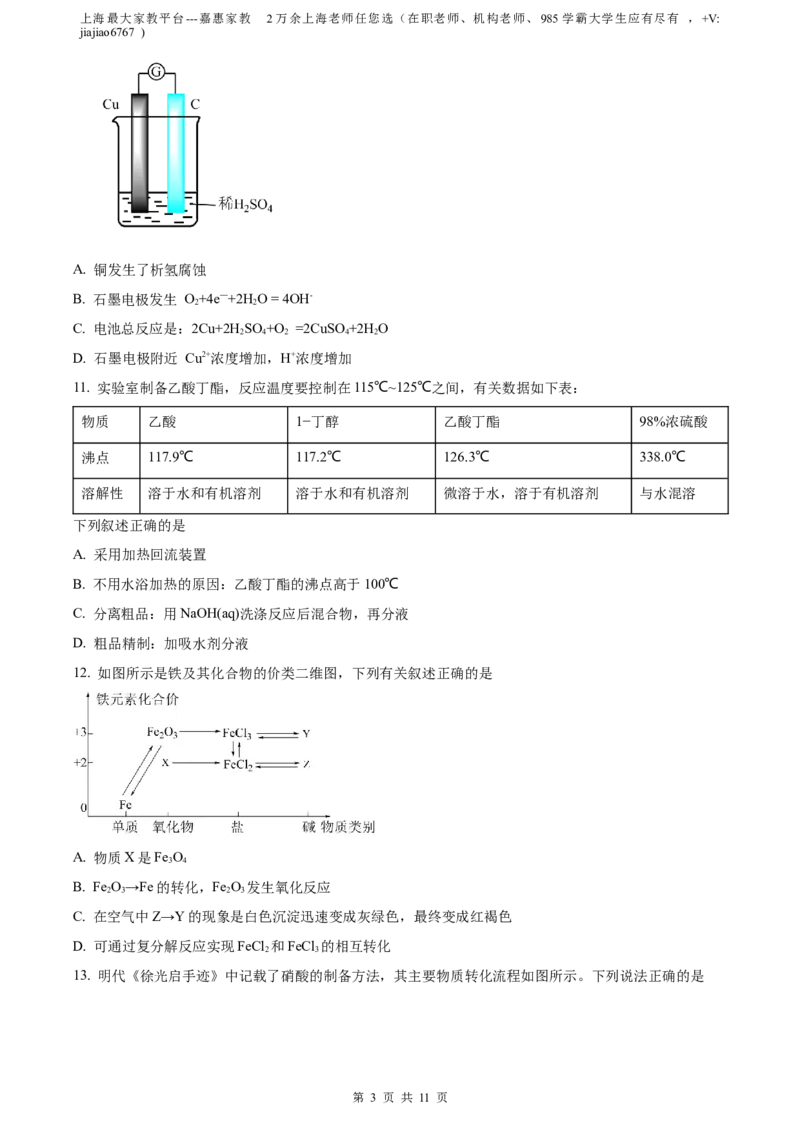
10. 将铜片与石墨连接浸入到稀硫酸溶液中(如图) ,过了较长时间后,发现溶液出现蓝色,下列说法正确
的是
第 2 页 共 11 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
A. 铜发生了析氢腐蚀
B. 石墨电极发生 O+4e—+2H O = 4OH-
2 2
C. 电池总反应是:2Cu+2H SO +O =2CuSO+2H O
2 4 2 4 2
D. 石墨电极附近 Cu2+浓度增加,H+浓度增加
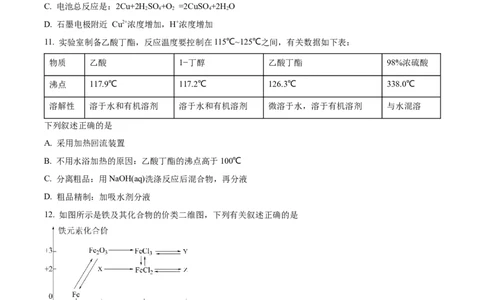
11. 实验室制备乙酸丁酯,反应温度要控制在115℃~125℃之间,有关数据如下表:
物质 乙酸 1−丁醇 乙酸丁酯 98%浓硫酸
沸点 117.9℃ 117.2℃ 126.3℃ 338.0℃
溶解性 溶于水和有机溶剂 溶于水和有机溶剂 微溶于水,溶于有机溶剂 与水混溶
下列叙述正确的是
A. 采用加热回流装置
B. 不用水浴加热的原因:乙酸丁酯的沸点高于100℃
C. 分离粗品:用NaOH(aq)洗涤反应后混合物,再分液
D. 粗品精制:加吸水剂分液
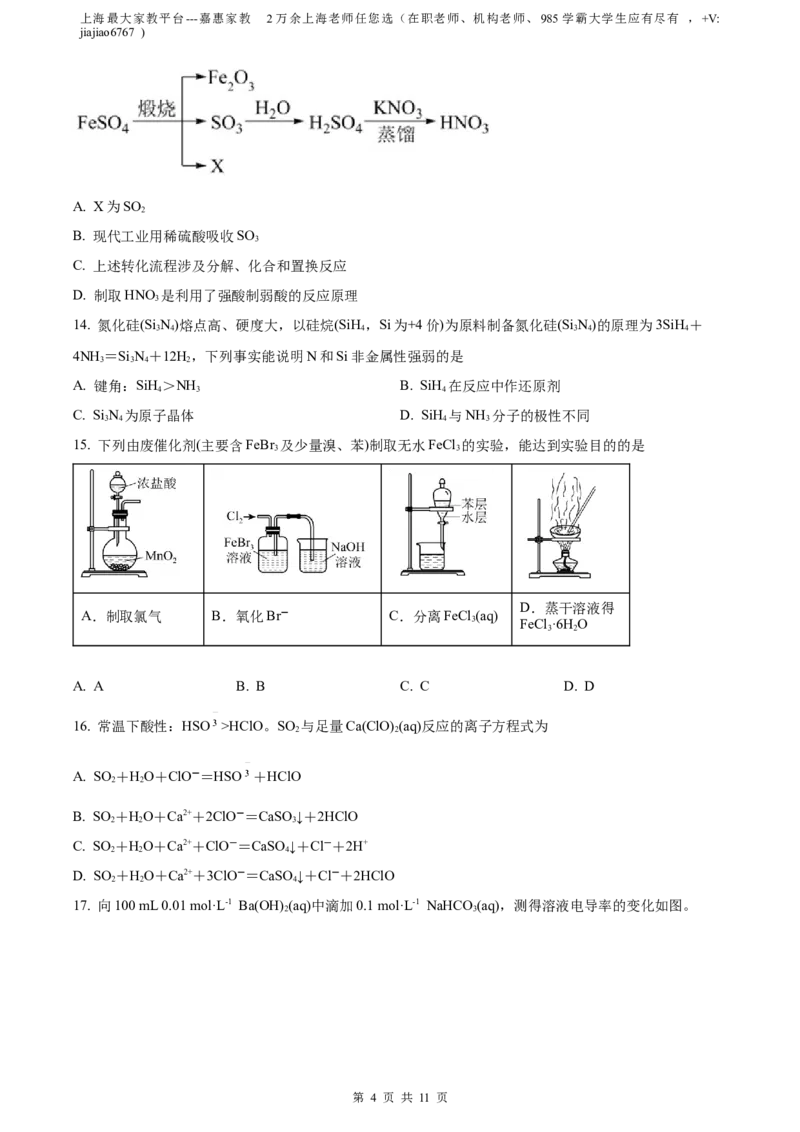
12. 如图所示是铁及其化合物的价类二维图,下列有关叙述正确的是
A. 物质X是Fe O
3 4
B. Fe O→Fe的转化,Fe O 发生氧化反应
2 3 2 3
C. 在空气中Z→Y的现象是白色沉淀迅速变成灰绿色,最终变成红褐色
D. 可通过复分解反应实现FeCl 和FeCl 的相互转化
2 3
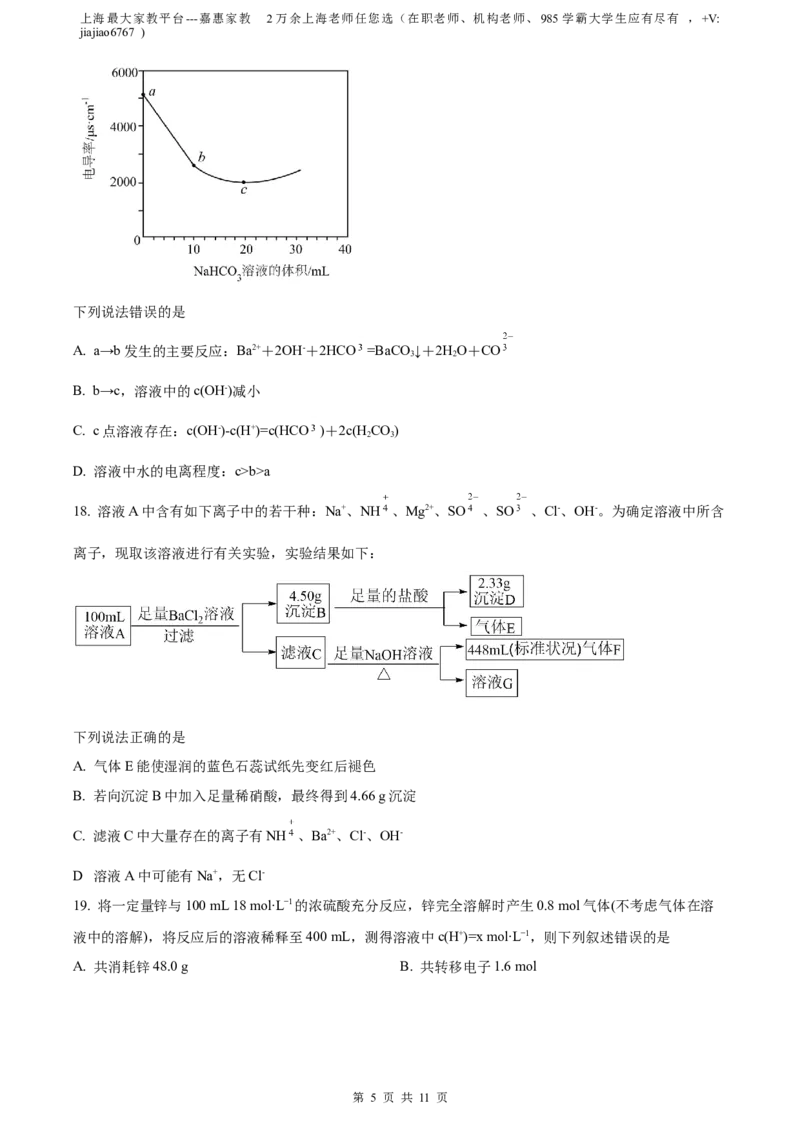
13. 明代《徐光启手迹》中记载了硝酸的制备方法,其主要物质转化流程如图所示。下列说法正确的是
第 3 页 共 11 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
A. X为SO
2
B. 现代工业用稀硫酸吸收SO
3
C. 上述转化流程涉及分解、化合和置换反应
D. 制取HNO 是利用了强酸制弱酸的反应原理
3
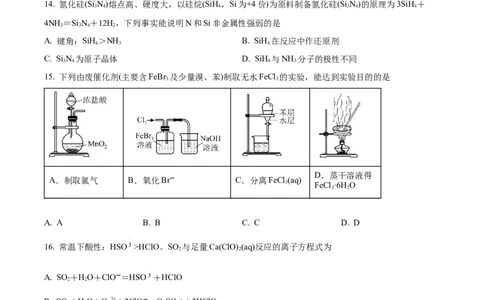
14. 氮化硅(Si N)熔点高、硬度大,以硅烷(SiH,Si为+4价)为原料制备氮化硅(Si N)的原理为3SiH+
3 4 4 3 4 4
4NH =Si N+12H,下列事实能说明N和Si非金属性强弱的是
3 3 4 2
A. 键角:SiH>NH B. SiH 在反应中作还原剂
4 3 4
C. Si N 为原子晶体 D. SiH 与NH 分子的极性不同
3 4 4 3
15. 下列由废催化剂(主要含FeBr 及少量溴、苯)制取无水FeCl 的实验,能达到实验目的的是
3 3
D.蒸干溶液得
A.制取氯气 B.氧化Br- C.分离FeCl (aq)
3 FeCl ·6H O
3 2
A. A B. B C. C D. D
16. 常温下酸性:HSO >HClO。SO 与足量Ca(ClO) (aq)反应的离子方程式为
2 2
A. SO +HO+ClO-=HSO +HClO
2 2
B. SO +HO+Ca2++2ClO-=CaSO↓+2HClO
2 2 3
C. SO +HO+Ca2++ClO-=CaSO↓+Cl-+2H+
2 2 4
D. SO +HO+Ca2++3ClO-=CaSO↓+Cl-+2HClO
2 2 4
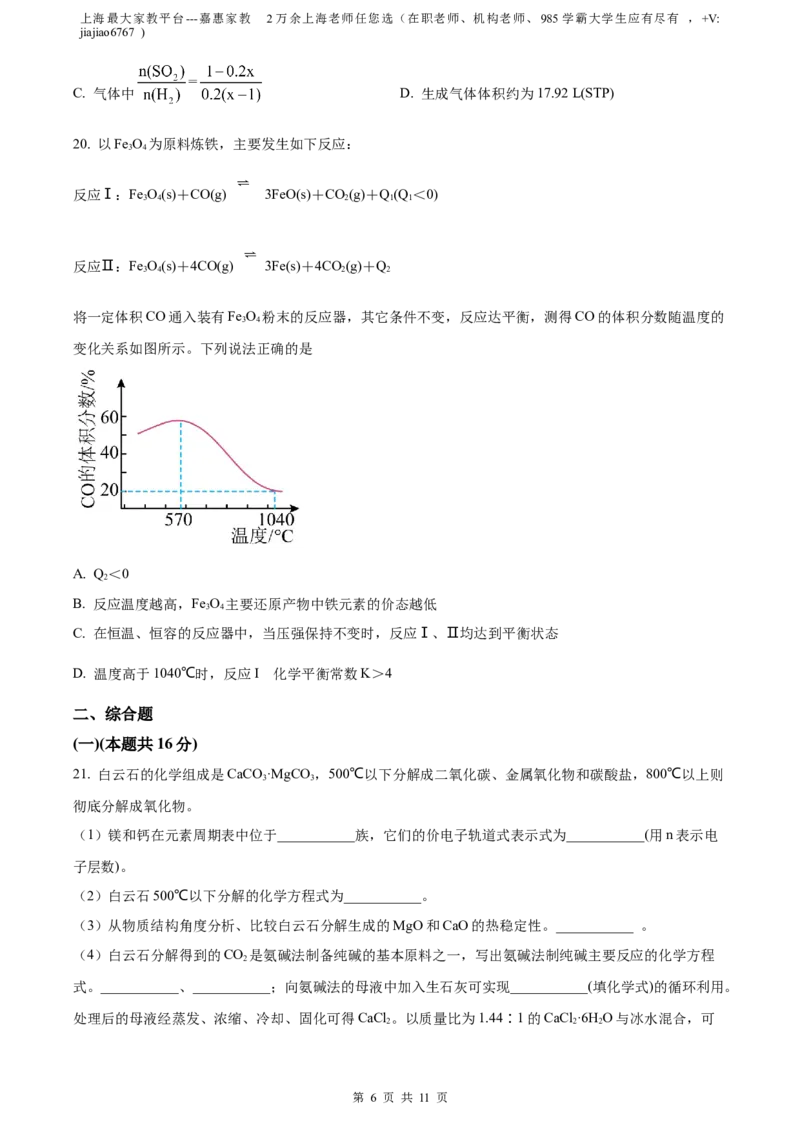
17. 向100 mL 0.01 mol·L-1 Ba(OH) (aq)中滴加0.1 mol·L-1 NaHCO (aq),测得溶液电导率的变化如图。
2 3
第 4 页 共 11 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
下列说法错误的是
A. a→b发生的主要反应:Ba2++2OH-+2HCO =BaCO ↓+2HO+CO
3 2
B. b→c,溶液中的c(OH-)减小
C. c点溶液存在:c(OH-)-c(H+)=c(HCO )+2c(HCO)
2 3
D. 溶液中水的电离程度:c>b>a
18. 溶液A中含有如下离子中的若干种:Na+、NH 、Mg2+、SO 、SO 、Cl-、OH-。为确定溶液中所含
离子,现取该溶液进行有关实验,实验结果如下:
下列说法正确的是
A. 气体E能使湿润的蓝色石蕊试纸先变红后褪色
B. 若向沉淀B中加入足量稀硝酸,最终得到4.66 g沉淀
C. 滤液C中大量存在的离子有NH 、Ba2+、Cl-、OH-
.
D 溶液A中可能有Na+,无Cl-
19. 将一定量锌与100 mL 18 mol∙L−1的浓硫酸充分反应,锌完全溶解时产生0.8 mol气体(不考虑气体在溶
液中的溶解),将反应后的溶液稀释至400 mL,测得溶液中c(H+)=x mol∙L−1,则下列叙述错误的是
A. 共消耗锌48.0 g B. 共转移电子1.6 mol
第 5 页 共 11 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
C. 气体中 D. 生成气体体积约为17.92 L(STP)
20. 以Fe O 为原料炼铁,主要发生如下反应:
3 4
反应Ⅰ:Fe O(s)+CO(g) 3FeO(s)+CO(g)+Q(Q <0)
3 4 2 1 1
反应Ⅱ:Fe O(s)+4CO(g) 3Fe(s)+4CO(g)+Q
3 4 2 2
将一定体积CO通入装有Fe O 粉末的反应器,其它条件不变,反应达平衡,测得CO的体积分数随温度的
3 4
变化关系如图所示。下列说法正确的是
A. Q<0
2
B. 反应温度越高,Fe O 主要还原产物中铁元素的价态越低
3 4
C. 在恒温、恒容的反应器中,当压强保持不变时,反应Ⅰ、Ⅱ均达到平衡状态
的
D. 温度高于1040℃时,反应I 化学平衡常数K>4
二、综合题
(一)(本题共16分)
21. 白云石的化学组成是CaCO ·MgCO ,500℃以下分解成二氧化碳、金属氧化物和碳酸盐,800℃以上则
3 3
彻底分解成氧化物。
(1)镁和钙在元素周期表中位于___________族,它们的价电子轨道式表示式为___________(用n表示电
子层数)。
(2)白云石500℃以下分解的化学方程式为___________。
(3)从物质结构角度分析、比较白云石分解生成的MgO和CaO的热稳定性。___________ 。
(4)白云石分解得到的CO 是氨碱法制备纯碱的基本原料之一,写出氨碱法制纯碱主要反应的化学方程
2
式。___________、___________;向氨碱法的母液中加入生石灰可实现___________(填化学式)的循环利用。
处理后的母液经蒸发、浓缩、冷却、固化可得CaCl 。以质量比为1.44∶1的CaCl ·6H O与冰水混合,可
2 2 2
第 6 页 共 11 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
获得-55℃的低温,配制该制冷剂时不使用无水CaCl 的原因是___________。
2
(二)(本题共13分)
22. Ⅰ.H S与CH 重整,不但可以消除污染,还可以制氢。主要反应如下:①CH(g)+2HS(g) CS(g)
2 4 4 2 2
+4H(g)+Q(Q<0)
2
(1)在恒温恒容条件下,可作为反应①达到平衡状态的判断依据是___________(选填编号)。
A. 混合气体密度不变
B. 容器内压强不变
C. 2v (H S)=v (CS)
正 2 逆 2
D. CH 与H 的物质的量分数之比保持不变
4 2
Ⅱ.在恒压条件下,以n(CH)∶n(H S)=1∶2的组成的混合气体发生反应①,达到平衡状态时,四种组分物
4 2
质的量分数随温度的变化如图所示。
(2)如图中表示CH、CS 变化的曲线分别是___________、___________(选填编号)。
4 2
(3)M点对应温度下,HS的转化率是___________。
2
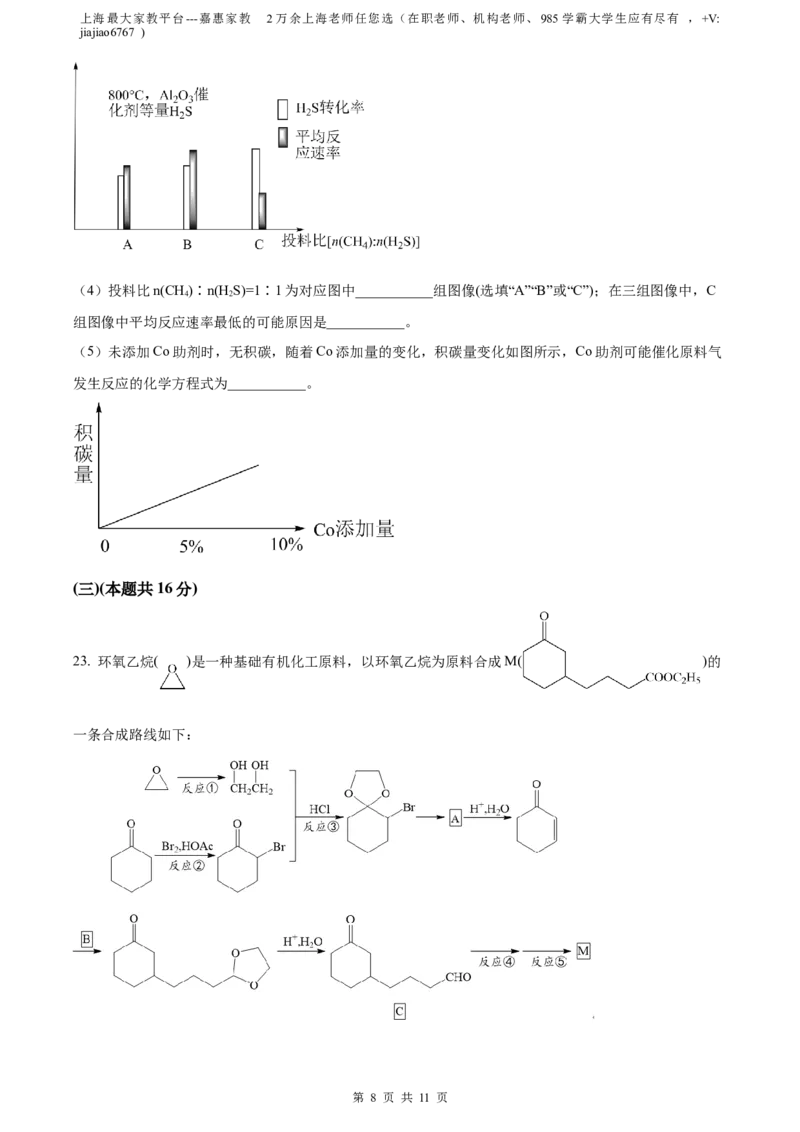
Ⅲ.在研究反应发生的适宜条件时发现:过多的CH 会导致Al O 催化剂失活;Co助剂有稳定催化剂的作用。
4 2 3
如图表示800℃,Al O 催化剂条件下投入等量HS,投料比[n(CH )∶n(H S)]分别为1∶1、1∶3、12∶1,
2 3 2 4 2
达平衡时HS转化率、平均反应速率。
2
第 7 页 共 11 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
(4)投料比n(CH)∶n(H S)=1∶1为对应图中___________组图像(选填“A”“B”或“C”);在三组图像中,C
4 2
组图像中平均反应速率最低的可能原因是___________。
(5)未添加Co助剂时,无积碳,随着Co添加量的变化,积碳量变化如图所示,Co助剂可能催化原料气
发生反应的化学方程式为___________。
(三)(本题共16分)
23. 环氧乙烷( )是一种基础有机化工原料,以环氧乙烷为原料合成M( )的
一条合成路线如下:
第 8 页 共 11 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
(1)在一定条件下,环氧乙烷可与H、HO、HBr等小分子发生类似加成的开环反应,如反应①。写出反
2 2
应①的化学方程式___________。
(2)反应②的反应类型是___________。设计反应③的目的是___________。
(3)A的结构简式为___________,C中含有的官能团有羰基和___________,写出一种满足下列条件的C
的结构简式___________。
①含六元碳环;②含三种不同化学环境的H原子;③能发生银镜反应
(4)反应⑤的反应条件是___________。
(5)以 和HOCH CHOH为主要原料合成B( )(无机试剂任选),将以下合成路
2 2
线补充完整。已知:RBr RMgBr
____________
(四)(本题共15分)
24. Ⅰ.氯及其化合物是卤素中最早被认识和制备的。KClO 热分解是实验室制取O 的方法之一,KClO
3 2 3
在不同条件下热分解结果如下:
实验 反应体系 第一放热温度/℃ 第二放热温度/℃
A KClO 400 480
3
B KClO+Fe O 360 390
3 2 3
C KClO+MnO 350
3 2
已知:①K(s)+ Cl(g)=KCl(s)+437kJ
2
②K(s)+ Cl(g)+ O=KClO (s)+398kJ
2 2 3
③K(s)+ Cl(g)+2O=KClO (s)+433kJ
2 2 4
(1)验A、B在第一放热温度时分解的热化学方程式为4KClO(s) 3KClO(s)+KCl(s)+Q,
3 4
Q=___________kJ。
第 9 页 共 11 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
的
(2)实验C制得 O 因混有杂质而有轻微的刺激性气味,杂质气体可能是___________,检验方法是
2
___________。
Ⅱ.甲苯(C HCH)与干燥的Cl 在光照下反应生成氯化苄(C HCHCl)。用下列方法分析粗产品的纯度:称
6 5 3 2 6 5 2
取0.255 g样品,与足量 4 mol∙L−1 NaOH(aq)混合加热回流1 h,冷却至室温,加入足量硝酸酸化后,用
25.00 mL 0.1000 mol∙L−1AgNO(aq)处理,再以NH Fe(SO ) 为指示剂,用0.1000 mol∙L−1 NH SCN(aq)滴定剩
3 4 4 2 4
余的AgNO(aq),发生反应:Ag++SCN-=AgSCN↓,消耗NH SCN(aq) 6.75 mL。
3 4
(3)滴定终点溶液为___________色,样品中氯化苄的质量分数为___________(保留两位有效数字)。
(4)通常上述测定结果高于样品中氯化苄的实际含量,任写两个可能的原因___________。
(5)上述方法不适用于氯苯(C HCl)的纯度分析,原因是___________。
6 5
第 10 页 共 11 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
第 11 页 共 11 页