文档内容
上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
上海市行知中学 2022 学年第二学期期中考试
高一年级化学学科试卷
(满分 100分,完卷时间 60分钟)
说明:
1.本试卷共六大题,每道大题中均包含三道选择题,其中前两道为单选题(各 2分),第三道可
能有 1个或 2 个正确选项。
2.作答必须涂或写在答题纸上,在试卷上作答一律不得分。
3.可能用到的相对原子质量 H-1 C-12 N-14 O-16 Na-23 Mg-24 Al-27 S-32 K-39
Fe-56 Cu-64 Ba-137
1. 从太空遥望,地球是一颗蓝色星球,浩瀚的海洋覆盖了70%以上的地球表面。海洋可谓地球的“聚宝
盆”,蕴藏着极为丰富的化学资源。氯、溴、碘等均可通过开发海洋资源获得。
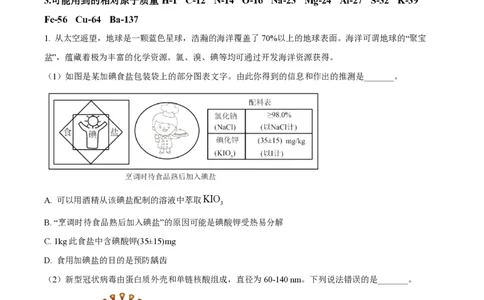
(1)如图是某加碘食盐包装袋上的部分图表文字。由此你得到的信息和作出的推测是_______。
A. 可以用酒精从该碘盐配制的溶液中萃取KIO
3
B. “烹调时待食品熟后加入碘盐”的原因可能是碘酸钾受热易分解
C. 1kg此食盐中含碘酸钾(35±15)mg
D. 食用加碘盐的目的是预防龋齿
(2)新型冠状病毒由蛋白质外壳和单链核酸组成,直径为60-140 nm。下列说法错误的是_______。
A. 新型冠状病毒扩散到空气中可能形成胶体
B. 连花清瘟胶囊成分中的石膏CaSO 2H O属于混合物
4 2
C. 止咳祛痰药:盐酸氨溴索中含有两种卤族元素
第 1 页 共 9 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
D. “84”消毒液中含强氧化性物质,可用于新型冠状病毒的消杀
(3)粗盐中存在Ca2、Mg2、SO2等可溶性杂质离子,要除去这些离子加入沉淀剂的顺序正确的是
4
_______。
Na CO BaCl
①过量的 2 3溶液 ②过量的 2溶液 ③过量的NaOH溶液
A. ①②③ B. ②①③ C. ③②① D. ①③②
(4)我国著名实业家吴蕴初建设的天原化工厂为我国第一个氯碱厂,其生产原理即为电解饱和食盐水,
阴极产物为_______。
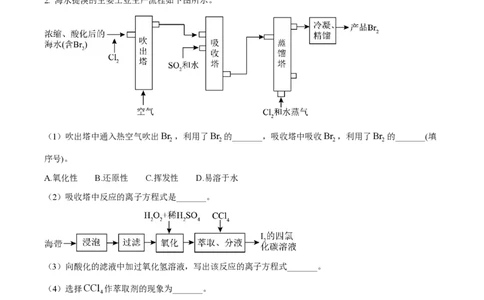
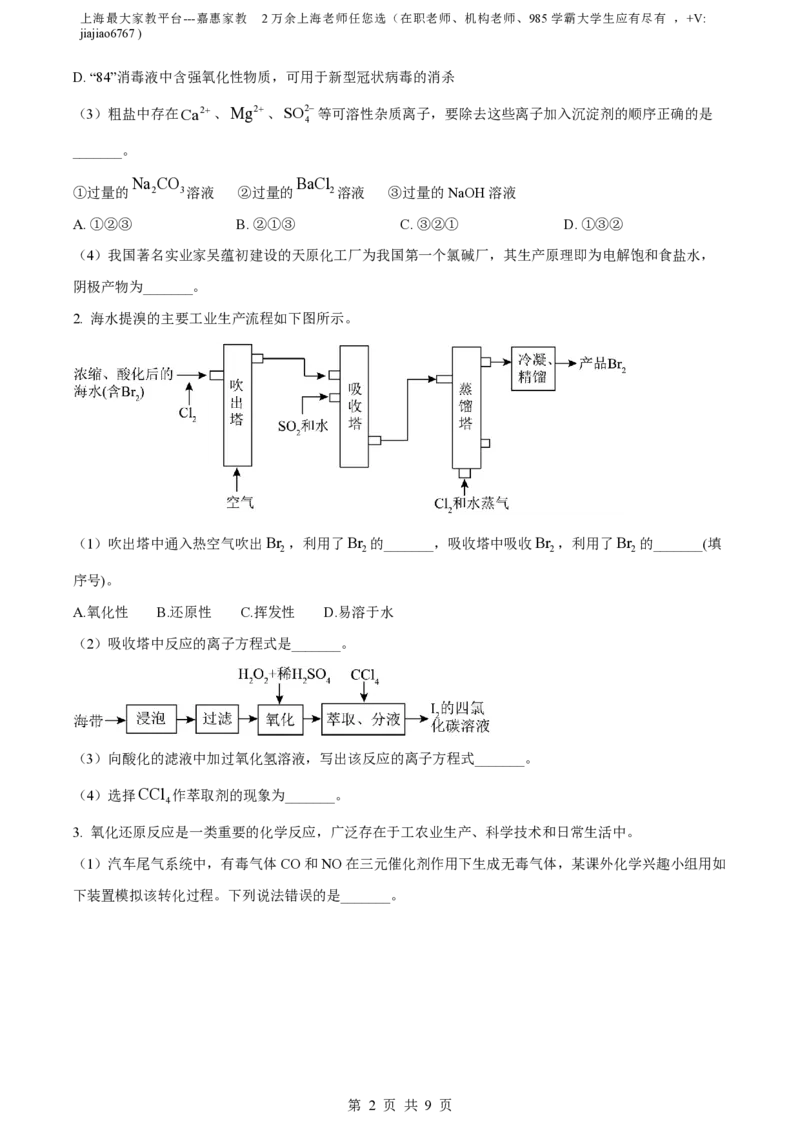
2. 海水提溴的主要工业生产流程如下图所示。
(1)吹出塔中通入热空气吹出Br ,利用了Br 的_______,吸收塔中吸收Br ,利用了Br 的_______(填
2 2 2 2
序号)。
A.氧化性 B.还原性 C.挥发性 D.易溶于水
(2)吸收塔中反应的离子方程式是_______。
(3)向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式_______。
(4)选择CCl 作萃取剂的现象为_______。
4
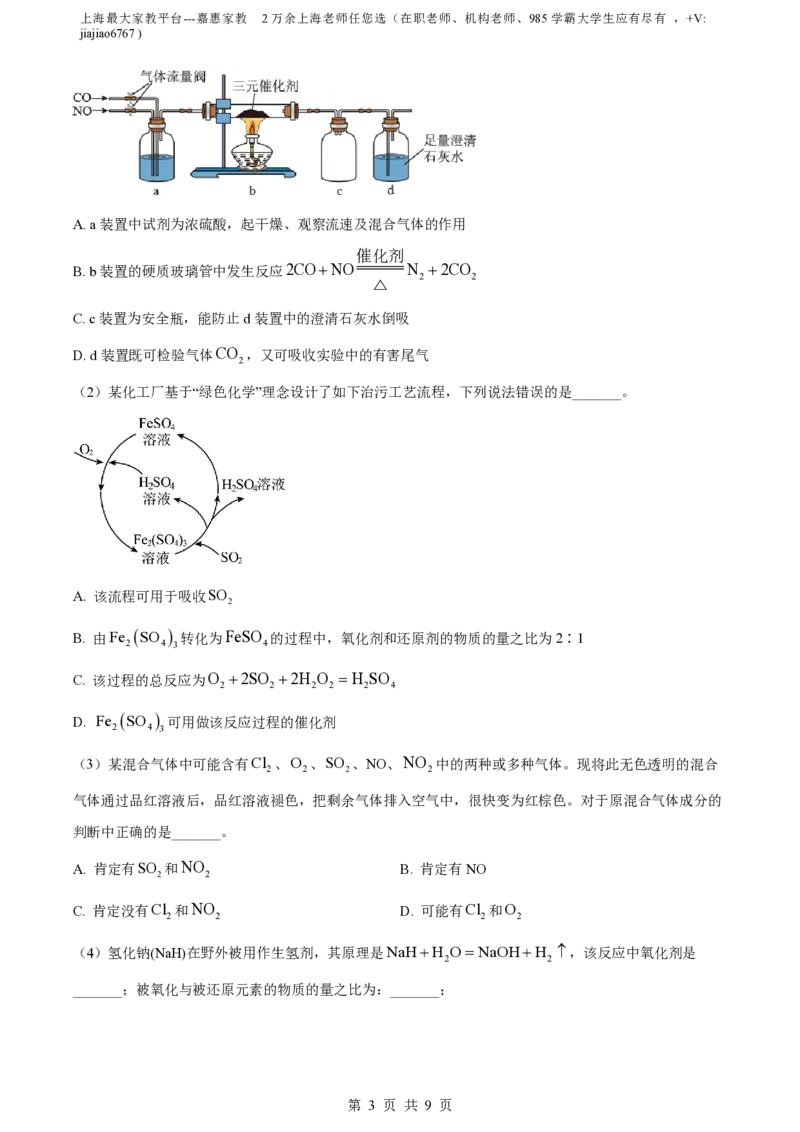
3. 氧化还原反应是一类重要的化学反应,广泛存在于工农业生产、科学技术和日常生活中。
(1)汽车尾气系统中,有毒气体CO和NO在三元催化剂作用下生成无毒气体,某课外化学兴趣小组用如
下装置模拟该转化过程。下列说法错误的是_______。
第 2 页 共 9 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
A. a装置中试剂为浓硫酸,起干燥、观察流速及混合气体的作用
催化剂
B. b装置的硬质玻璃管中发生反应2CONO N 2CO
2 2
△
C. c装置为安全瓶,能防止d装置中的澄清石灰水倒吸
D. d装置既可检验气体CO ,又可吸收实验中的有害尾气
2
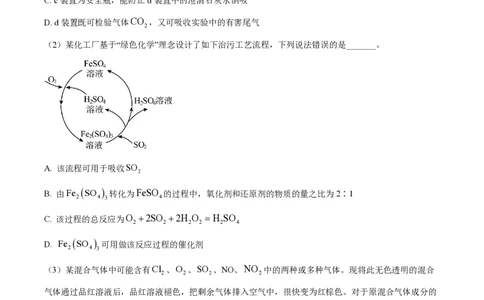
(2)某化工厂基于“绿色化学”理念设计了如下治污工艺流程,下列说法错误的是_______。
A. 该流程可用于吸收SO
2
B. 由Fe SO 转化为FeSO 的过程中,氧化剂和还原剂的物质的量之比为2∶1
2 4 3 4
C. 该过程的总反应为O 2SO 2H O H SO
2 2 2 2 2 4
D. Fe SO 可用做该反应过程的催化剂
2 4 3
(3)某混合气体中可能含有Cl 、O 、SO 、NO、NO 中的两种或多种气体。现将此无色透明的混合
2 2 2 2
气体通过品红溶液后,品红溶液褪色,把剩余气体排入空气中,很快变为红棕色。对于原混合气体成分的
判断中正确的是_______。
A. 肯定有SO 和NO B. 肯定有NO
2 2
C. 肯定没有Cl 和NO D. 可能有Cl 和O
2 2 2 2
(4)氢化钠(NaH)在野外被用作生氢剂,其原理是NaHH O NaOHH ,该反应中氧化剂是
2 2
_______;被氧化与被还原元素的物质的量之比为:_______;
第 3 页 共 9 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
(5)汽车剧烈碰撞时,安全气囊中发生反应:10NaN 2KNO K O5Na O16N 。该反应中氧
3 3 2 2 2
化产物与还原产物的质量比为_______;若氧化产物比还原产物多19.6 g,则反应生成的N 在标准状况下
2
的体积为_______L。
(6)高铁酸钠(Na FeO ),易溶于水,是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。工业上
2 4
制备高铁酸钠有多种方法。在次氯酸钠溶液中加入氢氧化钠和硫酸铁可制备高铁酸钠,此法被称为次氯酸
盐氧化法。写出制备高铁酸钠的离子方程式_______。
4. 硫是重要的非金属元素,也是人类较早认识的化学元素之一。人们对硫元素的利用,其本质就是通过各
种化学反应,实现含硫元素的物质之间的转化。
(1)硫可以形成分子式为S 、S 、S 、S 的单质,其中S 的分子球棍模型如图所示。下列有关说法正
2 4 6 8 8
确的是_______。
A. 1 mol S 单质中含有的S—S键个数为8N
8 A
B. S 、S 、S 、S 互为同位素
2 4 6 8
C. 硫的单质在足量的空气中完全燃烧可生成SO
3
D. S 的摩尔质量为32 g/mol
2
(2)将SO 气体通入BaCl 溶液中,没有看到明显现象,再遇入一种气体(或加入一种物质)后,可产生一
2 2
种沉淀,该气体(或物质)不可能是_______。
A. Cl B. NH C. CO D. H S
2 3 2 2
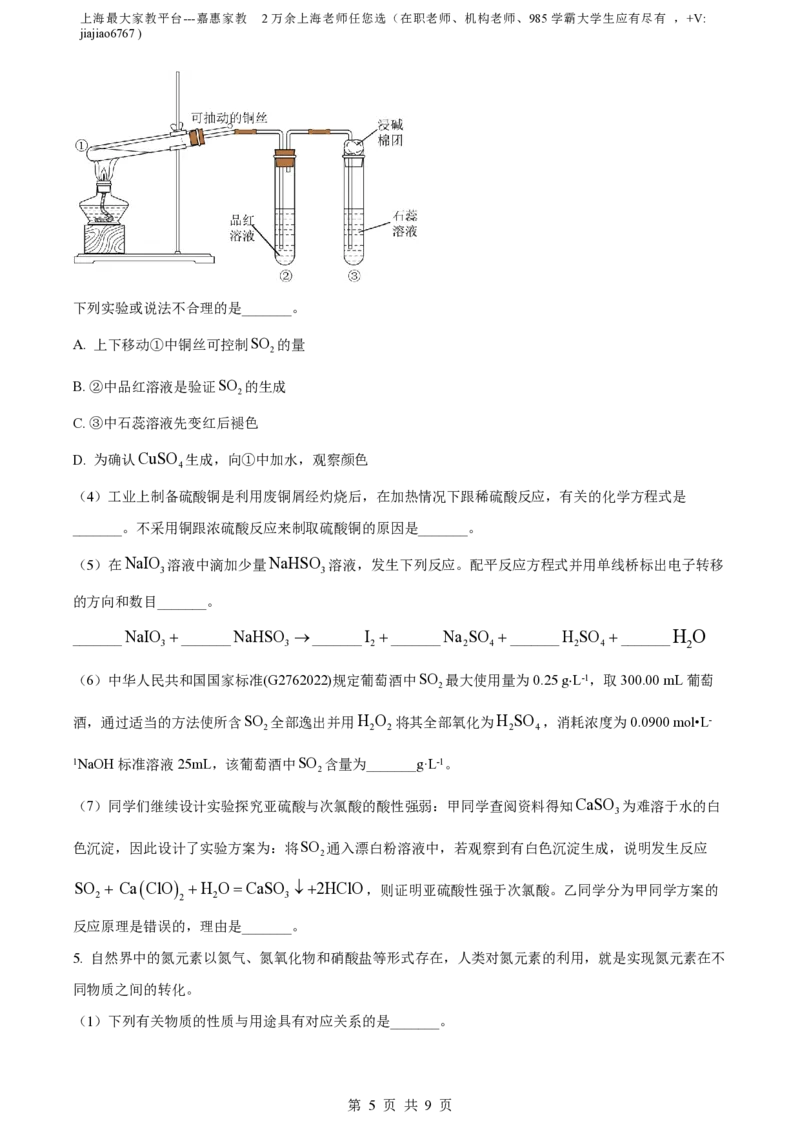
(3)用如图所示实验装置(部分夹持仪器已略去)探究铜丝与过量浓硫酸的反应。
第 4 页 共 9 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
下列实验或说法不合理的是_______。
A. 上下移动①中铜丝可控制SO 的量
2
B. ②中品红溶液是验证SO 的生成
2
C. ③中石蕊溶液先变红后褪色
D. 为确认CuSO 生成,向①中加水,观察颜色
4
(4)工业上制备硫酸铜是利用废铜屑经灼烧后,在加热情况下跟稀硫酸反应,有关的化学方程式是
_______。不采用铜跟浓硫酸反应来制取硫酸铜的原因是_______。
(5)在NaIO 溶液中滴加少量NaHSO 溶液,发生下列反应。配平反应方程式并用单线桥标出电子转移
3 3
的方向和数目_______。
_______NaIO _______NaHSO _______I _______Na SO _______H SO _______ H O
3 3 2 2 4 2 4 2
(6)中华人民共和国国家标准(G2762022)规定葡萄酒中SO 最大使用量为0.25 g⋅L-1,取300.00 mL葡萄
2
酒,通过适当的方法使所含SO 全部逸出并用H O 将其全部氧化为H SO ,消耗浓度为0.0900 mol•L-
2 2 2 2 4
1NaOH标准溶液25mL,该葡萄酒中SO 含量为_______g·L-1。
2
(7)同学们继续设计实验探究亚硫酸与次氯酸的酸性强弱:甲同学查阅资料得知CaSO 为难溶于水的白
3
色沉淀,因此设计了实验方案为:将SO 通入漂白粉溶液中,若观察到有白色沉淀生成,说明发生反应
2
SO CaClO H OCaSO 2HClO,则证明亚硫酸性强于次氯酸。乙同学分为甲同学方案的
2 2 2 3
反应原理是错误的,理由是_______。
5. 自然界中的氮元素以氮气、氮氧化物和硝酸盐等形式存在,人类对氮元素的利用,就是实现氮元素在不
同物质之间的转化。
(1)下列有关物质的性质与用途具有对应关系的是_______。
第 5 页 共 9 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
A. NH 易溶于水,可用作制冷剂 B. HNO 具有强氧化性,可用于制NH NO
3 3 4 3
C. NH HCO 受热易分解,可用作化肥 D. N 性质稳定,可用于食品保护
4 3 2
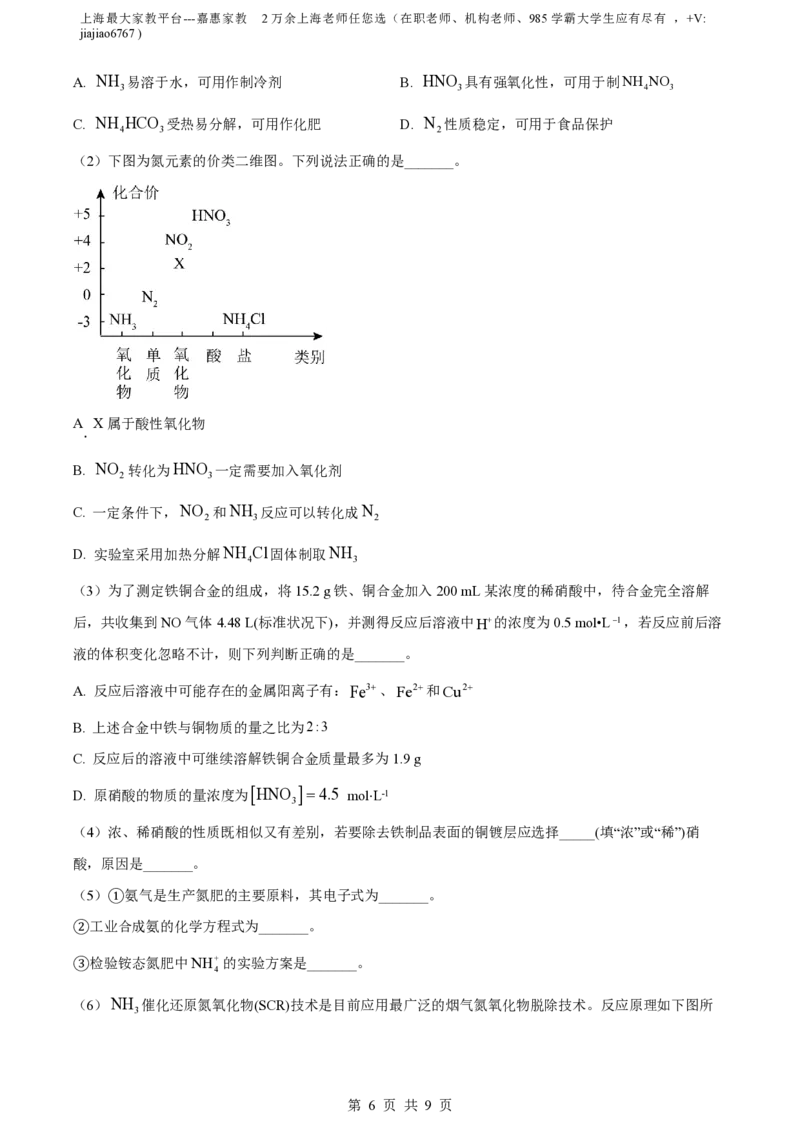
(2)下图为氮元素的价类二维图。下列说法正确的是_______。
A X属于酸性氧化物
.
B. NO 转化为HNO 一定需要加入氧化剂
2 3
C. 一定条件下,NO 和NH 反应可以转化成N
2 3 2
D. 实验室采用加热分解NH Cl固体制取NH
4 3
(3)为了测定铁铜合金的组成,将15.2 g铁、铜合金加入200 mL某浓度的稀硝酸中,待合金完全溶解
后,共收集到NO气体4.48 L(标准状况下),并测得反应后溶液中H的浓度为0.5 mol•L1,若反应前后溶
液的体积变化忽略不计,则下列判断正确的是_______。
A. 反应后溶液中可能存在的金属阳离子有:Fe3、Fe2和Cu2
B. 上述合金中铁与铜物质的量之比为2:3
C. 反应后的溶液中可继续溶解铁铜合金质量最多为1.9 g
D. 原硝酸的物质的量浓度为
HNO 4.5
mol⋅L-1
3
(4)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应选择_____(填“浓”或“稀”)硝
酸,原因是_______。
(5)①氨气是生产氮肥的主要原料,其电子式为_______。
②工业合成氨的化学方程式为_______。
③检验铵态氮肥中NH的实验方案是_______。
4
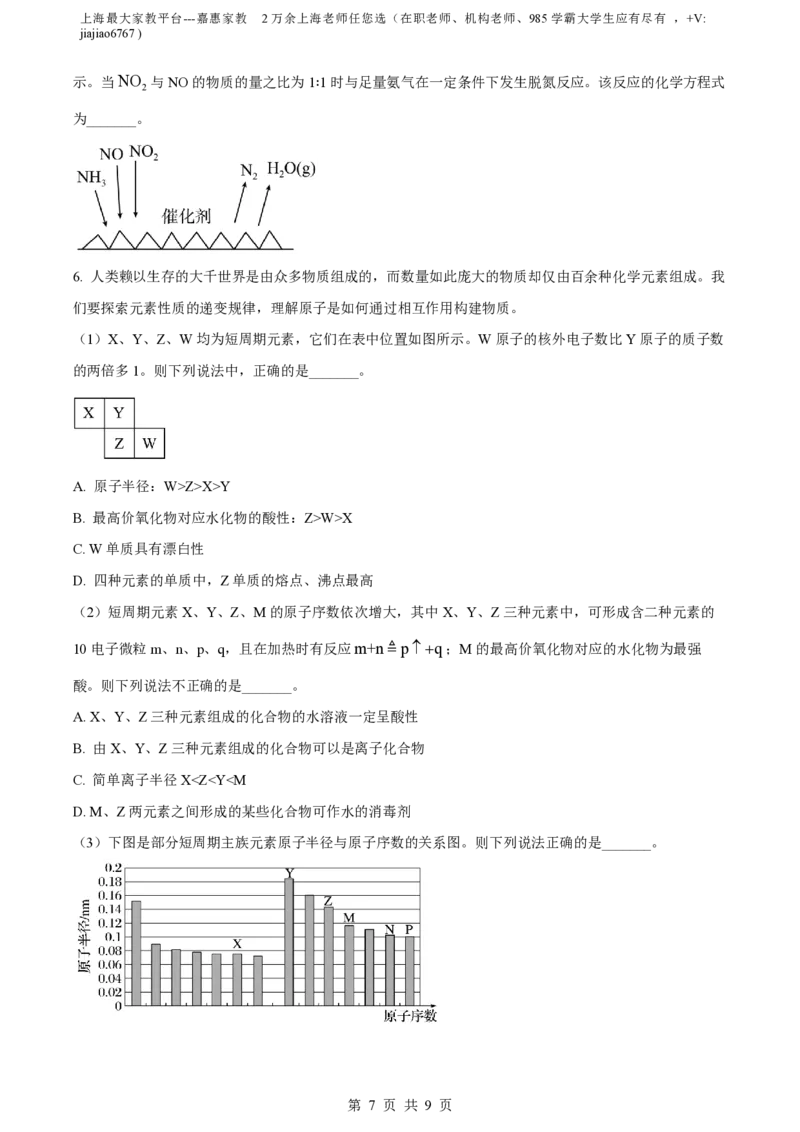
(6)NH 催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如下图所
3
第 6 页 共 9 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
示。当NO 与NO的物质的量之比为1∶1时与足量氨气在一定条件下发生脱氮反应。该反应的化学方程式
2
为_______。
6. 人类赖以生存的大千世界是由众多物质组成的,而数量如此庞大的物质却仅由百余种化学元素组成。我
们要探索元素性质的递变规律,理解原子是如何通过相互作用构建物质。
(1)X、Y、Z、W均为短周期元素,它们在表中位置如图所示。W原子的核外电子数比Y原子的质子数
的两倍多1。则下列说法中,正确的是_______。
A. 原子半径:W>Z>X>Y
B. 最高价氧化物对应水化物的酸性:Z>W>X
C. W单质具有漂白性
D. 四种元素的单质中,Z单质的熔点、沸点最高
(2)短周期元素X、Y、Z、M的原子序数依次增大,其中X、Y、Z三种元素中,可形成含二种元素的
10电子微粒m、n、p、q,且在加热时有反应m+n pq;M的最高价氧化物对应的水化物为最强
酸。则下列说法不正确的是_______。
A. X、Y、Z三种元素组成的化合物的水溶液一定呈酸性
B. 由X、Y、Z三种元素组成的化合物可以是离子化合物
C. 简单离子半径X⑥
d.最高价氧化物对应水化物的碱性:⑤>⑥
(4)比较②与③元素之间,非金属性较强的是,请举一例化学事实进行说明:_______。
(5)⑤的最高价氧化物所对应水化物的溶液与⑨的单质反应的离子方程式是_______。
8. 由金属元素或以金属元素为主制成的材料可应用于各个领域,小到日常民用,大到国防军工,都能看到
金属材料的身影。可以说,金属及其材料在人类文明进步和社会发展中起着至关重要的作用。
(1)下列有关钠的物理性质的叙述中正确的是_______。
①灰黑色金属;②质软,可以用小刀切割;③熔点低于100℃④密度比水大;⑤热和电的良导体
A. ②④ B. ②③⑤ C. ③⑤ D. ①②③④⑤
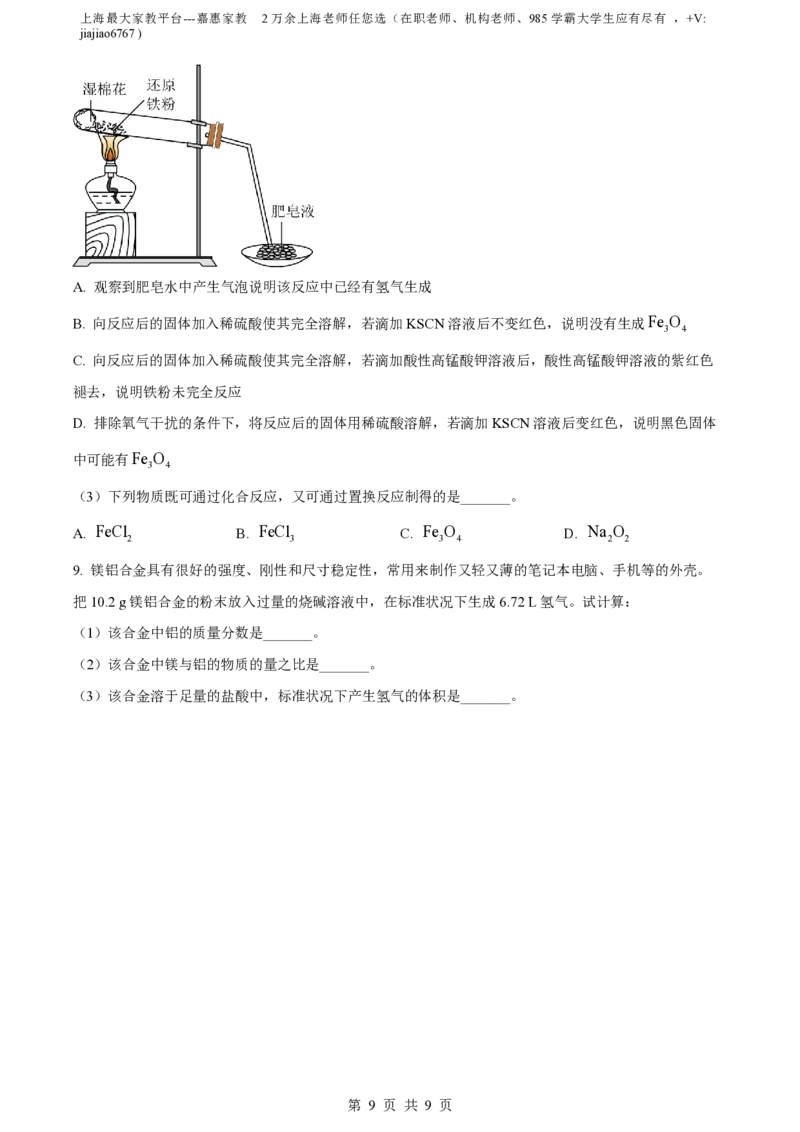
(2)某同学利用下图所示的实验装置进行铁跟水蒸气反应的实验,并研究反应后硬质试管中黑色固体物
质的成分。下列说法正确的是_______。
第 8 页 共 9 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
A. 观察到肥皂水中产生气泡说明该反应中已经有氢气生成
B. 向反应后的固体加入稀硫酸使其完全溶解,若滴加KSCN溶液后不变红色,说明没有生成Fe O
3 4
C. 向反应后的固体加入稀硫酸使其完全溶解,若滴加酸性高锰酸钾溶液后,酸性高锰酸钾溶液的紫红色
褪去,说明铁粉未完全反应
D. 排除氧气干扰的条件下,将反应后的固体用稀硫酸溶解,若滴加KSCN溶液后变红色,说明黑色固体
中可能有Fe O
3 4
(3)下列物质既可通过化合反应,又可通过置换反应制得的是_______。
A. FeCl B. FeCl C. Fe O D. Na O
2 3 3 4 2 2
9. 镁铝合金具有很好的强度、刚性和尺寸稳定性,常用来制作又轻又薄的笔记本电脑、手机等的外壳。
把10.2 g镁铝合金的粉末放入过量的烧碱溶液中,在标准状况下生成6.72 L氢气。试计算:
(1)该合金中铝的质量分数是_______。
(2)该合金中镁与铝的物质的量之比是_______。
(3)该合金溶于足量的盐酸中,标准状况下产生氢气的体积是_______。
第 9 页 共 9 页