文档内容
上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
2022 学年第二学期高三化学教学质量调研试卷
(时间60分钟,满分100分)
考生注意:
1.本考试设试卷和答题纸两部分,所有答题必须涂或写在答题纸上;做在试卷上一律不得分。
2.答题前,考生务必在答题纸上用钢笔或圆珠笔在答题纸正面清楚地填写姓名、准考证号。
3.答题纸与试卷在试题编号上是一一对应的,答题时应特别注意,不能错位。
相对原子质量:H-1 O-16 S-32 Na-23 Cu-64 Br-80 I-127
一、选择题(共40分,每小题2分,每小题只有一个正确选项)
1. 生活中处处有化学,下列叙述正确的是
A. HB铅笔芯的成分为二氧化铅 B. 碳酸氢钠可做食品膨松剂
C. 青铜和黄铜是不同结构的单质铜 D. 焰火中红色来源于钠盐灼烧
2. 下列说法不正确的是
A. 电解熔融氯化镁可制取金属镁 B. 电解饱和食盐水可制取氯气
C. 纯铁比生铁易生锈 D. 硫黄或硫铁矿可用于接触法制硫酸
3. 下列有关化学用语表示正确的是
A. 氟原子的结构示意图: B. 质子数为53中子数为78的碘原子:
C. 硫化钠的电子式: D. 明矾的化学式:Al (SO )
2 4 3
4. 下列过程中共价键被破坏的是
A. 氯气溶于水 B. 碘升华 C. 乙醇溶于水 D. NaOH溶于水
5. 苯是不饱和烃,不能使溴的四氯化碳溶液褪色,是因为
A. 苯能溶于四氯化碳 B. 苯是非极性分子
C. 苯能发生取代反应 D. 苯中不存在烯烃典型的碳碳双键
6. 下列说法不正确的是
A. 乙醇和丙三醇互为同系物
B. 和 互为同位素
C. 和 互为同素异形体
第 1 页 共 9 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
D. 丙酮( )和环氧丙烷( )互为同分异构体
7. 100%硫酸吸收SO 可生成焦硫酸(分子式为HSO 或HSO ·SO )。下列说法不正确的是
3 2 2 7 2 4 3
.
A 焦硫酸具有强吸水性
B. 焦硫酸具有强氧化性
C. 焦硫酸可与碱反应生成盐和水
D. 100%硫酸吸收SO 生成焦硫酸的变化是物理变化
3
8. 侯氏制碱法中没有用到的原料是
A. CaO B. NaCl C. NH D. CO
3 2
9. 关于化合物2−苯基丙烯( ),下列说法正确的是
A. 不能使稀高锰酸钾溶液褪色
B. 可以发生加成聚合反应
C. 分子中所有原子共平面
D. 易溶于水及甲苯
10. 下列反应不属于离子反应的是
A. 乙醇与乙酸 B. 氨水与醋酸
C. 碳酸钙与盐酸 D. 氯化铁溶液与硫氰化钾溶液
11. 下列有关性质的比较,不能用元素周期律解释的是( )
A. 酸性:HSO >HClO B. 金属性:Mg>Al
2 4
C. 碱性:NaOH>LiOH D. 稳定性:CH>SiH
4 4
12. 常温下,下列溶液中水的电离程度最大的是( )
A. pH=0的硫酸
B. 0.01mol/L NaOH溶液
C. pH=10的纯碱溶液
D. pH=5的氯化铵溶液
13. 除去下列物质中所含的少量杂质(括号内为杂质),所用除杂试剂合理的是
A. FeCl 溶液(CuCl )铁粉 B. C H(C H):H/催化剂
3 2 2 6 2 4 2
C. CO(SO ):酸性高锰酸钾溶液 D. 乙醛(乙酸):饱和碳酸钠溶液
2 2
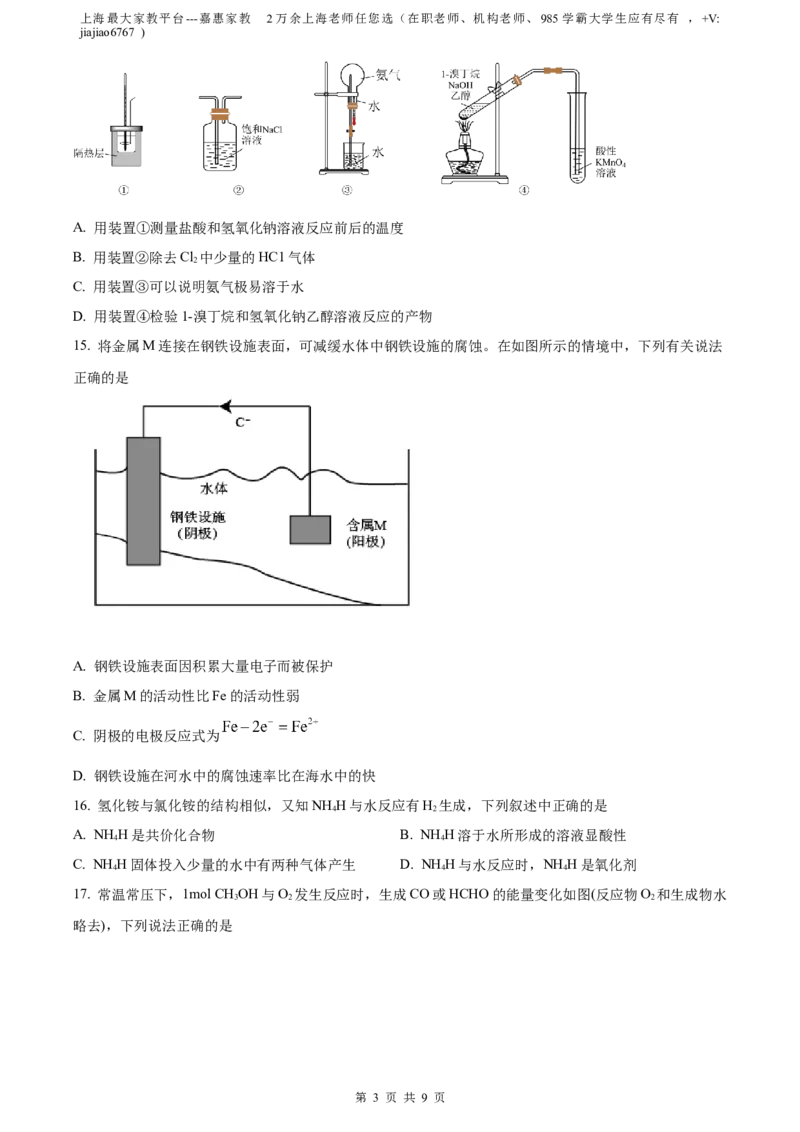
14. 下列实验方案中不能达到实验目的的是
第 2 页 共 9 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
A. 用装置①测量盐酸和氢氧化钠溶液反应前后的温度
B. 用装置②除去Cl 中少量的HC1气体
2
C. 用装置③可以说明氨气极易溶于水
D. 用装置④检验1-溴丁烷和氢氧化钠乙醇溶液反应的产物
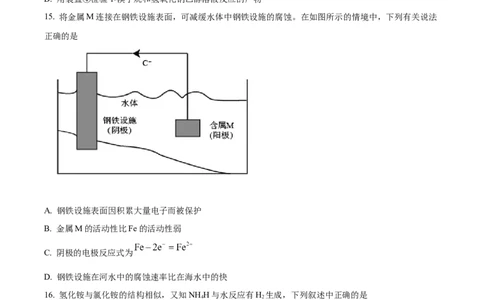
15. 将金属M连接在钢铁设施表面,可减缓水体中钢铁设施的腐蚀。在如图所示的情境中,下列有关说法
正确的是
A. 钢铁设施表面因积累大量电子而被保护
B. 金属M的活动性比Fe的活动性弱
C. 阴极的电极反应式为
D. 钢铁设施在河水中的腐蚀速率比在海水中的快
16. 氢化铵与氯化铵的结构相似,又知NH H与水反应有H 生成,下列叙述中正确的是
4 2
A. NH H是共价化合物 B. NH H溶于水所形成的溶液显酸性
4 4
C. NH H固体投入少量的水中有两种气体产生 D. NH H与水反应时,NH H是氧化剂
4 4 4
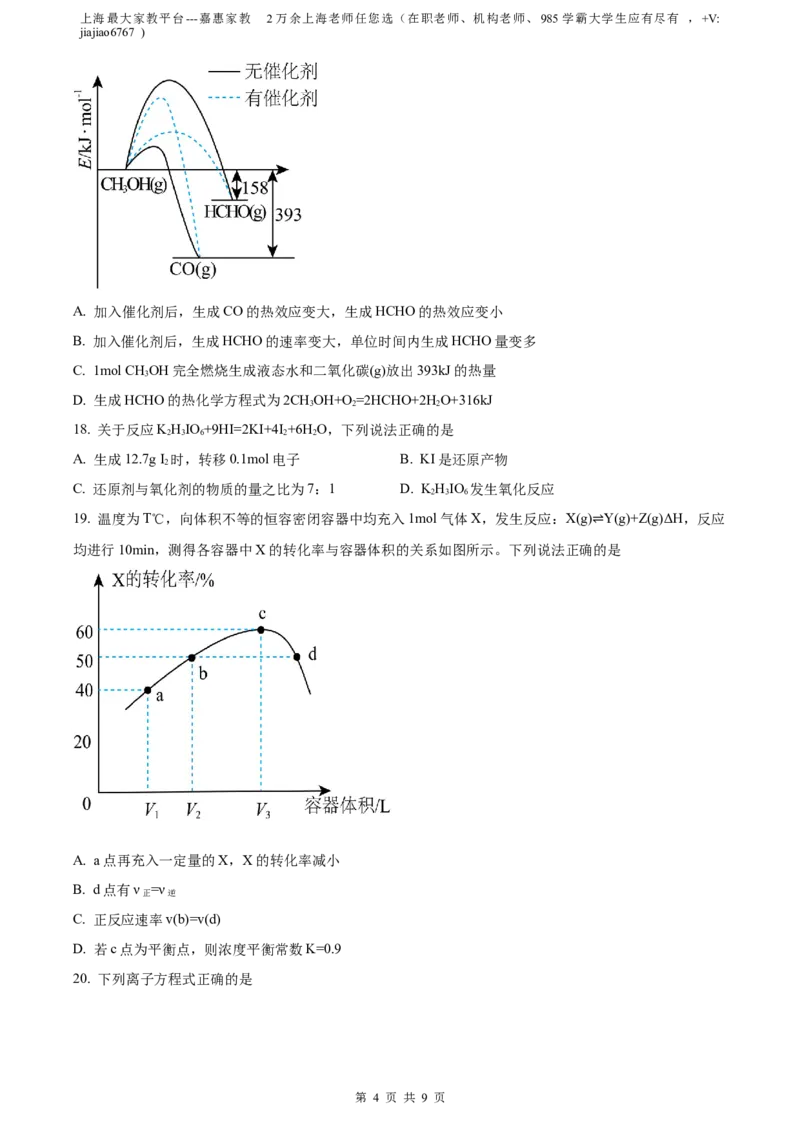
17. 常温常压下,1mol CHOH与O 发生反应时,生成CO或HCHO的能量变化如图(反应物O 和生成物水
3 2 2
略去),下列说法正确的是
第 3 页 共 9 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
A. 加入催化剂后,生成CO的热效应变大,生成HCHO的热效应变小
B. 加入催化剂后,生成HCHO的速率变大,单位时间内生成HCHO量变多
C. 1mol CHOH完全燃烧生成液态水和二氧化碳(g)放出393kJ的热量
3
D. 生成HCHO的热化学方程式为2CHOH+O =2HCHO+2H O+316kJ
3 2 2
18. 关于反应KHIO +9HI=2KI+4I +6H O,下列说法正确的是
2 3 6 2 2
A. 生成12.7g I 时,转移0.1mol电子 B. KI是还原产物
2
C. 还原剂与氧化剂的物质的量之比为7:1 D. KHIO 发生氧化反应
2 3 6
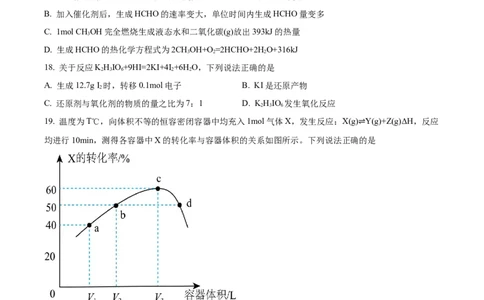
19. 温度为T℃,向体积不等的恒容密闭容器中均充入1mol气体X,发生反应:X(g) Y(g)+Z(g)ΔH,反应
均进行10min,测得各容器中X的转化率与容器体积的关系如图所示。下列说法正确⇌的是
A. a点再充入一定量的X,X的转化率减小
B. d点有ν =ν
正 逆
C. 正反应速率v(b)=v(d)
D. 若c点为平衡点,则浓度平衡常数K=0.9
20. 下列离子方程式正确的是
第 4 页 共 9 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
A. 足量的CO 通入饱和碳酸钠溶液中:CO+CO +H O=2HCO
2 2 2
B. 酸性条件下KIO 溶液与KI溶液反应生成I:5I-+IO +3H O=3I +6OH-
3 2 2 2
C. 向NH Al(SO ) 溶液中滴入Ba(OH) 使SO 恰好完全反应:2Ba2++4OH-+Al3++2SO =BaSO ↓+AlO
4 4 2 2 4
+2H O
2
的
D. NH HSO 溶液中逐滴加入足量 Ba(OH) 溶液:NH +HSO +Ba2++2OH-=BaSO ↓+NH·H O+HO
4 3 2 3 3 2 2
二、综合题(共60分)
21. 1962年首个稀有气体化合物XePtF 问世,目前已知的稀有气体化合物中,含氙( Xe)的最多,氪( Kr)
6 54 36
次之,氩( Ar)化合物极少。[BrOF ][AsF ]•xKrF 是[BrOF ]+、[AsF ]-与KrF 分子形成的加合物,回答下列
18 2 6 2 2 6 2
问题:
(1)As元素原子序数为33,在周期表中的位置是_______。As原子的价电子排布式为_______。与磷酸相
比,最高价氧化物的水化物酸性强弱的顺序是:_______。
的
(2)Ar、Kr、Xe原子半径大小顺序为_______。Ar、Kr、Xe原子 活泼性依序增强,原因是________。
(3)晶体熔点:KrF _______XeF (填“>”“<”或“=”),判断依据是______________。
2 2
(4)试猜想:[BrOF ][AsF ]•xKrF 晶体中的化学键类型有_______。
2 6 2
22. CS 是一种重要的化工原料。工业上可以利用硫(S )与CH 为原料制备CS,S 受热分解成气态S,发
2 8 4 2 8 2
生反应2S(g)+CH (g) CS(g)+2HS(g),回答下列问题:
2 4 2 2
的
(1)CH 立体构型为_______,CS 分子的电子式为_______。
4 2
(2)某温度下若S 完全分解成气态S。在恒温恒容密闭容器中S 与CH 物质的量比为2∶1时开始反应。
8 2 2 4
①当CS 的体积分数为10%时,CH 的转化率为_______。
2 4
②当以下数值不变时,能说明该反应达到平衡的是_______(填序号)。
的
a.气体密度 b.气体总压 c.CH 与S 体积比 d.CS 体积分数
4 2 2
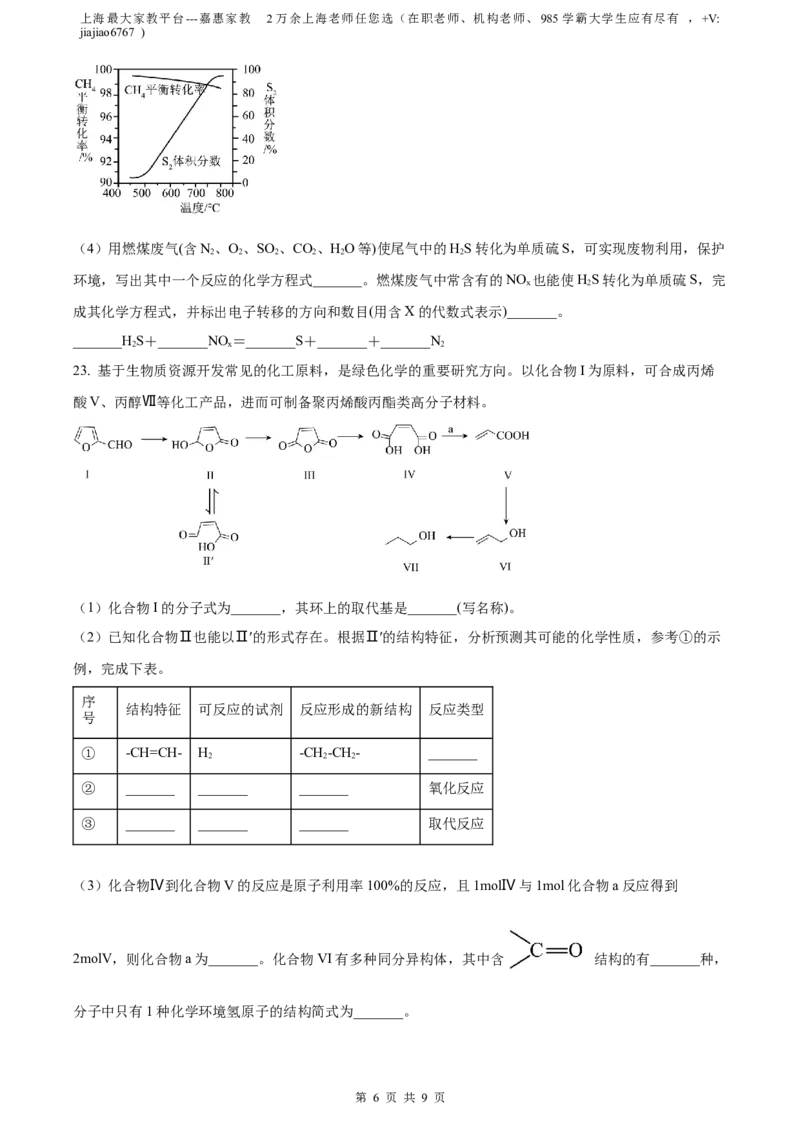
(3)一定条件下,CH 与S 反应中CH 的平衡转化率、S 分解产生S 的体积分数随温度的变化曲线如图
4 2 4 8 2
所示。据图分析,生成CS 的反应为_______(填“放热”或“吸热”)反应。工业上通常采用在600~650℃的条
2
件下进行此反应,不采用低于600℃可能的原因是:_______。
第 5 页 共 9 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
(4)用燃煤废气(含N、O、SO 、CO、HO等)使尾气中的HS转化为单质硫S,可实现废物利用,保护
2 2 2 2 2 2
环境,写出其中一个反应的化学方程式_______。燃煤废气中常含有的NO 也能使HS转化为单质硫S,完
x 2
成其化学方程式,并标出电子转移的方向和数目(用含X的代数式表示)_______。
_______HS+_______NO =_______S+_______+_______N
2 x 2
23. 基于生物质资源开发常见的化工原料,是绿色化学的重要研究方向。以化合物I为原料,可合成丙烯
酸V、丙醇Ⅶ等化工产品,进而可制备聚丙烯酸丙酯类高分子材料。
(1)化合物I的分子式为_______,其环上的取代基是_______(写名称)。
(2)已知化合物Ⅱ也能以Ⅱ′的形式存在。根据Ⅱ′的结构特征,分析预测其可能的化学性质,参考①的示
例,完成下表。
序
结构特征 可反应的试剂 反应形成的新结构 反应类型
号
① -CH=CH- H -CH-CH- _______
2 2 2
② _______ _______ _______ 氧化反应
③ _______ _______ _______ 取代反应
(3)化合物Ⅳ到化合物V的反应是原子利用率100%的反应,且1molⅣ与1mol化合物a反应得到
2molV,则化合物a为_______。化合物VI有多种同分异构体,其中含 结构的有_______种,
分子中只有1种化学环境氢原子的结构简式为_______。
第 6 页 共 9 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
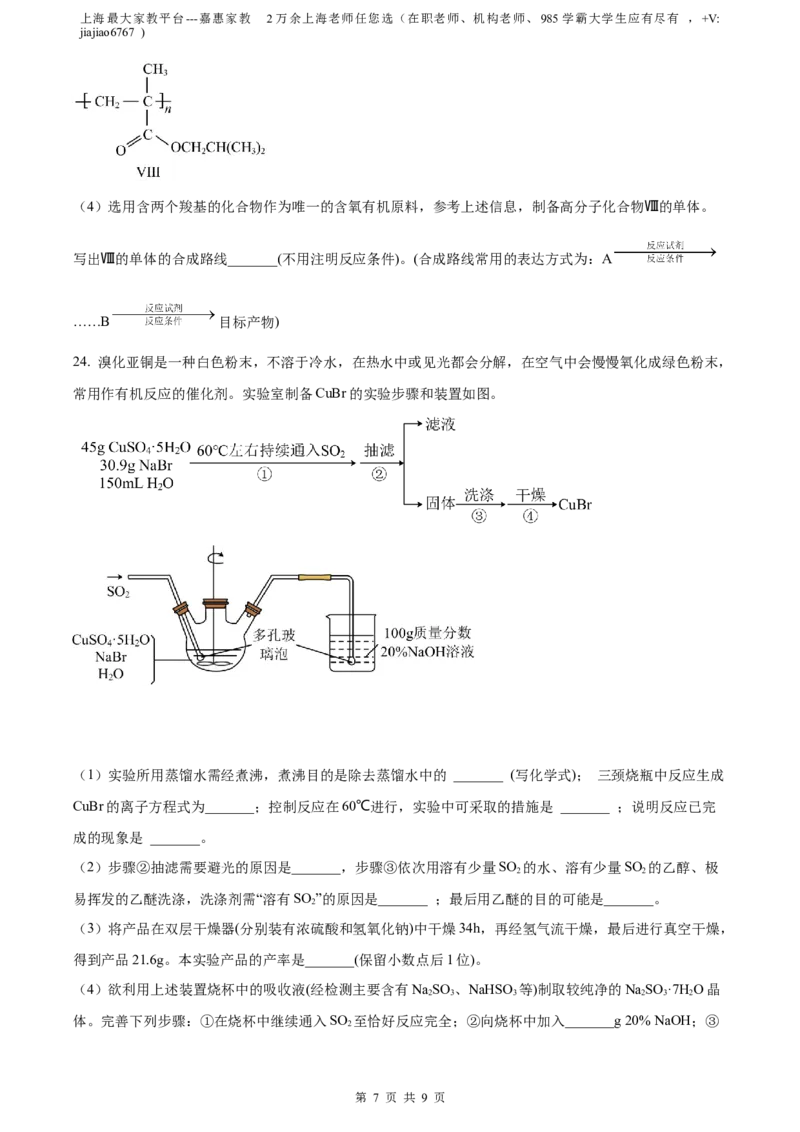
(4)选用含两个羧基的化合物作为唯一的含氧有机原料,参考上述信息,制备高分子化合物Ⅷ的单体。
写出Ⅷ的单体的合成路线_______(不用注明反应条件)。(合成路线常用的表达方式为:A
……B 目标产物)
24. 溴化亚铜是一种白色粉末,不溶于冷水,在热水中或见光都会分解,在空气中会慢慢氧化成绿色粉末,
常用作有机反应的催化剂。实验室制备CuBr的实验步骤和装置如图。
(1)实验所用蒸馏水需经煮沸,煮沸目的是除去蒸馏水中的 _______ (写化学式); 三颈烧瓶中反应生成
CuBr的离子方程式为_______;控制反应在60℃进行,实验中可采取的措施是 _______ ;说明反应已完
成的现象是 _______。
(2)步骤②抽滤需要避光的原因是_______,步骤③依次用溶有少量SO 的水、溶有少量SO 的乙醇、极
2 2
易挥发的乙醚洗涤,洗涤剂需“溶有SO ”的原因是_______ ;最后用乙醚的目的可能是_______。
2
(3)将产品在双层干燥器(分别装有浓硫酸和氢氧化钠)中干燥34h,再经氢气流干燥,最后进行真空干燥,
得到产品21.6g。本实验产品的产率是_______(保留小数点后1位)。
(4)欲利用上述装置烧杯中的吸收液(经检测主要含有NaSO 、NaHSO 等)制取较纯净的NaSO ·7H O晶
2 3 3 2 3 2
体。完善下列步骤:①在烧杯中继续通入SO 至恰好反应完全;②向烧杯中加入_______g 20% NaOH;③
2
第 7 页 共 9 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
加入少量维生素C溶液作抗氧化剂;④通过蒸发浓缩、_______、过滤、用乙醇洗涤2~3次;⑤置于真空
干燥箱中干燥
第 8 页 共 9 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
第 9 页 共 9 页