文档内容
2023 年普通高等学校招生考试化学科目(天津卷)
一、选择题
作者的备注:化学选择题总体简单,因此部分错误选项没有被成功还原,我们将把这些选项直
接空出。
1.下列化学知识,错误的是( )。
A.玻璃是晶体 B.铝合金是一种金属材料
C. D.
2.下列化学常识,错误的是( )
A.淀粉是一种多糖 B.葡萄糖有还原性 C.油脂是一种高分子 D.氨基酸具有两性
3.下列方法(试剂)中,无法鉴别Na CO 和BaCl 两种物质的是( )。
2 3 2
A.焰色试验 B.pH试纸 C.稀氨水 D.Na SO
2 4
4.下列常见物质及用途,错误的是( )。
A. B.SiO 可用于制造光导纤维
2
C.Fe O 是铁红,可以用作染料 D.钠起火,可以使用水基灭火器扑灭
2 3
5.下列比较C和Si非金属性的方法,错误的是( )。
A.单质氧化性 B.氧化物熔点 C.和氢气化合难易程度 D.最高价氧化物水化物酸性
6.题干给出一信息反应,反应物中有NaClO ,生成物中有ClO ,有关说法正确的是( )。
3 2
A.CO 是非极性分子 B.
2
C.NaClO 在反应中做还原剂 D.ClO 分子空间构型为直线形
3 2
7.研究人员用同位素标记法研究了一个反应过程,如下:
①H18O18OH+Cl =H18O18OCl+H++Cl-
2
②H18O18OCl=H++Cl-+18O
2
关于这个反应,说法正确的是( )
A.第一步反应是置换反应 B.
C. D.反应历程中O-O键没有发生断裂
8.如图所示,是芥酸的分子结构,关于芥酸,下列说法正确的是( )
A.芥酸是一种强酸 B.芥酸易溶于水 C.芥酸是顺式结构 D.分子式为C H O
22 44 2
第1页 | 共5页9.如图是反应装置,可以做下列( )
作者的备注:此处原卷给出装置图,发生装置为固液常温型,气体收集装置是导管长进短出的集气瓶,接尾
气处理装置。
A.稀硝酸与铁制备一氧化氮 B.浓盐酸与二氧化锰制备氯气
C.浓氨水与氢氧化钠制备氨气 D.浓硫酸与亚硫酸钠制备二氧化硫
10.在浓度为0.1 mol/L的NaH PO 溶液中,如下说法正确的是( )。
2 4
A.溶液中浓度最大的离子是H PO
2 4
B.cH PO +c H PO- +c HPO2- +c PO 2- =0.1 mol/L
3 4 2 4 4 4
C.c Na+ +c H+ =c H PO- +2c HPO2- +3c PO 2-
2 4 4 4
c H PO-
2 4
D.磷酸第二步电离平衡的平衡常数表达式为K=
c
H+
c
HPO
2-
4
11.已知pK =-lgK ,如图下表是几种不同有机酸的pK 大小,由此产生的推断,正确的是( )。
a a a
作者的备注:此处,原卷列表展示了CH FCOOH、CH ClCOOH、CH BrCOOH和CH COOH四种物
2 2 2 3
质的pK 依次增大。
a
A.对键合电子吸引力:FCH FCOOH
2 2
C.pK :CHFCOOHCH COONa
a 2 2 2 3
12.《武备志》记载了古人提纯硫的方法,其中这样描写到具体流程:“先将硫打豆粒样碎块,每斤硫黄用麻油
二斤,入锅烧滚,再下青柏叶半斤在油内,看柏枯黑色,捞去柏叶,然后入硫黄在滚油内。待油面上黄泡起至
半锅,随取起,安在冷水盆内,倒去硫上黄油,净硫凝,一并在锅底内者是。”下列说法错误的是( )。
A.“硫打豆粒样”是为了增大接触面积 B.“下青柏叶”“看柏枯黑色”是为了指示油温
C.“倒去硫上黄油”实现了固液分离 D.流程用到了蒸馏原理
二、简答题
13.关于铜,同学们进行了下列探究
(1)铜的价层电子排布式是__________,Cu+与Cu2+中半径较大的是__________。
(2)下图是铜的一种氯化物晶胞,则这种物质的化学式为__________。
第2页 | 共5页(3)已知铜可以与过氧化氢、稀盐酸反应,制备CuCl ,写出该反应化学方程式:____________________。
2
反应中,过氧化氢实际用量总是大于理论用量,原因是____________________。
(4)过氧化氢电子式为__________。
(5)下列物质都可以替代过氧化氢进行这个反应,最合适的是__________。
a.HNO b.O c.Cl
3 2 2
(6)同学们对氯化铜性质进行了探究。向得南氯化铜溶液中加入KI溶液,得到含有碘元素的沉淀,且反应后
所得溶液加入淀粉呈蓝色,则沉淀化学式为__________,过程中碘(离子)的作用为____________________。
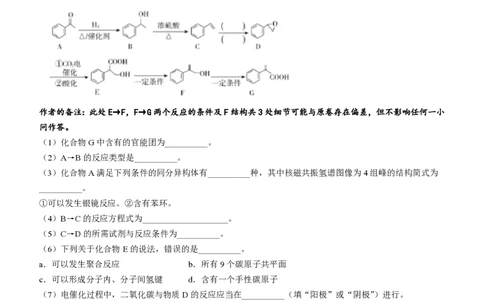
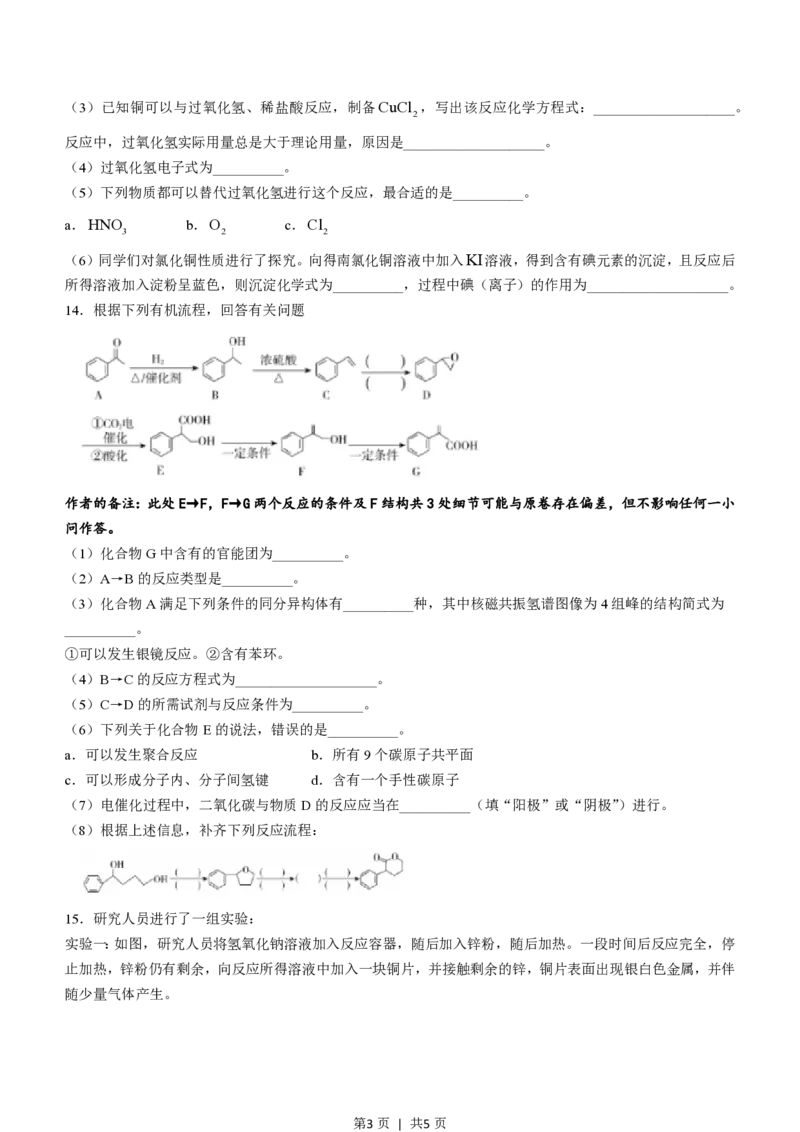
14.根据下列有机流程,回答有关问题
作者的备注:此处E→F,F→G两个反应的条件及F结构共3处细节可能与原卷存在偏差,但不影响任何一小
问作答。
(1)化合物G中含有的官能团为__________。
(2)A→B的反应类型是__________。
(3)化合物A满足下列条件的同分异构体有__________种,其中核磁共振氢谱图像为4组峰的结构简式为
__________。
①可以发生银镜反应。②含有苯环。
(4)B→C的反应方程式为____________________。
(5)C→D的所需试剂与反应条件为__________。
(6)下列关于化合物E的说法,错误的是__________。
a.可以发生聚合反应 b.所有9个碳原子共平面
c.可以形成分子内、分子间氢键 d.含有一个手性碳原子
(7)电催化过程中,二氧化碳与物质D的反应应当在__________(填“阳极”或“阴极”)进行。
(8)根据上述信息,补齐下列反应流程:
15.研究人员进行了一组实验:
实验一:如图,研究人员将氢氧化钠溶液加入反应容器,随后加入锌粉,随后加热。一段时间后反应完全,停
止加热,锌粉仍有剩余,向反应所得溶液中加入一块铜片,并接触剩余的锌,铜片表面出现银白色金属,并伴
随少量气体产生。
第3页 | 共5页实验二:研究人员将实验一得到的带有银白色金属的铜片加热,直到铜片表面变黄,立刻停止加热,置入水中
冷却。
已知:
Zn+2NaOH+2H O=Na [Zn(OH)] +H
2 2 4 2
Na Zn(OH) =2Na++Zn(OH) 2-
2 4 4
Zn(OH) 2- Û Zn2++4OH-
4
(1)如图,实验一使用的仪器为________,为了防止加热过程中液体沸腾溅出,采取的办法是________________。
(2)Na [Zn(OH)] 中含有的化学键包括__________。
2 4
a.离子键 b.极性共价键 c.非极性共价键 d.配位键
(3)写出氢氧化钠与锌反应的离子方程式:____________________。
(4)写出实验一中构成的原电池正负极反应:
负极:____________________;
正极:____________________,____________________。
(5)研究人员在铜片表面变黄后立刻停止加热,放入水中,这样做的目的是____________________。
(6)黄铜和黄金外表相似,但化学性质仍然有所区别。若使用硝酸对二者进行鉴别,则现象与结论为
____________________。
(7)若将铜片插入实验一过滤后的上清液中,可否仍然出现上述现象?请解释:
______________________________。
16.下面是制备硫酸的工业流程:
(1)S 的晶体类型是__________。
8
(2)第一步时,硫粉液化并与氧气共热生成二氧化硫。若反应温度超过硫粉沸点,部分硫粉会转化为硫蒸气,
与生成的二氧化硫一同参加第二步反应,关于这种情况说法正确的是__________。
a.硫粉消耗会增大 b.二氧化硫生成率降低 c.
(3)若每生成80g气体三氧化硫,放出98.3kJ能量,写出生成三氧化硫的反应的热化学方程式:
____________________,若反应温度升高,则二氧化硫转化率__________(填“升高”或“降低”)。
第4页 | 共5页(4)第二步反应中,从能量角度分析催化剂意义:____________________。
在第二步反应中,首先将反应物加热到450-600°C,通入催化剂层,进行第一轮反应,反应后体系温度升高,
导出产物与剩余反应物,与其他反应物进行热交换降温,随后再次通入催化剂层,如此进行四轮反应,使反应
转化率接近平衡转化率,得到较高产率的三氧化硫。
(5)通入催化剂层后,体系(剩余反应物与生成物)温度升高的原因在于____________________;每轮反应
后进行热交换降温的目的是__________。
(6)关于四轮反应,说法正确的是__________。
a.这一流程保证了在反应速率较大的情况下,转化率尽可能大
b.这一流程使这一反应最终达到平衡转化率
c.这一流程节约了能源
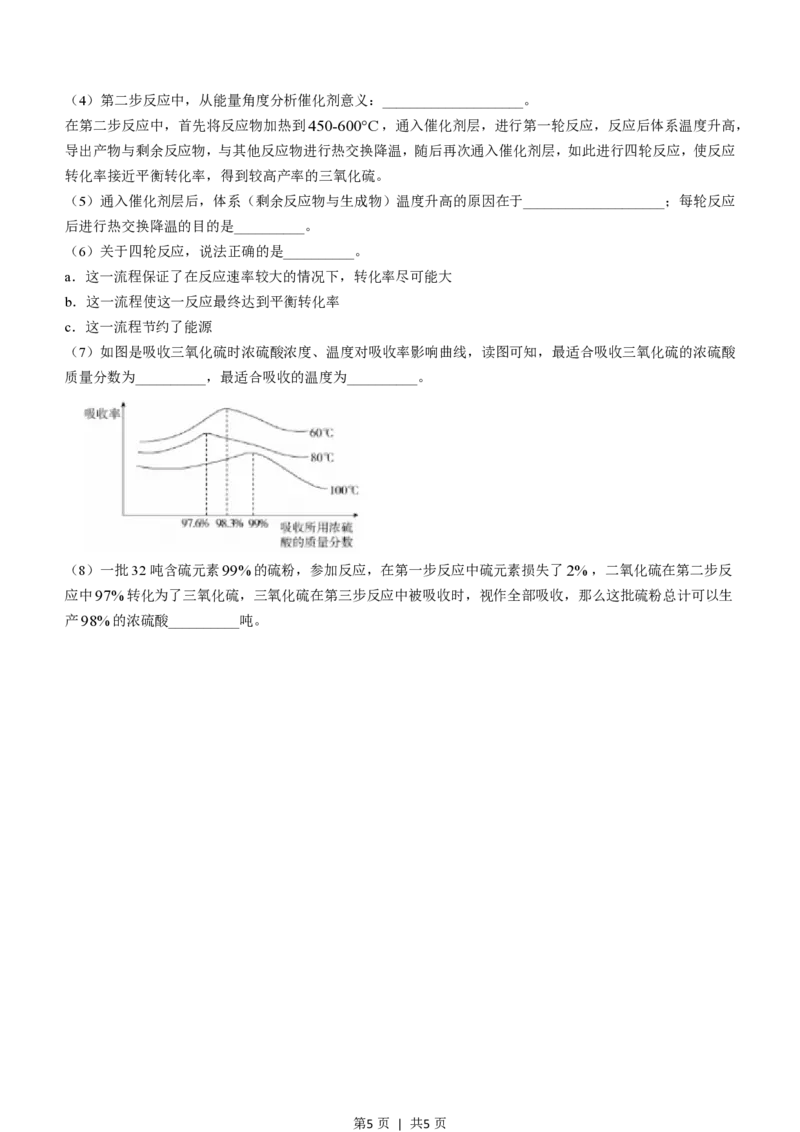
(7)如图是吸收三氧化硫时浓硫酸浓度、温度对吸收率影响曲线,读图可知,最适合吸收三氧化硫的浓硫酸
质量分数为__________,最适合吸收的温度为__________。
(8)一批32吨含硫元素99%的硫粉,参加反应,在第一步反应中硫元素损失了2%,二氧化硫在第二步反
应中97%转化为了三氧化硫,三氧化硫在第三步反应中被吸收时,视作全部吸收,那么这批硫粉总计可以生
产98%的浓硫酸__________吨。
第5页 | 共5页