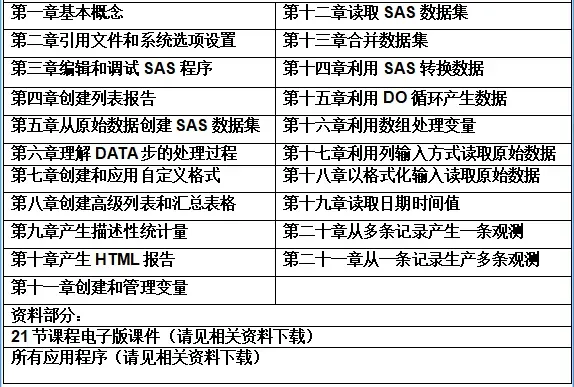
汇总|电子版CDISC-SDTM基本理论及实践系列文章
SDTM基本理论及一般假设
SDTM基本原理(SDTM Standard Domain Models)
SDTM Domain Models假定(一般domain假定)
SDTM – Coding和Controlled Terminology一般假设
Special-Purpose Domains模型
SDTM-DM SAS Programs Assumptions
CO – Assumptions for the Comments Domain Model
CDISC-SDTM-SV–Assumptions for the SUBJECT VISITS Domain Model
CDISC-SDTM-SV–SAS Programs Assumptions
CDISC-SDTM-SE–Assumptions for the Subject Elements Domain Model
CDISC-SDTM-SE–SAS Programs Assumptions
SDTM Standard Domain Models:Special-Purpose Domains
Interventions模型
CDISC-SDTM-CM–SAS Programs Assumptions
CDISC-SDTM-SU–Assumptions for the Substance Use Domain Model
CDISC-SDTM-PR–Assumptions for the Procedures Domain Model
CDISC-SDTM-EX–Assumptions for the Exposure Domain Model
SDTM-EC–Assumptions for the Exposure as Collected Domain
Events模型
SDTM-Adverse Events (AE)一般假设和程序考虑
SDTM-Adverse Events (AE)一般假设和程序考虑(附加篇)
SDTM-Clinical Events (CE,临床事件)一般假设
SDTM-Protocol Deviations(DV,方案偏离)一般假设
SDTM-Healthcare Encounters (HO,就诊)一般假设
SDTM-Medical History (MH,既往病史)一般假设
Findings模型
Trial Design Model
Oncology
抗肿瘤药物临床试验技术指导原则 (2012-05-15)
SDTM-Oncology-Tumor Identification (TU,肿瘤标识符)一般假设
SDTM-Oncology-Tumor Results (TR,肿瘤结果)一般假设
SDTM-Oncology-Disease Response (RS,疾病反应)一般假设
抗肿瘤药物临床试验终点技术指导原则 (2012-05-15)
获取电子版资料请关注微信公众号:法迈医讯,扫码添加小编团团微信回复:" SDTM电子版 "获取资料
好课推荐
课程背景
随着国内临床试验的发展,以及创新药研发力度的加大,越来越多的毕业生和职场人士加入到临床试验研发流程当中,成为整个产业链当中的重要一环。然而随着行业发展,市场对专业技术人才的需求缺口越来越大,出现了企业招不到合适的人才,很多人又找不到合适的工作,为了给业内输送越来越多统计编程岗位的人才,我们开设了本系列录播课程,以帮助大家掌握和应用统计编程岗必备的专业技能,让大家实现更好的职业发展,同时也满足企业的人才缺口!
课程目录
模块一:CDISC---SDTM
模块二:CDISC---ADaM
模块三:CDISC---Define--XML
模块四:项目管理--Lead部分
模块五:SAS编程Base和SQL&Macro
课程亮点
课程简介
本课程一共分五大版块,全面而系统地讲解SAS程序员统计编程相关知识和技巧。课程总时长将近100小时,课程内容包括对相关指导原则的深度解读、实际项目经验分享、参考程序、数据集和项目模板分享等等,特别注重专业知识的强化和引申扩充,帮助大家学习行业所需的知识体系。购买课程学员将获取所有课程的相关资料(包括指导原则、文献、论文、模板、程序、数据集等等)
本课程面向医药行业、构建行业知识体系、面向实际就业,是为所有医药数据分析职场小白量身打造的职业技能强化课程。
福利一:凡是购买套课学员讲师将全程在线解答学员课程相关及大家实际工作和学习中遇到的问题.
福利二:凡是购买全套课程的学员,如有需要,平台可帮忙推荐工作机会
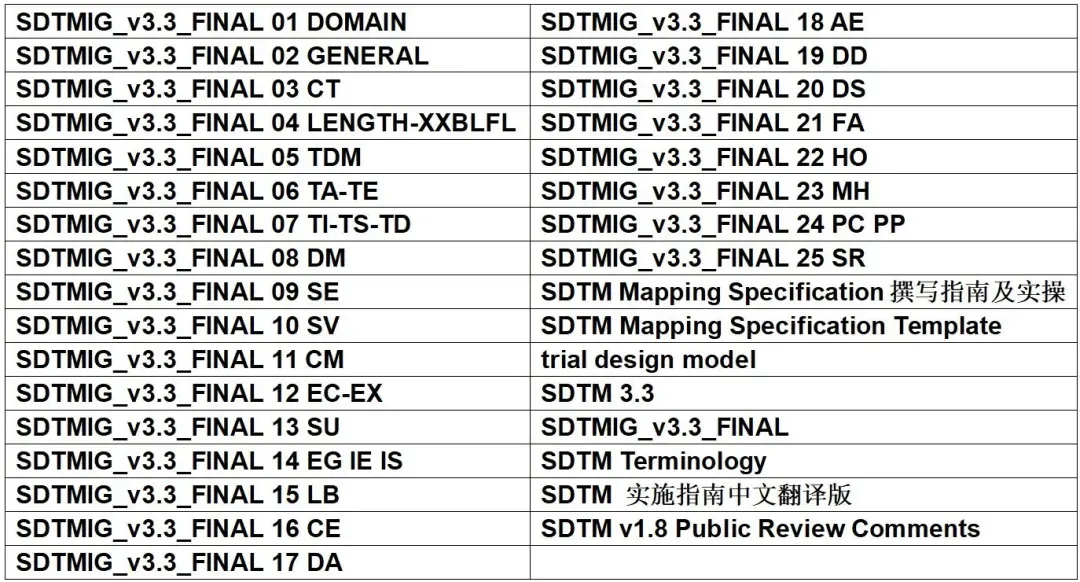
模块一:CDISC---SDTM
SDTMIG_v3.3_FINAL,由CDISC Submission Data Standards Team 发布于2018.11.20,解读视频包括SDTM基本理论,试验设计和特殊domain模块等内容。此系列重点关注trial design domain,如TS每一个parameter的创建方法,常见及较为复杂试验设计的综合考虑,如ARM和Element Map方法,SDTM编程的基本理论详细解读,特殊及重要domain的运用和举例。本模块视频时长:17小时31分钟25秒
SDTM Metadata Submission Guidelines v2.0,由CDISC SDS MSG Team发布于2021-03-30,这一版较1.2版变化较大,尤其是关于aCRF的制作方面。视频包括对SDTM-MSG_v2.0通读,样本数据和aCRF举例。 本模块视频时长:2小时30分钟58秒
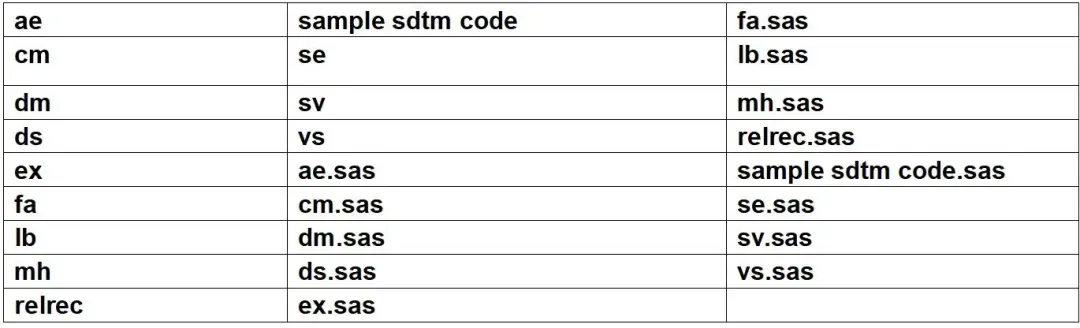
SDTM编程domain创建方法讲解视频及程序本模块视频时长:2小时44分钟55秒
SDTM编程宏讲解视频及参考SAS程序本模块视频时长:1小时55分钟28秒
购课赠送:SDTMIG 3.2超详细解读及基本问题分享电子版(204页电子书)
扫码试听
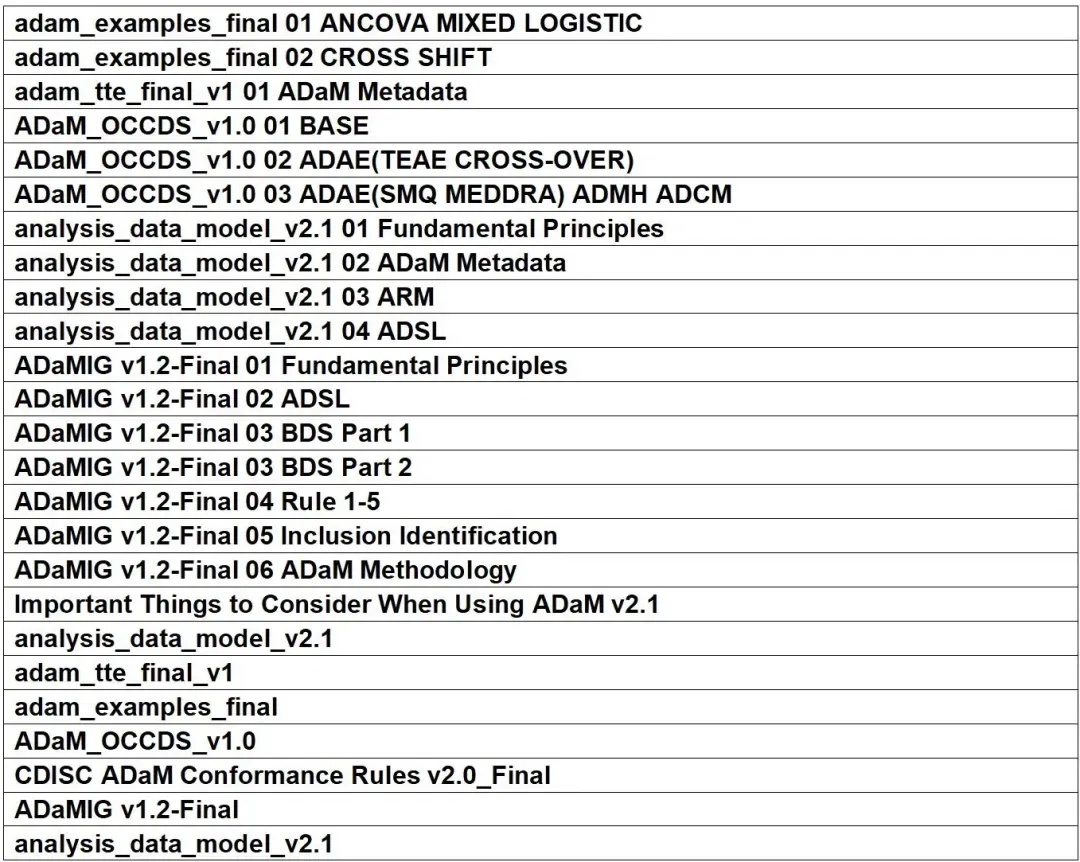
模块二:CDISC--ADaM
ADaM部分指导原则精读视频 ,视频时长:16小时2分钟14秒
ADaM编程部分数据集参考程序及讲解视频 视频时长:1小时4分钟47秒
ADaM部分SAS宏程序及讲解视频 视频时长:21分钟50秒
ADaM Specification基本理论及实操讲解视频时长:44分钟30秒
扫码试听 模块三:CDISC--Define-XML
Define-XML制作视频,利用Pinnacle 21 Community软件创建SDTM/ADaM Define.xml的全面详细地指导过程,包括数据验证及解释,Review Guide撰写,一般考虑和实际操作方法等。模块三视频总时长:8小时7分15秒
Define-XML部分:PDF格式文件使用规范(含参考程序) 扫码试听
模块四:项目管理--Lead部分
模块四包含两个部分课程视频总时长:5小时29分钟2秒
项目管理-Lead讲解视频及引用资料,详细介绍了项目管理层面对技术和管理能力的基本要求及一般考虑
项目管理-Lead程序及讲解视频
扫码试听
模块五:SAS编程
SAS高级编程技能之SQL & Macro系列录播课程,本课程为SAS高级编程课程,课程包含16节视频课+所有课件/程序/数据集等资料,旨在提高学员SAS编程技能,是提升学员的工作能力的强化课程。视频时长:11小时11分钟 24秒
购课赠送:21节SAS初级编程系列课程(含视频/程序/课件/数据等)本视频一共21节课程,包含视频/程序/课件/数据等,是一套非常全面而系统的系列课,本系列视频课程适合于初级SAS学习者. 本模块视频时长:14小时28分钟4秒
扫码试听 适合人群
小白、在校学生
实习生、初入职场人士
对统计编程感兴趣计划转行到临床SAS程序员的在职人士
讲师简介
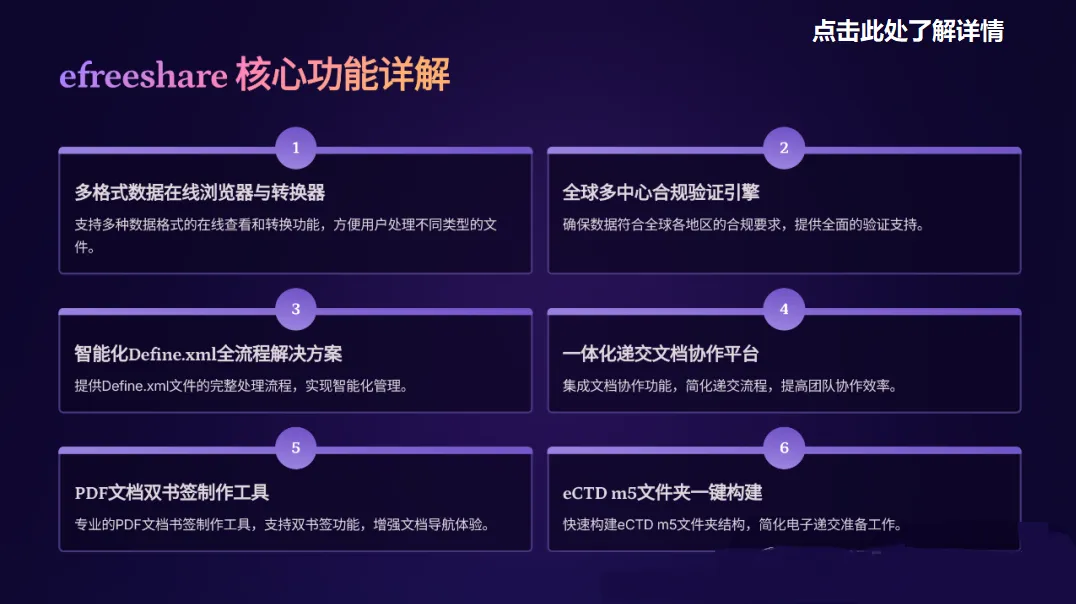
团长老师 法迈新媒体合作资深讲师,数量经济学硕士;efreeshare系统开发负责人 十几年临床试验行业经验,深耕于统计编程、生物统计、数据管理等,拥有扎实的专业知识和丰富的项目经验,完成上百个向FDA和CDE递交的统计编程项目,善于搭建团队和项目管理,非常熟悉业内的流程和业务,积累了丰富的经验,摸索出培养统计编程人才的一套成熟的教学体系。 已在平台(微信公众号:法迈医讯)推出作品:
21节SAS初级编程系列课程
生物统计学方法讲解与应用系列培训课程
CDISC-SDTM基本理论及实践系列文章汇总
SAS编程应用及相关知识分享系列文章汇总
ICH指导原则E3/E6/E8/E9系列解读录播课程
统计程序员TFLs编程系列录播课程
等等干货文章资料与课程
报名咨询
课程详细请咨询扫描二维码添加助教“团团” 微信
欢迎加入1474+人的中国临床试验千人通讯录
精品课程推荐
《AI赋能Protocol撰写Workshop》训练AI按要求帮你完成专业的protocol撰写,附课程试听!
统计师必看:从实际案例系统学习临床试验前沿设计方法 生翼计划:临床SAS程序员实战项目训练营开营啦!真实临床试验项目数据练手,模拟工作环境,体验工作日常!
药物警戒体系全套SOPs:符合国家局核查标准!符合B证现场检查!
精品资料包推荐
真实世界研究全套资料包! 临床试验贝叶斯设计资料包:17本书籍+14篇文献干货满满! FDA药物警戒资料包 领取|临床研究统计方法必看的15本知名书籍! 领取| 临床SAS编程和数据管理全套干货资料包! 药物警戒全套精华资料包 收藏|知名书籍:临床试验的贝叶斯自适应方法 法规|ICH-GCP中英文对照(最完整版) 收藏|E9:临床试验统计原则(另附中英文对照词汇表) 免费公开课|21节SAS Base初级编程系列课程 限时领取|杜克临床研究所的临床试验手册 汇总|临床试验十七个相关知识点 免费领取|临床研究几本经典书籍 ! 最全汇总:Define-XML 2.1指导原则讲解视频 分享|专属生物统计师的几本经典书籍 汇总|电子版CDISC-SDTM基本理论及实践系列文章 限时领取|8.72G临床试验精华资料包(共180个文件)送给临研人的福利! 限时领取|符合国际标准的全套临床SOP资料包,651个文件供你参考学习! 汇总帖:CDISC标准干货文章和资料精选 汇总帖:生物统计系列干货文章和资料精选 汇总帖:SDTM干货文章和资料精选 免费领取|ADC(抗体药物偶联物)知名书籍:研发,临床,注册及市场发展 领取|生物等效性试验(BE试验)比较全面的知名书籍! 汇总|CDE ICH指导原则全系列培训视频 必看|学习生物制药CMC必看的23本书籍! 限时免费|书籍: 临床数据管理实用指南第三版 收藏|抗肿瘤药物创新研发必看16本书籍! 福利|专属CRC的全套资料包免费领取 收藏|547页CDASHIG v2.3 FINAL 领取知名书籍:新临床试验人员的基本概念&药物开发中的定量决策 汇总|生物统计系列十五篇干货文章! 收藏|临床研究设计与方案撰写资料包!! 汇总|生物统计系列十五篇干货文章! 汇总|生物统计学常用统计分析方法系列文章 汇总|SAS编程应用及相关知识分享系列文章 收藏|药物临床试验必备文件及相关管理要求 限时领取|CRA应看的5本知名书籍! >>>> 公众号推荐
欢迎关注法迈新媒体
更多,更及时的干货内容,请加我们的微信公众号:法迈医讯,诚邀业内人士及机构向我们投稿。投稿邮箱:bellama@pharmanews.cn 【免责声明】文章为网络整理,不代表“法迈医讯”立场。如因作品内容、版权等存在问题,请于本文刊发30日内联系法迈医讯进行删除或洽谈版权使用事宜。
法迈医讯作为法迈新媒体微信公众号矩阵之一, 法迈新媒体是国内一家面向制药行业供应链综合服务平台,致力于服务全球制药行业从业人员。以创新的互网+模式服务于行业用户,形成以“资源整合,知识共享”为核心,微信公众号矩阵、社群矩阵为分支的新媒体模式,力争打造国内活跃和具影响力的专业化平台 !
 夜雨聆风
夜雨聆风