AI+液体活检:PRIME模型大幅提升早期非小细胞肺癌进展风险预测准确率
MRD检测已经广泛应用于非小细胞肺癌(NSCLC)预后及复发预测,但当前临床常用的ctDNA MRD检测存在灵敏度不足的问题,超50%MRD阴性患者仍会复发。近期发表于《Military Medical Research》的研究开发了可解释AI模型PRIME,整合液体活检、基因组变异与临床特征,将进展风险预测AUC提升至0.82~0.85,为个性化治疗决策提供了全新工具。
模型构建:多队列整合+可解释AI构建通用预测模型
研究团队纳入了全球6个队列共493例I-III期NSCLC患者的781份血液样本,覆盖手术、根治性放化疗、放化疗+免疫巩固三种常见根治性治疗模式,同时兼容固定panel和个性化panel两种主流ctDNA测序技术,最大程度贴合真实世界临床场景。 研究者首先统一了不同队列的MRD判读标准,筛选出与疾病进展独立相关的特征,随后对6种经典机器学习算法进行训练与验证,最终选择性能最优的神经网络模型构建PRIME,并通过SHAP分析量化每个特征的贡献度,解决传统AI模型“黑箱”不可解释的问题。
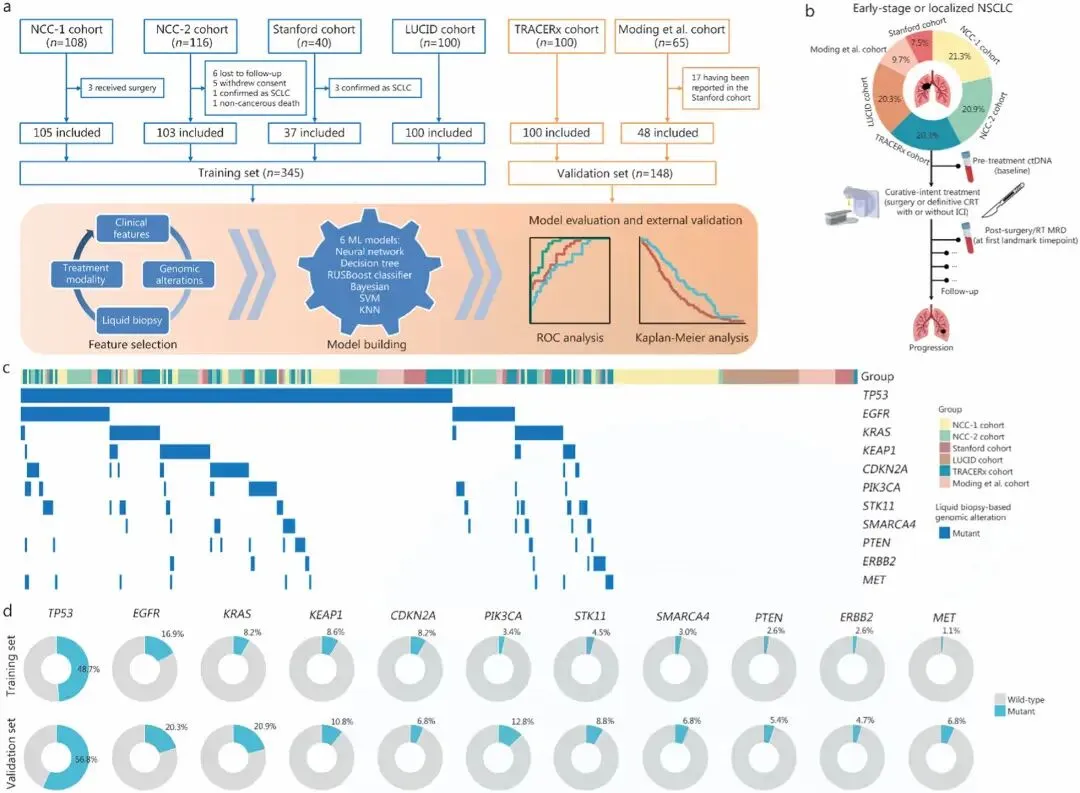 图1. 研究整体设计:纳入6个队列的I-III期NSCLC患者多维度数据,构建并验证PRIME预测模型
图1. 研究整体设计:纳入6个队列的I-III期NSCLC患者多维度数据,构建并验证PRIME预测模型
模型性能:7个核心特征实现精准风险分层
1. 筛选出7个独立预测因子
通过单因素分析,研究者最终确定7个与NSCLC根治后进展风险显著相关的特征,纳入模型训练:临床分期、治疗前ctDNA状态、治疗方式、治疗后MRD、外周血KEAP1突变、STK11突变、CDKN2A突变。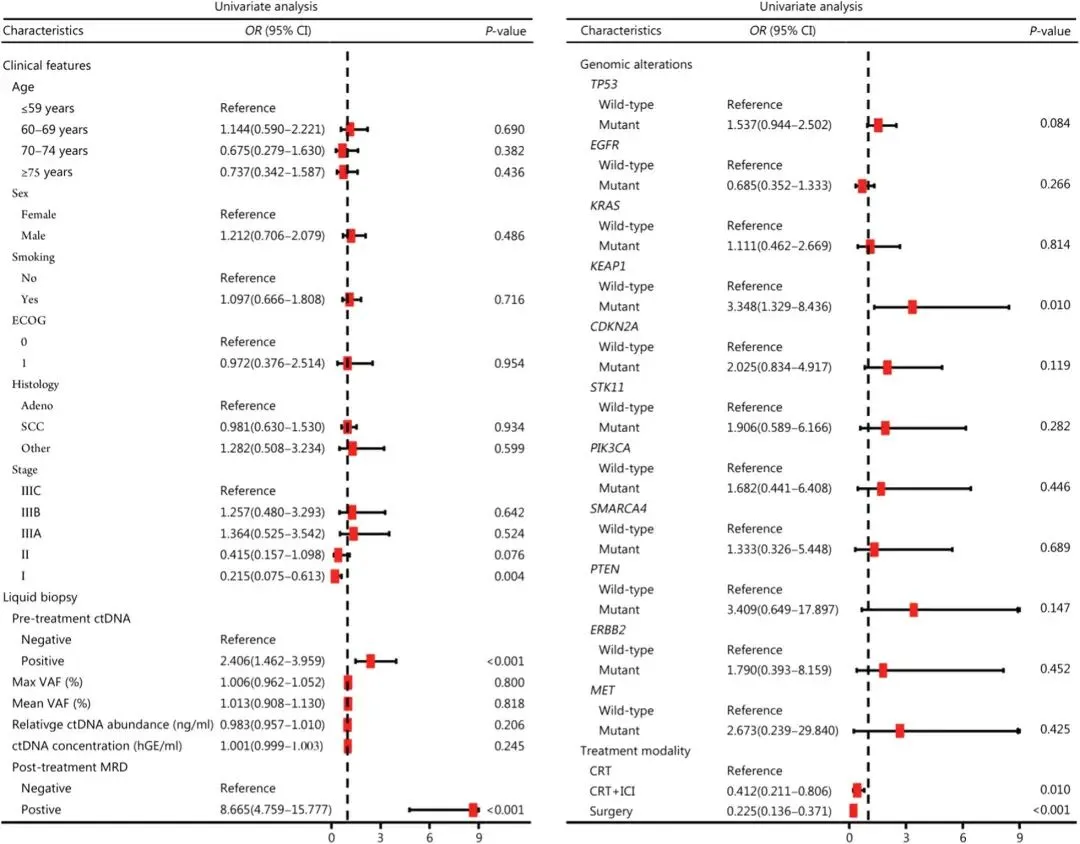 图2. 训练集疾病进展潜在预测因子森林图,7个特征达到统计学显著性纳入模型
图2. 训练集疾病进展潜在预测因子森林图,7个特征达到统计学显著性纳入模型
2. 三个基因突变提示不良预后,机制明确
研究发现携带外周血KEAP1、STK11、CDKN2A突变的患者进展率分别达53.8%、52.0%、46.9%,位列所有突变的前三位,TCGA队列的组织测序数据也验证了这三个突变的不良预后价值。进一步机制分析显示:这三个突变会共同诱导抑制性肿瘤免疫微环境,下调巨噬细胞分化、肥大细胞活化、B细胞介导的体液免疫通路,将肿瘤变为免疫“冷肿瘤”,最终导致患者预后更差。
3. PRIME模型性能显著优于单指标检测
最终构建的神经网络版PRIME模型表现最优:训练集AUC达0.85(95%CI 0.81~0.89),独立外部验证集AUC达0.82(95%CI 0.74~0.89),显著优于单个MRD检测(AUC 0.71)、临床分期(AUC 0.60)等单一指标。 SHAP可解释性分析显示:MRD(贡献度+0.306)、治疗方式(贡献度+0.128)、治疗前ctDNA(贡献度+0.043)是模型贡献度最高的三个预测因子,结果符合临床认知。
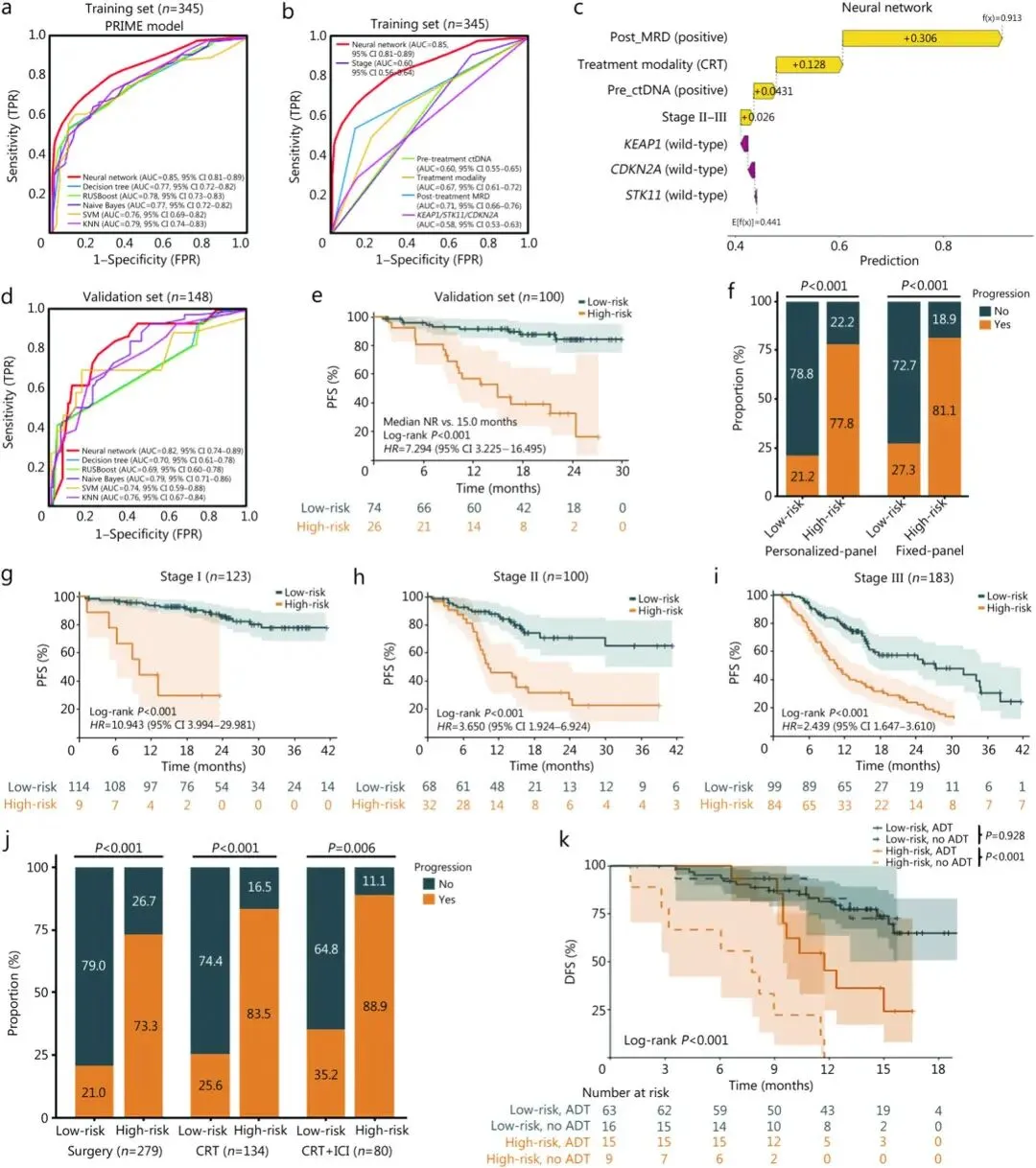 图3. PRIME模型性能与可解释性分析:a 训练集6种机器学习算法ROC对比;b PRIME与单个预测因子ROC对比;c SHAP分析各特征贡献度;d 验证集模型ROC曲线;e 验证集高低风险患者PFS对比
图3. PRIME模型性能与可解释性分析:a 训练集6种机器学习算法ROC对比;b PRIME与单个预测因子ROC对比;c SHAP分析各特征贡献度;d 验证集模型ROC曲线;e 验证集高低风险患者PFS对比
4. 可直接指导辅助治疗决策
PRIME模型识别的高风险患者无进展生存期(PFS)显著差于低风险患者,且在不同分期、不同治疗模式的亚组中均保持稳定的分层效力。 尤其值得关注的是:高风险患者术后接受辅助治疗的获益显著(P<0.001),而低风险患者接受辅助治疗无明显生存获益(P=0.928),提示PRIME可直接用于指导辅助治疗的个性化选择,避免低风险患者承受不必要的治疗副作用。
临床前景
相较于现有同类模型,PRIME有三个不可替代的优势:
-
跨平台适用性强:兼容固定panel和个性化panel两种ctDNA测序技术,无需患者使用特定检测平台,适配真实世界不同医疗机构的检测条件,推广门槛极低; -
可解释性高:通过SHAP量化每个特征的贡献度,输出结果符合临床逻辑,更容易获得医生与患者的信任,符合临床监管要求; -
样本易获取:所有预测因子均来自外周血与常规临床信息,无需获取肿瘤组织,尤其适合无法取得足够组织样本的局晚期NSCLC患者。
目前研究团队已经启动前瞻性II期临床试验(NCT06998719)进一步验证PRIME的临床价值,未来还将拓展模型的应用场景,用于预测围手术期免疫治疗的获益人群。当然该研究也存在一定局限性:纳入人群覆盖不同分期与治疗模式存在一定异质性,未来需要更大规模的前瞻性队列进一步验证模型的普适性。
总结
PRIME模型首次实现了“液体活检多组学特征+可解释AI”的有机结合,解决了长期以来早期NSCLC根治后复发预测准确率不足、难以落地临床的痛点,不仅预测性能优异,还完美适配真实世界的多样化临床场景。未来随着前瞻性验证的完成,该模型有望纳入临床常规诊疗路径,真正实现早期肺癌患者的风险分层与个性化治疗,进一步提升患者的长期生存率。
原文信息
-
PRIME: an interpretable artificial intelligence model based on liquid biopsy improves prediction of progression risk in non-small cell lung cancer. Mil Med Res. 2026 Jan 6;12(1):94. -
https://doi.org/10.1186/s40779-025-00679-z
都看到了这里,辛苦关注一下吧!☟☟☟
 夜雨聆风
夜雨聆风




