JACS | 破解AI蛋白设计超稳定之谜:介观结构化水壳机制,让蛋白耐受120℃高温与极端变性条件
-
极端热稳定性突破:DSC结果显示,野生型泛素的熔解温度(Tm)约为60℃,而R4、R10变体在升温至120℃时仍未出现明显的解折叠峰,热稳定性提升超60℃;
-
核心结构高度保守:NMR化学位移分析(图1)显示,R4、R10与野生型泛素的主链构象、疏水核心堆积完全一致,氢键强度(ΔδNH/ΔT)无显著差异,排除了分子内相互作用优化的可能性; 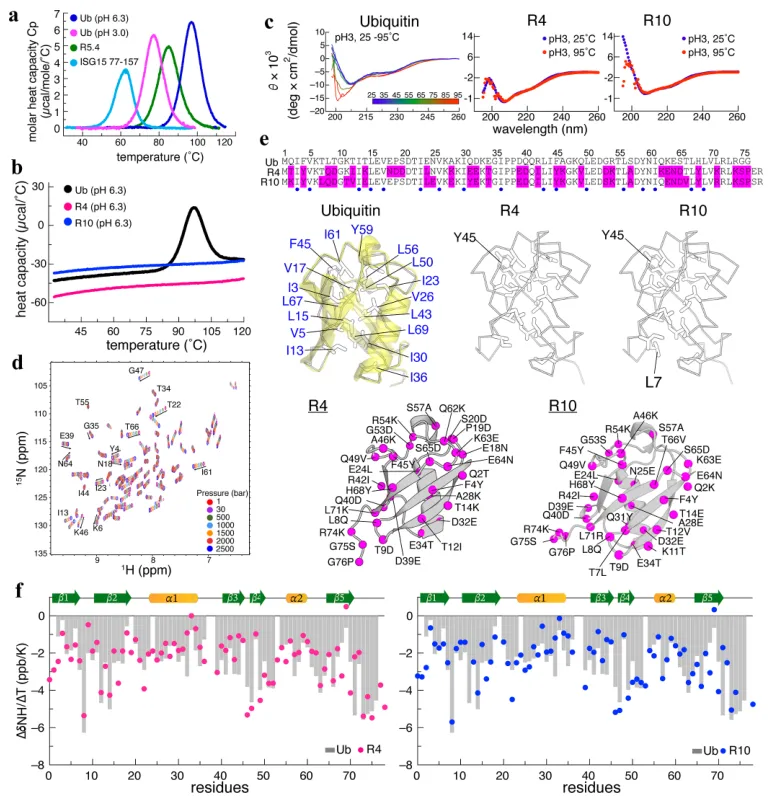
-
关键异常线索:NMR弛豫实验发现,R4、R10的旋转相关时间τc从野生型的4.15 ns分别提升至5.2 ns、5.5 ns,而流体力学半径(RH)无显著变化——这一矛盾结果直接指向:蛋白与周围溶剂的相互作用发生了根本性改变。
-
HDX-NMR直接验证溶剂防护效应:48小时氢氘交换实验后,野生型泛素仅12个残基保留>20%的信号,而R4、R10分别有27、32个残基实现了全局的交换保护,慢交换残基覆盖了蛋白全序列,证明水化层显著阻挡了重水的入侵(图2); 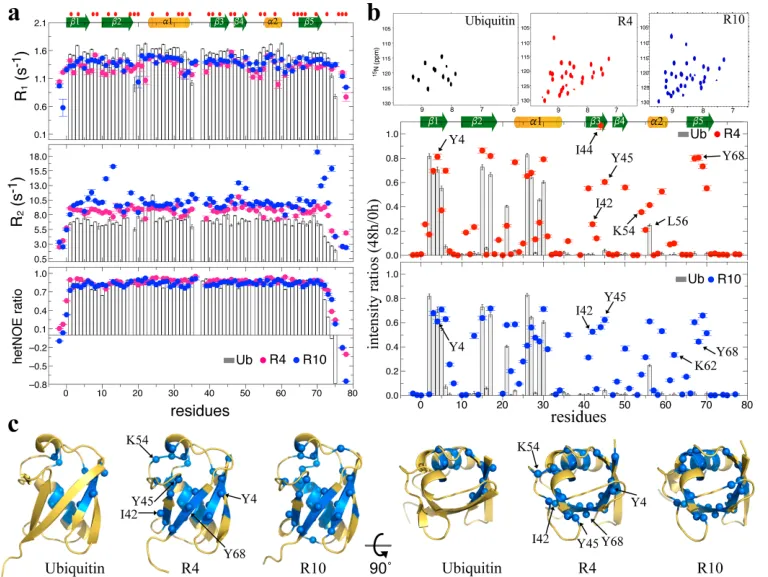
-
MD模拟揭示水壳的介观结构:模拟结果显示,R4的一级水化层(0-3.5 Å)水分子停留时间是野生型的40倍,二级水化层(3.5-10 Å)更是达到100倍;同时,变体水化层内的蛋白-水氢键、水-水氢键数量提升5%-10%,形成了高度有序的介观结构化网络,而非天然蛋白周围的无序水分子;
-
能量层面的直接支撑:变体蛋白与溶剂的非键相互作用能显著降低,意味着蛋白-水的结合更稳定,从热力学层面解释了水壳的稳定效应。
-
极端条件下的结构完整性:野生型泛素在pH 3.0 + 8M尿素中完全解折叠,而R4在相同条件下,HSQC谱图仍呈现出折叠蛋白的特征性分散峰(图3a);CD光谱显示,即使升温至95℃,R4的二级结构特征完全不变,无任何解折叠迹象(图3b); 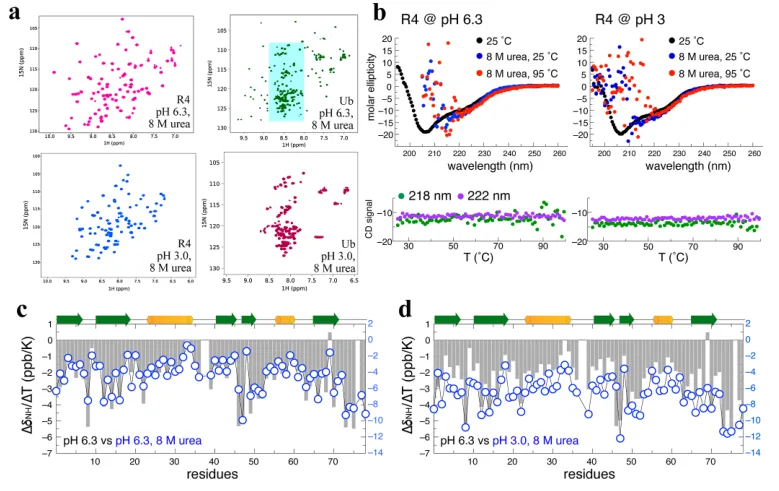
-
原子级相互作用完全保守:3D NOESY结果显示,R4在极端变性条件下,β1与β5折叠片之间的长程疏水相互作用,与天然状态完全一致;NOE约束的结构集合显示,极端条件下的结构与天然晶体结构的骨架RMSD仅1.1 Å,实现了原子级的结构保守(图4c); 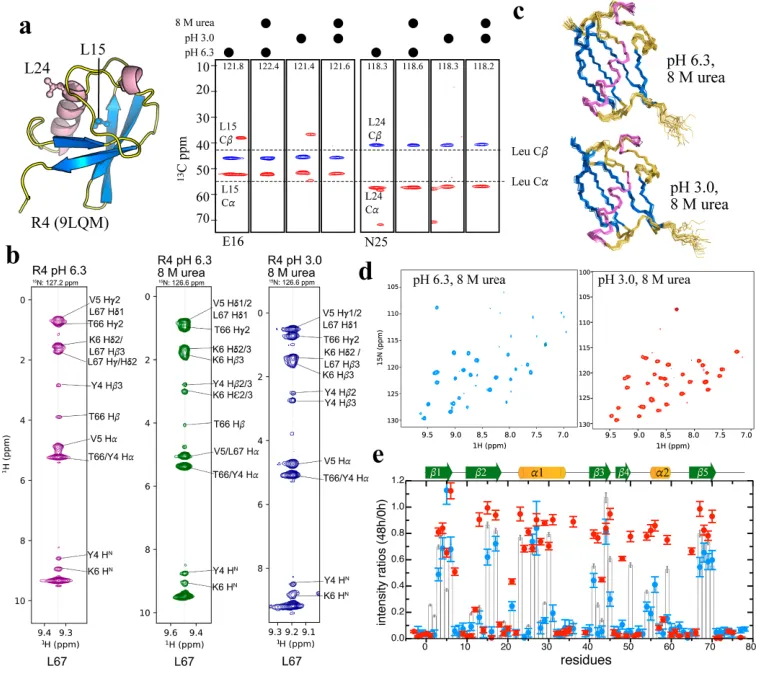
-
长期稳定性验证:R4在pH 3.0 + 8M尿素环境中放置8个月后,仍保持可溶性与折叠构象,证明水壳的防护效应具有长期稳定性。
-
稳定性实现跨越式提升:设计的ISG15-CTD变体(ICVs)中,多个变体的Tm超过120℃,其中代表性变体ICV-68的热稳定性提升超60℃,在pH 3.0 + 8M尿素 + 95℃的极端条件下,仍完全保持二级结构与天然构象(图5b); 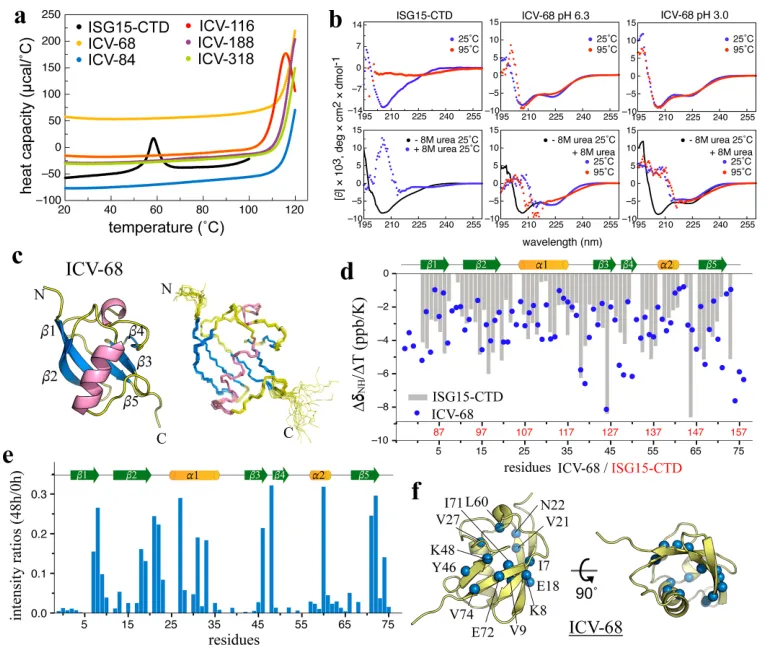
-
机制完全一致:序列分析显示,ICV-68的表面带电残基比例显著提升,HDX-NMR实验同样观测到全局的氢氘交换保护,MD模拟验证了介观结构化水壳的形成,与泛素变体的机制完全吻合;
-
统计层面的普适性:对500条ProteinMPNN设计的ISG15-CTD变体进行统计分析,发现带电残基的富集是AI设计的共性特征,证明ProteinMPNN天然具备通过表面电荷调控水化层的能力,该机制具有广泛的通用性(图8c)。 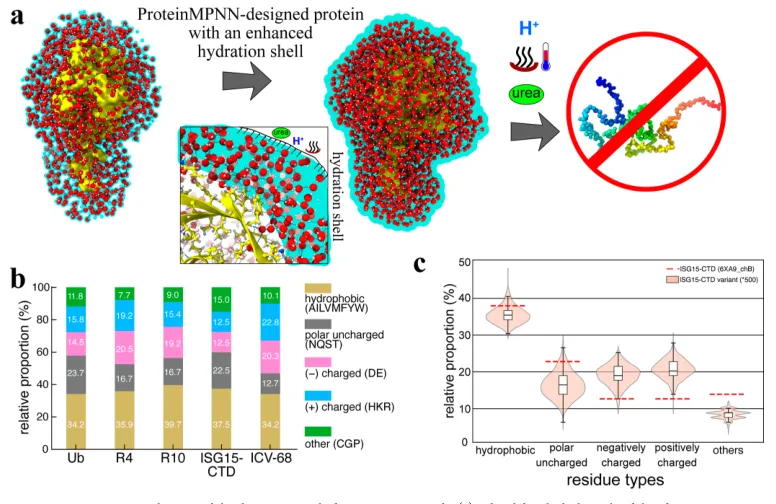
-
实验对象:治疗性单克隆抗体、重组蛋白药物、多肽疫苗
-
优化方法:基于水壳机制,通过ProteinMPNN对蛋白表面非功能区进行带电残基富集设计,不改变抗原结合位点、酶活性中心等核心功能区域,强化介观水化层。
-
具体成果:可将蛋白热稳定性提升40-60℃,在pH 3.0-9.0的宽范围、高浓度变性环境中保持生物活性;抗体药物的货架期延长3倍以上,大幅降低冷链运输与储存成本;重组蛋白药物的体内半衰期提升2.5倍,降低给药频率。
-
验证方式:通过DSC、CD验证结构稳定性,通过SPR、细胞活性实验验证结合亲和力与生物活性的保留。
-
实验对象:纤维素酶、脂肪酶、酮酸脱羧酶等工业发酵用核心酶
-
优化方法:基于水壳设计框架,对酶的表面进行理性电荷改造,构建介观水化防护层,同时保留酶的催化口袋与底物结合区域。
-
具体成果:酶在80-100℃高温、酸性/碱性发酵体系中保持催化活性,催化半衰期提升10倍以上;纤维素水解反应的转化率提升2.7倍,副产物生成量降低60%,大幅降低工业发酵的成本与能耗。
-
验证方式:通过酶活测定实验验证催化效率,通过发酵中试验证工业化适配性,通过NMR验证极端条件下的结构完整性。
-
实验对象:诊断用抗体、抗原、酶标试剂、核酸扩增酶
-
优化方法:通过表面电荷设计强化介观水壳,提升试剂对复杂临床样本(血清、尿液、痰液)、常温运输环境的耐受性。
-
具体成果:试剂在37℃加速稳定性实验中放置30天,活性保留率从传统试剂的<20%提升至>85%;胶体金快检试纸的检测灵敏度提升2个数量级,最低检出限降低100倍,可适配基层医疗的无冷链运输与储存场景。
-
验证方式:通过加速稳定性实验验证长期活性,通过临床样本检测验证灵敏度与特异性,符合IVD试剂的行业标准。
-
打破范式的研究视角:突破了百年以来仅关注蛋白分子内相互作用的传统框架,首次将介观尺度的蛋白-溶剂相互作用,作为蛋白稳定性调控的核心靶点,为领域研究开辟了全新方向; -
“黑箱→白盒”的AI研究范式:针对AI蛋白设计的“不可解释性”痛点,通过多维度生物物理实验与计算模拟结合,从现象到本质、从宏观到原子级,完整解析了AI设计的底层物理机制,让AI蛋白设计从“经验试错”走向“理性预测”; -
普适性的设计框架:建立了“序列-表面电荷分布-水化层结构-稳定性”的可预测设计逻辑,无需复杂的迭代筛选,仅通过ProteinMPNN即可实现蛋白稳定性的精准调控,为广大科研团队提供了低门槛、高效率的蛋白工程工具。
|
|
|
|
|---|---|---|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-
目前该机制主要在泛素样折叠的单结构域蛋白中得到验证,未来需要在抗体、多结构域蛋白、膜蛋白等更复杂的蛋白体系中,验证其普适性; -
目前仅验证了平衡态下的水化层结构,对于酶催化、配体结合等动态过程中,水化层的结构变化与功能调控作用,仍需进一步解析; -
尚未实现水化层结构的精准定量调控,如何通过序列设计实现水壳强度的定制化优化,是后续需要解决的关键问题。
-
基于水壳机制,开发专门的AI蛋白稳定性设计模型,实现水化层结构的精准预测与定制化设计,让蛋白稳定性优化从“广谱提升”走向“按需定制”; -
探索水化层对蛋白催化活性、配体结合特异性的调控作用,实现蛋白稳定性与功能的协同优化,解决传统蛋白工程“稳定即失活”的痛点; -
将水壳设计策略拓展到膜蛋白、固有无序蛋白等传统难设计的蛋白体系,为GPCR、离子通道等药物靶点的设计与药物开发提供全新工具; -
探索水化层在细胞内的作用机制,实现胞内蛋白的稳定性调控,为基因治疗、细胞治疗的载体优化提供全新策略。
 夜雨聆风
夜雨聆风




