Nat Med|AI 决策支持工具|AI 预判手术生死:结直肠癌围手术期能否实现"一人一策"?
|
|
一、为什么这项研究重要?
✦
|
1.领它卡住的是”结直肠癌手术并发症高、再入院率高”的真实痛点。
2. 它是”开发→验证→临床实施→经济学评估”的完整闭环。
|
二、核心结果拆解
✦
|
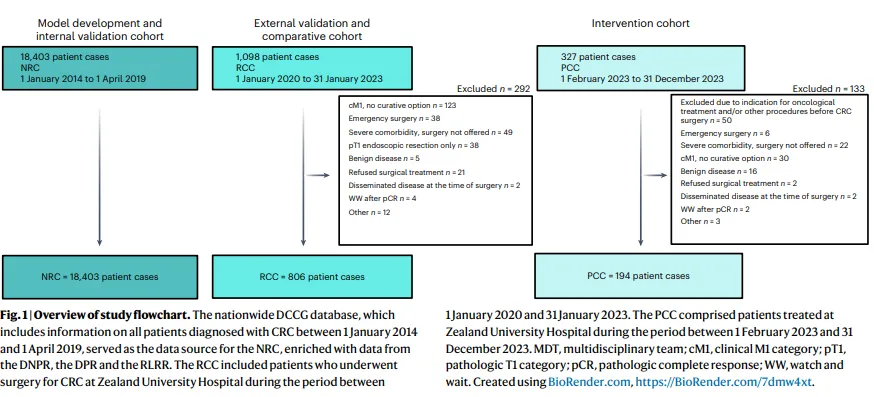
证据点1:这项研究够不够真实? Figure 1· 左侧展示从 8,694 变量 → 68 候选 → 58 最终变量的筛选流程;右侧用四色金字塔或矩阵展示 A/B/C/D 四个风险组的定义阈值及对应的临床干预强度(基础优化 / 标准优化 / 强化优化 / 最高强度优化)。让读者理解”预测模型不是只给数字,而是直接驱动治疗路径”。 模型开发基于丹麦全国结直肠癌登记处 19,403 例患者,从 8,694 个初始候选变量中经临床监督筛选,最终保留 58 个预测因子进入模型。验证采用三轨设计:开发集(13,803 例)、内部时间验证集(4,600 例)、外部验证集(806 例)。临床实施阶段纳入前瞻性队列(PCC)194 例,与回顾性对照队列(RCC)806 例比较。 这意味着: 数据来源国家级登记系统,变量筛选有临床专家参与,验证跨越时间和中心,实施阶段是真实临床决策支持。 证据点 2:核心结果到底强在哪里?
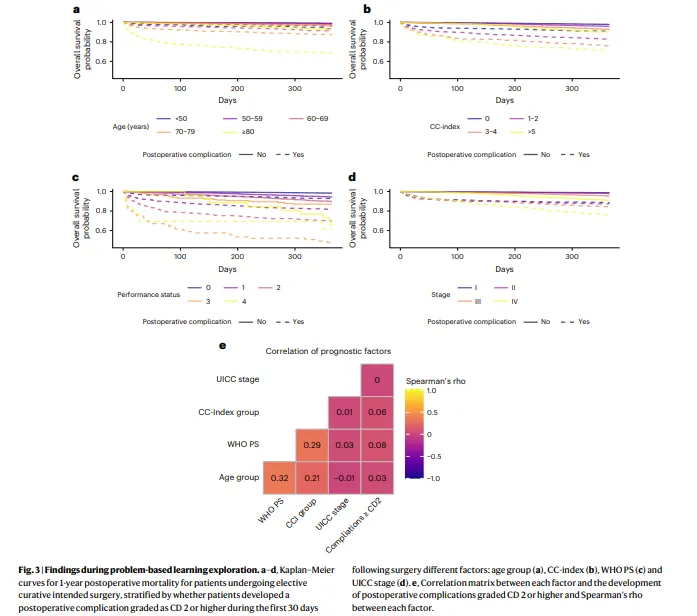
Figure 3· 上半部分展示开发集、内部验证集、外部验证集的三条 ROC 曲线及 AUROC;中间展示校准曲线,标注模型在低风险区校准良好、高风险区略有高估的特点;下半部分用四组柱状图展示 A/B/C/D 风险组在 1 年死亡率、严重并发症、再入院率上的梯度差异。回答”模型准不准”和”分层有没有临床意义”两个问题。 模型区分度良好:AUROC 0.82(开发)/ 0.77(内部验证)/ 0.79(外部验证)。更重要的是风险分层后的临床结局呈现单调递增:D 组(>15% 死亡风险)的 1 年死亡率、严重并发症率、再入院率均显著高于 A 组。 临床实施后的硬终点改善尤为突出:严重术后并发症(CCI>20)发生率从 28.0% 降至 19.1%;任何内科并发症从 37.3% 降至 23.7%;90 天内并发症次数从 0.76 降至 0.48;再入院率从 0.31 降至 0.20。医生对模型风险分层的采纳一致性极高(Kappa=0.926)。 这意味着: AI 不是只预测风险,而是通过标准化风险分层,让”该强化的患者得到强化、该保守的患者避免过度治疗”,从而系统性降低并发症负担。 证据点 3:它真正改变的是什么?
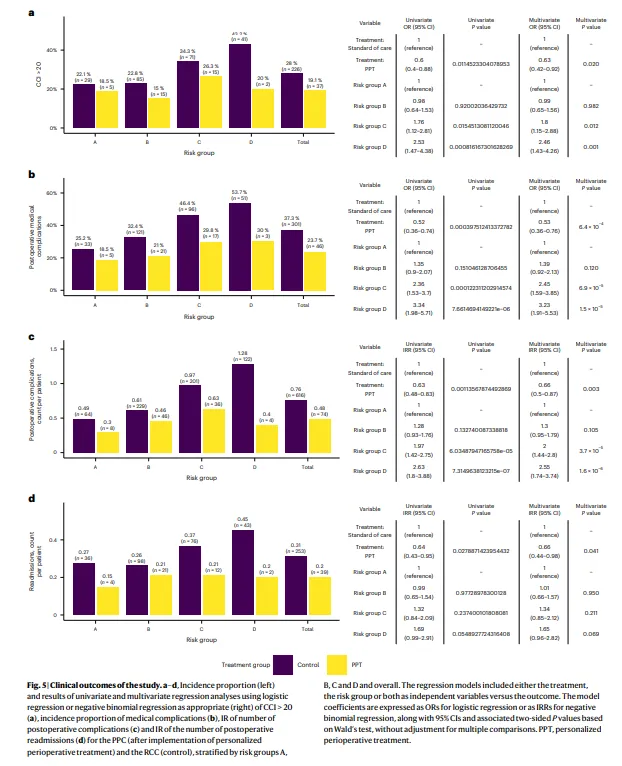
Figure 5· 左侧用分组柱状图对比 PCC(AI 实施后)与 RCC(对照)在严重并发症、任何内科并发症、并发症次数、再入院率四项指标上的绝对发生率;右侧用成本效益平面散点图展示 10,000 次模拟中 AI 策略与标准护理的成本-QALY 分布,突出 96.56% 模拟点落在”降低成本且增加 QALY”的象限。回答”值不值得推广”的问题。 研究不仅做了临床验证,还做了卫生经济学分析。AI 指导的个性化治疗组平均每患者 1 年内医疗成本为 25,159 美元,对照组为 28,007 美元,节省 2,848 美元,同时增加 0.020 QALYs。在 96.56% 的模拟中,AI 策略均呈现”降低成本+改善健康”的优势。 这意味着: 这篇文章直接回答了医院管理者最关心的问题——AI 决策支持不仅改善临床结局,还在短期内实现了成本节省,为大规模推广提供了经济学依据。 |
三、这项研究的启发
✦
|
1️⃣ 它改变的不是一个预测公式,而是”围手术期风险管理”的工作流。传统模式下,术前风险评估依赖医生主观综合判断;AI 模式下,多维度数据被整合为标准化风险分组,直接匹配到预设的优化 bundle 强度。这提示我们:AI 在临床中的最大价值,可能不在于”比医生看得更准”,而在于”让不同医生看得一样准、做得一样规范”。 |
四、王师兄小结
✦
|
这【可借鉴的研究选题方向】 如果你也想在”AI 围手术期决策支持”方向继续做延伸,这篇文章至少给了以下 5 个可借鉴方向:
这些方向都符合本文的成功范式:以国家级真实世界数据开发模型,经多轨验证后嵌入临床路径,用前后对照队列证明硬终点改善,并辅以卫生经济学分析支撑规模化决策。 |

— END —
✦ 永远相信美好的事情即将发生 ✦
✦ 永远相信投稿的文章即将接收 ✦
AI Exploring Everyday
专注分享有趣研究
追踪最新科研进展
期待启发科研思路
👉 关注「光速科研AI」
 夜雨聆风
夜雨聆风