2026年1月,国家药品监督管理局药品审评中心(CDE)正式发布《AI辅助新药研发技术指导原则(征求意见稿)》,这是中国首个系统规范人工智能在药物研发全流程中应用的纲领性技术文件。该原则立足AI技术特性与药物研发专业性,明确以人为本、风险导向等关键准则,既为监管机构、国际标准组织及相关方搭建了协作框架,也规范了数据治理、模型开发等核心环节,推动AI在药物研发中的负责任创新与规范化应用。与此同时,2026年4月2日,国家药监局进一步发布《关于“人工智能+药品监管”的实施意见》,提出了2030年初建AI与监管融合创新体系、2035年建成智慧治理新格局的十年发展目标。
一、政策背景:
中国AI制药监管体系的历史性构建
从智慧监管到AI深度融合
人工智能技术与生物医药产业的深度融合正在重塑全球制药行业的创新格局。根据中商产业研究院数据,2023年全球AI制药市场规模为13.8亿美元,预计2026年将达到29.94亿美元,2021—2026年年复合增长率达30.47%。中国AI制药市场同步高速发展,2020年市场规模为0.8亿元,2023年跃升至4.1亿元,2024年达到5.6亿元,同比增长36.59%,2025年突破6亿元。
政策层面,中美两国密集出台利好政策。2025年1月,美国FDA发布《考虑使用人工智能支持药品和生物制品监管决策》指南草案,提供了基于风险的框架来评估和建立AI模型的可信度,这是FDA关于AI在药物开发中的首次正式行动。中国方面,2025年1月国务院办公厅发布《关于全面深化药品医疗器械监管改革促进医药产业高质量发展的意见》,为监管现代化确立总体目标框架;2026年4月,国家药监局发布《关于“人工智能+药品监管”的实施意见》,提出监管数智化的七大重点方向和五项基础支撑任务。
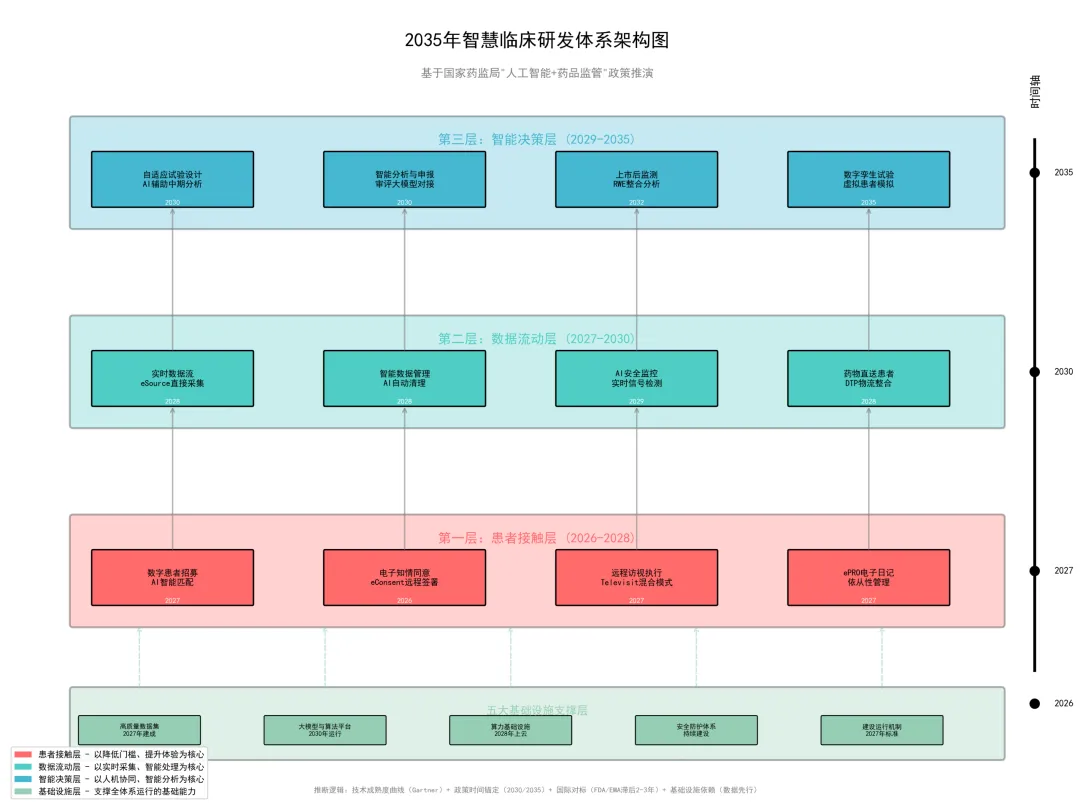
▲图 1:2035智慧临床研发体系架构图——政策驱动下AI制药的三层架构与五大基础设施
《AI辅助新药研发技术指导原则》的核心定位
CDE发布的《AI辅助新药研发技术指导原则》是上述宏观政策框架在药物研发具体环节的制度性落地。该原则明确了以下核心定位:
01
人机协同的基本范式。
AI是辅助工具,而非替代决策主体。原则要求建立“数智赋能、人工复核、全程留痕”的人机协同机制,强调模型输出的可解释性和可追溯性。
02
风险分层的管理框架。
借鉴FDA指南的“基于风险的可信度评估框架”,原则对AI模型在不同研发阶段的应用提出了差异化的验证要求。模型对监管决策的影响越大,所需的可信度证据越充分。
03
数据治理的优先地位。
原则将高质量数据集建设列为最优先的基础支撑任务,“场景驱动、急用先行”,围绕核心业务场景分阶段推进数据集建设。
04
全生命周期覆盖。
原则涵盖靶点发现、先导化合物优化、临床前研究、临床试验设计、生产工艺开发到上市后监测的全链条应用场景。
二、AI制药的技术演进:
从结构预测到分子生成
蛋白质结构预测的突破性进展
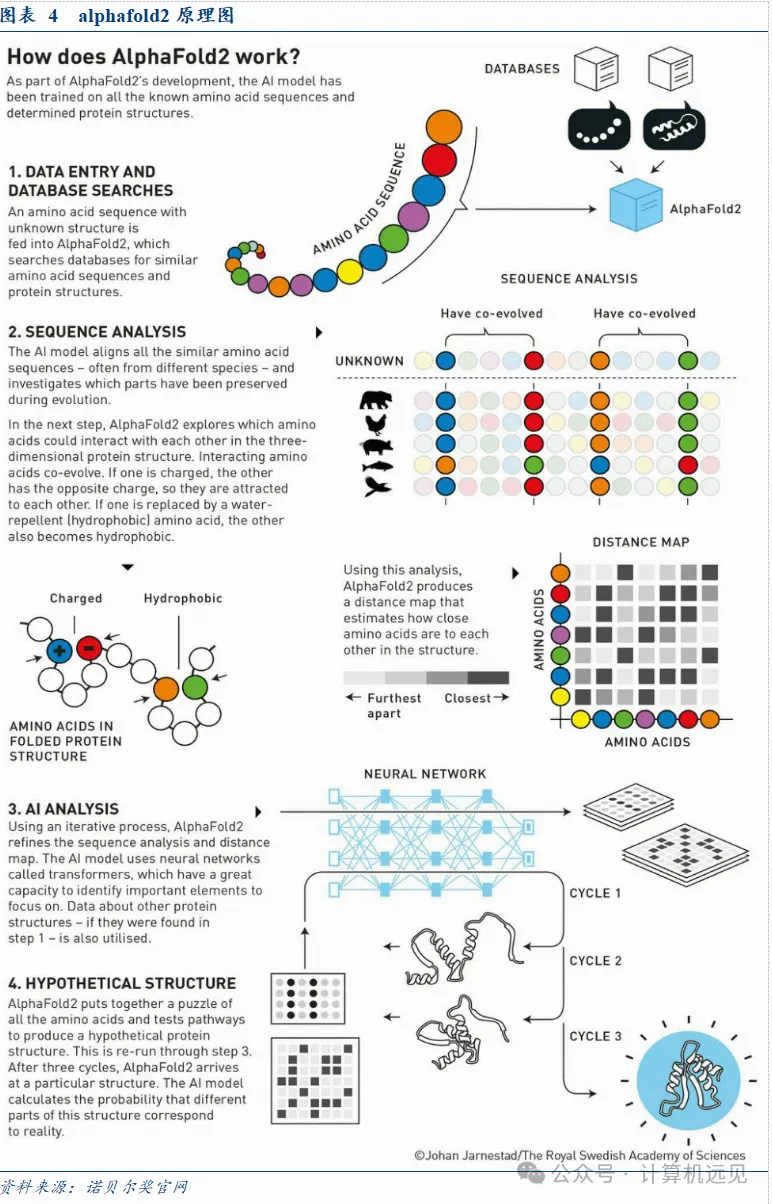
AI制药行业的技术演进正经历从单一算法驱动向多模态智能融合的深刻变革。这一变革的里程碑式突破来自DeepMind的AlphaFold系列。2020年推出的AlphaFold2在第14届CASP竞赛中实现了原子级精度的蛋白质结构预测(GDT分数突破90分),首次证明AI能够媲美X射线晶体学和冷冻电镜等实验方法,将原本需要数月甚至数年、花费数百万美元的结构解析过程压缩至数小时。
2024年发布的AlphaFold3更引入扩散模型架构,将预测能力扩展至蛋白质-配体、抗体-抗原等复合物相互作用,为基于结构的药物设计提供了动态化、精细化的底层基础设施。中国科学院上海药物研究所徐华强团队在《Acta Pharmacologica Sinica》发表的研究系统评估了AlphaFold3在GPCR-小分子复合物预测中的表现:在整体受体骨架预测方面,AlphaFold3表现优秀,Cα均方根偏差(RMSD)平均仅为0.98 Å,优于AlphaFold2的1.64 Å。但在小分子配体定位方面,AlphaFold3表现出显著不稳定性,配体重原子RMSD平均高达4.28 ± 5.77 Å,尤其在新型配体和别构调节剂上更为显著。这一发现提示:尽管AlphaFold3在结构预测上实现了革命性突破,但在真实药物开发场景中仍需谨慎验证,特别是对于新颖或未充分表征的结合模式。

▲图 AlphaFold系列技术演进对比图
生成式AI驱动的分子设计
在分子设计领域,生成式AI技术经历了从GANs到Transformer的范式跃迁。2016年英矽智能率先将生成对抗网络应用于靶点发现,2019年其开发的生成式张量强化学习模型GENTRL仅用21天即完成DDR1激酶抑制剂分子的设计、合成与体外验证,相比传统研发周期提速15倍。基于Transformer架构的Pharma.AI平台更将“从靶点发现到临床候选药物确定”的全流程压缩至18个月——而传统流程通常需要4.5年。
在新型药物模式方面,AlphaFold3已展现出对PROTAC(蛋白降解靶向嵌合体)三元复合物的建模能力。2025年发表于《Digital Discovery》的研究系统评估了AlphaFold3在62个PROTAC复合物上的表现:AlphaFold3在配体定位方面表现优异,产生了33个RMSD < 1 Å的三元复合物和46个RMSD < 4 Å的复合物,为计算靶向蛋白降解药物设计提供了新的技术路径。
▲图 生成式AI分子设计技术演进时间线——从GANs到Transformer的范式跃迁
三、AI制药的产业实践:
从研发效率到临床验证
研发效率的量级提升
AI技术在药物研发各环节展现出显著的优势。根据英伟达公开信息,早期发现阶段耗时可缩短至原先的三分之一,成本降至二百分之一;药物发现与临床前研究周期整体缩减近40%。根据TechEmergence数据,AI技术可将临床阶段新药研发成功率从12%提升至约14%。更令人瞩目的是,ScienceDirect发表的一项综合评述指出,与传统行业基准相比,AI驱动的新药在I期临床试验中的成功率高达80-90%。
在临床试验环节,中国电信发布的“AI药物研发公共服务平台”试运行期间已服务13家创新药企、20余项临床试验,受试者患者招募准确率从25%升至85%,实现3倍效能跃升。
标志性案例:Rentosertib
2025年6月3日,一个里程碑时刻被载入AI制药史册:英矽智能在《Nature Medicine》上发表了业界首个完成临床药效概念验证的AI药物——TNIK抑制剂Rentosertib(ISM001-055)在IIa期临床试验的安全性和有效性数据。这是全球第一个在靶点发现和分子生成两端皆由生成式AI平台主导的候选分子,并已进入多中心双盲随机对照的临床IIa期试验。
研发流程与效率:Rentosertib的诞生是英矽智能Pharma.AI平台两个核心子模块协同作用的结果——PandaOmics(靶点发现引擎)整合深度学习与因果推断算法,从海量多组学数据中精准锁定TNIK为特发性肺纤维化的潜在抗纤维化靶点;Chemistry42(生成式分子设计模块)整合40多种分子生成与筛选模型,在多重约束条件下高效筛选候选分子。最终,英矽智能仅合成了少于80个分子,就确定了Rentosertib作为临床前候选药物。相比传统早期药物发现所需的2.5至4年时间,英矽智能自2021年至2024年间提名的22个候选新药项目,平均仅用12至18个月便实现了从项目立项到临床前候选分子的转化,整体研发成本也从传统的4.14亿美元大幅降低至20万美元。
临床数据与疗效信号:IIa期临床试验数据显示,Rentosertib达到主要研究终点,即具有可控的安全性和耐受性。接受60 mg每日一次Rentosertib治疗的患者,用力肺活量(FVC)平均改善幅度最大,FVC均值增加98.4毫升,而对照组FVC均值下降20.3毫升。研究中进行的探索性生物标志物分析进一步验证了通过AI方法发现的TNIK靶点的生物学机制,研究结果支持Rentosertib具有潜在的抗纤维化和抗炎作用。
英矽智能CEO Alex Zhavoronkov在2025年BIO USA大会上宣告:“我们创造了第一个案例,其中AI发现的靶点和AI设计的分子在人体中证明了疗效。”
目前,英矽智能由AI驱动发现的产品管线中已有10个分子获得临床试验许可。2025年11月,英矽智能与礼来达成授权及药物研发合作,获得1.15亿美元首付款,交易总价值最高可达约27.5亿美元,充分证明了AI制药能力已获得全球顶级药企的高度认可。
产业生态的全面繁荣
中国AI制药产业链已形成“上游数据算力支撑——中游AI平台赋能——下游药企应用落地”的完整分工体系。在中游平台层,晶泰科技依托“AI模型预测-机器人执行湿实验-数据反哺AI模型训练-多智能体调度”的研发飞轮,2025年全年营收达8.03亿元,同比增长201.2%,首次实现年度盈利,成为AI应用领域率先盈利的港股上市公司。其药物发现解决方案业务收入5.38亿元,同比增长418.9%,客户覆盖17家全球排名前20的国际药企。2025年8月,晶泰科技与DoveTree签署总订单规模约470亿港元(59.9亿美元)的管线合作协议,创下AI制药领域订单规模的纪录。
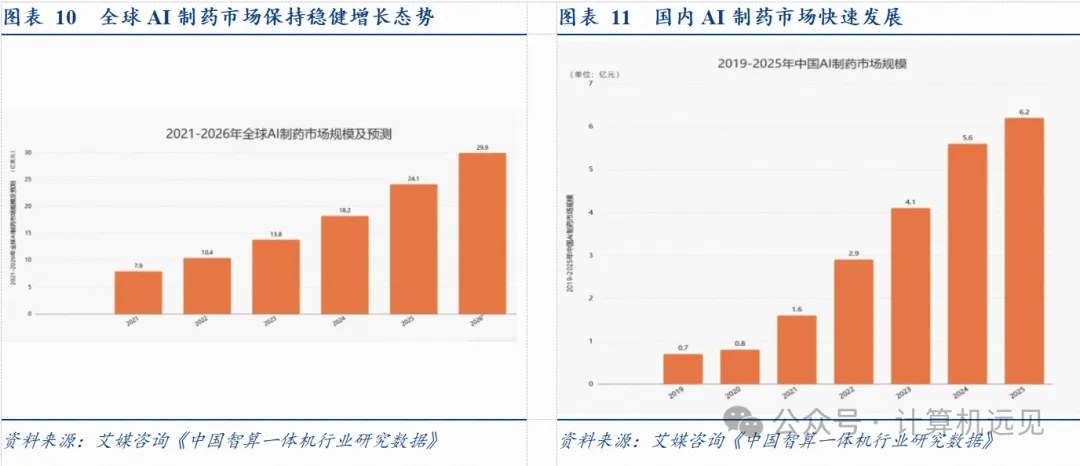
▲图 全球及中国AI制药市场规模增长趋势(2020-2026E)
四、指导原则的核心要点解读
01
数据治理:AI制药的“地基”
指导原则将“高质量数据集建设”列为最优先的基础支撑任务,体现了“基础设施决定上层建筑”的核心逻辑。这一导向与国际监管趋势高度一致:FDA指南强调,模型训练所用数据的质量、相关性和代表性直接影响AI模型的可信度。
当前行业数据面临质量参差、标准不一、孤岛林立的结构性挑战。指导原则要求按照“场景驱动、急用先行”原则,围绕药品全生命周期监管中的核心业务场景及AI应用的实际需求,分阶段分步骤推进药品监管高质量数据集建设。在实践层面,“联邦学习+隐私计算”正成为数据协作的主流范式,允许多方在不共享原始数据的前提下联合训练模型。头部企业如Recursion已转向“自动化湿实验”构建数据飞轮:通过“AI设计-机器人执行-实时反馈”的闭环,以标准化、高通量方式自主产生高质量专有数据,从“数据消费者”转型为“数据生产者”。
02
模型可信度与验证体系
指导原则要求加强AI风险监测评估,制定算法透明度要求和模型验证规范,加强模型算法、数据资源、基础设施、应用系统等安全能力建设。这是AI制药监管框架的核心支柱。FDA的指南提出了基于风险的可信度评估框架,要求申办者根据模型对监管决策的影响程度确定所需的验证证据水平。
中国科学界的评估研究为模型验证提供了重要参考。中国科学院上海药物研究所的研究发现,AlphaFold3在预测数据库中已有同类复合物时表现较好,而在面对新型化合物或未被充分表征的结合模式时预测准确性大幅下降。对于别构调节剂复合物,AlphaFold3的预测精度尤其受限——几乎所有评估案例中都未能正确识别实际的结合口袋,平均RMSD达到11.72 ± 12.56 Å。这些发现为CDE制定模型验证规范提供了关键的科学依据:不同应用场景下的AI模型需采用差异化的验证标准,高风险场景需配套更严格的实验验证。
03
临床试验的AI应用规范
指导原则在研制环节明确要求“持续推进临床试验数据治理规范化,研究制定临床试验电子化记录技术指南、计算机化系统验证指南等配套规范”。这标志着中国在AI辅助临床试验方面的监管框架正在加速构建。
FDA的AI开发指南已覆盖非临床、临床、上市后和制造等全生命周期阶段。FDA披露,从2016年至2023年,CDER已收到超过500个包含AI组件的提交申请,且数量呈指数级增长。这一趋势同样反映在中国市场:IQVIA的AI患者招募工具使招募周期缩短30-50%;Medidata的智能数据监控将数据清理时间减少40%;复星医药通过AI优化临床试验方案,方案修订次数降低25%。
中国电信AI药物研发公共服务平台在受试者患者招募方面的突破——准确率从25%升至85%,实现3倍效能跃升——说明AI赋能的临床试验工具已进入实际落地阶段,而指导原则的出台恰为这些创新实践提供了明确的合规边界。

▲图 AI技术在药物研发各环节的效率提升——早期发现耗时缩短至1/3、成本降至1/200
五、挑战与展望:
AI制药的“未完成时”
1. 科学层面的局限性
尽管AI在药物研发中展现出巨大潜力,但科学层面的局限性依然不容忽视。AlphaFold3的研究评估清晰表明,现有AI模型在处理新颖配体结合模式、别构调节机制和动态构象变化方面仍有显著不足。这意味着AI目前更擅长“已知空间的加速搜索”,而非“未知空间的突破性发现”。
此外,AI模型的可解释性仍是制约其在高风险监管场景中应用的核心瓶颈。指导原则对“模型可解释性”的强调,正是对这一挑战的回应。
2. 监管与产业的协同进化
指导原则的发布标志着中国AI制药监管框架从“探索期”进入“规范期”,但真正实现“监管与产业数智化协同发展”仍需多方共同努力。药监部门需要在鼓励创新与保障安全之间找到动态平衡;制药企业需要从战略层面布局数据治理和AI能力建设;技术服务商需要将算法创新与监管合规要求深度结合。
2030年是一个关键节点——届时“人工智能与药品监管融合创新体系”将初步构建,审评审批大模型等核心应用将全面运行。而2035年,“数智驱动、智能敏捷、自主可控、生态协同的智慧化药品安全治理新格局”将基本形成。
3. 企业的行动路线图
面对政策窗口期,建议制药企业从以下维度制定行动路线图:
01
立即启动数据治理审计。 高质量数据集是指导原则五大基础支撑之首,企业的试验数据如果不标准、不可追溯,将无法被AI系统有效分析。建议在6个月内完成CDISC标准的全面审计,输出《数据标准化差距分析报告》。
02
建立AI模型验证与评估体系。 按照指导原则的风险分层框架,对自身使用的AI工具进行可信度评估,建立模型版本管理和验证文档。
03
布局AI赋能的关键场景。 优先在AI患者招募、智能数据管理和电子化知情同意(eConsent)等相对成熟且收益明确的场景进行试点,积累经验后逐步拓展至更复杂的应用场景。
04
加强跨学科人才培养。 提升团队的数字思维、数字技能和数字素养,培养既懂药物研发又理解AI技术的复合型人才。
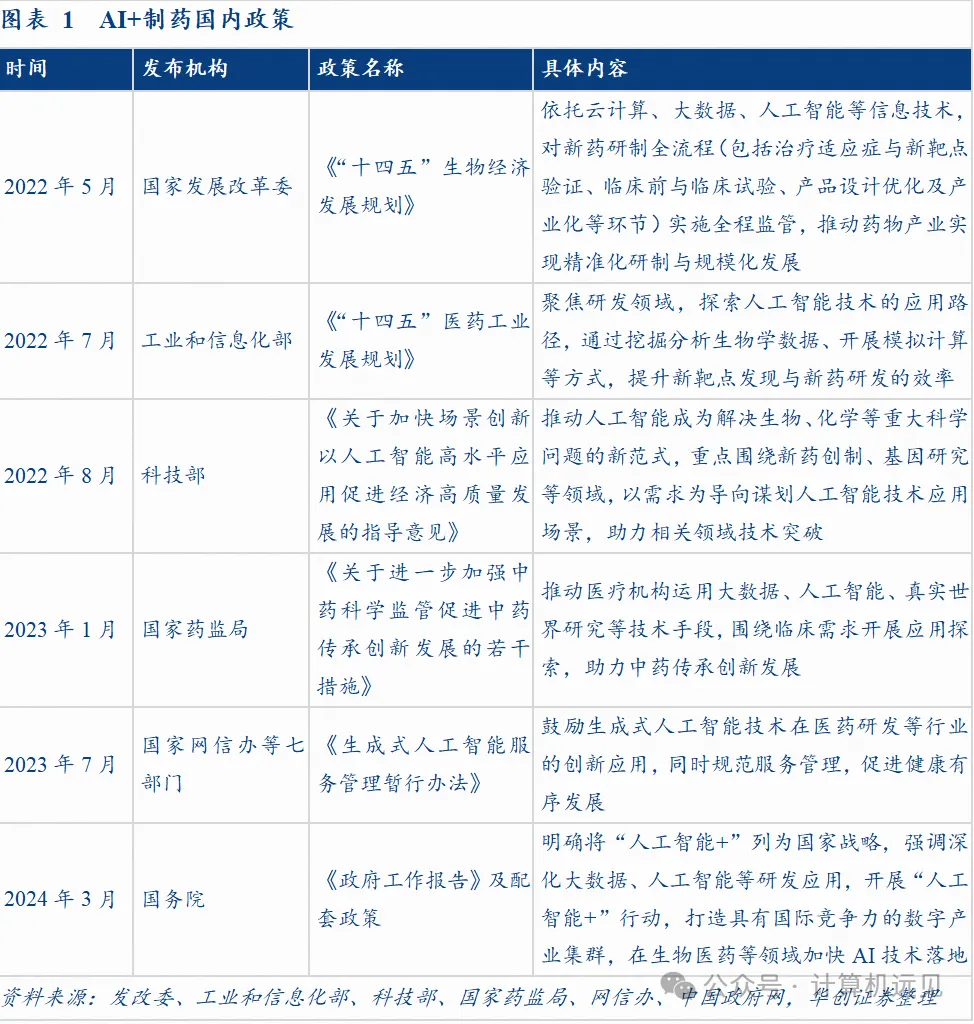
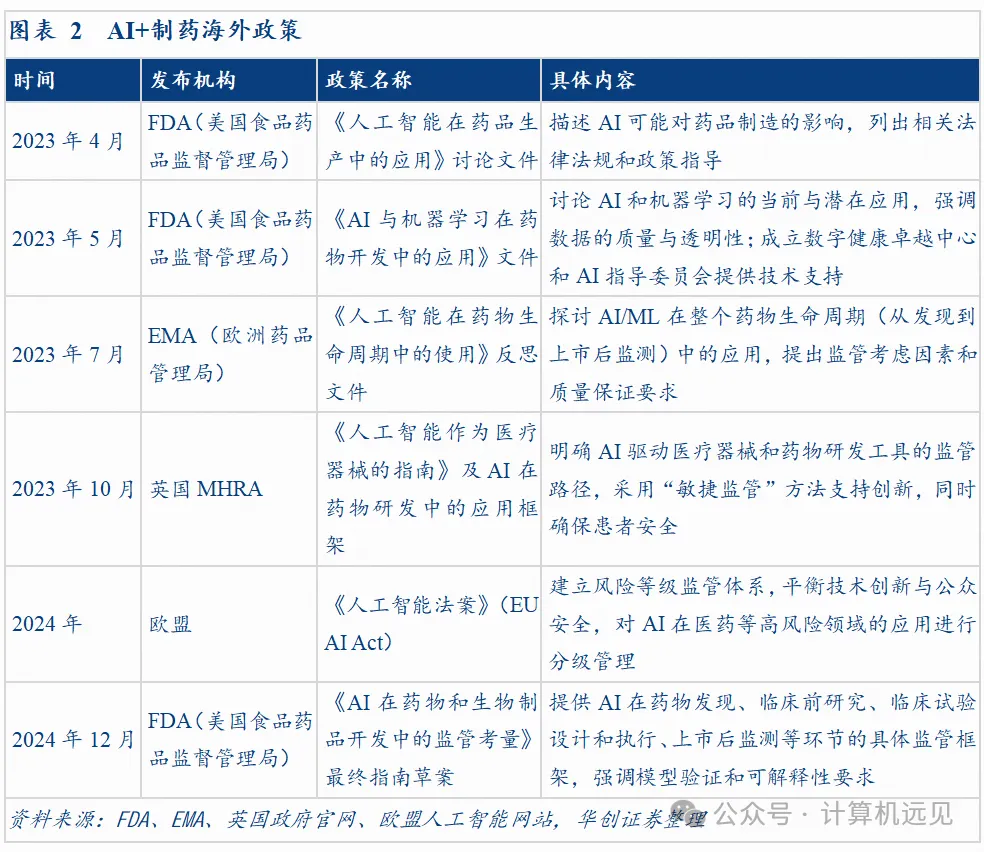
▲图 中美AI制药监管政策演进时间线(2022-2026)
旭瑞生物始终致力于生命科学前沿技术的研究与应用转化。我们相信,AI技术不是冰冷的算法,而是加速创新药走向患者的“催化剂”。我们将持续跟踪《AI辅助新药研发技术指导原则》的实施动态,深耕AI驱动药物研发的关键技术领域,为行业提供高质量的数据治理方案与智能化研发服务。以科学严谨的态度拥抱技术变革,以患者需求为核心驱动产业创新——旭瑞生物将持续进行AI制药领域的深度研究,为推动中国创新药走向世界、为生命科学与人类健康事业做出应有贡献。

 夜雨聆风
夜雨聆风