文档内容
专练 45 盐类水解、离子浓度的比较
授课提示:对应学生用书89页
1.[2024·安徽卷]环境保护工程师研究利用NaS、FeS和HS处理水样中的Cd2+。
2 2
已知25 ℃时,HS饱和溶液浓度约为0.1 mol·L-1,K (H S)=10-6.97,K (H S)=10-
2 a1 2 a2 2
12.90,K (FeS)=10-17.20,K (CdS)=10-26.10。
sp sp
下列说法错误的是( )
A.NaS溶液中:c(H+)+c(Na+)=c(OH-)+c(HS-)+2c(S2-)
2
B.0.01 mol·L-1 Na S溶液中:c(Na+)>c(S2-)>c(OH-)>c(HS-)
2
C.向c(Cd2+)=0.01 mol·L-1的溶液中加入FeS,可使c(Cd2+)<10-8 mol·L-1
D.向 c(Cd2+)=0.01 mol·L-1的溶液中通入 HS 气体至饱和,所得溶液中:c(H
2
+)>c(Cd2+)
答案:B
解析:NaS溶液中存在电荷守恒:c(Na+)+c(H+)=c(OH-)+c(HS-)+2c(S2-),A项正
2
确;Na
2
S溶液中存在水解平衡:S2-+H
2
O⇌HS-+OH-、HS-+H
2
O⇌H
2
S+OH-,且第一
步水解程度远大于第二步水解程度,K (S2-)====10-1.10,又c(HS-)一定小于0.01 mol·L
h
-1,则>>1,故c(OH-)>c(S2-),B项错误;由题给条件可知,K (FeS)>K (CdS),向c(Cd2
sp sp
+)=0.01 mol·L-1的溶液中加入FeS,发生沉淀转化:Cd2++FeS⇌CdS+Fe2+,该反应的平
衡常数K=====108.90>105,反应能进行完全,最后所得溶液为CdS的饱和溶液,则溶
液中c(Cd2+)==10-13.05 mol·L-1<10-8 mol·L-1,故C项正确;向c(Cd2+)=0.01 mol·L-1的
溶液中通入H
2
S气体至饱和,发生反应:Cd2++H
2
S⇌CdS+2H+,该反应的平衡常数K=
===106.23>105,反应能进行完全,所得溶液中c(H+)=0.02 mol·L-1,此时溶液中HS达
2
到饱和,c(H S)=0.1 mol·L-1,代入K===106.23,解得c(Cd2+)=4×10-9.23 mol·L-1c(NHCHCOOH)·c(NH CHCOO-),D错误。
2 2 2 2
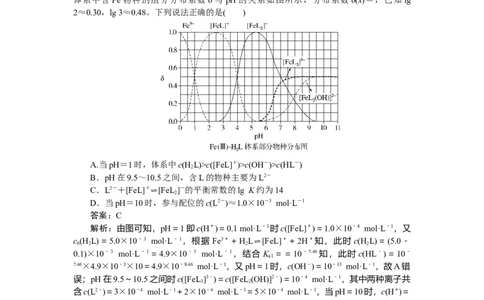
3.[2023·湖北卷]HL为某邻苯二酚类配体,其 pK =7.46,pK =12.4。常温下构建
2 a1 a2
Fe(Ⅲ)—H L溶液体系,其中c(Fe3+)=2.0×10-4 mol·L-1,c(H L)=5.0×10-3 mol·L-1。
2 0 0 2
体系中含 Fe 物种的组分分布系数 δ与pH的关系如图所示,分布系数 δ(x)=,已知 lg
2≈0.30,lg 3≈0.48。下列说法正确的是( )
A.当pH=1时,体系中c(H L)>c([FeL]+)>c(OH-)>c(HL-)
2
B.pH在9.5~10.5之间,含L的物种主要为L2-
C.L2-+[FeL]+ ⇌[FeL
2
]-的平衡常数的lg K约为14
D.当pH=10时,参与配位的c(L2-)≈1.0×10-3 mol·L-1
答案:C
解析:由图可知,pH=1即c(H+)=0.1 mol·L-1时c([FeL]+)=1.0×10-4 mol·L-1,又
c
0
(H
2
L)=5.0×10-3 mol·L-1,根据 Fe3++H
2
L⇌[FeL]++2H+知,此时 c(H
2
L)=(5.0-
0.1)×10-3 mol·L-1=4.9×10-3 mol·L-1,结合 K ==10-7.46知,此时 c(HL-)=10-
a1
7.46×4.9×10-3×10=4.9×10-9.46 mol·L-1,又pH=1时,c(OH-)=10-13 mol·L-1,故A错
误;pH在9.5~10.5之间时c([FeL ]3-)=c([FeL (OH)]2-)=10-4 mol·L-1,其中两种离子共
3 2
含c(L2-)=3×10-4 mol·L-1+2×10-4 mol·L-1=5×10-4 mol·L-1,当pH=10时,c(H+)=
10-10 mol·L-1,根据K ===10-7.46,c(HL-)=102.54c(H L),即c(HL-)>c(H L),由K =
a1 2 2 a2
=10-12.4,得c(HL-)=102.4c(L2-),即c(HL-)>c(L2-),B错误;该反应的平衡常数K=,
由题图知,当 c([FeL ]-)=c([FeL]+)时,pH=4,由 K ·K =10-19.86=得①式 10-
2 a1 a2
19.86×c(H L)=10-8c(L2-) ①,此时 c(H L)=5.0×10-3 mol·L-1-3×10-4 mol·L-1=
2 2
4.7×10-3 mol·L-1,代入①式,c(L2-)==4.7×10-14.86 mol·L-1,则K==2.1×1013.86,故
lg K=13.86+lg 2.1=14,C正确;pH=10时c([FeL ]3-)=c([FeL (OH)]2-)=1×10-4 mol·L
3 2
-1,则参与配位的L2-的总浓度为3×10-4 mol·L-1+2×10-4 mol·L-1=5×10-4 mol·L-1,
D错误。
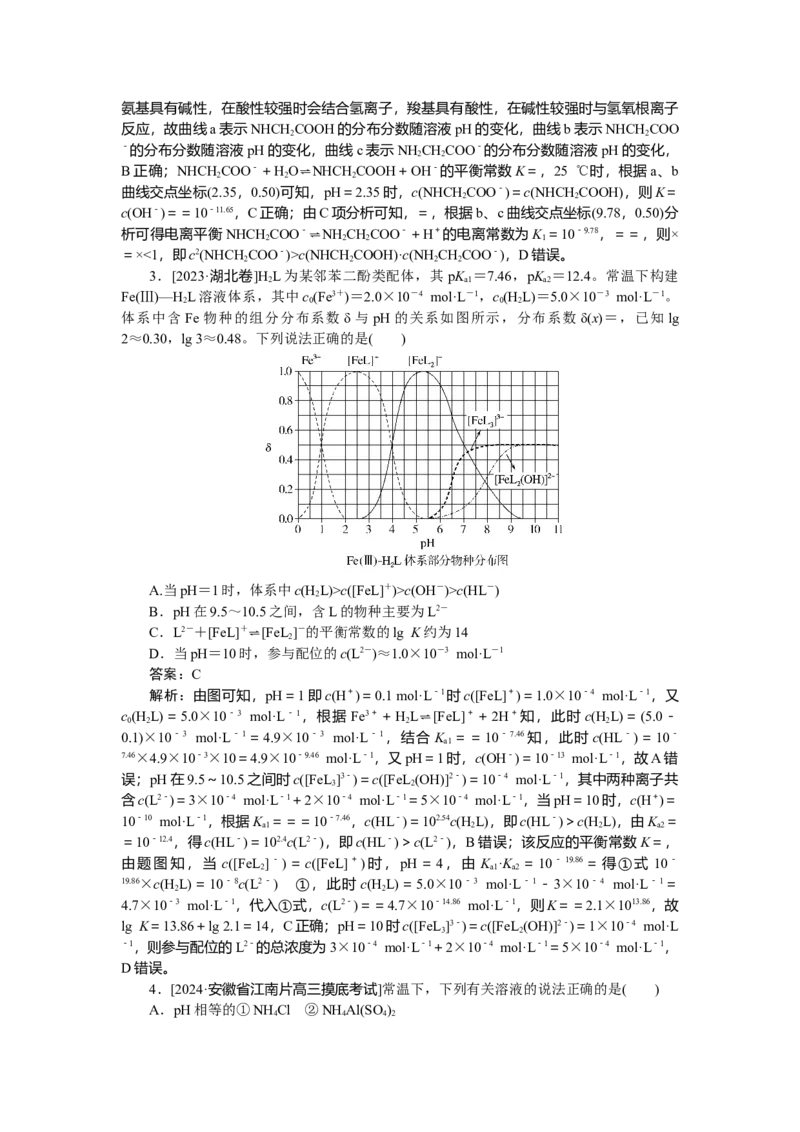
4.[2024·安徽省江南片高三摸底考试]常温下,下列有关溶液的说法正确的是( )
A.pH相等的①NH Cl ②NH Al(SO )
4 4 4 2③NH HSO 溶液:浓度的大小顺序为①>②>③
4 4
B.HA 的电离常数 K =4.93×10-10,则等浓度的 NaA、HA 混合溶液中:c(Na+)
a
>c(HA)>c(A-)
C.NaHCO 溶液加水稀释,c(Na+)与c(HCO)的比值将减小
3
D.已知在相同条件下酸性HF>CH COOH,则物质的量浓度相等的NaF与CHCOOK
3 3
溶液中:c(Na+)-c(F-) >c(K+)-c(CHCOO-)
3
答案:A
解析:①NH Cl中Cl-不影响NH水解,②NH Al(SO ) 中Al3+水解抑制NH水解,
4 4 4 2
③NH HSO 溶液中NH HSO 电离产生的H+抑制NH水解,而且比②中Al3+水解对NH水
4 4 4 4
解的影响程度大,所以pH相等的①NH Cl ②NH Al(SO ) ③NH HSO 溶液:浓度的大
4 4 4 2 4 4
小顺序为①>②>③,A正确;NaA中水解平衡常数K ===2.02×10-5,水解平衡常数大
b
于电离平衡常数,则等浓度的 NaA、HA混合溶液中:c(HA)>c(Na+)>c(A-),B错误;
NaHCO 溶液加水稀释,促进 HCO 的水解,n(HCO)减小,n(Na+)不变,则 c(Na+)与
3
c(HCO)的比值将增大, C错误; 根据越弱越水解可知CHCOOK碱性比NaF碱性强,根
3
据电荷守恒 CHCOOK 溶液中 c(CHCOO-)+c(OH-)=c(K+)+c(H+),所以 c(K+)-
3 3
c(CHCOO-)=c(OH-)-c(H+),NaF溶液中c(F-)+c(OH-)=c(Na+)+c(H+),所以c(Na+)
3
-c(F-)=c(OH-)-c(H+),CHCOOK溶液碱性强,CHCOOK溶液中c(OH-)-c(H+)大于
3 3
NaF溶液中c(OH-)-c(H+),c(K+)-c(CHCOO-)>c(Na+)-c(F-),D错误。
3
5.
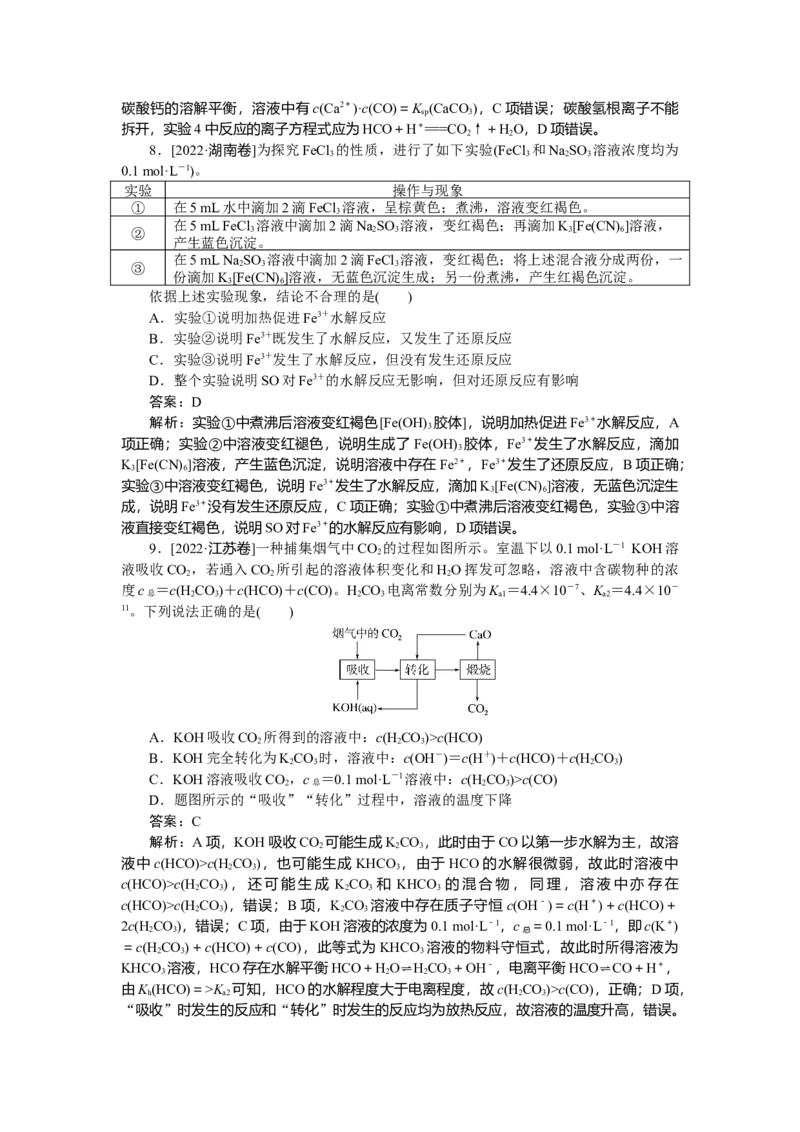
[2024·专题模块测试]常温下,将CO 通入2 L pH=12的KOH溶液中,溶液中水电离
2
出的OH-离子浓度(c)与通入的CO 的体积(V)的关系如图所示。下列叙述不正确的是( )
2
A.a点溶液中:水电离出的c(H+)=1×10-12 mol·L-1
B.b点溶液中:c(H+)=1×10-7 mol·L-1
C.c点溶液中:c(K+)=2[c(CO)+c(HCO)+c(H CO)]
2 3
D.d点溶液中:c(K+)=2c(CO)+c(HCO)
答案:B
解析:a点溶质为KOH,pH=12,此时溶液中H+全来自水的电离,因此水电离出的
c(H+)=1×10-12 mol·L-1,故A项正确;c点溶液中,水电离出的OH-离子浓度最大,说
明此时的溶液是碳酸钾溶液,则b点溶液是KCO 和KOH的混合溶液,溶液显碱性,因此
2 3
c(H+)<1×10-7 mol·L-1,故B项错误;c点溶液为KCO 溶液,因此根据物料守恒可知
2 3
c(K+)=2[c(CO)+c(HCO)+c(H CO)],故C项正确;d点溶液为中性溶液,即 c(H+)=
2 3
c(OH-),由电荷守恒可得c(K+)=2c(CO)+c(HCO),故D项正确。
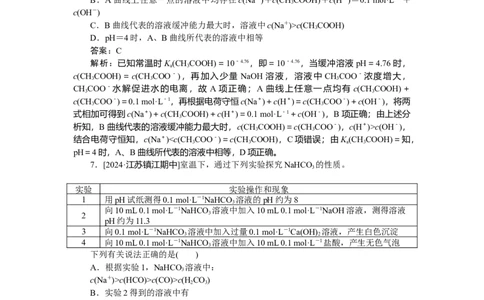
6.[2024·兰州市高三诊断考试]可用缓冲容量β来描述缓冲溶液的缓冲能力大小,β越
大,缓冲能力越大。如图是常温下CHCOOH和CHCOONa组成的缓冲溶液的βpH关系图,
3 3
其中 A、B 两条曲线分别对应 c =c(CHCOOH)+c(CHCOO-)=0.1 mol·L-1和 c =
总 3 3 总
c(CHCOOH)+c(CHCOO-)=0.2 mol·L-1。已知常温下,K(CHCOOH)=10-4.76,下列说
3 3 a 3
法不正确的是( )A.向pH=4.76的上述缓冲溶液中加入少量NaOH溶液,水的电离程度会增大
B.A曲线上任意一点的溶液中均存在c(Na+)+c(CHCOOH)+c(H+)=0.1 mol·L-1+
3
c(OH-)
C.B曲线代表的溶液缓冲能力最大时,溶液中c(Na+)>c(CHCOOH)
3
D.pH=4时,A、B曲线所代表的溶液中相等
答案:C
解析:已知常温时K(CHCOOH)=10-4.76,即=10-4.76,当缓冲溶液pH=4.76时,
a 3
c(CHCOOH)=c(CHCOO-),再加入少量 NaOH 溶液,溶液中 CHCOO-浓度增大,
3 3 3
CHCOO-水解促进水的电离,故 A 项正确;A 曲线上任意一点均有 c(CHCOOH)+
3 3
c(CHCOO-)=0.1 mol·L-1,再根据电荷守恒c(Na+)+c(H+)=c(CHCOO-)+c(OH-),将两
3 3
式相加可得到c(Na+)+c(CHCOOH)+c(H+)=0.1 mol·L-1+c(OH-),B项正确;由上述分
3
析知,B曲线代表的溶液缓冲能力最大时,c(CHCOOH)=c(CHCOO-),c(H+)>c(OH-),
3 3
结合电荷守恒知,c(Na+)c(HCO)>c(CO)>c(H CO)
2 3
B.实验2得到的溶液中有
c(OH-)=c(H+)+c(HCO)+2c(H CO)
2 3
C.实验3反应静置后的上层清液中有
c(Ca2+)·c(CO)>K (CaCO)
sp 3
D.实验4中反应的离子方程式:
CO+2H+===CO ↑+HO
2 2
答案:B
解析:NaHCO 溶液显碱性,说明溶液中碳酸氢根离子水解程度大于其电离程度,由
3
实验 1 可得出:c(Na+)>c(HCO)>c(H CO)>c(CO),A 项错误;实验 2 所得溶液溶质为
2 3
NaCO ,溶液中存在碳酸根离子的水解以及水的电离,则有质子守恒:c(OH-)=c(H+)+
2 3
c(HCO)+2c(H CO),B项正确;实验3反应静置后的上层清液为碳酸钙的饱和溶液,存在
2 3碳酸钙的溶解平衡,溶液中有c(Ca2+)·c(CO)=K (CaCO),C项错误;碳酸氢根离子不能
sp 3
拆开,实验4中反应的离子方程式应为HCO+H+===CO ↑+HO,D项错误。
2 2
8.[2022·湖南卷]为探究FeCl 的性质,进行了如下实验(FeCl 和NaSO 溶液浓度均为
3 3 2 3
0.1 mol·L-1)。
实验 操作与现象
① 在5 mL水中滴加2滴FeCl 溶液,呈棕黄色;煮沸,溶液变红褐色。
3
在5 mL FeCl 溶液中滴加2滴NaSO 溶液,变红褐色;再滴加K[Fe(CN) ]溶液,
② 3 2 3 3 6
产生蓝色沉淀。
在5 mL Na SO 溶液中滴加2滴FeCl 溶液,变红褐色;将上述混合液分成两份,一
③ 2 3 3
份滴加K[Fe(CN) ]溶液,无蓝色沉淀生成;另一份煮沸,产生红褐色沉淀。
3 6
依据上述实验现象,结论不合理的是( )
A.实验①说明加热促进Fe3+水解反应
B.实验②说明Fe3+既发生了水解反应,又发生了还原反应
C.实验③说明Fe3+发生了水解反应,但没有发生还原反应
D.整个实验说明SO对Fe3+的水解反应无影响,但对还原反应有影响
答案:D
解析:实验①中煮沸后溶液变红褐色[Fe(OH) 胶体],说明加热促进Fe3+水解反应,A
3
项正确;实验②中溶液变红褪色,说明生成了 Fe(OH) 胶体,Fe3+发生了水解反应,滴加
3
K[Fe(CN) ]溶液,产生蓝色沉淀,说明溶液中存在Fe2+,Fe3+发生了还原反应,B项正确;
3 6
实验③中溶液变红褐色,说明Fe3+发生了水解反应,滴加K[Fe(CN) ]溶液,无蓝色沉淀生
3 6
成,说明Fe3+没有发生还原反应,C项正确;实验①中煮沸后溶液变红褐色,实验③中溶
液直接变红褐色,说明SO对Fe3+的水解反应有影响,D项错误。
9.[2022·江苏卷]一种捕集烟气中CO 的过程如图所示。室温下以0.1 mol·L-1 KOH溶
2
液吸收CO ,若通入CO 所引起的溶液体积变化和HO挥发可忽略,溶液中含碳物种的浓
2 2 2
度c =c(H CO)+c(HCO)+c(CO)。HCO 电离常数分别为K =4.4×10-7、K =4.4×10-
总 2 3 2 3 a1 a2
11。下列说法正确的是( )
A.KOH吸收CO 所得到的溶液中:c(H CO)>c(HCO)
2 2 3
B.KOH完全转化为KCO 时,溶液中:c(OH-)=c(H+)+c(HCO)+c(H CO)
2 3 2 3
C.KOH溶液吸收CO,c =0.1 mol·L-1溶液中:c(H CO)>c(CO)
2 总 2 3
D.题图所示的“吸收”“转化”过程中,溶液的温度下降
答案:C
解析:A项,KOH吸收CO 可能生成KCO ,此时由于CO以第一步水解为主,故溶
2 2 3
液中c(HCO)>c(H CO),也可能生成 KHCO ,由于HCO的水解很微弱,故此时溶液中
2 3 3
c(HCO)>c(H CO),还可能生成 KCO 和 KHCO 的混合物,同理,溶液中亦存在
2 3 2 3 3
c(HCO)>c(H CO),错误;B项,KCO 溶液中存在质子守恒 c(OH-)=c(H+)+c(HCO)+
2 3 2 3
2c(H CO),错误;C项,由于KOH溶液的浓度为0.1 mol·L-1,c =0.1 mol·L-1,即c(K+)
2 3 总
=c(H CO)+c(HCO)+c(CO),此等式为KHCO 溶液的物料守恒式,故此时所得溶液为
2 3 3
KHCO
3
溶液,HCO存在水解平衡HCO+H
2
O⇌H
2
CO
3
+OH-,电离平衡HCO⇌CO+H+,
由K (HCO)=>K 可知,HCO的水解程度大于电离程度,故c(H CO)>c(CO),正确;D项,
h a2 2 3
“吸收”时发生的反应和“转化”时发生的反应均为放热反应,故溶液的温度升高,错误。