文档内容
专练 48 化学反应原理综合题
授课提示:对应学生用书95页
1.[2023·新课标卷]氨是最重要的化学品之一,我国目前氨的生产能力位居世界首位。
回答下列问题:
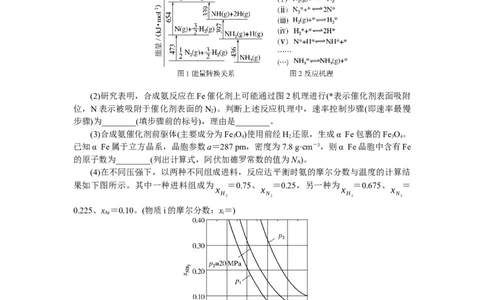
(1)根据图1数据计算反应N(g)+H(g)===NH(g)的ΔH=________kJ·mol-1。
2 2 3
(2)研究表明,合成氨反应在Fe催化剂上可能通过图2机理进行(*表示催化剂表面吸附
位,N表示被吸附于催化剂表面的N)。判断上述反应机理中,速率控制步骤(即速率最慢
2
步骤)为________(填步骤前的标号),理由是________。
(3)合成氨催化剂前驱体(主要成分为Fe O)使用前经H 还原,生成α Fe包裹的Fe O。
3 4 2 3 4
已知α Fe属于立方晶系,晶胞参数a=287 pm,密度为7.8 g·cm-3,则α Fe晶胞中含有Fe
的原子数为________(列出计算式,阿伏加德罗常数的值为N )。
A
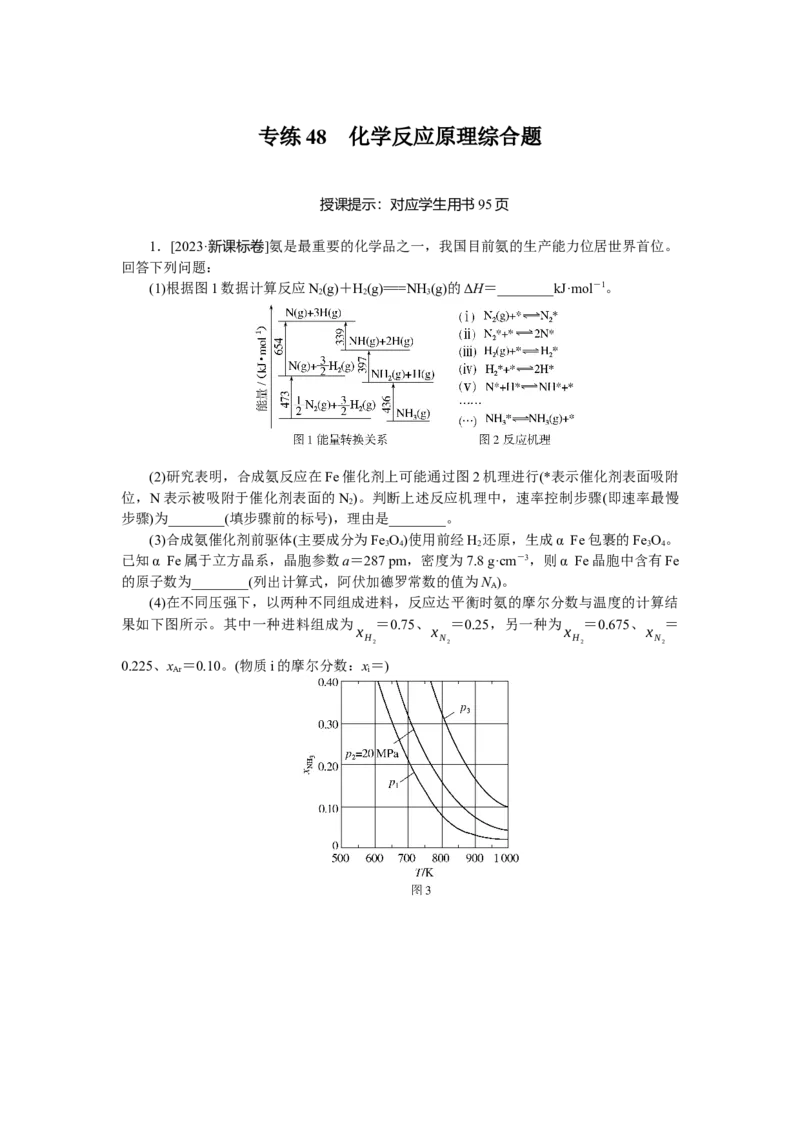
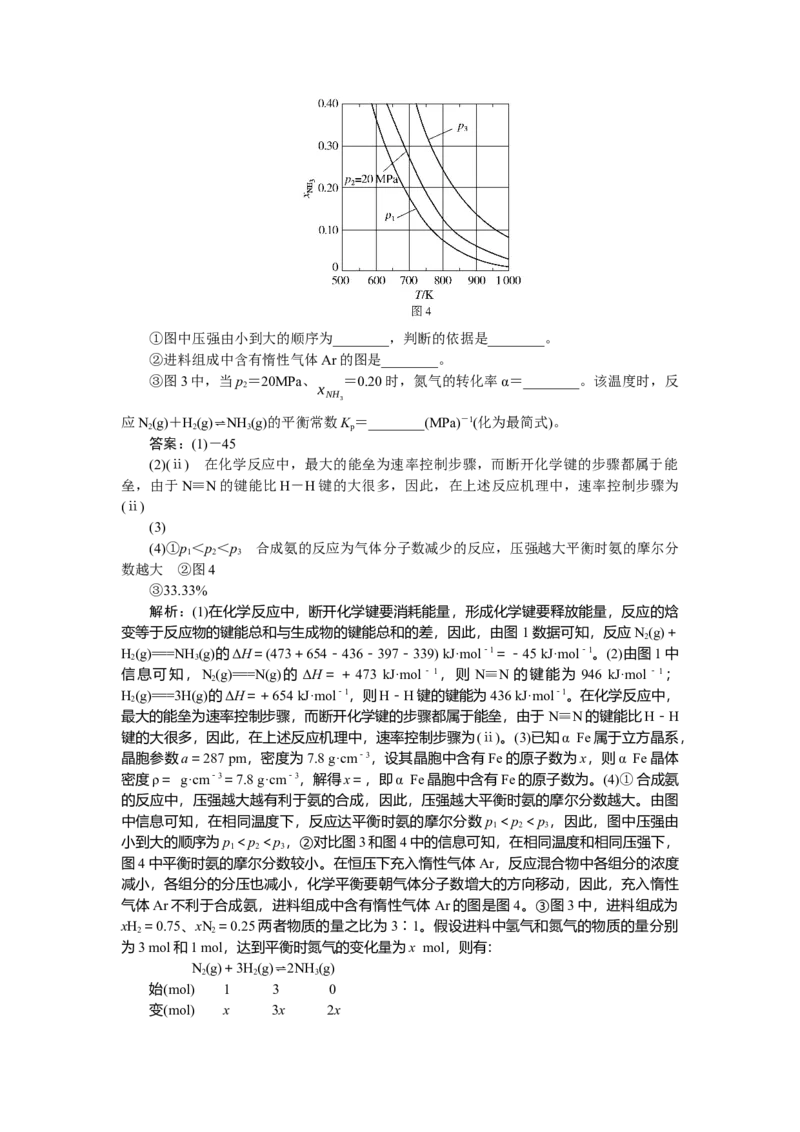
(4)在不同压强下,以两种不同组成进料,反应达平衡时氨的摩尔分数与温度的计算结
果如下图所示。其中一种进料组成为 =0.75、 =0.25,另一种为 =0.675、 =
x x x x
H N H N
2 2 2 2
0.225、x =0.10。(物质i的摩尔分数:x=)
Ar i①图中压强由小到大的顺序为________,判断的依据是________。
②进料组成中含有惰性气体Ar的图是________。
③图3中,当p =20MPa、 =0.20时,氮气的转化率α=________。该温度时,反
2 x
NH
3
应N
2
(g)+H
2
(g)⇌NH
3
(g)的平衡常数K
p
=________(MPa)-1(化为最简式)。
答案:(1)-45
(2)(ⅱ) 在化学反应中,最大的能垒为速率控制步骤,而断开化学键的步骤都属于能
垒,由于N≡N的键能比H-H键的大很多,因此,在上述反应机理中,速率控制步骤为
(ⅱ)
(3)
(4)①p<p<p 合成氨的反应为气体分子数减少的反应,压强越大平衡时氨的摩尔分
1 2 3
数越大 ②图4
③33.33%
解析:(1)在化学反应中,断开化学键要消耗能量,形成化学键要释放能量,反应的焓
变等于反应物的键能总和与生成物的键能总和的差,因此,由图 1数据可知,反应N(g)+
2
H(g)===NH(g)的ΔH=(473+654-436-397-339) kJ·mol-1=-45 kJ·mol-1。(2)由图1中
2 3
信息可知,N(g)===N(g)的 ΔH=+473 kJ·mol-1,则 N≡N 的键能为 946 kJ·mol-1;
2
H(g)===3H(g)的ΔH=+654 kJ·mol-1,则H-H键的键能为436 kJ·mol-1。在化学反应中,
2
最大的能垒为速率控制步骤,而断开化学键的步骤都属于能垒,由于N≡N的键能比H-H
键的大很多,因此,在上述反应机理中,速率控制步骤为(ⅱ)。(3)已知α Fe属于立方晶系,
晶胞参数a=287 pm,密度为7.8 g·cm-3,设其晶胞中含有Fe的原子数为x,则α Fe晶体
密度ρ= g·cm-3=7.8 g·cm-3,解得x=,即α Fe晶胞中含有Fe的原子数为。(4)①合成氨
的反应中,压强越大越有利于氨的合成,因此,压强越大平衡时氨的摩尔分数越大。由图
中信息可知,在相同温度下,反应达平衡时氨的摩尔分数 p <p <p ,因此,图中压强由
1 2 3
小到大的顺序为p <p <p ,②对比图3和图4中的信息可知,在相同温度和相同压强下,
1 2 3
图4中平衡时氨的摩尔分数较小。在恒压下充入惰性气体Ar,反应混合物中各组分的浓度
减小,各组分的分压也减小,化学平衡要朝气体分子数增大的方向移动,因此,充入惰性
气体Ar不利于合成氨,进料组成中含有惰性气体 Ar的图是图4。③图3中,进料组成为
xH =0.75、xN =0.25两者物质的量之比为3∶1。假设进料中氢气和氮气的物质的量分别
2 2
为3 mol和1 mol,达到平衡时氮气的变化量为x mol,则有:
N
2
(g)+3H
2
(g)⇌2NH
3
(g)
始(mol) 1 3 0
变(mol) x 3x 2x平(mol) 1-x 3-3x 2x
当 p =20MPa、 =0.20 时, ==0.20,解得 x=,则氮气的转化率 α=
2 x x
NH NH
3 3
≈33.33%,平衡时N 、H 、NH 的物质的量分别为 mol、2 mol、 mol,其物质的量分数分
2 2 3
别为、、,则该温度下K′
p
==(MPa)-2。因此,该温度时,反应N
2
(g)+H
2
(g)⇌NH
3
(g)的平
衡常数K === (MPa)-1。
p
2.[2024·全国甲卷]甲烷转化为多碳化合物具有重要意义。一种将甲烷溴化再偶联为丙
烯(C H)的研究所获得的部分数据如下。回答下列问题:
3 6
(1)已知如下热化学方程式:
CH(g)+Br (g)===CH Br(g)+HBr(g)
4 2 3
ΔH=-29 kJ·mol-1
1
3CHBr(g)=C H(g)+3HBr(g)
3 3 6
ΔH=+20 kJ·mol-1
2
计算反应3CH(g)+3Br (g)===C H(g)+6HBr(g)的ΔH=________ kJ·mol-1。
4 2 3 6
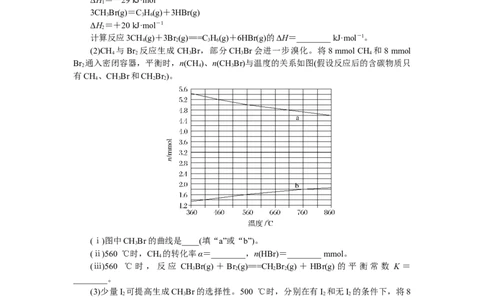
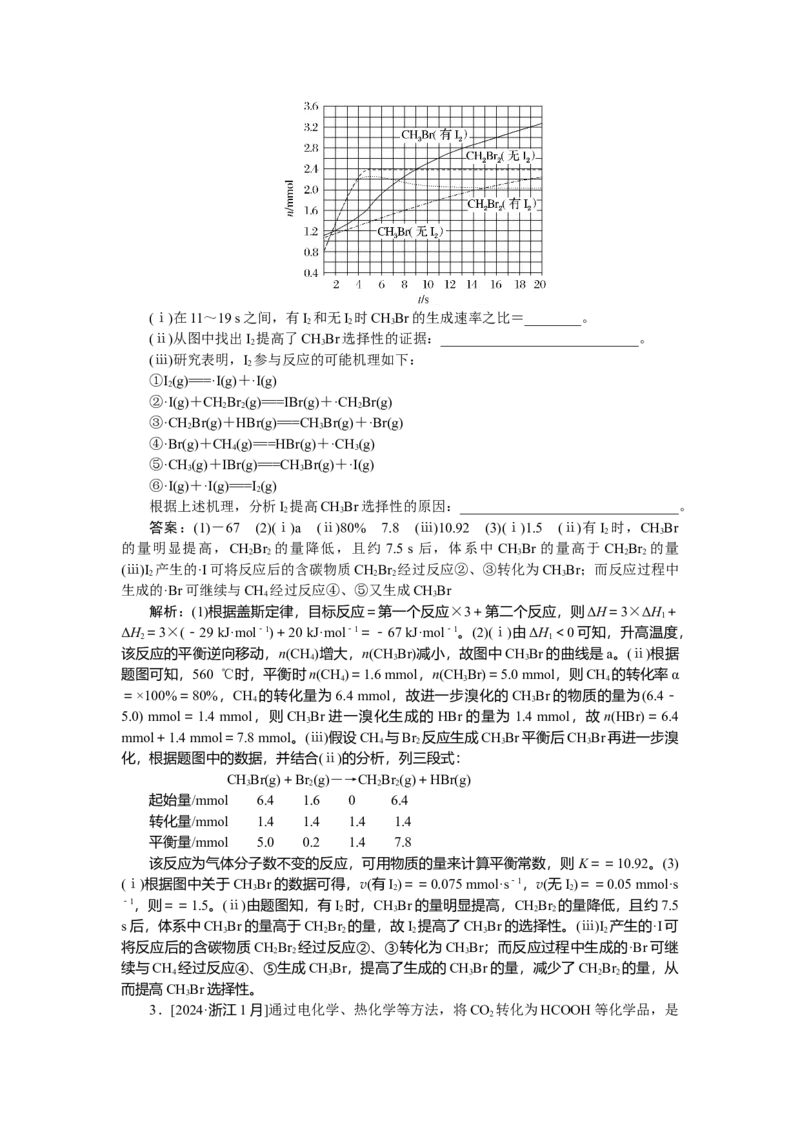
(2)CH 与Br 反应生成CHBr,部分CHBr会进一步溴化。将8 mmol CH 和8 mmol
4 2 3 3 4
Br 通入密闭容器,平衡时,n(CH)、n(CHBr)与温度的关系如图(假设反应后的含碳物质只
2 4 3
有CH、CHBr和CHBr )。
4 3 2 2
(ⅰ)图中CHBr的曲线是____(填“a”或“b”)。
3
(ⅱ)560 ℃时,CH 的转化率α=________,n(HBr)=________ mmol。
4
(ⅲ)560 ℃时,反应 CHBr(g) +Br (g)===CH Br (g)+HBr(g) 的平衡常数 K =
3 2 2 2
________。
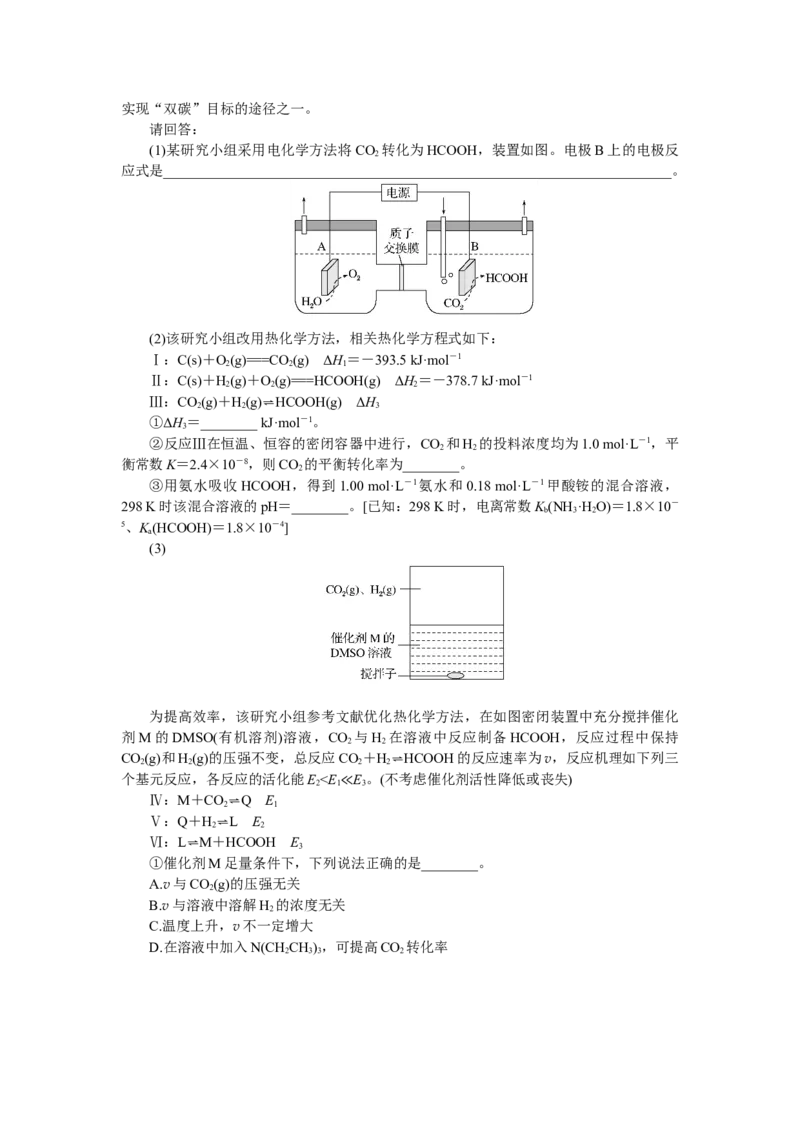
(3)少量I 可提高生成CHBr的选择性。500 ℃时,分别在有I 和无I 的条件下,将8
2 3 2 2
mmol CH 和8 mmol Br 通入密闭容器,溴代甲烷的物质的量(n)随时间(t)的变化关系如图。
4 2(ⅰ)在11~19 s之间,有I 和无I 时CHBr的生成速率之比=________。
2 2 3
(ⅱ)从图中找出I 提高了CHBr选择性的证据:____________________________。
2 3
(ⅲ)研究表明,I 参与反应的可能机理如下:
2
①I(g)===·I(g)+·I(g)
2
②·I(g)+CHBr (g)===IBr(g)+·CHBr(g)
2 2 2
③·CHBr(g)+HBr(g)===CH Br(g)+·Br(g)
2 3
④·Br(g)+CH(g)===HBr(g)+·CH(g)
4 3
⑤·CH(g)+IBr(g)===CH Br(g)+·I(g)
3 3
⑥·I(g)+·I(g)===I (g)
2
根据上述机理,分析I 提高CHBr选择性的原因:_______________________________。
2 3
答案:(1)-67 (2)(ⅰ)a (ⅱ)80% 7.8 (ⅲ)10.92 (3)(ⅰ)1.5 (ⅱ)有I 时,CHBr
2 3
的量明显提高,CHBr 的量降低,且约 7.5 s 后,体系中 CHBr 的量高于 CHBr 的量
2 2 3 2 2
(ⅲ)I 产生的·I可将反应后的含碳物质CHBr 经过反应②、③转化为CHBr;而反应过程中
2 2 2 3
生成的·Br可继续与CH 经过反应④、⑤又生成CHBr
4 3
解析:(1)根据盖斯定律,目标反应=第一个反应×3+第二个反应,则ΔH=3×ΔH +
1
ΔH =3×(-29 kJ·mol-1)+20 kJ·mol-1=-67 kJ·mol-1。(2)(ⅰ)由ΔH <0可知,升高温度,
2 1
该反应的平衡逆向移动,n(CH)增大,n(CHBr)减小,故图中CHBr的曲线是a。(ⅱ)根据
4 3 3
题图可知,560 ℃时,平衡时n(CH)=1.6 mmol,n(CHBr)=5.0 mmol,则CH 的转化率α
4 3 4
=×100%=80%,CH 的转化量为6.4 mmol,故进一步溴化的CHBr的物质的量为(6.4-
4 3
5.0) mmol=1.4 mmol,则CHBr进一溴化生成的 HBr的量为 1.4 mmol,故n(HBr)=6.4
3
mmol+1.4 mmol=7.8 mmol。(ⅲ)假设CH 与Br 反应生成CHBr平衡后CHBr再进一步溴
4 2 3 3
化,根据题图中的数据,并结合(ⅱ)的分析,列三段式:
CHBr(g)+Br (g)―→CHBr (g)+HBr(g)
3 2 2 2
起始量/mmol 6.4 1.6 0 6.4
转化量/mmol 1.4 1.4 1.4 1.4
平衡量/mmol 5.0 0.2 1.4 7.8
该反应为气体分子数不变的反应,可用物质的量来计算平衡常数,则 K==10.92。(3)
(ⅰ)根据图中关于CHBr的数据可得,v(有I)==0.075 mmol·s-1,v(无I)==0.05 mmol·s
3 2 2
-1,则==1.5。(ⅱ)由题图知,有I 时,CHBr的量明显提高,CHBr 的量降低,且约7.5
2 3 2 2
s后,体系中CHBr的量高于CHBr 的量,故I 提高了CHBr的选择性。(ⅲ)I 产生的·I可
3 2 2 2 3 2
将反应后的含碳物质CHBr 经过反应②、③转化为CHBr;而反应过程中生成的·Br可继
2 2 3
续与CH 经过反应④、⑤生成CHBr,提高了生成的CHBr的量,减少了CHBr 的量,从
4 3 3 2 2
而提高CHBr选择性。
3
3.[2024·浙江1月]通过电化学、热化学等方法,将CO 转化为HCOOH等化学品,是
2实现“双碳”目标的途径之一。
请回答:
(1)某研究小组采用电化学方法将CO 转化为HCOOH,装置如图。电极B上的电极反
2
应式是________________________________________________________________________。
(2)该研究小组改用热化学方法,相关热化学方程式如下:
Ⅰ:C(s)+O(g)===CO (g) ΔH=-393.5 kJ·mol-1
2 2 1
Ⅱ:C(s)+H(g)+O(g)===HCOOH(g) ΔH=-378.7 kJ·mol-1
2 2 2
Ⅲ:CO
2
(g)+H
2
(g)⇌HCOOH(g) ΔH
3
①ΔH=________ kJ·mol-1。
3
②反应Ⅲ在恒温、恒容的密闭容器中进行,CO 和H 的投料浓度均为1.0 mol·L-1,平
2 2
衡常数K=2.4×10-8,则CO 的平衡转化率为________。
2
③用氨水吸收HCOOH,得到1.00 mol·L-1氨水和0.18 mol·L-1甲酸铵的混合溶液,
298 K时该混合溶液的pH=________。[已知:298 K时,电离常数K (NH ·H O)=1.8×10-
b 3 2
5、K(HCOOH)=1.8×10-4]
a
(3)
为提高效率,该研究小组参考文献优化热化学方法,在如图密闭装置中充分搅拌催化
剂M的DMSO(有机溶剂)溶液,CO 与H 在溶液中反应制备HCOOH,反应过程中保持
2 2
CO
2
(g)和H
2
(g)的压强不变,总反应CO
2
+H 2⇌HCOOH的反应速率为v,反应机理如下列三
个基元反应,各反应的活化能Ec 时,v不再显著增大。请解释原因
0
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
答案:(1)CO +2e-+2H+===HCOOH (2)①+14.8 ②2.4×10-8 ③10 (3)①CD
2
②当c≤c 时,v随c增大而增大,因M是基元反应Ⅳ的反应物(直接影响基元反应Ⅵ中反
0
应物L的生成);c>c 时,v不再显著增加,因受限于CO(g)和H(g)在溶液中的溶解速度
0 2 2
(或浓度)
解析:(1)电极B上CO 转化为HCOOH,发生还原反应,电极反应式为CO +2e-+
2 2
2H+===HCOOH。(2)① 根据盖斯定律,由Ⅲ=Ⅱ-Ⅰ可得 ΔH =ΔH -ΔH =-378.7
3 2 1
kJ·mol-1+393.5 kJ·mol-1=+14.8 kJ·mol-1。②设转化的CO 的浓度为x mol·L-1,可列三
2
段式:
CO
2
(g)+H
2
(g)⇌HCOOH(g)
起始浓度/(mol·L-1) 1.0 1.0 0
转化浓度/(mol·L-1) x x x
平衡浓度/(mol·L-1) 1.0-x 1.0-x x
则K==2.4×10-8,解得x≈2.4×10-8,则CO 的平衡转化率为×100%=2.4×10-8。
2
③甲酸铵水解:NH+HCOO-+H
2
O⇌NH
3
·H
2
O+HCOOH,由氨水和甲酸铵的浓度知,甲
酸铵的水解受抑制,由电离和水解都很微弱知,溶液中 c(NH)≈0.18 mol·L-1,
c(NH ·H O)≈1.00 mol·L-1,根据K (NH ·H O)=,知c(OH-)== mol·L-1=10-4 mol·L
3 2 b 3 2
-1,c(H+)=10-10 mol·L-1,故pH=10。(3)①v与CO(g)的压强有关,压强越大,溶液中
2
CO 的浓度越大,v越大,A项错误;v与溶液中溶解H 的量有关,氢气浓度越大,反应速
2 2
率越快,B项错误;温度升高,气体在溶液中溶解度变小,总反应速率不一定增大,C项
正确;N(CH CH) 会与HCOOH反应,使得反应Ⅳ、Ⅴ、Ⅵ平衡均正向移动,可提高CO
2 3 3 2
的转化率,D项正确。