文档内容
化 学 试 卷
相对原子质量: H—1 C—12 O—16 Na—23 S—32 Cl—35.5
一、选择题(本题包括6个小题,共12分。每小题只有一个选项符合题意)
1、 生活中的下列现象,属于化学变化的是( )
A、铁丝弯曲 B、冰雪融化 C、食物腐烂 D、汽油挥发
2、“老干妈”是我们贵阳市的著名品牌。图1是其系列产品“风味豆豉辣椒”标签的部分内
容。配料中富含蛋白质的是( )
老干妈风味豆豉辣椒
图
配料:大豆、植物油、辣椒、味精、食盐等
1
A、大豆 B、食盐 C、植物油 D、辣椒
3、2009年4月27日贵阳市环保局在人民广场举行了关于“提倡市民使用无磷洗涤用品”
的宣传活动,贵阳市将于5月1日起全面实施“禁磷令”。这里的“磷”应理解为
( )
A、分子 B、 原子 C、离子 D、元素
4、下列关于金属的描述不正确的是( )
A、金属材料包括纯金属和合金
B、铁丝在氧气中燃烧生成黑色的Fe O
2 3
C、铁制品在潮湿的空气中易生锈
D、用Fe、Cu、盐酸作试剂进行实验,可得出活动性Fe>H>Cu的结论
5、 图2、3是电解水的实验及电解时水分子分解的示意图。有关叙述正确的是( )
图2 电解水 图3 水分子分解
A、a试管中产生的气体是O
2
B、、a、b试管中产生气体的质量比为2 : 1
C、水分解的过程中,氢原子和氧原子数都没发生变化
通电
D、电解水的化学方程式为: HO H↑ + O↑
2 2 2
6、对下列化学事实的解释不正确的是( )
化学事实 解释
生石灰可做食品包装袋内的干燥剂 生石灰可吸水并与水发生化学反应
A
常温时,在90g水中加入10g NaCl搅拌,
溶质质量
NaCl全部溶解,即得质量分数为10% 的 = ×
B 溶质的质量分数
NaCl溶液 100% 溶液质量
C 金刚石可用作钻头 金刚石是天然存在的最硬的物质
某化肥与熟石灰研磨后,无刺激性气味的 无氨气放出,一定不是氮肥
D
氨气产生二、非选择题(本题包括7个小题,共48分)
7、化学——人类进步的关键。化学中物质的多彩、符号用语的独特、在各行业的重要作
用,无不显现出她的魅力、她的美。我们不但应喜欢化学、学好化学,更应感谢化学!请完成
下列填空。
(1)色彩: 物质 铜 KMnO MnO CuSO 溶液
4 2 4
颜色 红色 紫色 黑色
(2)分类:
物质类别 单质 酸 盐
化学式 CO HSO NaOH
2 2 4
(3)符号:指出下列符号用语中“2”的意义。
+2
+6 2 4
① H
2
_____________,② CO _____,③ ___________。
(4)用途:利用CO的________性,把铁矿石冶炼成铁。 a
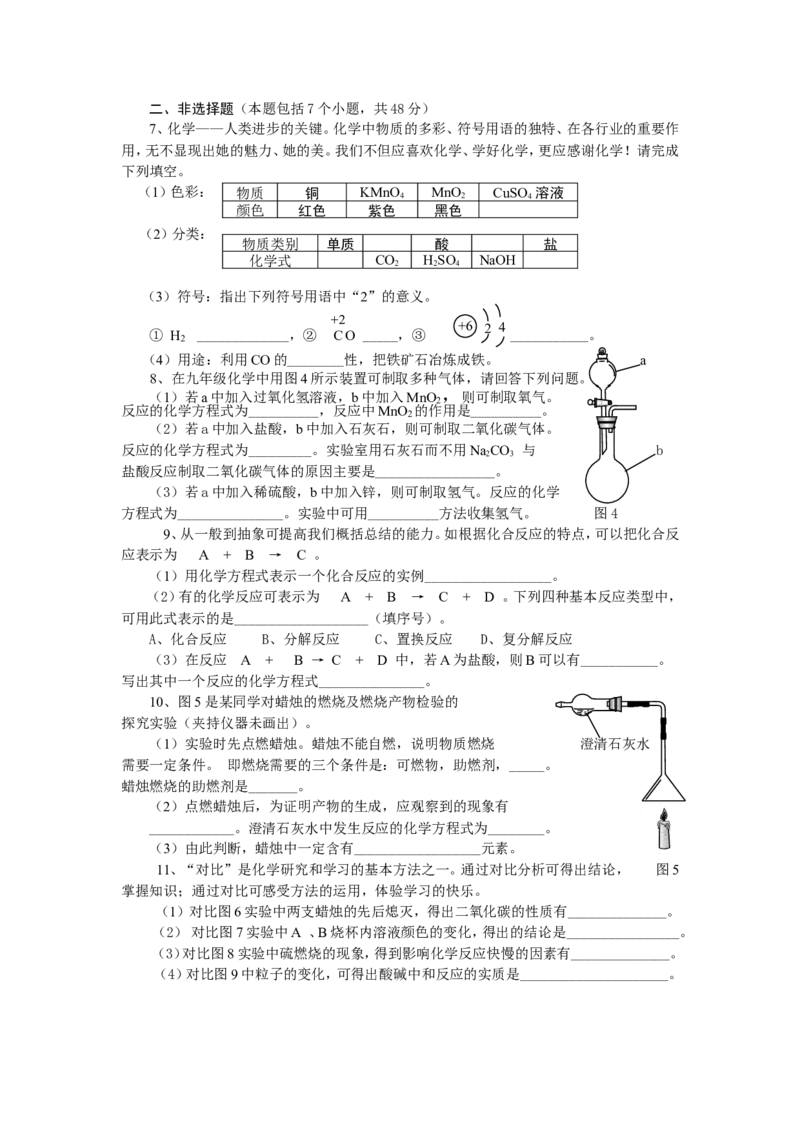
8、在九年级化学中用图4所示装置可制取多种气体,请回答下列问题。
,
(1)若a中加入过氧化氢溶液,b中加入MnO 则可制取氧气。
2
反应的化学方程式为__________,反应中MnO 的作用是__________。
2
(2)若a中加入盐酸,b中加入石灰石,则可制取二氧化碳气体。
反应的化学方程式为_________。实验室用石灰石而不用NaCO 与 b
2 3
盐酸反应制取二氧化碳气体的原因主要是_________________。
(3)若a中加入稀硫酸,b中加入锌,则可制取氢气。反应的化学
方程式为_______________。实验中可用__________方法收集氢气。 图4
9、从一般到抽象可提高我们概括总结的能力。如根据化合反应的特点,可以把化合反
应表示为 A + B → C 。
(1)用化学方程式表示一个化合反应的实例__________________。
(2)有的化学反应可表示为 A + B → C + D 。下列四种基本反应类型中,
可用此式表示的是___________________(填序号)。
A、化合反应 B、分解反应 C、置换反应 D、复分解反应
(3)在反应 A + B → C + D 中,若A为盐酸,则B可以有___________。
写出其中一个反应的化学方程式_______________。
10、图5是某同学对蜡烛的燃烧及燃烧产物检验的
探究实验(夹持仪器未画出)。
(1)实验时先点燃蜡烛。蜡烛不能自燃,说明物质燃烧 澄清石灰水
需要一定条件。 即燃烧需要的三个条件是:可燃物,助燃剂,_____。
蜡烛燃烧的助燃剂是_______。
(2)点燃蜡烛后,为证明产物的生成,应观察到的现象有
____________。澄清石灰水中发生反应的化学方程式为________。
(3)由此判断,蜡烛中一定含有__________________元素。
11、“对比”是化学研究和学习的基本方法之一。通过对比分析可得出结论, 图5
掌握知识;通过对比可感受方法的运用,体验学习的快乐。
(1)对比图6实验中两支蜡烛的先后熄灭,得出二氧化碳的性质有______________。
(2) 对比图7实验中A 、B烧杯内溶液颜色的变化,得出的结论是________________。
(3)对比图8实验中硫燃烧的现象,得到影响化学反应快慢的因素有______________。
(4)对比图9中粒子的变化,可得出酸碱中和反应的实质是_____________________。图6 图7 图8 图9
12、图10是一瓶浓硫酸标签上的部分内容,某探究小组的同学对这瓶硫酸进行了如下
探究,请你参与。
硫 酸
[查阅资料]浓硫酸有强腐蚀性,溶于水会放热;硫酸钡不溶于 500mL
水也不溶于酸。 化学式: H 2 SO 4
相对分子质量:98
[探究一] 浓硫酸稀释时会放热。
密度:1.84g/cm3
(1)稀释浓硫酸时,所需仪器主要有_______________, 质量分数:98%
质 量 分 数 :
应如何稀释浓硫酸?____________________。测量稀释前后溶液
98%
的温度,有明显升高的现象。结论:浓硫酸溶于水放热。
[探究二]稀硫酸与氢氧化钠溶液能发生反应。 图10
实验步骤 实验现象 实验结论
先用pH试纸测定稀硫酸的pH,再 pH逐渐变大, 稀硫酸与氢氧化钠
逐滴加入氢氧化钠溶液并不断振 最后pH≥7 溶液能发生反应
荡,同时测混合液的pH
(2)稀硫酸与氢氧化钠溶液反应的化学方程式为______________________________。
_
(3)实验中仅从溶液pH变大,而不强调pH≥7,不能得出稀硫酸与氢氧化钠溶液一定发
生反应的结论,理由是______________________________。
[探究三]由于该试剂瓶瓶口密封签已破损,同学们怀疑该浓硫酸的质量分数与标签不
相符。
[提出问题]该浓硫酸的质量分数是否发生变化?
[实验探究](4)取该浓硫酸和足量BaCl 溶液反应,过滤、洗涤、干燥沉淀。实验中如何
2
确定硫酸已完全反应___________。
(5)为达到实验目的,实验中必须要测知的数据是___________。
[探究结论] (6)由实验测得的数据计算出的硫酸的质量分数与标签不符。该硫酸的质
量分数应__________ 98%(填“大于” 或“小于”)。
13、某纯碱试样中含有杂质氯化钠,为测定试样中NaCO 的含量,取等质量的四份试
2 3
样与溶质质量分数相同的盐酸进行实验。实验数据记录如下表。
编 号 ① ② ③ ④
纯碱试样的质量/g 60 60 60 60
盐酸的体积/mL 50 100 150 200
生成气体的质量/g 7.3 14.6 22 22
(1)盐酸的体积消耗150mL后气体质量不再增加,说明纯碱试样中NaCO_______(填
2 3
“完全”或“未完全”)反应。
(2)该纯碱中NaCO 的质量分数是多少?
2 3
化学答案和评分标准说明:1、答题时若出现其他正确合理答案,同样给分。
2、化学方程式书写中:化学式错误不给分,未配平、条件或沉淀符号有错扣1分。
一、化学选择题(本题包括6个小题,共12分。每小题只有一个选项符合题意)
1.C 2.A 3.D 4.B 5.C 6.D
二、化学非选择题(本题包括7个小题,共48分)
7.(每空1分,共9分)
(1)蓝色
(2) 物质类别 氧化物 碱
化学式 O NaCl
2
(3)①1个氢分子由2个氢原子构成 ②一氧化碳中碳元素的化合价为+2价
③碳原子核外第一电子层有2个电子 (4)还原性
8.(每个方程式2分,其余每空1分,共9分)
MnO2
(1)2HO ===== 2H O+O ↑ 催化作用
2 2 2 2
(2)CaCO +2HCl ===CaCl +H O+CO↑ 产生二氧化碳的速率太快,不易控制
3 2 2 2
(3)Zn + H
2
SO
4
== ZnSO
4
+ H
2
↑ 排水法或向下排空气法
9. (每空2分,共8分)
点燃
(1)2H +O == 2HO (2)C D (3)Fe、CuO、NaOH、CaCO 等
2 2 2 3
NaOH + HCl ==NaCl + H
2
O
10.(方程式2分,其余每空1分,共6分)
(1) 着火点 空气或氧气
(2) 漏斗内壁有小水珠出现,澄清石灰水变浑浊 Ca(OH)
2
+ CO
2
==CaCO
3
↓+ H
2
O
(3)C、H元素
11. (每空1分,共4分)
(1)二氧化碳的密度比空气密度大,二氧化碳不支持燃烧、本身也不燃烧
(2)氨分子在不断运动,氨水能使无色酚酞溶液变为红色
(3)反应物浓度大小 (4)氢离子与氢氧根离子结合生成水
12、(每空1分,共7分)
(1)烧杯、玻璃棒 将浓硫酸沿烧杯壁慢慢注入水中,并不断搅拌
(2)2NaOH + H SO == Na SO + 2H O (3)硫酸被水稀释其pH也会变大
2 4 2 4 2
(4)取过滤后的清液,滴入BaCl 溶液,若无沉淀产生,则硫酸已完全反应
2
(5)沉淀的质量和所取用浓硫酸的体积 (6)小于
13.(共5分) (1)完全 (1分)
(2) 解:设每份试样中碳酸钠的质量为x
NaCO + 2HCl = 2NaCl + HO + CO↑ (1分)
2 3 2 2
106 44
x 22g
106 x
=
(1分) 44 22g
x=53g
(1分)
53g/60g×100%=88.3% (1分)
答:该纯碱中碳酸钠的质量分数为88.3%。