文档内容
贵阳市2013年初中毕业生学业考试试题卷
化 学
相对原子质量:H—1 C—12 O—16 Mg—24 S—32 Fe—56 Zn—65
一、化学选择题(本题包括6个小题,共12分。每小题只有一个选项符合题意。)
1.2013年5月,全国科协年会在贵阳举行,其“生态文明与绿色发展”等相关内容为贵阳市
生态文明城市建设注入了新的内涵。在生态文明城市建设中,下列做法不当的是
A.扩大湿地公园面积,改善空气质量 B.发展城市轨道交通,倡导低碳出行
C.大力发展火力发电,满足用电需求 D.学好化学科学知识,提升科学素养
2.对“桂花十里飘香”的下列解释正确的是
A.分子在不断运动 B.分子间有间隔 C.分子体积很小 D.分子质量很小
3.贵州盛产金银花,从金银花中提取的绿原酸(化学式为C H O)有很高的药用价值。下列
16 18 9
有关绿原酸的说法正确的是
A.绿原酸属于混合物 B.绿原酸由碳、氢、氧三种元素组成
C.绿原酸的相对分子质量为354g D.绿原酸中氢元素的质量分数最大
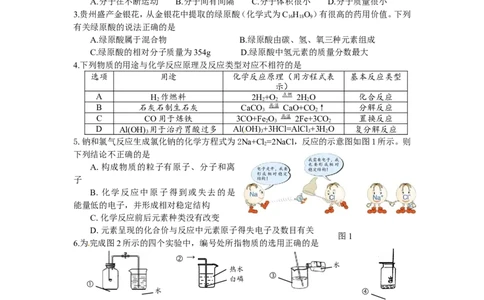
4.下列物质的用途与化学反应原理及反应类型对应不相符的是
选项 用途 化学反应原理(用方程式表 基本反应类型
示)
A H 作燃料 2H+O 点燃 2HO 化合反应
2 2 2 2
B 石灰石制生石灰 CaCO 高温 CaO+CO ↑ 分解反应
3 2
C CO用于炼铁 3CO+Fe O 高温 2Fe+3CO 置换反应
2 3 2
D Al(OH) 用于治疗胃酸过多 Al(OH) +3HCl=AlCl +3H O 复分解反应
3 3 3 2
5.钠和氯气反应生成氯化钠的化学方程式为2Na+Cl =2NaCl,反应的示意图如图1所示。则
2
下列结论不正确的是
我需要电子,我
A.构成物质的粒子有原子、分子和离 也要形成相对
电子走开,我要 稳定结构!
形成相对稳定
子 结构!
B.化学反应中原子得到或失去的是
能量低的电子,并形成相对稳定结构
C.化学反应前后元素种类没有改变
D.元素呈现的化合价与反应中元素原子得失电子及数目有关
图1
6.为完成图2所示的四个实验中,编号处所指物质的选用正确的是
→
②
水
热水
③
白磷
①
水 ④
测定空气中氧气含量 使热水中的白磷燃烧
图2
用水稀释浓硫酸 硫在氧气中燃烧
A.①木炭 B.②氮气 C.③浓硫酸 D.④氢氧化钠溶液
四、化学非选择题(本题包括7个小题,共48分)
35.一年的化学学习,我们感受到了化学的重要和化学的美,形成了一些化学观念。
(1)物质的多样性。人们发现和合成的物质已有几千万种。写出一种你熟悉的物质的类
别和化学式 。
(2)物质由微粒构成。如金刚石由碳原子构成,水由 构成。
(3)物质是变化的。如汽油挥发是物理变化, 是化学变化。(4)物质间可以转化。如C可以转化为CO,其转化的化学方程式为 。
2
(5)化学反应伴随能量变化。人类需要的大部分能量由化学反应产生。如酒精燃烧即是
反应(填“放热”或“吸热”)。
家乡味土豆片
36.化学就在我们身边。 (每100g中含量)
蛋白质 2.3g
(1)土豆是我们喜爱的一种食品,图3所示是“家乡味土豆
糖类 20g
片”的主要营养成分。土豆中能为人体提供能量的营养素是 多种维生素 50mg
Ca、P、Fe 120mg
。多食用土豆和牛奶有利于身体健康,理由是 。
油脂 1.1g
(2)土豆等农作物的生长需要化肥。下列化肥中属于氮肥的
......
是 。 图3
A.NH Cl B.K CO C.CO(NH ) D.Ca (PO )
4 2 3 2 2 3 4 2
(3)贵阳市家用燃料的下列变迁,让我们认识了化学的重要价值。
煤或木柴 → 液化石油气或管道煤气 → 天然气
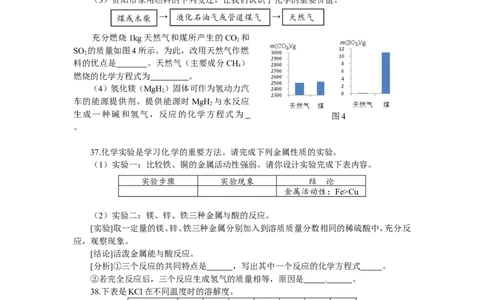
充分燃烧1kg天然气和煤所产生的CO 和
2
SO 的质量如图4所示。为此,改用天然气作燃
2
料的优点是 。天然气(主要成分CH )
4
燃烧的化学方程式为 。
(4)氢化镁(MgH )固体可作为氢动力汽
2
车的能源提供剂。提供能源时MgH 与水反应
2
生成一种碱和氢气,反应的化学方程式为 图4
。
37.化学实验是学习化学的重要方法。请完成下列金属性质的实验。
(1)实验一:比较铁、铜的金属活动性强弱。请你设计实验完成下表内容。
实验步骤 实验现象 结 论
金属活动性:Fe>Cu
(2)实验二:镁、锌、铁三种金属与酸的反应。
[实验]取一定量的镁、锌、铁三种金属分别加入到溶质质量分数相同的稀硫酸中,充分反
应,观察现象。
[结论]活泼金属能与酸反应。
[分析]①三个反应的共同特点是 ,写出其中一个反应的化学方程式 。
②若完全反应后,三个反应生成氢气的质量相等,原因是 。
38.下表是KCl在不同温度时的溶解度。
温度/℃ 0 10 20 30 40 50 60
[来源:学科
网ZXXK]
溶解度/g 27.6 31.0 34.0 37.0 x 42.6 45.5
[来
源:学科网]
小明为测定x的值,取4份40℃的水各50g,分别进行实验,并记录数据如下表。
实验编号 实验1 实验2 实验3 实验4
KCl质量/g 5 15 25 35
溶液质量/g 55 65 70 70
请回答下列问题。
(1)实验中需要用到的仪器有 (只写一种)。
(2)要使实验2的溶液达到饱和,可采取的方法是 。(3)由实验可知,40℃时KCl的溶解度x为 g。
(4)小明现要配制质量分数为30%的KCl溶液100g,为达实验目的其主要操作是 。
[来源:学科网ZXXK]
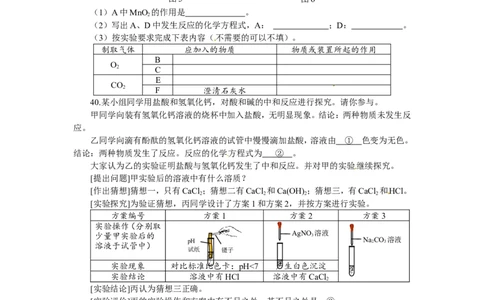
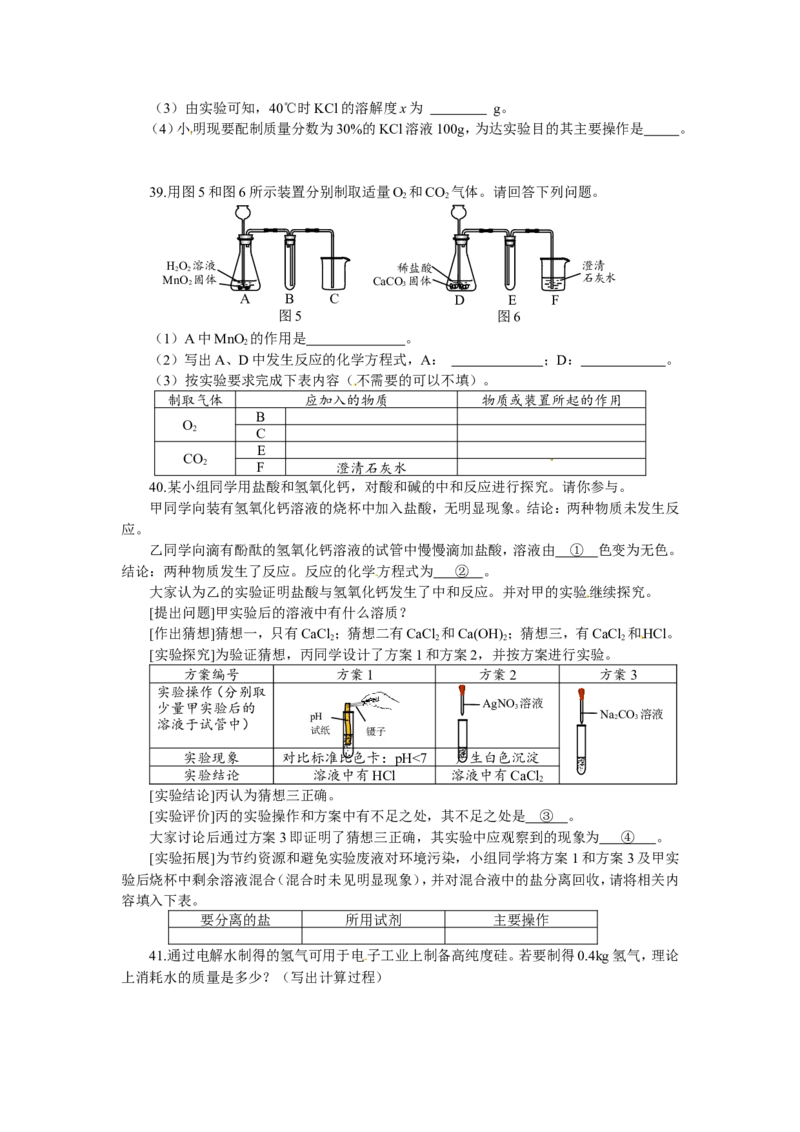
39.用图5和图6所示装置分别制取适量O 和CO 气体。请回答下列问题。
2 2
H 2 O 2 溶液 稀盐酸 澄清
MnO 2 固体 CaCO 3 固体 石灰水
A B C D E F
图5 图6
(1)A中MnO 的作用是 。
2
(2)写出A、D中发生反应的化学方程式,A: ;D: 。
(3)按实验要求完成下表内容(不需要的可以不填)。
制取气体 应加入的物质 物质或装置所起的作用
B
O
2[来源:Zxxk.Com] C
E
CO
2 F 澄清石灰水
40.某小组同学用盐酸和氢氧化钙,对酸和碱的中和反应进行探究。请你参与。
甲同学向装有氢氧化钙溶液的烧杯中加入盐酸,无明显现象。结论:两种物质未发生反
应。
乙同学向滴有酚酞的氢氧化钙溶液的试管中慢慢滴加盐酸,溶液由 ① 色变为无色。
结论:两种物质发生了反应。反应的化学方程式为 ② 。
大家认为乙的实验证明盐酸与氢氧化钙发生了中和反应。并对甲的实验继续探究。
[提出问题]甲实验后的溶液中有什么溶质?
[作出猜想]猜想一,只有CaCl ;猜想二有CaCl 和Ca(OH) ;猜想三,有CaCl 和HCl。
2 2 2 2
[实验探究]为验证猜想,丙同学设计了方案1和方案2,并按方案进行实验。
方案编号 方案1 方案2 方案3
实验操作(分别取
少量甲实验后的 AgNO 3 溶液
溶液于试管中) pH Na 2 CO 3 溶液
试纸 镊子
实验现象 对比标准比色卡:pH<7 产生白色沉淀
实验结论 溶液中有HCl 溶液中有CaCl
2
[实验结论]丙认为猜想三正确。
[实验评价]丙的实验操作和方案中有不足之处,其不足之处是 ③ 。
大家讨论后通过方案3即证明了猜想三正确,其实验中应观察到的现象为 ④ 。
[实验拓展]为节约资源和避免实验废液对环境污染,小组同学将方案1和方案3及甲实
验后烧杯中剩余溶液混合(混合时未见明显现象),并对混合液中的盐分离回收,请将相关内
容填入下表。
要分离的盐 所用试剂 主要操作
41.通过电解水制得的氢气可用于电子工业上制备高纯度硅。若要制得0.4kg氢气,理论
上消耗水的质量是多少?(写出计算过程)贵阳市2013年初中毕业生学业考试试题卷
化学参考答案及评分标准
一、化学选择题(本题包括6个小题,共12分。每小题只有一个选项符合题意。)
1.C 2.A 3.B 4.C 5. B 6.D
四、化学非选择题(本题包括7个小题,除注明分数外,每个化学方程式2分,其余每空1分,
共48分)
35.(6分)
(1)酸 HCO
2 3
(2)水分子
(3)蜡烛燃烧
(4)C+O 点燃 CO
2 2
(5)放热
36.(8分)
(1)糖类、蛋白质、油脂 营养丰富,均衡
(2)AC(3)防止形成酸雨,保护环境 CH+2O 点燃 CO+2HO
4 2 2 2
(4)MgH +2HO=Mg(OH) +2H ↑
2 2 2 2
37.(7分)
(1) 实验步骤 实验现象 实验结论
向硫酸铜溶液 铁钉表面有红色固体析出,
中投入铁钉 溶液由蓝色变为浅绿色
(2)①都是置换反应
Mg+HSO =MgSO +H ↑或Zn+HSO =ZnSO +H ↑或Fe+HSO =FeSO+H ↑
2 4 4 2 2 4 4 2 2 4 4 2
②当三种金属过量,盐酸完全反应时,则生成氢气质量相等;当盐酸过量,三种金属完全反应,
且质量比为m ∶m ∶m =24∶65∶56时,则生成氢气质量相等(2分)
Mg Zn Fe
38.(5分)
(1)烧杯
(2)增加溶质、降低温度、蒸发溶剂
(3)40
(4)水的温度升高至50℃以上,称取30gKCl固体溶于70g水中(2分)
39.(10分)
(1)作催化剂
(2)A:2HO M == nO =2 2HO+O ↑ D:CaCO +2HCl=CaCl +HO+CO ↑
2 2 2 2 3 2 2 2
(3)
制取气体 应加入的物质 物质或装置所起的作用
B 水 排水收集氧气
O
2 C 承接B中排出的水
E 收集二氧化碳
CO
2 F 检验生成的CO(或验满)
2
40.(9分)
①红
②Ca(OH) +2HCl=CaCl +2HO
2 2 2
③方案1中使用pH试纸的操作不对;方案2中加AgNO 产生白色沉淀说明溶液中有Cl-,并
3
不能说明溶液中一定有CaCl 。(2分)
2
④先有气体产生,后有白色沉淀生成。
要分离的盐 所用试剂 主要操作
CaCl NaCl NaCO,HCl 混合物中加入NaCO 溶液至不再产
2 2 3 2 3
生沉淀,过滤,将滤液蒸发即得NaCl;
将过滤后的固体加稀盐酸至不再产生
气体,对溶液加热蒸发即得CaCl 。
2
41.(3分)
【解】设:理论上消耗水的质量为x。
2HO通电 2H↑+O ↑ 1分
2 2 2
36 4
x 0.4kg
36/ x = 4/0.4kg 1分
x=3.6kg 1分答:理论上消耗水的质量为3.6kg。