文档内容
2016 年河南省普通高中招生考试试卷
化 学
注意事项:
1.本试卷共4页,四个大题,满分 50分,考试时间
50分钟。
[来源:学*科*网Z*X*X*K]
2.本试卷上不要作答,请按答题卡上注意事项的要求直接把答案填写在答题卡上,答在试卷上的答案无
效。
相对原子质量:H:1 C:12 N:14 O:16 Mg:24 Al:27 Cl:35.5 Fe:56 Zn:65
一、选择题(本题包括12个小题,每小题只有一个选项符合题意,每小题1分,共12分)
1.河南烩面营养美味,下列用的食材中富含蛋白质的是
A.羊肉 B.青菜 C.小麦粉 D.花生油
2.下列物质的用途中,利用其化学性质的是
A.铜用于制作电线 B.金刚石用于切割大理石
C.干冰用于人工降雨 D.熟石灰用于改良酸性土壤
3.下列物品废弃后可能会带来“白色污染”的是
A.塑料袋 B.报纸 C.玻璃瓶 D.铝质制饮料罐
4.下列化肥中,属于复合肥料的是
A.CO(NH) B.KNO C.KSO D.Ca (PO )
2 2 3 2 4 3 4 2
5.下列有关水的说法中正确的是
A.水和冰块混合得到混合物
B.水的蒸发和水通电分解都属于物理变化
C.硬水是指含有较多可溶性钙、镁化合物的水
D.水沸腾时可冲起壶盖,说明温度升高分子会变大
6.下列图示的实验操作中不正确的是
[来源:Z_xx_k.Com]
A.闻气体气味 B.称固体质量 C.读液体体积 D.稀释浓硫酸
7.下列各组物质中,都由离子构成的一组是
A.NaCl、CuSO B.CH、HCl C.Si、CO D.Ar、Au
4 4 2
8.右图是甲、乙的溶解度曲线,下列说法不正确的是
A.t℃时,乙的溶解度大于甲的溶解度
1
B.t℃时,甲、乙的饱和溶液中溶质的质量分数相等
2
C.降低温度能使接近饱和的甲溶液变为饱和溶液D.t℃时,75g甲的饱和溶液中加入50g水,可以
3 [来源:学。科。网]
得到质量分数为25%的溶液
9.下列化学方程式中符合题意且书写 正确的是
A.正常雨水偏弱酸性原因: SO +H O = HSO
3 2 2 4
B.生活中用天然气作燃料: C HOH +3O 2CO +3H O
2 5 2 2 2
C.用小苏打治疗胃酸过多症:NaHCO +HCl =NaCl +CO +H O
3 2 2
D.工业上用熟石灰制烧碱: Ca(OH) +2NaNO =Ca(NO) +2NaOH
2 3 3 2
10.偏二甲肼(C HN)与NO 反应放出的能量能把火箭送入太空。 该化学方程式为C HN + 2N O =
2 8 2 2 4 2 8 2 2 4
2X↑+ 3N ↑+ 4H O↑。下列说法正确的是
2 2
A.X的化学式为CO B.偏二甲肼中碳的质量分数为40%
C.该反应属于分解反应 D.生成N 和HO的质量比为14:9
2 2
11.X、Y、Z有如右图所示的转化(“→”表示反应一步实现,部分物质和反应条件已略去),则符合要求
的X、Y、Z依次为
A.Cu、CuO、Cu(OH) B.C、CO、HCO
2 2 3
C.CaO、Ca(OH) 、CaCO D.HO、H、HO
2 3 2 2 2 2
12.相同质量的镁铝锌分别与相同质量20%的盐酸充分反应,产生氢气质量(直接用各金属表示)大小关
系有以下几种猜测:①Mg>Al>Zn;②Al>Mg>Zn;③Al=Mg=Zn;④Al=Mg>Zn;⑤Al=Zn>Mg;
⑥Al>Mg=Zn。其中合理的个数为
A.5个 B.4个 C.3个 D.2个
二、填空题(本题包括6个小题,每空1分,共16分)
13.空气中体积分数约为78% 的气体是______;地
壳中含量居前两位的元素所形成化合物的化学式为________。
14.右图是元素周期表中的一格。氖的相对原子质量为________;其原 子结构示意图为
_________,该元素在元素周期表中位于第二周期的______(填“最左边”、 “中间”或“最
右边”)。
15 . 煤 在 空 气 中 燃 烧 需 满 足 的 条 件 是 _________ ; 灯 帽 盖 灭 酒 精 灯 的 灭
火 原 理 是 _____ ; 氢 气 燃 烧 的 化 学 方 程 式 为
_______________。
16.右图是某反应的微观示意图,其化学方程式为_____________;以上反应生成的酸能与碱中和,如果
将Cl 通入石灰乳中可制取漂白粉[有效成分Ca(ClO) ], 化 学 方 程 式 为
2 2
______________。
17.葡萄糖酸锌 (C H O Zn )中所含人体必需的微量元素是______。2015年诺贝尔奖获得者屠呦呦发
12 22 14
现 的 青 蒿 素 是 一 种 抗 疟 疾 药 , 若 14.1g 青 蒿 素 燃 烧 生 成 33.0gCO 和 9.9gH O
2 2
,则青蒿素中氧的质量与其燃烧消耗氧气的质量之比
为________。
18.为减少污染并变废为宝,某化学小组在实验室探究工业废水的综合利用,设计了以下流程图并完成
了回收铜和硫酸锌的实验。
[ 来 源:Z+xx+k.Com](1)X的成分为_________;操作Ⅰ需用的玻璃仪器有烧杯、玻璃棒和________。
(2)加入B时反应的化学方程式为____________________。
(3)操作Ⅱ中玻璃棒的作用是_______________
____。
三、简答题(本题包括4个小题,共12分)
19.(2分)盐酸除铁锈(Fe O)的化学方程式为_________。金属铝较活泼,为什么通常铝制品却很耐腐
2 3
蚀?
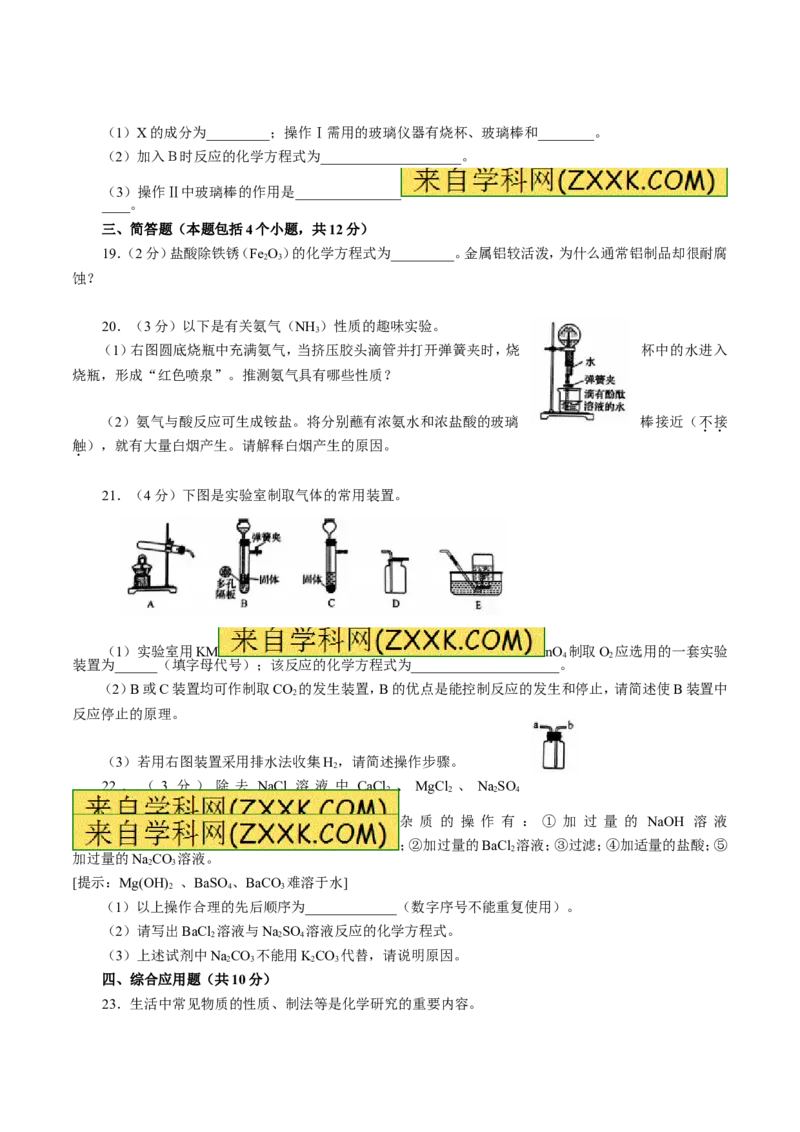
20.(3分)以下是有关氨气(NH )性质的趣味实验。
3
(1)右图圆底烧瓶中充满氨气,当挤压胶头滴管并打开弹簧夹时,烧 杯中的水进入
烧瓶,形成“红色喷泉”。推测氨气具有哪些性质?
(2)氨气与酸反应可生成铵盐。将分别蘸有浓氨水和浓盐酸的玻璃 棒接近(不接
触),就有大量白烟产生。请解释白烟产生的原因。
21.(4分)下图是实验室制取气体的常用装置。
(1)实验室用KM nO 制取O 应选用的一套实验
4 2
装置为______(填字母代号);该反应的化学方程式为_____________________。
(2)B或C装置均可作制取CO 的发生装置,B的优点是能控制反应的发生和停止,请简述使B装置中
2
反应停止的原理。
(3)若用右图装置采用排水法收集H,请简述操作步骤。
2
22 . ( 3 分 ) 除 去 NaCl 溶 液 中 CaCl 、 MgCl 、 NaSO
2 2 2 4
杂 质 的 操 作 有 : ① 加 过 量 的 NaOH 溶 液
;②加过量的BaCl 溶液;③过滤;④加适量的盐酸;⑤
2
加过量的NaCO 溶液。
2 3
[提示:Mg(OH) 、BaSO、BaCO 难溶于水]
2 4 3
(1)以上操作合理的先后顺序为_____________(数字序号不能重复使用)。
(2)请写出BaCl 溶液与NaSO 溶液反应的化学方程式。
2 2 4
(3)上述试剂中NaCO 不能用KCO 代替,请说明原因。
2 3 2 3
四、综合应用题(共10分)
23.生活中常见物质的性质、制法等是化学研究的重要内容。(1)复分解反应发生后,生成物肯定不会是_________(填“单质”或“化合物”)。
(2)盐酸与氢氧化钠溶液反应时溶液pH的变化如右图所示。
下列说法正确的是____________。
a. m点所示溶液为碱性
b. n点所示溶液中加紫色石蕊溶液显红色
c. p点所示溶液中溶质为NaCl和NaOH
d. 该图所对应操作是将盐酸滴入氢氧化钠溶液中
(3)浓硫酸和浓盐酸敞口放置均会变稀,这是为什么?
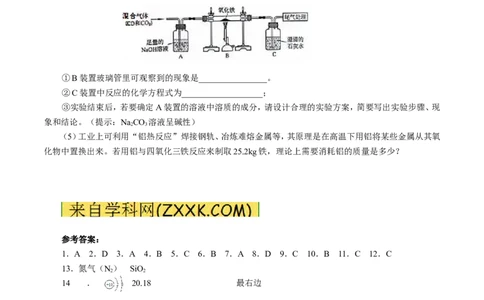
(4)下图装置可做一氧化碳还原氧化铁的实验,并检验生成的气体产物。
①B装置玻璃管里可观察到的现象是________________。
②C装置中反应的化学方程式为___________________;
③实验结束后,若要确定A装置的溶液中溶质的成分,请设计合理的实验方案,简要写出实验步骤、现
象和结论。(提示:NaCO 溶液呈碱性)
2 3
(5)工业上可利用“铝热反应”焊接钢轨、冶炼难熔金属等,其原理是在高温下用铝将某些金属从其氧
化物中置换出来。若用铝与四氧化三铁反应来制取25.2kg铁,理论上需要消耗铝的质量是多少?
参考答案:
1.A 2.D 3.A 4.B 5.C 6.B 7.A 8.D 9.C 10.B 11.C 12.C
13.氮气(N) SiO
2 2
14 . 20.18 最右边
点燃
15.温度达到煤的着火点 隔绝空气 2H+O 2HO
2 2 2
16.Cl +H O= HCl+HClO 2Cl +2Ca(OH) =CaCl +Ca(ClO) +2H O
2 2 2 2 2 2 2
17.Zn(锌) 4:28.8(5:36)
18.(1)Zn、Cu (2)Zn+ HSO = ZnSO +H ↑
2 4 4 2
(3)搅拌,防止局部过热液体飞溅
19.Fe O +6HCl = 2FeCl +3H O
2 3 3 2
铝与氧气反应生成一层致密的氧化铝薄膜,阻止铝进一步氧化
20.(1)易溶于水 水溶液显碱性 (2)浓盐酸挥发出的HCl与浓氨水挥发出的NH 反应生成白色固
3
体NH Cl
421.(1)AD(或AE) 2KMnO KMnO +MnO +O ↑
4 2 4 2 2
(2)关闭弹簧夹,产生的气体把酸液压回到长颈漏斗中,石灰石和盐酸脱离,反应停止。
(3)集气瓶中注满水,插入带导管的橡皮塞,向导气管a通入H,直至排净集气瓶中的水。
2
22.(1)②①⑤③④ (或 ①②⑤③④)
(2)BaCl +Na SO =BaSO ↓+2NaCl
2 2 4 4 [来源:Zxxk.Com]
(3)若用KCO,会引入新杂质KCl
2 3
23.(1)单质 (2)c
(3)浓硫酸有吸水性,溶剂量增加,溶液变稀;浓盐酸有挥发性,溶质的量减少,溶液变稀。
(4)①红色固体变黑色 ② Ca(OH) +CO = CaCO ↓+H O ③取少量 A 装置中的
2 2 3 2
溶液,加入足量的BaCl 溶液,若有白色沉淀生成,则
2
溶质中含有NaCO;静置,向上层清液中滴加无色酚酞溶液,若溶液变红色,则溶质中还含有NaOH。
2 3
(5)设需要消耗铝的质量为x
8Al +3Fe O 4Al O +9Fe
3 4 2 3
216 504
x 25.2kg
216/504=x /25.2kg 解得
x=10.8kg