文档内容
2018 北京市中考化学真题及答案
一、选择题(每小题1分,共12分)
1.(1分)下列物质能使紫色石蕊溶液变红的是( )
A.CO B.O C.NaCl D.NaOH
2 2
2.(1分)下列含金属元素的物质是( )
A.HSO B.AlO C.NO D.PO
2 4 2 3 2 2 5
3.(1分)一些物质的pH范围如下,其中呈碱性的是( )
A.油污净(12~13) B.西瓜汁(5~6)C.洁厕灵(1~2)D.橘子汁(3~4)
4.(1分)下列金属不能与CuSO 溶液反应的是( )
4
A.Ag B.Fe C.Zn D.Al
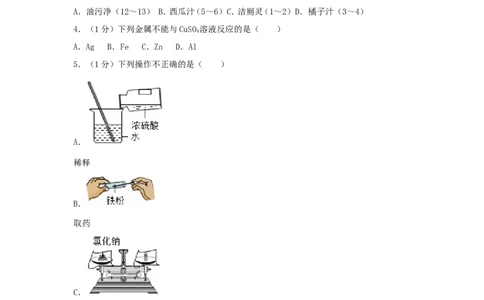
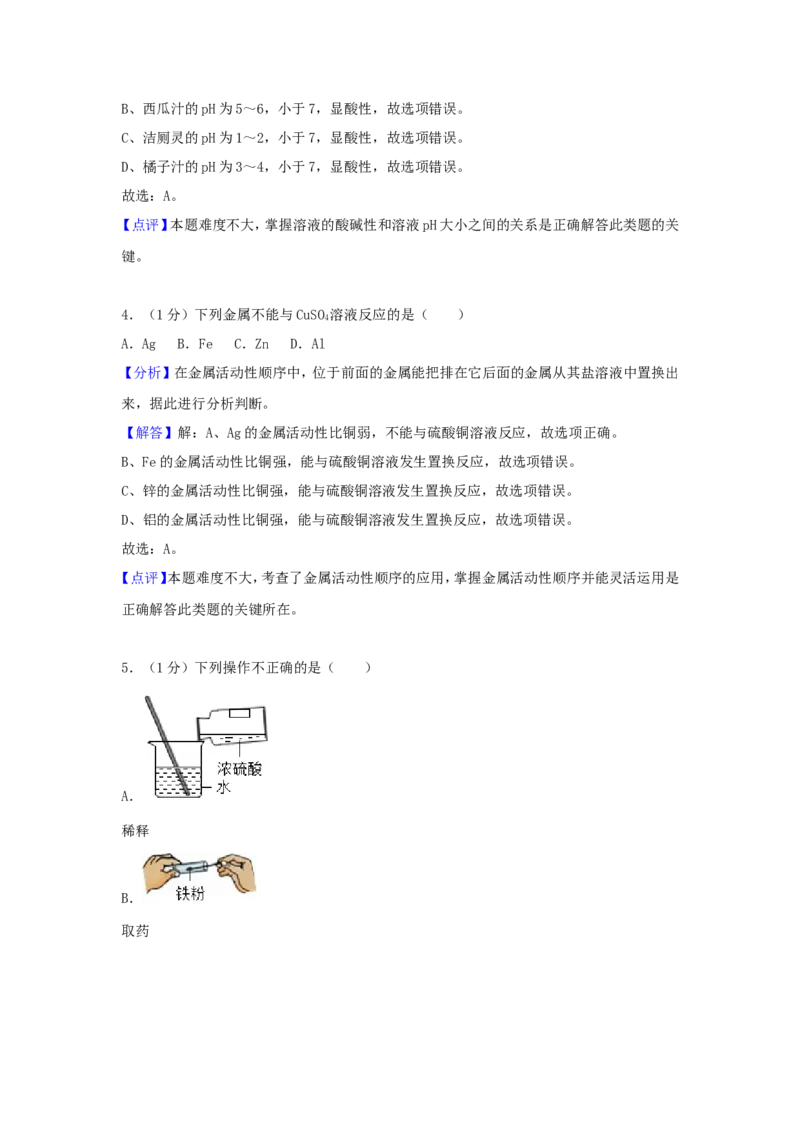
5.(1分)下列操作不正确的是( )
A.
稀释
B.
取药
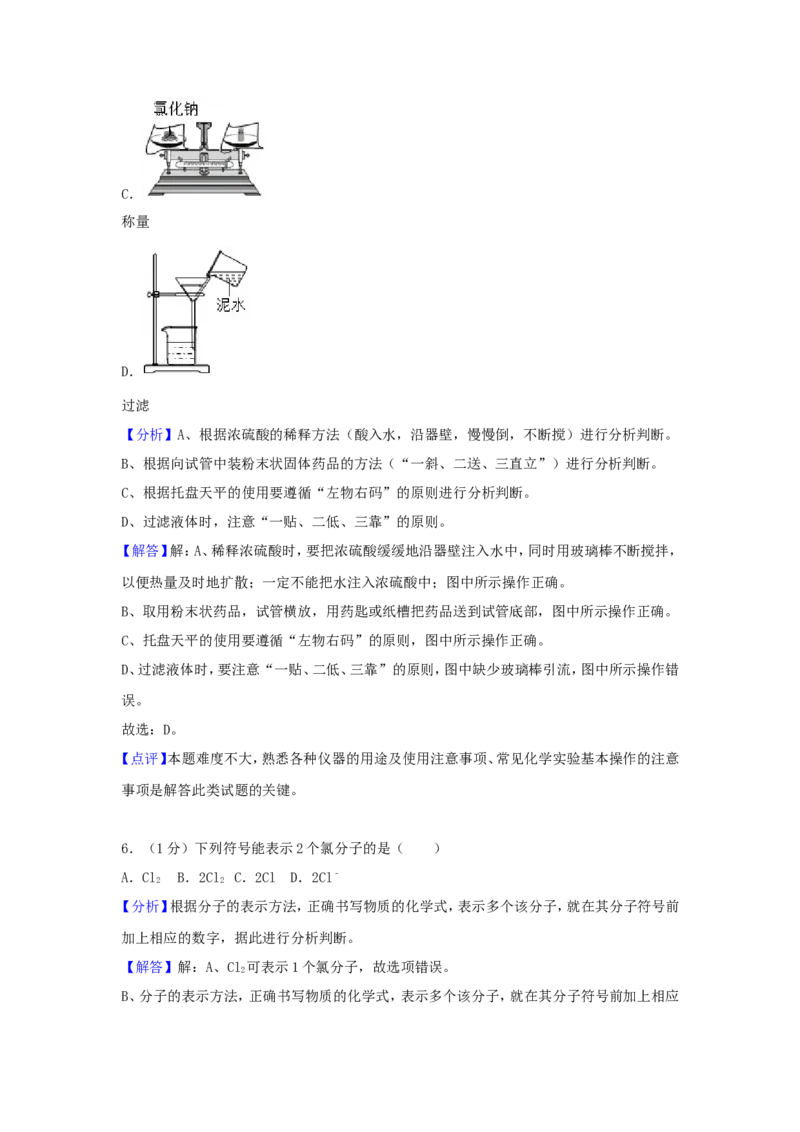
C.
称量
D.
过滤6.(1分)下列符号能表示2个氯分子的是( )
A.Cl B.2Cl C.2Cl D.2Cl﹣
2 2
7.(1分)下列物质能与NaOH反应的是( )
A.Fe B.CO C.FeO D.NaCl
2 2 3
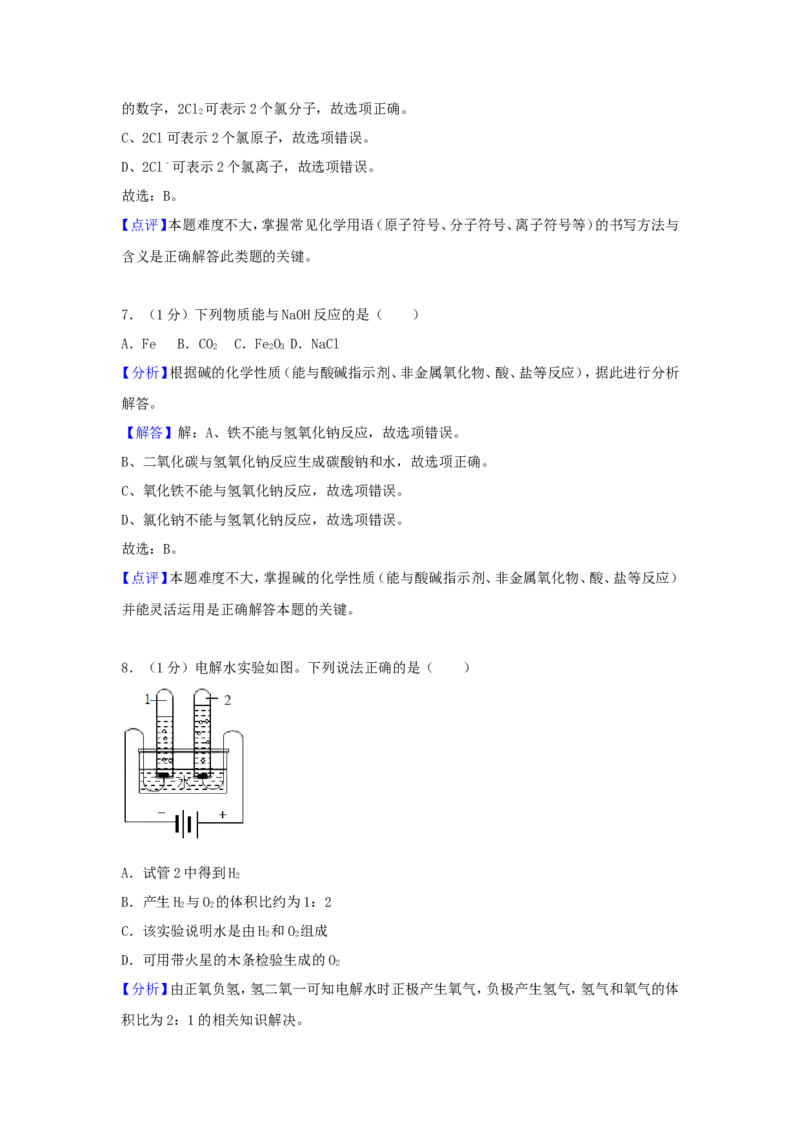
8.(1分)电解水实验如图。下列说法正确的是( )
A.试管2中得到H
2
B.产生H 与O 的体积比约为1:2
2 2
C.该实验说明水是由H 和O 组成
2 2
D.可用带火星的木条检验生成的O
2
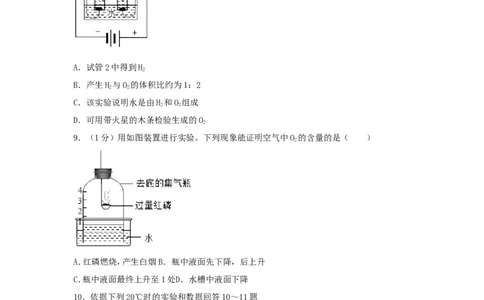
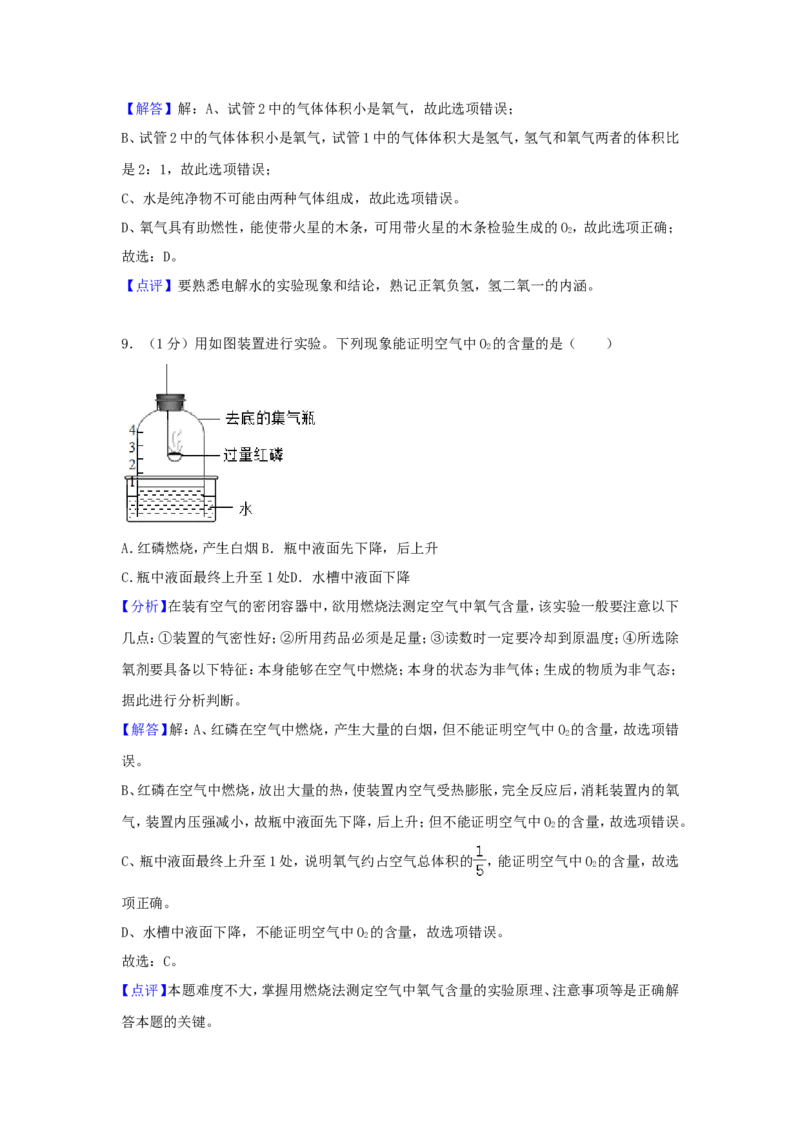
9.(1分)用如图装置进行实验。下列现象能证明空气中O 的含量的是( )
2
A.红磷燃烧,产生白烟 B.瓶中液面先下降,后上升
C.瓶中液面最终上升至1处D.水槽中液面下降
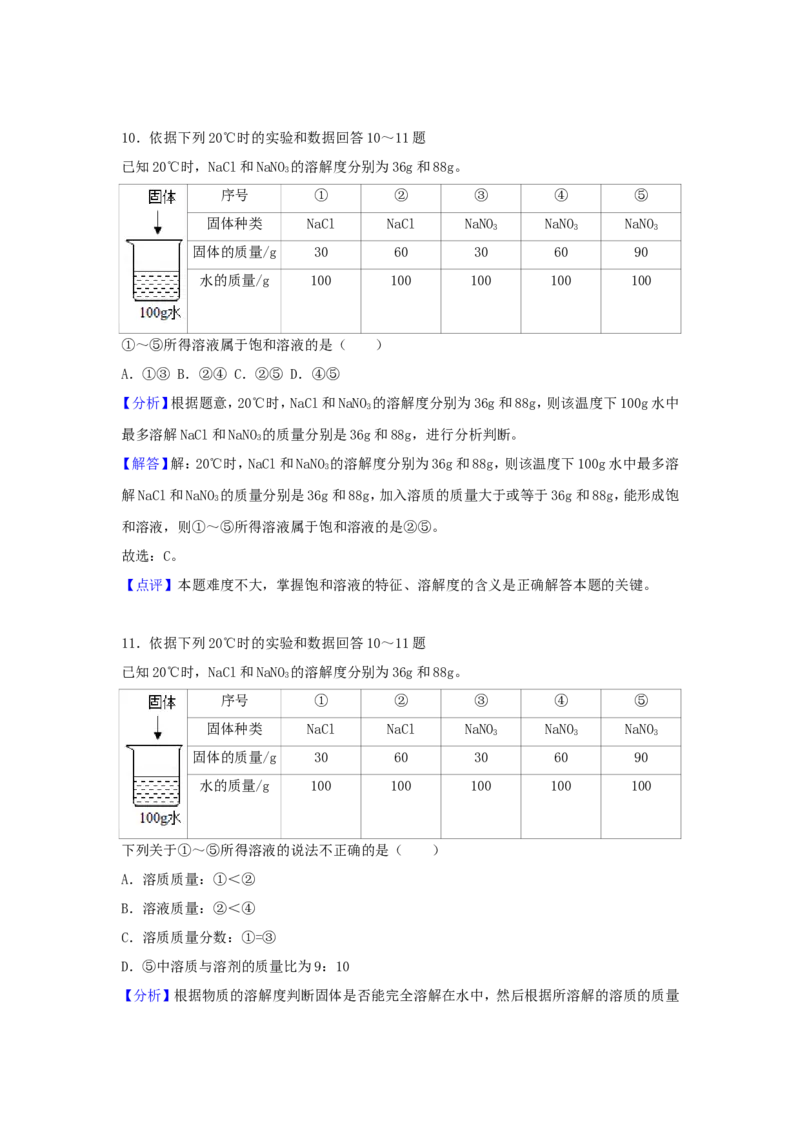
10.依据下列20℃时的实验和数据回答10~11题
已知20℃时,NaCl和NaNO 的溶解度分别为36g和88g。
3
序号 ① ② ③ ④ ⑤
固体种类 NaCl NaCl NaNO NaNO NaNO
3 3 3
固体的质量/g 30 60 30 60 90
水的质量/g 100 100 100 100 100
①~⑤所得溶液属于饱和溶液的是( )A.①③ B.②④ C.②⑤ D.④⑤
11.依据下列20℃时的实验和数据回答10~11题
已知20℃时,NaCl和NaNO 的溶解度分别为36g和88g。
3
序号 ① ② ③ ④ ⑤
固体种类 NaCl NaCl NaNO NaNO NaNO
3 3 3
固体的质量/g 30 60 30 60 90
水的质量/g 100 100 100 100 100
下列关于①~⑤所得溶液的说法不正确的是( )
A.溶质质量:①<②
B.溶液质量:②<④
C.溶质质量分数:①=③
D.⑤中溶质与溶剂的质量比为9:10
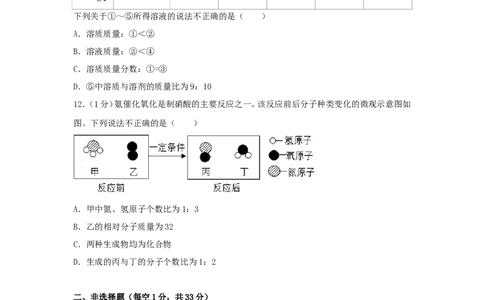
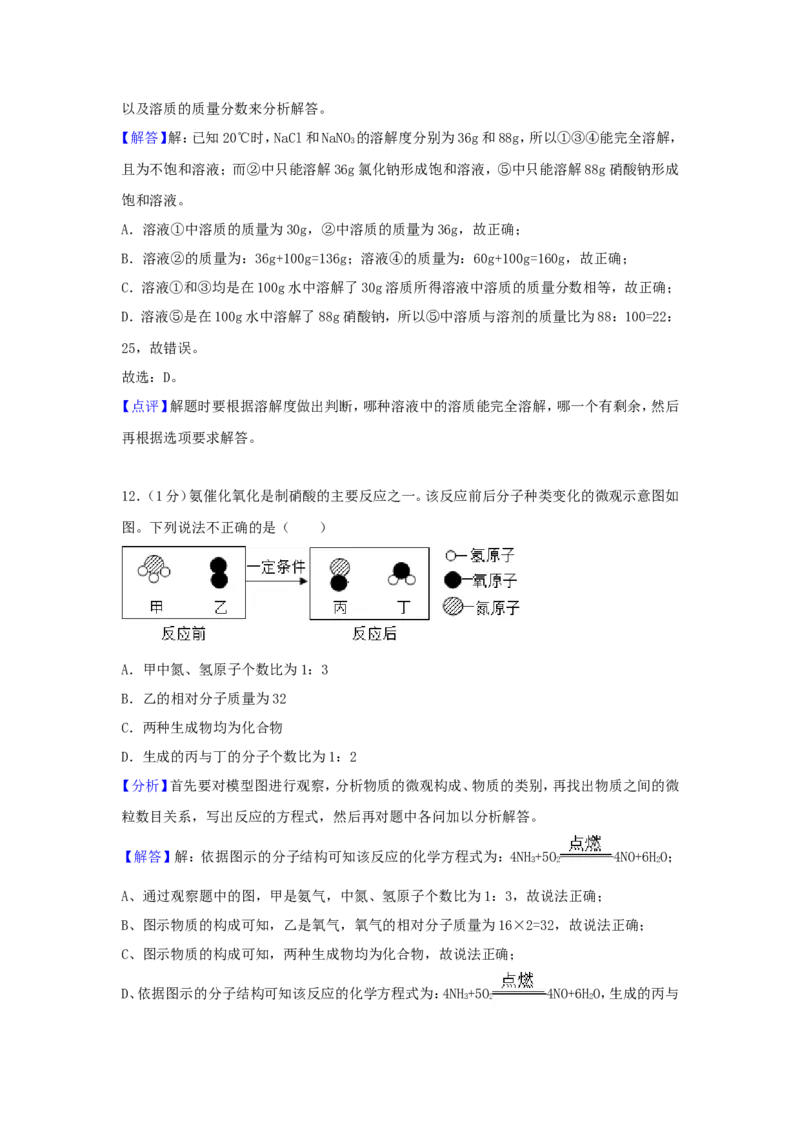
12.(1分)氨催化氧化是制硝酸的主要反应之一。该反应前后分子种类变化的微观示意图如
图。下列说法不正确的是( )
A.甲中氮、氢原子个数比为1:3
B.乙的相对分子质量为32
C.两种生成物均为化合物
D.生成的丙与丁的分子个数比为1:2
二、非选择题(每空1分,共33分)
13.(2分)补齐连线。从A或B中任选一个作答,若均作答,按A计分。
A 物质﹣用途 B 物质﹣﹣主要成分
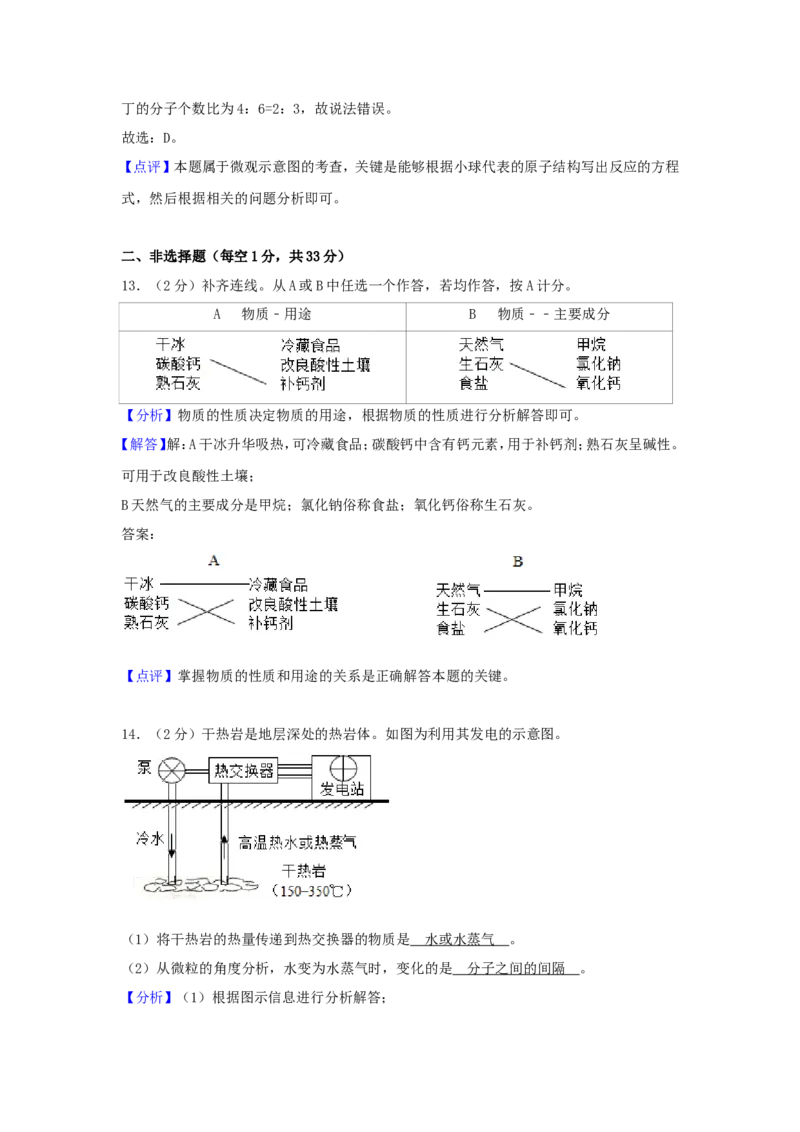
14.(2分)干热岩是地层深处的热岩体。如图为利用其发电的示意图。(1)将干热岩的热量传递到热交换器的物质是 。
(2)从微粒的角度分析,水变为水蒸气时,变化的是 。
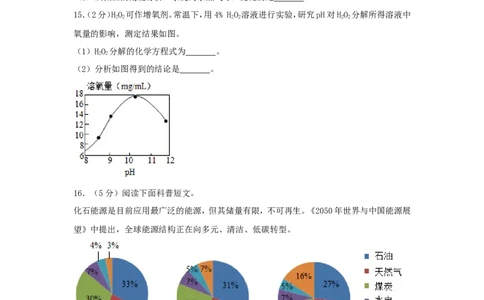
15.(2分)HO 可作增氧剂。常温下,用4% HO 溶液进行实验,研究pH对HO 分解所得溶液中
2 2 2 2 2 2
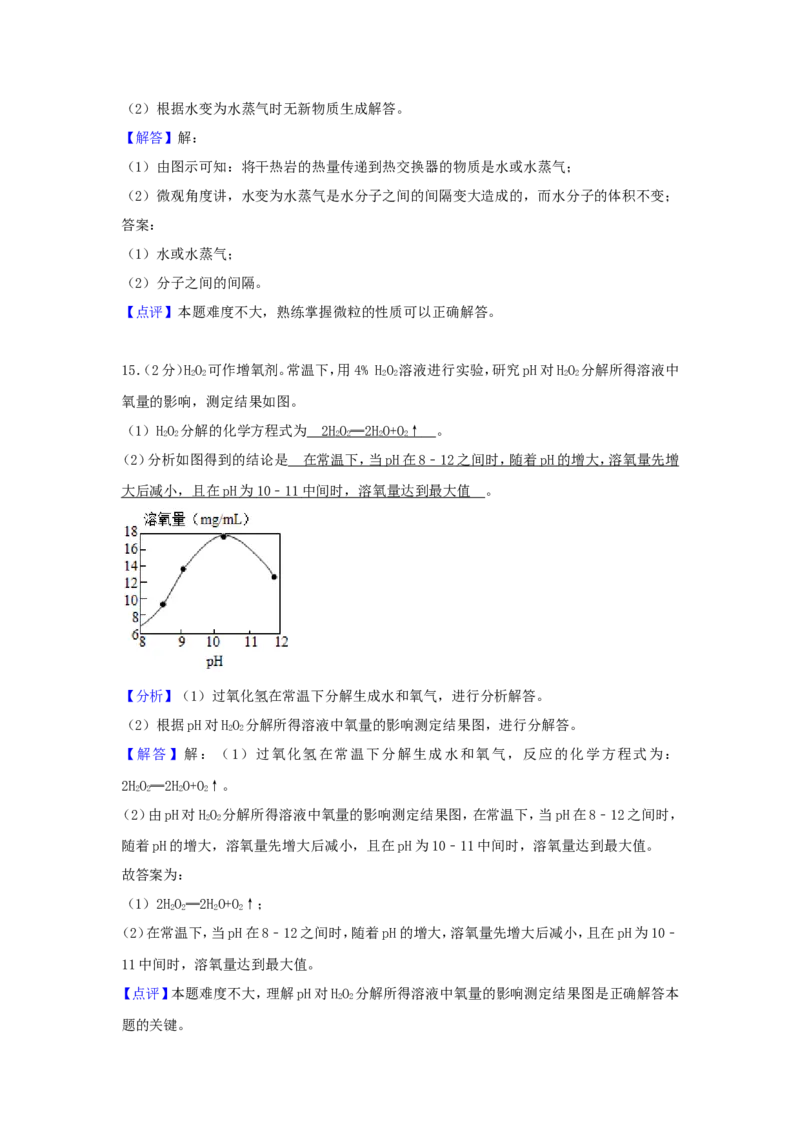
氧量的影响,测定结果如图。
(1)HO 分解的化学方程式为 。
2 2
(2)分析如图得到的结论是 。
16.(5分)阅读下面科普短文。
化石能源是目前应用最广泛的能源,但其储量有限,不可再生。《2050年世界与中国能源展
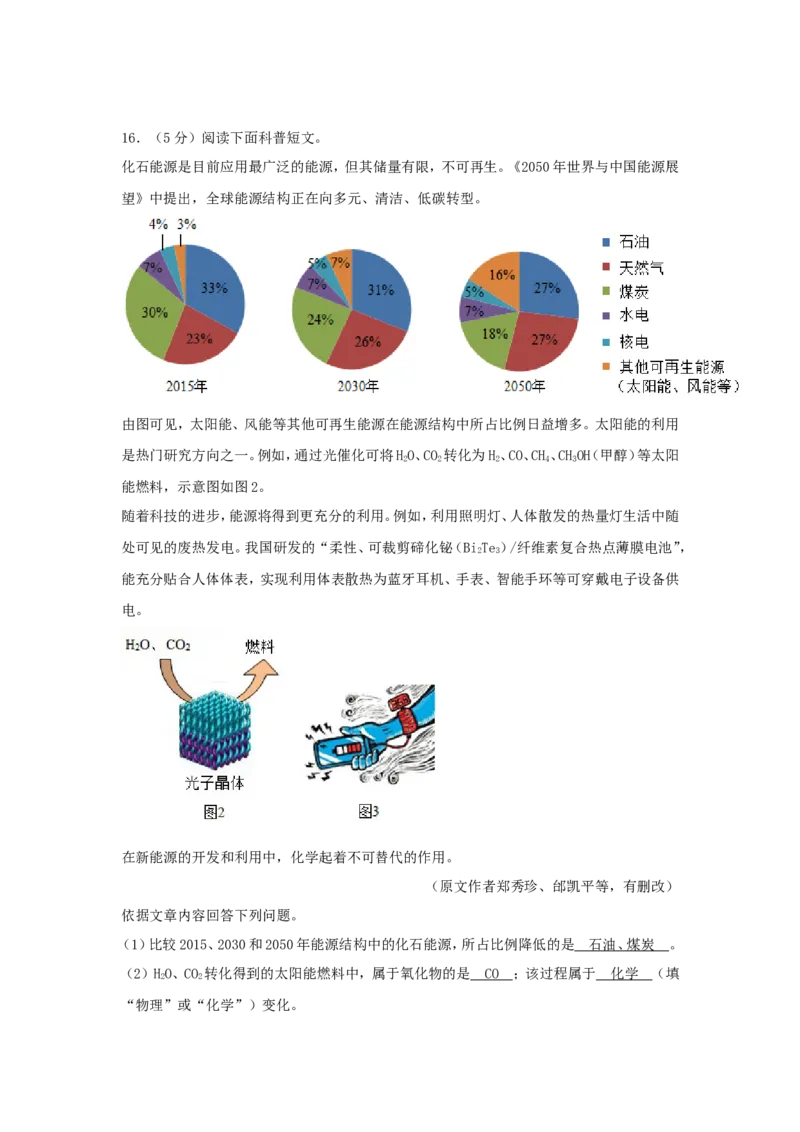
望》中提出,全球能源结构正在向多元、清洁、低碳转型。
由图可见,太阳能、风能等其他可再生能源在能源结构中所占比例日益增多。太阳能的利用
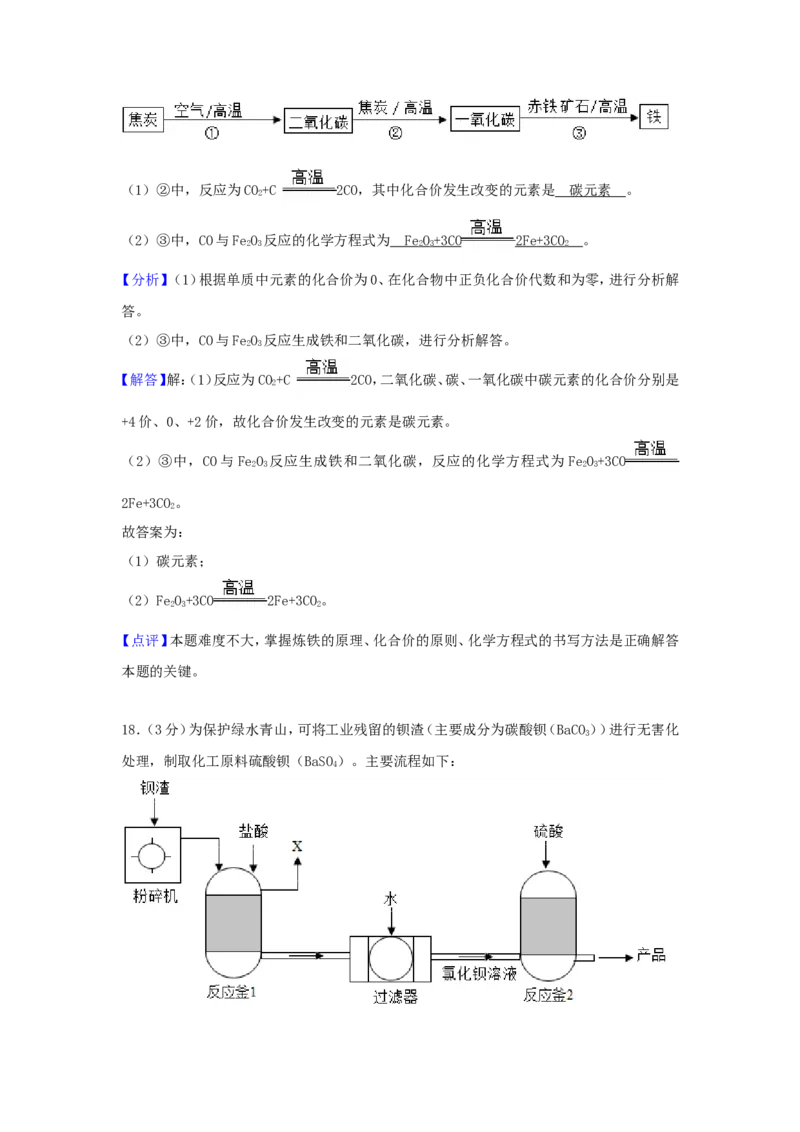
是热门研究方向之一。例如,通过光催化可将HO、CO 转化为H、CO、CH、CHOH(甲醇)等太阳
2 2 2 4 3
能燃料,示意图如图2。
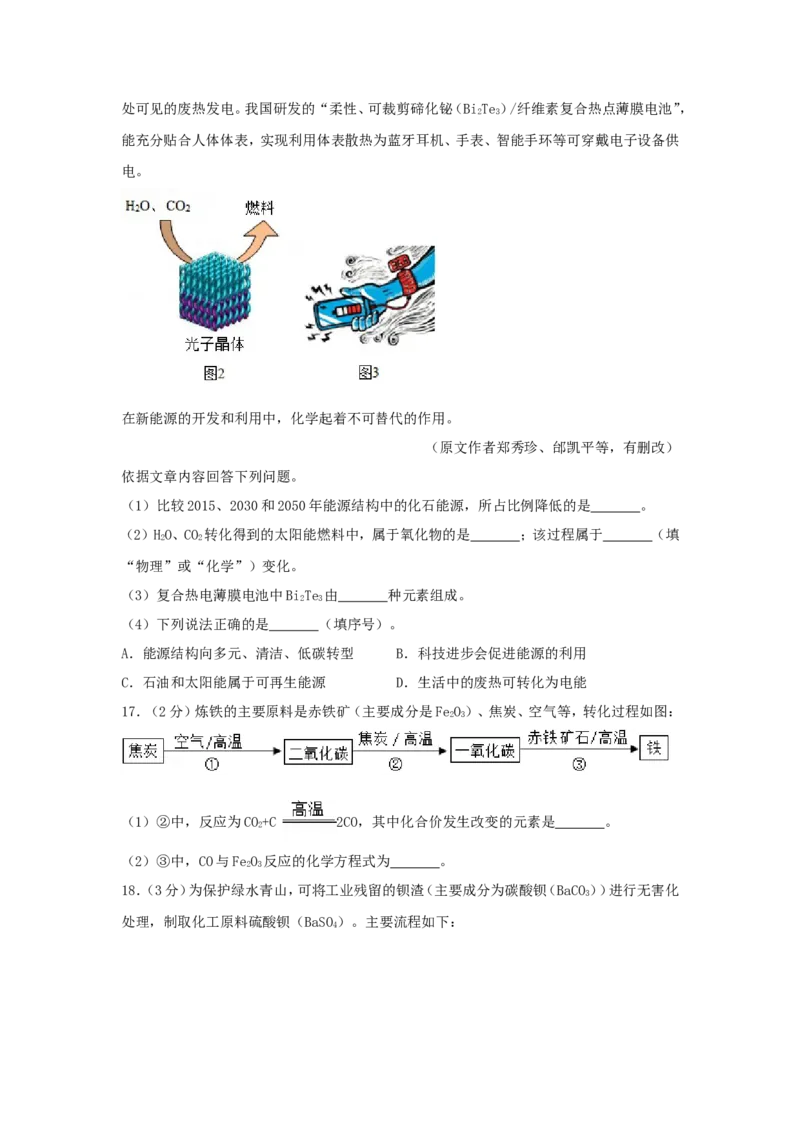
随着科技的进步,能源将得到更充分的利用。例如,利用照明灯、人体散发的热量灯生活中随处可见的废热发电。我国研发的“柔性、可裁剪碲化铋(BiTe)/纤维素复合热点薄膜电池”,
2 3
能充分贴合人体体表,实现利用体表散热为蓝牙耳机、手表、智能手环等可穿戴电子设备供
电。
在新能源的开发和利用中,化学起着不可替代的作用。
(原文作者郑秀珍、邰凯平等,有删改)
依据文章内容回答下列问题。
(1)比较2015、2030和2050年能源结构中的化石能源,所占比例降低的是 。
(2)HO、CO 转化得到的太阳能燃料中,属于氧化物的是 ;该过程属于 (填
2 2
“物理”或“化学”)变化。
(3)复合热电薄膜电池中BiTe 由 种元素组成。
2 3
(4)下列说法正确的是 (填序号)。
A.能源结构向多元、清洁、低碳转型 B.科技进步会促进能源的利用
C.石油和太阳能属于可再生能源 D.生活中的废热可转化为电能
17.(2分)炼铁的主要原料是赤铁矿(主要成分是FeO)、焦炭、空气等,转化过程如图:
2 3
(1)②中,反应为CO+C 2CO,其中化合价发生改变的元素是 。
2
(2)③中,CO与FeO 反应的化学方程式为 。
2 3
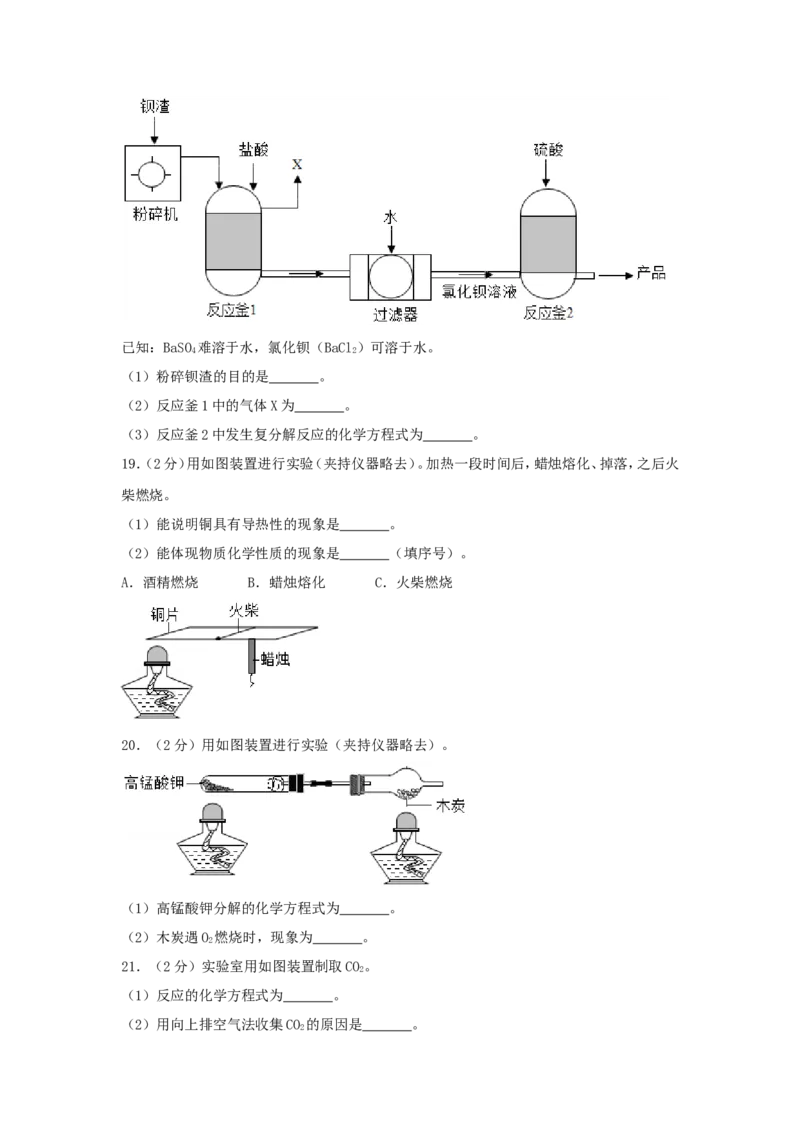
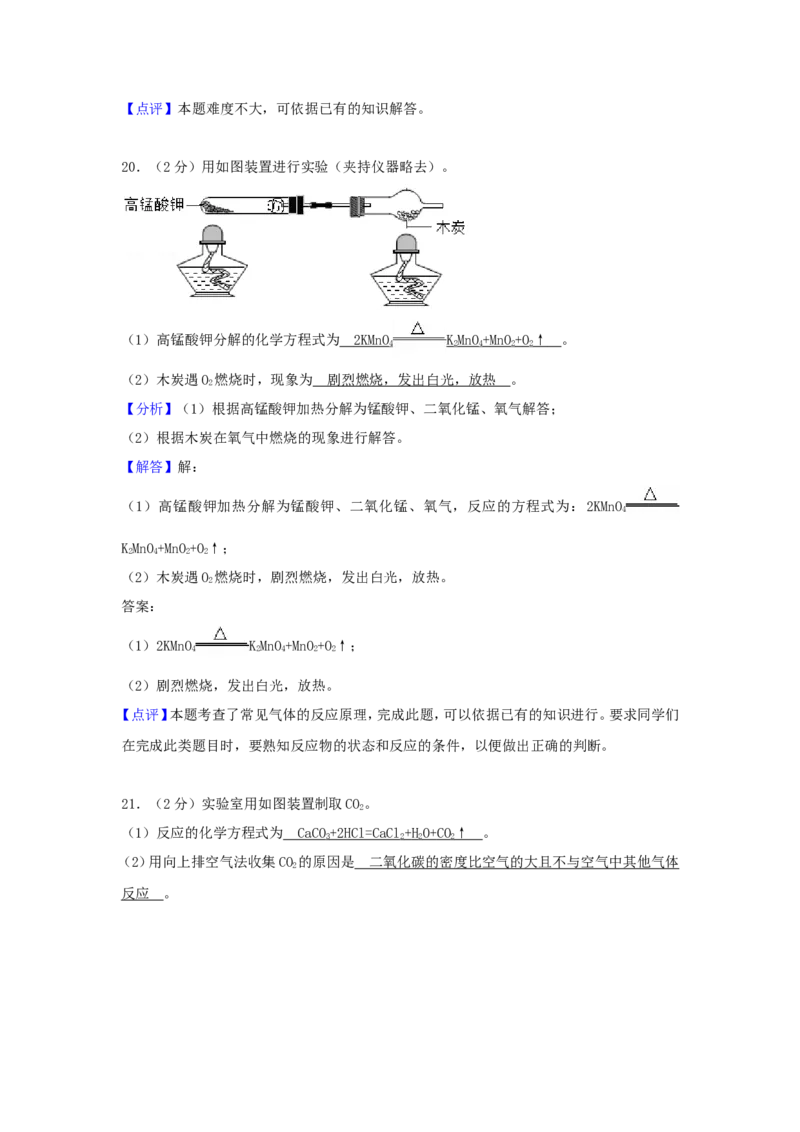
18.(3分)为保护绿水青山,可将工业残留的钡渣(主要成分为碳酸钡(BaCO))进行无害化
3
处理,制取化工原料硫酸钡(BaSO)。主要流程如下:
4已知:BaSO 难溶于水,氯化钡(BaCl)可溶于水。
4 2
(1)粉碎钡渣的目的是 。
(2)反应釜1中的气体X为 。
(3)反应釜2中发生复分解反应的化学方程式为 。
19.(2分)用如图装置进行实验(夹持仪器略去)。加热一段时间后,蜡烛熔化、掉落,之后火
柴燃烧。
(1)能说明铜具有导热性的现象是 。
(2)能体现物质化学性质的现象是 (填序号)。
A.酒精燃烧 B.蜡烛熔化 C.火柴燃烧
20.(2分)用如图装置进行实验(夹持仪器略去)。
(1)高锰酸钾分解的化学方程式为 。
(2)木炭遇O 燃烧时,现象为 。
2
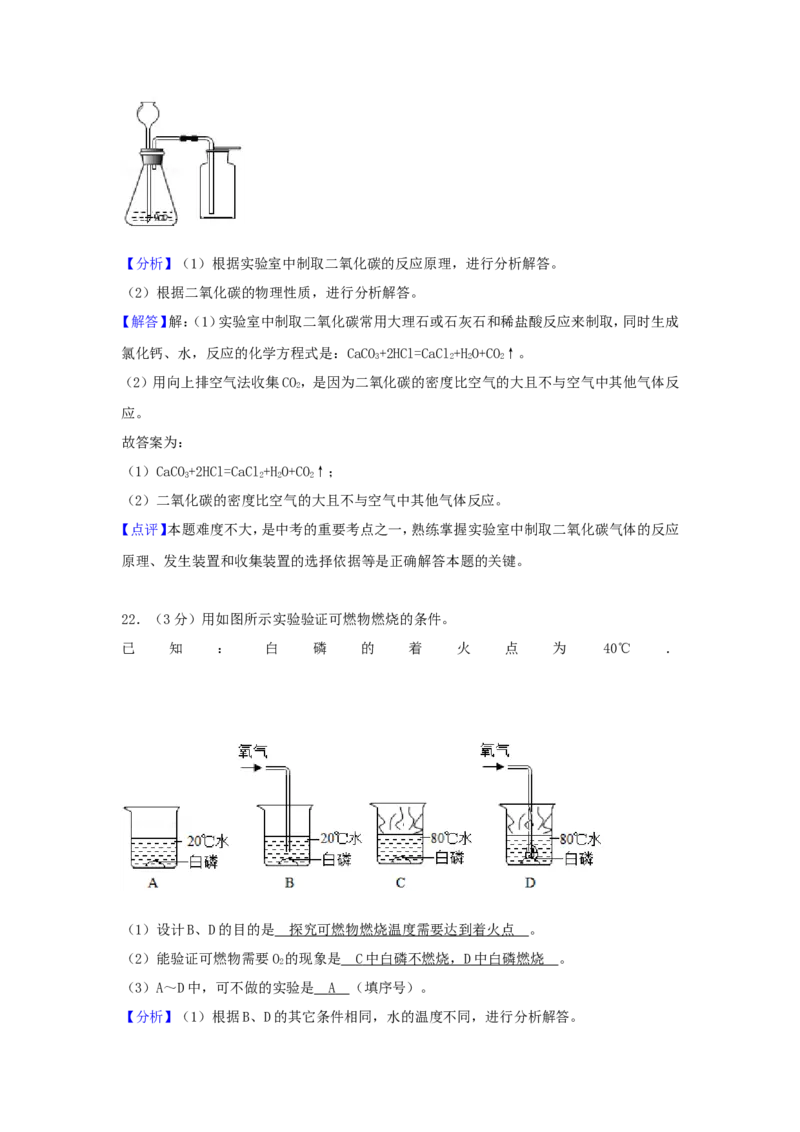
21.(2分)实验室用如图装置制取CO。
2
(1)反应的化学方程式为 。
(2)用向上排空气法收集CO 的原因是 。
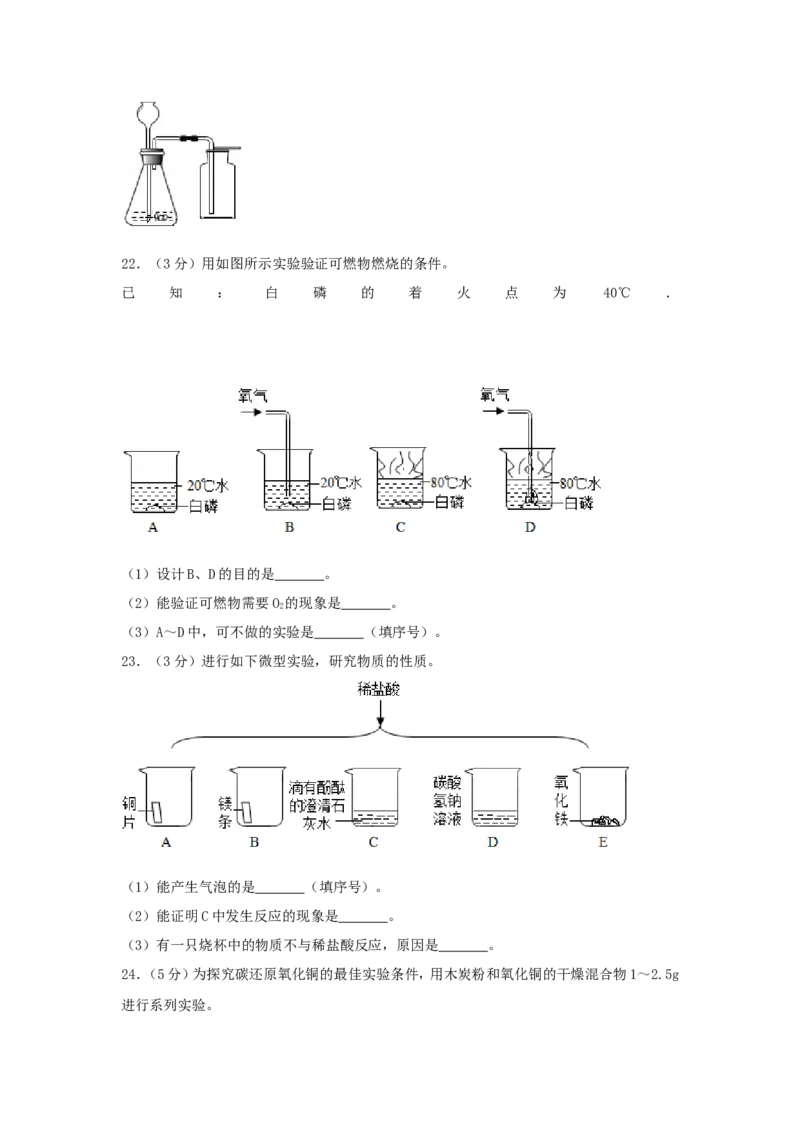
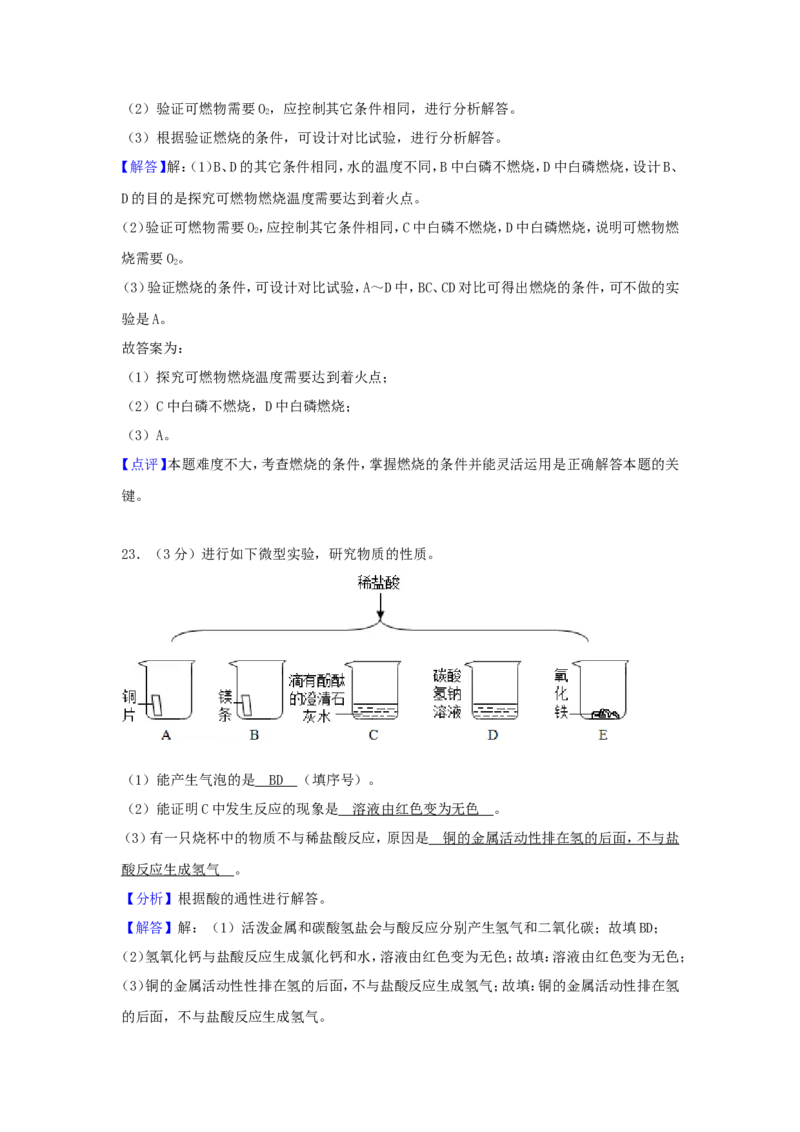
222.(3分)用如图所示实验验证可燃物燃烧的条件。
已 知 : 白 磷 的 着 火 点 为 40℃ .
(1)设计B、D的目的是 。
(2)能验证可燃物需要O 的现象是 。
2
(3)A~D中,可不做的实验是 (填序号)。
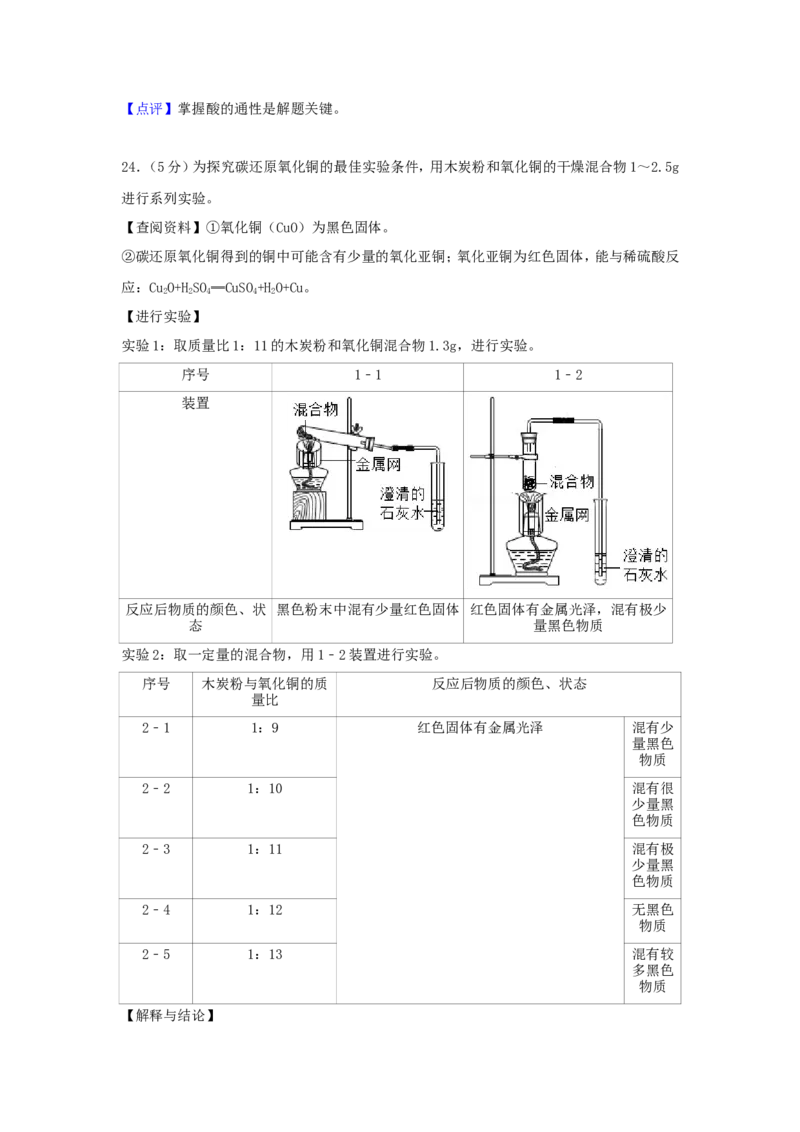
23.(3分)进行如下微型实验,研究物质的性质。
(1)能产生气泡的是 (填序号)。
(2)能证明C中发生反应的现象是 。
(3)有一只烧杯中的物质不与稀盐酸反应,原因是 。
24.(5分)为探究碳还原氧化铜的最佳实验条件,用木炭粉和氧化铜的干燥混合物1~2.5g
进行系列实验。【查阅资料】①氧化铜(CuO)为黑色固体。
②碳还原氧化铜得到的铜中可能含有少量的氧化亚铜;氧化亚铜为红色固体,能与稀硫酸反
应:CuO+HSO═CuSO+HO+Cu。
2 2 4 4 2
【进行实验】
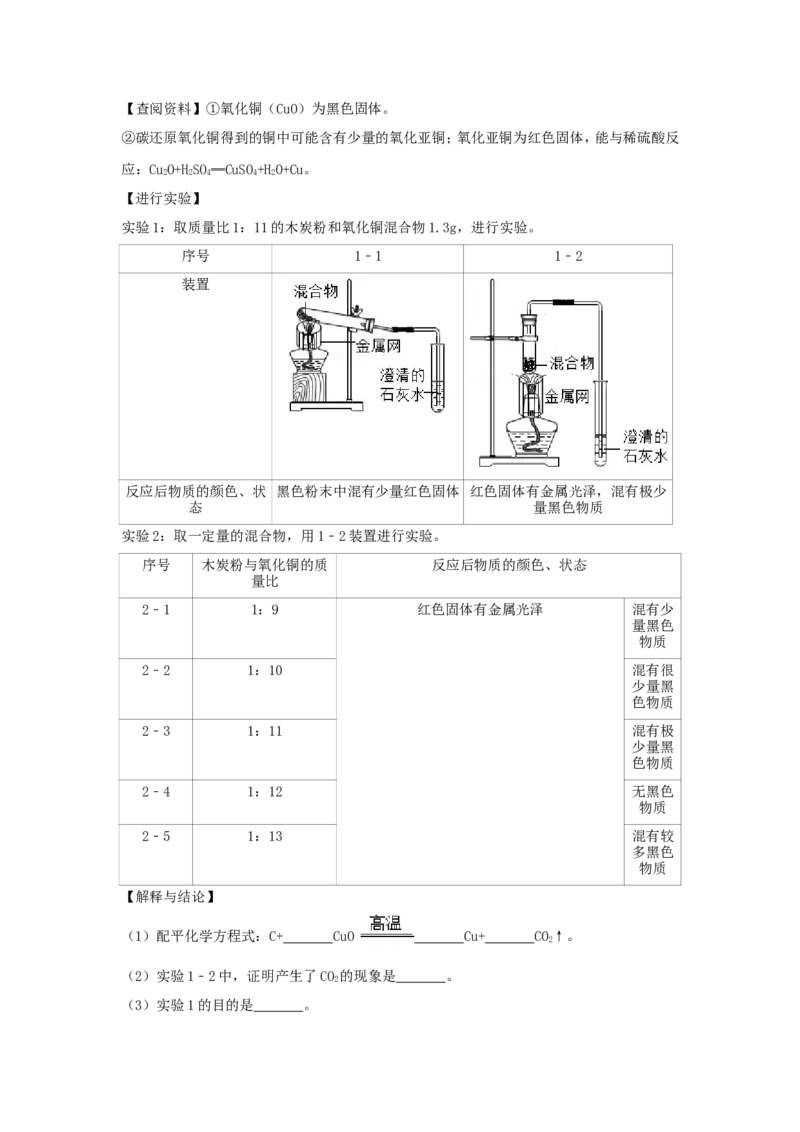
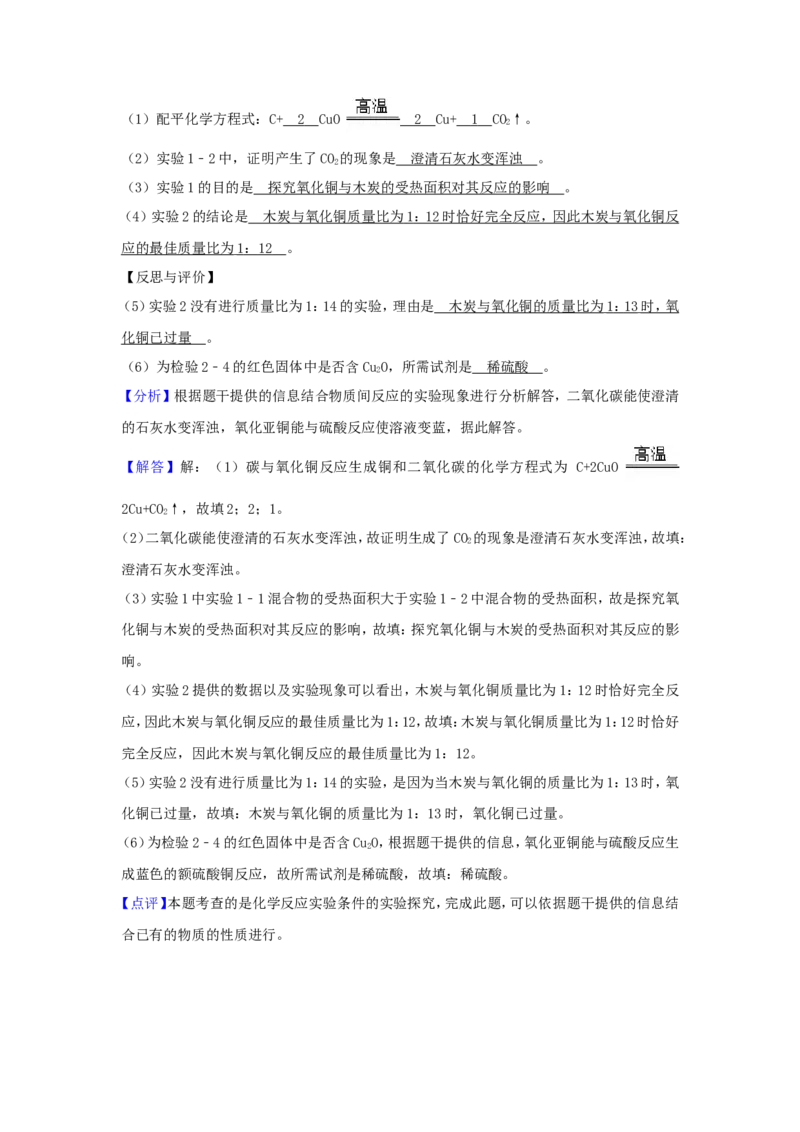
实验1:取质量比1:11的木炭粉和氧化铜混合物1.3g,进行实验。
序号 1﹣1 1﹣2
装置
反应后物质的颜色、状 黑色粉末中混有少量红色固体 红色固体有金属光泽,混有极少
态 量黑色物质
实验2:取一定量的混合物,用1﹣2装置进行实验。
序号 木炭粉与氧化铜的质 反应后物质的颜色、状态
量比
2﹣1 1:9 红色固体有金属光泽 混有少
量黑色
物质
2﹣2 1:10 混有很
少量黑
色物质
2﹣3 1:11 混有极
少量黑
色物质
2﹣4 1:12 无黑色
物质
2﹣5 1:13 混有较
多黑色
物质
【解释与结论】
(1)配平化学方程式:C+ CuO Cu+ CO↑。
2
(2)实验1﹣2中,证明产生了CO 的现象是 。
2
(3)实验1的目的是 。(4)实验2的结论是 。
【反思与评价】
(5)实验2没有进行质量比为1:14的实验,理由是 。
(6)为检验2﹣4的红色固体中是否含CuO,所需试剂是 。
22018年北京市中考化学试卷
参考答案与试题解析
一、选择题(每小题1分,共12分)
1.(1分)下列物质能使紫色石蕊溶液变红的是( )
A.CO B.O C.NaCl D.NaOH
2 2
【分析】紫色石蕊溶液遇酸性溶液变红,遇碱性溶液变蓝,进行分析判断。
【解答】解:A、二氧化碳与水反应生成碳酸,碳酸能使紫色石蕊溶液变红,故选项说法正确。
B、氧气不能使紫色石蕊溶液变红,故选项错误。
C、氯化钠溶液显中性,不能使紫色石蕊溶液变红,故选项错误。
D、氢氧化钠溶液显碱性,能使紫色石蕊溶液变蓝,故选项错误。
故选:A。
【点评】本题难度不大,掌握紫色石蕊溶液遇酸碱溶液的变色情况是正确解答本题的关键。
2.(1分)下列含金属元素的物质是( )
A.HSO B.AlO C.NO D.PO
2 4 2 3 2 2 5
【分析】根据化学元素汉字名称的偏旁可辨别元素的种类,金属元素名称一般有“钅”字旁,
固态非金属元素名称有“石”字旁,气态非金属元素名称有“气”字头;据此进行解答分析。
【解答】解:A、H、S、O均为非金属元素,错误;
B、铝为金属元素,正确;
C、N、O均为非金属元素,错误;
D、均为非金属元素,错误。
故选:B。
【点评】本题考查元素,题目难度不大,关键是要熟记常见元素的符号,要注意汉字中是否含
有钅字旁。
3.(1分)一些物质的pH范围如下,其中呈碱性的是( )
A.油污净(12~13) B.西瓜汁(5~6)C.洁厕灵(1~2)D.橘子汁(3~4)
【分析】当溶液的pH等于7时,呈中性;当溶液的pH小于7时,呈酸性;当溶液的pH大于7时,
呈碱性;据此进行分析判断。
【解答】解:A、油污净的pH为12~13,大于7,显碱性,故选项正确。B、西瓜汁的pH为5~6,小于7,显酸性,故选项错误。
C、洁厕灵的pH为1~2,小于7,显酸性,故选项错误。
D、橘子汁的pH为3~4,小于7,显酸性,故选项错误。
故选:A。
【点评】本题难度不大,掌握溶液的酸碱性和溶液pH大小之间的关系是正确解答此类题的关
键。
4.(1分)下列金属不能与CuSO 溶液反应的是( )
4
A.Ag B.Fe C.Zn D.Al
【分析】在金属活动性顺序中,位于前面的金属能把排在它后面的金属从其盐溶液中置换出
来,据此进行分析判断。
【解答】解:A、Ag的金属活动性比铜弱,不能与硫酸铜溶液反应,故选项正确。
B、Fe的金属活动性比铜强,能与硫酸铜溶液发生置换反应,故选项错误。
C、锌的金属活动性比铜强,能与硫酸铜溶液发生置换反应,故选项错误。
D、铝的金属活动性比铜强,能与硫酸铜溶液发生置换反应,故选项错误。
故选:A。
【点评】本题难度不大,考查了金属活动性顺序的应用,掌握金属活动性顺序并能灵活运用是
正确解答此类题的关键所在。
5.(1分)下列操作不正确的是( )
A.
稀释
B.
取药C.
称量
D.
过滤
【分析】A、根据浓硫酸的稀释方法(酸入水,沿器壁,慢慢倒,不断搅)进行分析判断。
B、根据向试管中装粉末状固体药品的方法(“一斜、二送、三直立”)进行分析判断。
C、根据托盘天平的使用要遵循“左物右码”的原则进行分析判断。
D、过滤液体时,注意“一贴、二低、三靠”的原则。
【解答】解:A、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,
以便热量及时地扩散;一定不能把水注入浓硫酸中;图中所示操作正确。
B、取用粉末状药品,试管横放,用药匙或纸槽把药品送到试管底部,图中所示操作正确。
C、托盘天平的使用要遵循“左物右码”的原则,图中所示操作正确。
D、过滤液体时,要注意“一贴、二低、三靠”的原则,图中缺少玻璃棒引流,图中所示操作错
误。
故选:D。
【点评】本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意
事项是解答此类试题的关键。
6.(1分)下列符号能表示2个氯分子的是( )
A.Cl B.2Cl C.2Cl D.2Cl﹣
2 2
【分析】根据分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其分子符号前
加上相应的数字,据此进行分析判断。
【解答】解:A、Cl 可表示1个氯分子,故选项错误。
2
B、分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其分子符号前加上相应的数字,2Cl 可表示2个氯分子,故选项正确。
2
C、2Cl可表示2个氯原子,故选项错误。
D、2Cl﹣可表示2个氯离子,故选项错误。
故选:B。
【点评】本题难度不大,掌握常见化学用语(原子符号、分子符号、离子符号等)的书写方法与
含义是正确解答此类题的关键。
7.(1分)下列物质能与NaOH反应的是( )
A.Fe B.CO C.FeO D.NaCl
2 2 3
【分析】根据碱的化学性质(能与酸碱指示剂、非金属氧化物、酸、盐等反应),据此进行分析
解答。
【解答】解:A、铁不能与氢氧化钠反应,故选项错误。
B、二氧化碳与氢氧化钠反应生成碳酸钠和水,故选项正确。
C、氧化铁不能与氢氧化钠反应,故选项错误。
D、氯化钠不能与氢氧化钠反应,故选项错误。
故选:B。
【点评】本题难度不大,掌握碱的化学性质(能与酸碱指示剂、非金属氧化物、酸、盐等反应)
并能灵活运用是正确解答本题的关键。
8.(1分)电解水实验如图。下列说法正确的是( )
A.试管2中得到H
2
B.产生H 与O 的体积比约为1:2
2 2
C.该实验说明水是由H 和O 组成
2 2
D.可用带火星的木条检验生成的O
2
【分析】由正氧负氢,氢二氧一可知电解水时正极产生氧气,负极产生氢气,氢气和氧气的体
积比为2:1的相关知识解决。【解答】解:A、试管2中的气体体积小是氧气,故此选项错误;
B、试管2中的气体体积小是氧气,试管1中的气体体积大是氢气,氢气和氧气两者的体积比
是2:1,故此选项错误;
C、水是纯净物不可能由两种气体组成,故此选项错误。
D、氧气具有助燃性,能使带火星的木条,可用带火星的木条检验生成的O,故此选项正确;
2
故选:D。
【点评】要熟悉电解水的实验现象和结论,熟记正氧负氢,氢二氧一的内涵。
9.(1分)用如图装置进行实验。下列现象能证明空气中O 的含量的是( )
2
A.红磷燃烧,产生白烟 B.瓶中液面先下降,后上升
C.瓶中液面最终上升至1处D.水槽中液面下降
【分析】在装有空气的密闭容器中,欲用燃烧法测定空气中氧气含量,该实验一般要注意以下
几点:①装置的气密性好;②所用药品必须是足量;③读数时一定要冷却到原温度;④所选除
氧剂要具备以下特征:本身能够在空气中燃烧;本身的状态为非气体;生成的物质为非气态;
据此进行分析判断。
【解答】解:A、红磷在空气中燃烧,产生大量的白烟,但不能证明空气中O 的含量,故选项错
2
误。
B、红磷在空气中燃烧,放出大量的热,使装置内空气受热膨胀,完全反应后,消耗装置内的氧
气,装置内压强减小,故瓶中液面先下降,后上升;但不能证明空气中O 的含量,故选项错误。
2
C、瓶中液面最终上升至1处,说明氧气约占空气总体积的 ,能证明空气中O 的含量,故选
2
项正确。
D、水槽中液面下降,不能证明空气中O 的含量,故选项错误。
2
故选:C。
【点评】本题难度不大,掌握用燃烧法测定空气中氧气含量的实验原理、注意事项等是正确解
答本题的关键。10.依据下列20℃时的实验和数据回答10~11题
已知20℃时,NaCl和NaNO 的溶解度分别为36g和88g。
3
序号 ① ② ③ ④ ⑤
固体种类 NaCl NaCl NaNO NaNO NaNO
3 3 3
固体的质量/g 30 60 30 60 90
水的质量/g 100 100 100 100 100
①~⑤所得溶液属于饱和溶液的是( )
A.①③ B.②④ C.②⑤ D.④⑤
【分析】根据题意,20℃时,NaCl和NaNO 的溶解度分别为36g和88g,则该温度下100g水中
3
最多溶解NaCl和NaNO 的质量分别是36g和88g,进行分析判断。
3
【解答】解:20℃时,NaCl和NaNO 的溶解度分别为36g和88g,则该温度下100g水中最多溶
3
解NaCl和NaNO 的质量分别是36g和88g,加入溶质的质量大于或等于36g和88g,能形成饱
3
和溶液,则①~⑤所得溶液属于饱和溶液的是②⑤。
故选:C。
【点评】本题难度不大,掌握饱和溶液的特征、溶解度的含义是正确解答本题的关键。
11.依据下列20℃时的实验和数据回答10~11题
已知20℃时,NaCl和NaNO 的溶解度分别为36g和88g。
3
序号 ① ② ③ ④ ⑤
固体种类 NaCl NaCl NaNO NaNO NaNO
3 3 3
固体的质量/g 30 60 30 60 90
水的质量/g 100 100 100 100 100
下列关于①~⑤所得溶液的说法不正确的是( )
A.溶质质量:①<②
B.溶液质量:②<④
C.溶质质量分数:①=③
D.⑤中溶质与溶剂的质量比为9:10
【分析】根据物质的溶解度判断固体是否能完全溶解在水中,然后根据所溶解的溶质的质量以及溶质的质量分数来分析解答。
【解答】解:已知20℃时,NaCl和NaNO 的溶解度分别为36g和88g,所以①③④能完全溶解,
3
且为不饱和溶液;而②中只能溶解36g氯化钠形成饱和溶液,⑤中只能溶解88g硝酸钠形成
饱和溶液。
A.溶液①中溶质的质量为30g,②中溶质的质量为36g,故正确;
B.溶液②的质量为:36g+100g=136g;溶液④的质量为:60g+100g=160g,故正确;
C.溶液①和③均是在100g水中溶解了30g溶质所得溶液中溶质的质量分数相等,故正确;
D.溶液⑤是在100g水中溶解了88g硝酸钠,所以⑤中溶质与溶剂的质量比为88:100=22:
25,故错误。
故选:D。
【点评】解题时要根据溶解度做出判断,哪种溶液中的溶质能完全溶解,哪一个有剩余,然后
再根据选项要求解答。
12.(1分)氨催化氧化是制硝酸的主要反应之一。该反应前后分子种类变化的微观示意图如
图。下列说法不正确的是( )
A.甲中氮、氢原子个数比为1:3
B.乙的相对分子质量为32
C.两种生成物均为化合物
D.生成的丙与丁的分子个数比为1:2
【分析】首先要对模型图进行观察,分析物质的微观构成、物质的类别,再找出物质之间的微
粒数目关系,写出反应的方程式,然后再对题中各问加以分析解答。
【解答】解:依据图示的分子结构可知该反应的化学方程式为:4NH+5O 4NO+6HO;
3 2 2
A、通过观察题中的图,甲是氨气,中氮、氢原子个数比为1:3,故说法正确;
B、图示物质的构成可知,乙是氧气,氧气的相对分子质量为16×2=32,故说法正确;
C、图示物质的构成可知,两种生成物均为化合物,故说法正确;
D、依据图示的分子结构可知该反应的化学方程式为:4NH+5O 4NO+6HO,生成的丙与
3 2 2丁的分子个数比为4:6=2:3,故说法错误。
故选:D。
【点评】本题属于微观示意图的考查,关键是能够根据小球代表的原子结构写出反应的方程
式,然后根据相关的问题分析即可。
二、非选择题(每空1分,共33分)
13.(2分)补齐连线。从A或B中任选一个作答,若均作答,按A计分。
A 物质﹣用途 B 物质﹣﹣主要成分
【分析】物质的性质决定物质的用途,根据物质的性质进行分析解答即可。
【解答】解:A干冰升华吸热,可冷藏食品;碳酸钙中含有钙元素,用于补钙剂;熟石灰呈碱性。
可用于改良酸性土壤;
B天然气的主要成分是甲烷;氯化钠俗称食盐;氧化钙俗称生石灰。
答案:
【点评】掌握物质的性质和用途的关系是正确解答本题的关键。
14.(2分)干热岩是地层深处的热岩体。如图为利用其发电的示意图。
(1)将干热岩的热量传递到热交换器的物质是 水或水蒸气 。
(2)从微粒的角度分析,水变为水蒸气时,变化的是 分子之间的间隔 。
【分析】(1)根据图示信息进行分析解答;(2)根据水变为水蒸气时无新物质生成解答。
【解答】解:
(1)由图示可知:将干热岩的热量传递到热交换器的物质是水或水蒸气;
(2)微观角度讲,水变为水蒸气是水分子之间的间隔变大造成的,而水分子的体积不变;
答案:
(1)水或水蒸气;
(2)分子之间的间隔。
【点评】本题难度不大,熟练掌握微粒的性质可以正确解答。
15.(2分)HO 可作增氧剂。常温下,用4% HO 溶液进行实验,研究pH对HO 分解所得溶液中
2 2 2 2 2 2
氧量的影响,测定结果如图。
(1)HO 分解的化学方程式为 2 HO ═ 2 H O + O ↑ 。
2 2 2 2 2 2
(2)分析如图得到的结论是 在常温下,当 p H 在 8﹣1 2 之间时,随着 p H 的增大,溶氧量先增
大后减小,且在 p H 为 10﹣1 1 中间时,溶氧量达到最大值 。
【分析】(1)过氧化氢在常温下分解生成水和氧气,进行分析解答。
(2)根据pH对HO 分解所得溶液中氧量的影响测定结果图,进行分解答。
2 2
【解答】解:(1)过氧化氢在常温下分解生成水和氧气,反应的化学方程式为:
2HO═2HO+O↑。
2 2 2 2
(2)由pH对HO 分解所得溶液中氧量的影响测定结果图,在常温下,当pH在8﹣12之间时,
2 2
随着pH的增大,溶氧量先增大后减小,且在pH为10﹣11中间时,溶氧量达到最大值。
故答案为:
(1)2HO═2HO+O↑;
2 2 2 2
(2)在常温下,当pH在8﹣12之间时,随着pH的增大,溶氧量先增大后减小,且在pH为10﹣
11中间时,溶氧量达到最大值。
【点评】本题难度不大,理解pH对HO 分解所得溶液中氧量的影响测定结果图是正确解答本
2 2
题的关键。16.(5分)阅读下面科普短文。
化石能源是目前应用最广泛的能源,但其储量有限,不可再生。《2050年世界与中国能源展
望》中提出,全球能源结构正在向多元、清洁、低碳转型。
由图可见,太阳能、风能等其他可再生能源在能源结构中所占比例日益增多。太阳能的利用
是热门研究方向之一。例如,通过光催化可将HO、CO 转化为H、CO、CH、CHOH(甲醇)等太阳
2 2 2 4 3
能燃料,示意图如图2。
随着科技的进步,能源将得到更充分的利用。例如,利用照明灯、人体散发的热量灯生活中随
处可见的废热发电。我国研发的“柔性、可裁剪碲化铋(BiTe)/纤维素复合热点薄膜电池”,
2 3
能充分贴合人体体表,实现利用体表散热为蓝牙耳机、手表、智能手环等可穿戴电子设备供
电。
在新能源的开发和利用中,化学起着不可替代的作用。
(原文作者郑秀珍、邰凯平等,有删改)
依据文章内容回答下列问题。
(1)比较2015、2030和2050年能源结构中的化石能源,所占比例降低的是 石油、煤炭 。
(2)HO、CO 转化得到的太阳能燃料中,属于氧化物的是 C O ;该过程属于 化学 (填
2 2
“物理”或“化学”)变化。(3)复合热电薄膜电池中BiTe 由 2 种元素组成。
2 3
(4)下列说法正确的是 AB D (填序号)。
A.能源结构向多元、清洁、低碳转型 B.科技进步会促进能源的利用
C.石油和太阳能属于可再生能源 D.生活中的废热可转化为电能
【分析】(1)根据题中信息进行分析解答;
(2)根据氧化物的定义解答;
(3)根据物质的元素组成解答;
(4)
A.根据能源结构的变化解答;
B.根据科技进步会促进能源的利用解答
C.根据石油不属于可再生能源解答;
D.根据生活中的废热可转化为电能解答。
【解答】解:
(1)比较2015、2030和2050年能源结构中的化石能源,所占比例降低的是石油、煤炭;
(2)通过光催化可将HO、CO 转化为H、CO、CH、CHOH(甲醇)等太阳能燃料,HO、CO 转化得到
2 2 2 4 3 2 2
的太阳能燃料中,属于氧化物的是
CO;该过程中有新物质生成,属于化学变化;
(3)复合热电薄膜电池中BiTe 由2种元素组成。
2 3
(4)
A.能源结构向多元、清洁、低碳转型,故正确;
B.科技进步会促进能源的利用,故正确;
C.石油不属于可再生能源,故错误;
D.生活中的废热可转化为电能,故正确;
答案:
(1)石油、煤炭;
(2)CO;化学;
(3)2;
(4)ABD
【点评】此题考查知识点较多,可依据已有的知识进行解答。能读懂题意,从原题情景中提炼
出有用的信息是解决该题的关键。
17.(2分)炼铁的主要原料是赤铁矿(主要成分是FeO)、焦炭、空气等,转化过程如图:
2 3(1)②中,反应为CO+C 2CO,其中化合价发生改变的元素是 碳元素 。
2
(2)③中,CO与FeO 反应的化学方程式为 F eO + 3C O 2F e + 3C O 。
2 3 2 3 2
【分析】(1)根据单质中元素的化合价为0、在化合物中正负化合价代数和为零,进行分析解
答。
(2)③中,CO与FeO 反应生成铁和二氧化碳,进行分析解答。
2 3
【解答】解:(1)反应为CO+C 2CO,二氧化碳、碳、一氧化碳中碳元素的化合价分别是
2
+4价、0、+2价,故化合价发生改变的元素是碳元素。
(2)③中,CO与FeO 反应生成铁和二氧化碳,反应的化学方程式为FeO+3CO
2 3 2 3
2Fe+3CO。
2
故答案为:
(1)碳元素;
(2)FeO+3CO 2Fe+3CO。
2 3 2
【点评】本题难度不大,掌握炼铁的原理、化合价的原则、化学方程式的书写方法是正确解答
本题的关键。
18.(3分)为保护绿水青山,可将工业残留的钡渣(主要成分为碳酸钡(BaCO))进行无害化
3
处理,制取化工原料硫酸钡(BaSO)。主要流程如下:
4已知:BaSO 难溶于水,氯化钡(BaCl)可溶于水。
4 2
(1)粉碎钡渣的目的是 增大反应物的接触面积,加快反应速率,使其充分反应 。
(2)反应釜1中的气体X为 二氧化碳 。
(3)反应釜2中发生复分解反应的化学方程式为 BaC l + HSO=BaSO ↓ + 2HC l 。
2 2 4 4
【分析】(1)根据影响反应速率的因素进行分析;
(2)根据碳酸钡和盐酸反应生成氯化钡、水和二氧化碳进行分析;
(3)根据氯化钡和硫酸反应生成硫酸钡沉淀和盐酸进行分析。
【解答】解:(1)粉碎钡渣的目的是:增大反应物的接触面积,加快反应速率,使其充分反应;
(2)碳酸钡和盐酸反应生成氯化钡、水和二氧化碳,所以反应釜1中的气体X为:二氧化碳;
(3)反应釜2中发生的复分解反应是氯化钡和硫酸反应生成硫酸钡沉淀和盐酸,化学方程式
为:BaCl+HSO=BaSO↓+2HCl。
2 2 4 4
故答案为:(1)增大反应物的接触面积,加快反应速率,使其充分反应;
(2)二氧化碳;
(3)BaCl+HSO=BaSO↓+2HCl。
2 2 4 4
【点评】合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会
设计实验、进行实验、分析实验,为学好化学知识奠定基础。
19.(2分)用如图装置进行实验(夹持仪器略去)。加热一段时间后,蜡烛熔化、掉落,之后火
柴燃烧。
(1)能说明铜具有导热性的现象是 蜡烛熔化或火柴燃烧 。
(2)能体现物质化学性质的现象是 A C (填序号)。
A.酒精燃烧 B.蜡烛熔化 C.火柴燃烧
【分析】(1)铜具有导热性,可使火柴燃烧,蜡烛熔化;
(2)化学性质是物质通过化学变化表现出来的。
【解答】解:(1)铜具有导热性,可使火柴燃烧,蜡烛熔化;故填:蜡烛熔化或火柴燃烧;
(2)化学性质是物质通过化学变化表现出来的,酒精、火柴燃烧说明酒精火柴具有可燃性;故
填:AC。【点评】本题难度不大,可依据已有的知识解答。
20.(2分)用如图装置进行实验(夹持仪器略去)。
(1)高锰酸钾分解的化学方程式为 2KMn O KMnO + Mn O + O ↑ 。
4 2 4 2 2
(2)木炭遇O 燃烧时,现象为 剧烈燃烧,发出白光,放热 。
2
【分析】(1)根据高锰酸钾加热分解为锰酸钾、二氧化锰、氧气解答;
(2)根据木炭在氧气中燃烧的现象进行解答。
【解答】解:
(1)高锰酸钾加热分解为锰酸钾、二氧化锰、氧气,反应的方程式为:2KMnO
4
KMnO+MnO+O↑;
2 4 2 2
(2)木炭遇O 燃烧时,剧烈燃烧,发出白光,放热。
2
答案:
(1)2KMnO KMnO+MnO+O↑;
4 2 4 2 2
(2)剧烈燃烧,发出白光,放热。
【点评】本题考查了常见气体的反应原理,完成此题,可以依据已有的知识进行。要求同学们
在完成此类题目时,要熟知反应物的状态和反应的条件,以便做出正确的判断。
21.(2分)实验室用如图装置制取CO。
2
(1)反应的化学方程式为 CaC O + 2HCl=CaC l + H O + C O ↑ 。
3 2 2 2
(2)用向上排空气法收集CO 的原因是 二氧化碳的密度比空气的大且不与空气中其他气体
2
反应 。【分析】(1)根据实验室中制取二氧化碳的反应原理,进行分析解答。
(2)根据二氧化碳的物理性质,进行分析解答。
【解答】解:(1)实验室中制取二氧化碳常用大理石或石灰石和稀盐酸反应来制取,同时生成
氯化钙、水,反应的化学方程式是:CaCO+2HCl=CaCl+HO+CO↑。
3 2 2 2
(2)用向上排空气法收集CO,是因为二氧化碳的密度比空气的大且不与空气中其他气体反
2
应。
故答案为:
(1)CaCO+2HCl=CaCl+HO+CO↑;
3 2 2 2
(2)二氧化碳的密度比空气的大且不与空气中其他气体反应。
【点评】本题难度不大,是中考的重要考点之一,熟练掌握实验室中制取二氧化碳气体的反应
原理、发生装置和收集装置的选择依据等是正确解答本题的关键。
22.(3分)用如图所示实验验证可燃物燃烧的条件。
已 知 : 白 磷 的 着 火 点 为 40℃ .
(1)设计B、D的目的是 探究可燃物燃烧温度需要达到着火点 。
(2)能验证可燃物需要O 的现象是 C 中白磷不燃烧, D 中白磷燃烧 。
2
(3)A~D中,可不做的实验是 A (填序号)。
【分析】(1)根据B、D的其它条件相同,水的温度不同,进行分析解答。(2)验证可燃物需要O,应控制其它条件相同,进行分析解答。
2
(3)根据验证燃烧的条件,可设计对比试验,进行分析解答。
【解答】解:(1)B、D的其它条件相同,水的温度不同,B中白磷不燃烧,D中白磷燃烧,设计B、
D的目的是探究可燃物燃烧温度需要达到着火点。
(2)验证可燃物需要O,应控制其它条件相同,C中白磷不燃烧,D中白磷燃烧,说明可燃物燃
2
烧需要O。
2
(3)验证燃烧的条件,可设计对比试验,A~D中,BC、CD对比可得出燃烧的条件,可不做的实
验是A。
故答案为:
(1)探究可燃物燃烧温度需要达到着火点;
(2)C中白磷不燃烧,D中白磷燃烧;
(3)A。
【点评】本题难度不大,考查燃烧的条件,掌握燃烧的条件并能灵活运用是正确解答本题的关
键。
23.(3分)进行如下微型实验,研究物质的性质。
(1)能产生气泡的是 B D (填序号)。
(2)能证明C中发生反应的现象是 溶液由红色变为无色 。
(3)有一只烧杯中的物质不与稀盐酸反应,原因是 铜的金属活动性排在氢的后面,不与盐
酸反应生成氢气 。
【分析】根据酸的通性进行解答。
【解答】解:(1)活泼金属和碳酸氢盐会与酸反应分别产生氢气和二氧化碳;故填BD;
(2)氢氧化钙与盐酸反应生成氯化钙和水,溶液由红色变为无色;故填:溶液由红色变为无色;
(3)铜的金属活动性性排在氢的后面,不与盐酸反应生成氢气;故填:铜的金属活动性排在氢
的后面,不与盐酸反应生成氢气。【点评】掌握酸的通性是解题关键。
24.(5分)为探究碳还原氧化铜的最佳实验条件,用木炭粉和氧化铜的干燥混合物1~2.5g
进行系列实验。
【查阅资料】①氧化铜(CuO)为黑色固体。
②碳还原氧化铜得到的铜中可能含有少量的氧化亚铜;氧化亚铜为红色固体,能与稀硫酸反
应:CuO+HSO═CuSO+HO+Cu。
2 2 4 4 2
【进行实验】
实验1:取质量比1:11的木炭粉和氧化铜混合物1.3g,进行实验。
序号 1﹣1 1﹣2
装置
反应后物质的颜色、状 黑色粉末中混有少量红色固体 红色固体有金属光泽,混有极少
态 量黑色物质
实验2:取一定量的混合物,用1﹣2装置进行实验。
序号 木炭粉与氧化铜的质 反应后物质的颜色、状态
量比
2﹣1 1:9 红色固体有金属光泽 混有少
量黑色
物质
2﹣2 1:10 混有很
少量黑
色物质
2﹣3 1:11 混有极
少量黑
色物质
2﹣4 1:12 无黑色
物质
2﹣5 1:13 混有较
多黑色
物质
【解释与结论】(1)配平化学方程式:C+ 2 CuO 2 Cu+ 1 CO↑。
2
(2)实验1﹣2中,证明产生了CO 的现象是 澄清石灰水变浑浊 。
2
(3)实验1的目的是 探究氧化铜与木炭的受热面积对其反应的影响 。
(4)实验2的结论是 木炭与氧化铜质量比为 1 : 1 2 时恰好完全反应,因此木炭与氧化铜反
应的最佳质量比为 1 : 1 2 。
【反思与评价】
(5)实验2没有进行质量比为1:14的实验,理由是 木炭与氧化铜的质量比为 1 : 1 3 时,氧
化铜已过量 。
(6)为检验2﹣4的红色固体中是否含CuO,所需试剂是 稀硫酸 。
2
【分析】根据题干提供的信息结合物质间反应的实验现象进行分析解答,二氧化碳能使澄清
的石灰水变浑浊,氧化亚铜能与硫酸反应使溶液变蓝,据此解答。
【解答】解:(1)碳与氧化铜反应生成铜和二氧化碳的化学方程式为 C+2CuO
2Cu+CO↑,故填2;2;1。
2
(2)二氧化碳能使澄清的石灰水变浑浊,故证明生成了CO 的现象是澄清石灰水变浑浊,故填:
2
澄清石灰水变浑浊。
(3)实验1中实验1﹣1混合物的受热面积大于实验1﹣2中混合物的受热面积,故是探究氧
化铜与木炭的受热面积对其反应的影响,故填:探究氧化铜与木炭的受热面积对其反应的影
响。
(4)实验2提供的数据以及实验现象可以看出,木炭与氧化铜质量比为1:12时恰好完全反
应,因此木炭与氧化铜反应的最佳质量比为1:12,故填:木炭与氧化铜质量比为1:12时恰好
完全反应,因此木炭与氧化铜反应的最佳质量比为1:12。
(5)实验2没有进行质量比为1:14的实验,是因为当木炭与氧化铜的质量比为1:13时,氧
化铜已过量,故填:木炭与氧化铜的质量比为1:13时,氧化铜已过量。
(6)为检验2﹣4的红色固体中是否含CuO,根据题干提供的信息,氧化亚铜能与硫酸反应生
2
成蓝色的额硫酸铜反应,故所需试剂是稀硫酸,故填:稀硫酸。
【点评】本题考查的是化学反应实验条件的实验探究,完成此题,可以依据题干提供的信息结
合已有的物质的性质进行。