文档内容
2019 年上海市中考化学试卷解析
一、选择题(共20分)下列各题均只有一个正确选项,请将正确选项的代号用 2B铅笔填
涂在答题纸的相应位置上,更改答案时,用橡皮擦去,重新填涂.
1.属于稀有气体的是( )
A.氮气 B.氦气 C.氢气 D.氧气
2.能使紫色石蕊试液变蓝的是( )
A.水 B.石灰水 C.稀硫酸 D.稀盐酸
3.灼烧氯化钠,火焰呈( )
A.黄色 B.红色 C.绿色 D.紫色
4.能提供氮元素的化肥是( )
A.KCl B.K CO C.NH Cl D.Ca(H PO )
2 3 4 2 4 2
5.Fe O 中Fe的化合价是( )
2 3
A.﹣3 B.﹣2 C.+2 D.+3
6.放入一定量水中,充分搅拌后形成乳浊液的是( )
A.蔗糖 B.麻油 C.食盐 D.白醋
7.图示实验操作规范的是( )
A. 取用液体 B. 滴加液体
C. 量筒读数 D. 加热液体
8.净水过程中可加入的吸附剂是( )
A.活性炭 B.生石灰 C.熟石灰 D.烧碱
9.在氧气中燃烧,产生明亮蓝紫色火焰的是( )
A.硫 B.红磷 C.铁丝 D.氢气
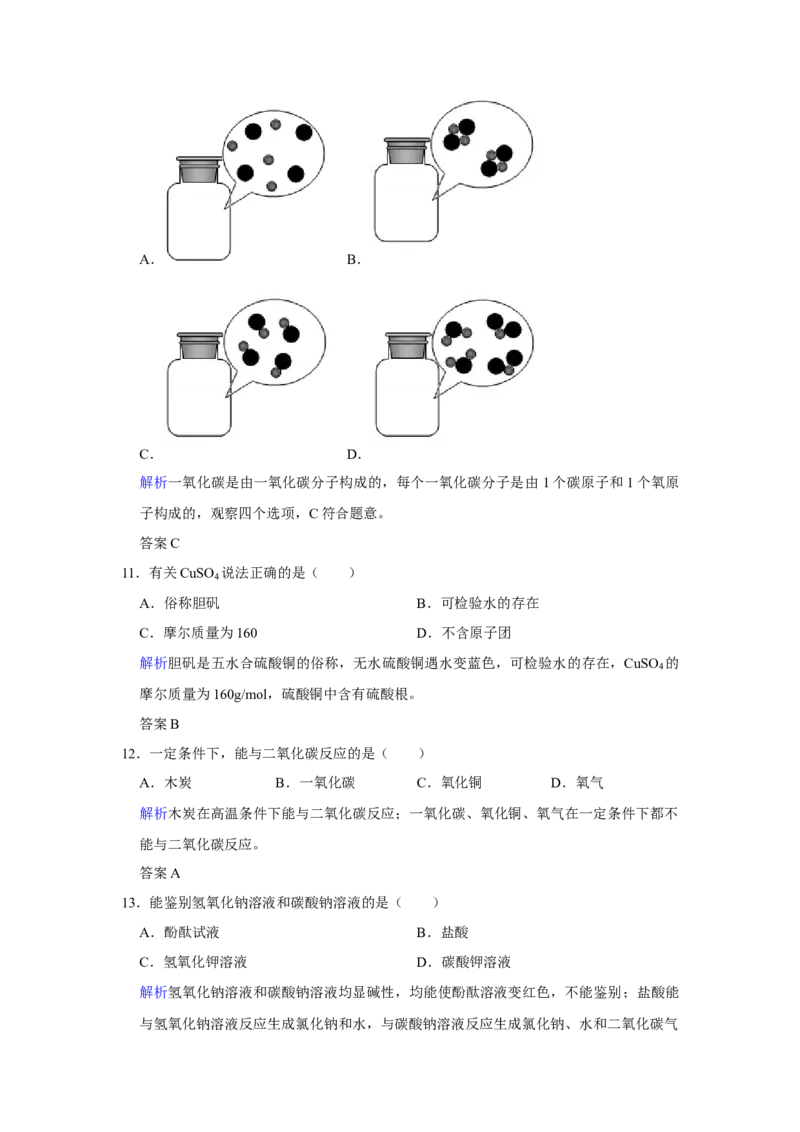
10.瓶中CO气体分子的微观示意图为(“ ”表示C原子,“ ”表示O原子)(
)A. B.
C. D.
11.有关CuSO 说法正确的是( )
4
A.俗称胆矾 B.可检验水的存在
C.摩尔质量为160 D.不含原子团
12.一定条件下,能与二氧化碳反应的是( )
A.木炭 B.一氧化碳 C.氧化铜 D.氧气
13.能鉴别氢氧化钠溶液和碳酸钠溶液的是( )
A.酚酞试液 B.盐酸
C.氢氧化钾溶液 D.碳酸钾溶液
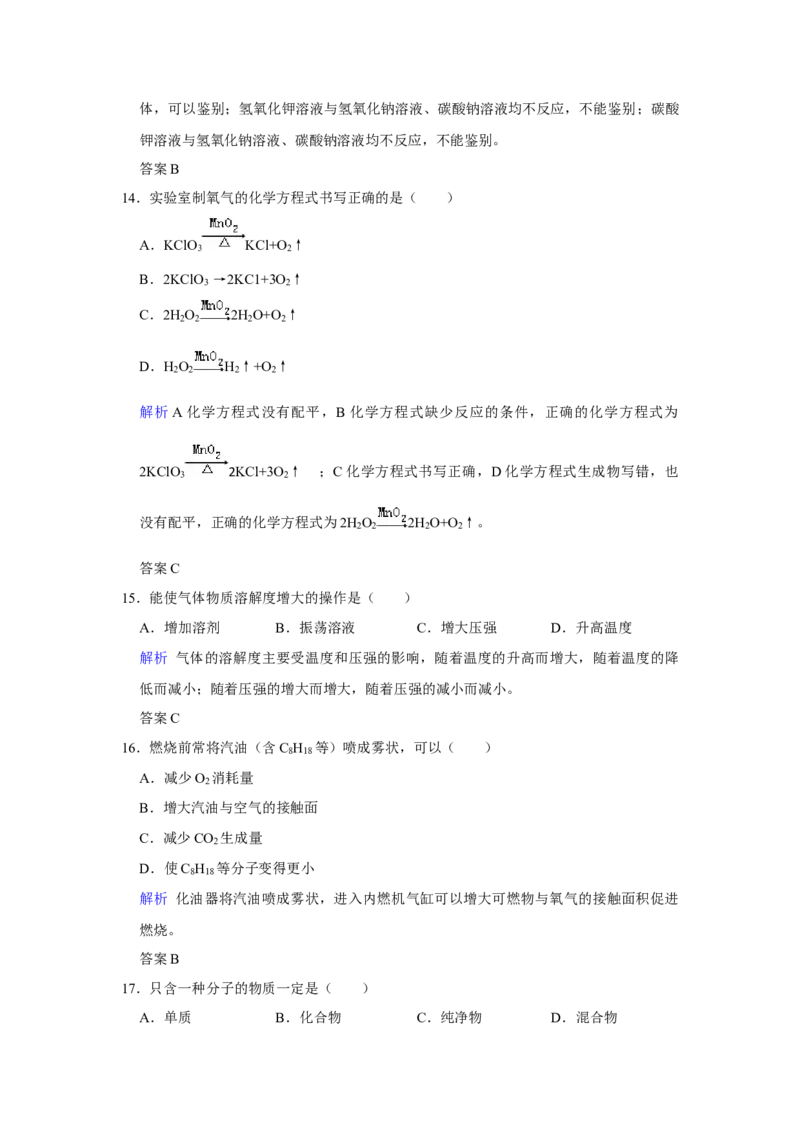
14.实验室制氧气的化学方程式书写正确的是( )
A.KClO KCl+O ↑
3 2
B.2KClO
3
→2KC1+3O
2
↑
C.2H O 2H O+O ↑
2 2 2 2
D.H O H ↑+O ↑
2 2 2 2
15.能使气体物质溶解度增大的操作是( )
A.增加溶剂 B.振荡溶液 C.增大压强 D.升高温度
16.燃烧前常将汽油(含C H 等)喷成雾状,可以( )
8 18
A.减少O 消耗量
2B.增大汽油与空气的接触面
C.减少CO 生成量
2
D.使C H 等分子变得更小
8 18
17.只含一种分子的物质一定是( )
A.单质 B.化合物 C.纯净物 D.混合物
18.25℃时,pH=1的盐酸与pH=13的氢氧化钠溶液混合,立即测定混合液的温度T,然
后测定混合液的pH(25℃时)。有关判断合理的是( )
A.T=25℃pH=7 B.T=25℃1≤pH≤13
C.T>25℃pH=14 D.T>25℃1<pH<13
19.含氧元素质量相同的SO 和SO ,具有相同的( )
2 3
A.硫元素质量 B.质量 C.氧原子个数 D.分子个数
20.一定量甲烷(CH )在氧气中不完全燃烧,生成一氧化碳、二氧化碳和水的物质的量
4
之比可能为( )
A.1:1:2 B.2:1:4 C.2:3:6 D.3:1:8
七、填空题(共21分)请根据要求在答题纸相应的位置作答.
21.(8分)新中国成立70年来,我国化学工业得到长足发展。
积极开发燃料酒精等石油替代品。酒精(C H O)由 种元素组成,属于 (选
2 6
①填“有机物”或“无机物”)。酒精燃烧属于 (选填“物理”或“化学”)变化。
人造金刚石世界闻名。金刚石硬度大,可用于 。金刚石、 (填物质名称)和
②碳60互为同素异形体,其中碳元素以 (选填“游离”或“化合”)态存在。
光伏产品遍及全球。生产中涉及反应:SiO +2C Si+2X↑.X的化学式是 。
2
③
1mol SiO 中约含 个Si原子。
2
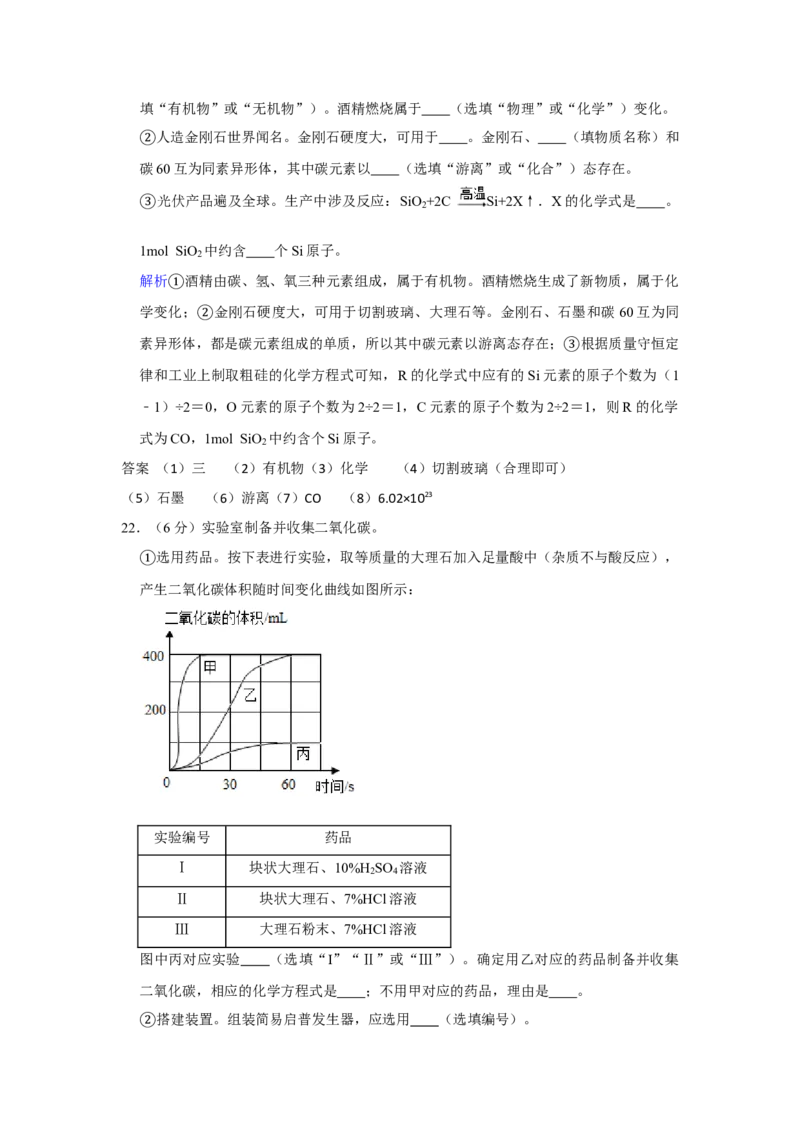
22.(6分)实验室制备并收集二氧化碳。
选用药品。按下表进行实验,取等质量的大理石加入足量酸中(杂质不与酸反应),
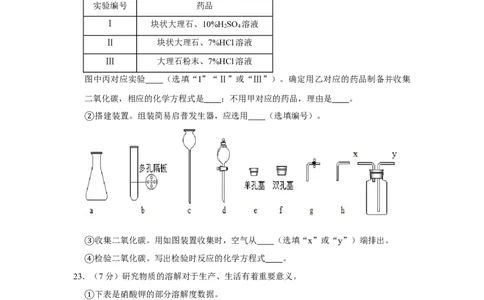
①产生二氧化碳体积随时间变化曲线如图所示:实验编号 药品
Ⅰ 块状大理石、10%H SO 溶液
2 4
Ⅱ 块状大理石、7%HCl溶液
Ⅲ 大理石粉末、7%HCl溶液
图中丙对应实验 (选填“I”“Ⅱ”或“Ⅲ”)。确定用乙对应的药品制备并收集
二氧化碳,相应的化学方程式是 ;不用甲对应的药品,理由是 。
搭建装置。组装简易启普发生器,应选用 (选填编号)。
②
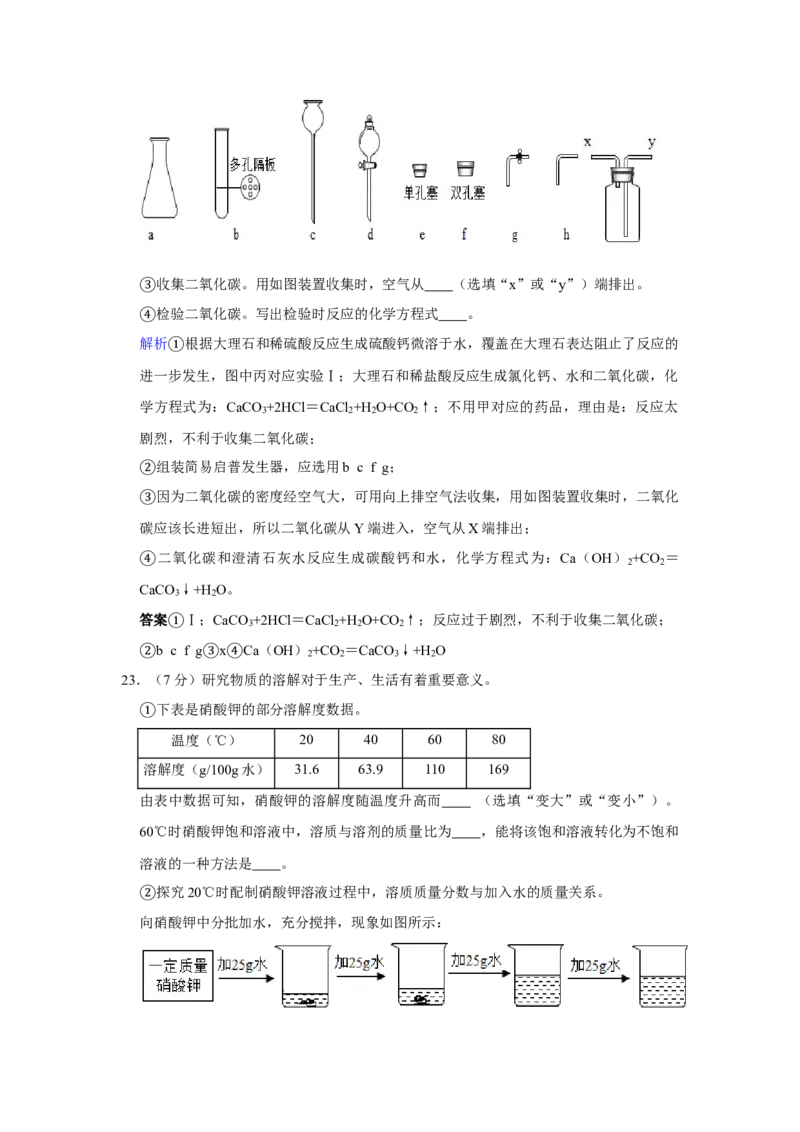
收集二氧化碳。用如图装置收集时,空气从 (选填“x”或“y”)端排出。
③检验二氧化碳。写出检验时反应的化学方程式 。
23.④(7分)研究物质的溶解对于生产、生活有着重要意义。
下表是硝酸钾的部分溶解度数据。
① 温度(℃) 20 40 60 80
溶解度(g/100g水) 31.6 63.9 110 169
由表中数据可知,硝酸钾的溶解度随温度升高而 (选填“变大”或“变小”)。
60℃时硝酸钾饱和溶液中,溶质与溶剂的质量比为 ,能将该饱和溶液转化为不饱和
溶液的一种方法是 。
探究20℃时配制硝酸钾溶液过程中,溶质质量分数与加入水的质量关系。
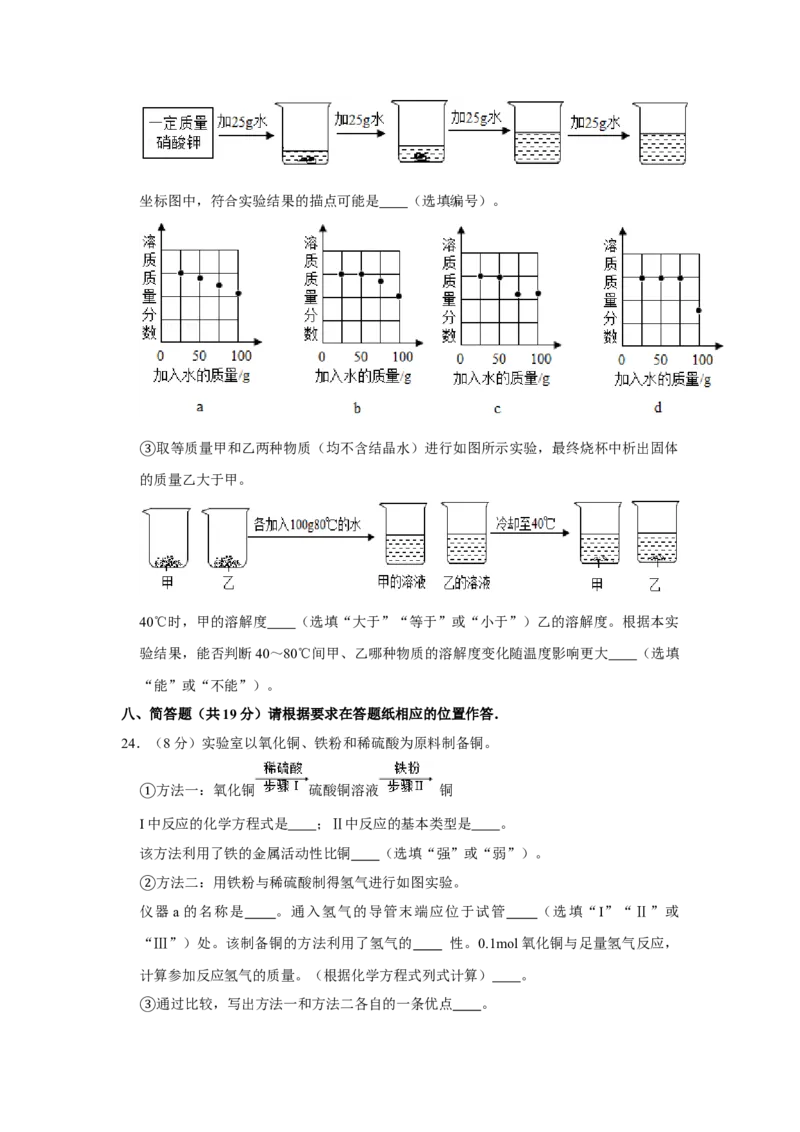
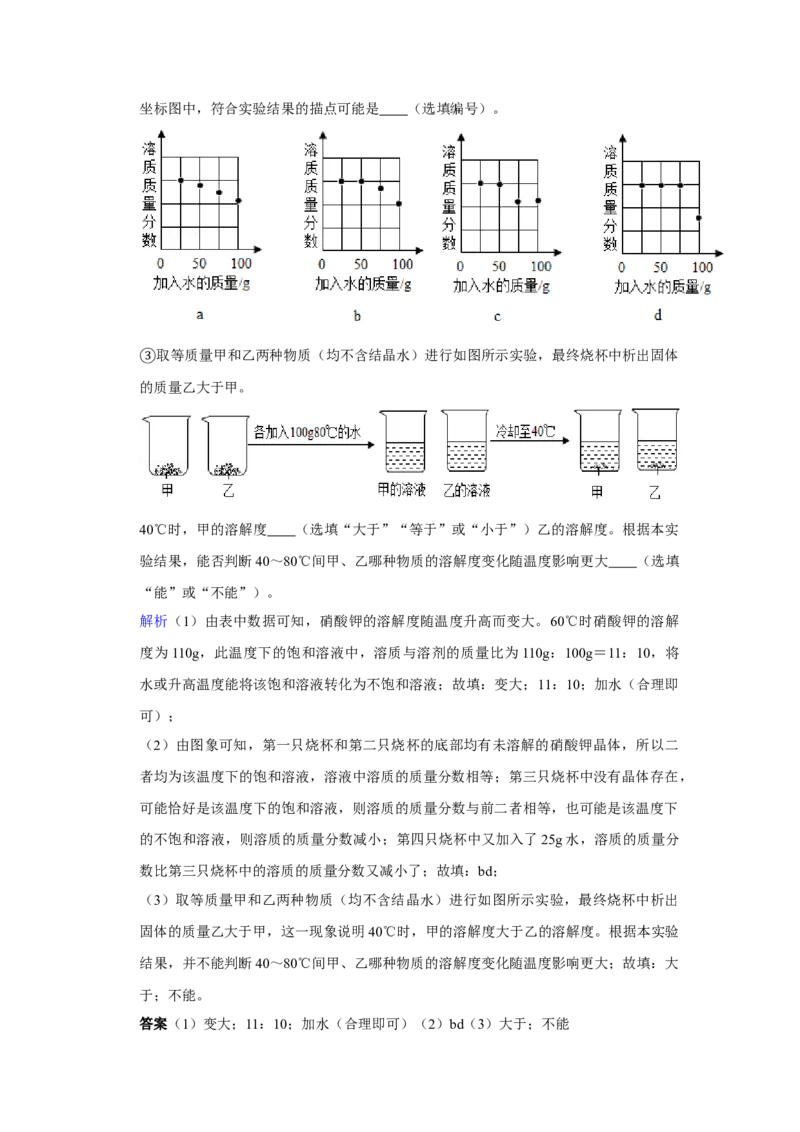
②向硝酸钾中分批加水,充分搅拌,现象如图所示:坐标图中,符合实验结果的描点可能是 (选填编号)。
取等质量甲和乙两种物质(均不含结晶水)进行如图所示实验,最终烧杯中析出固体
③的质量乙大于甲。
40℃时,甲的溶解度 (选填“大于”“等于”或“小于”)乙的溶解度。根据本实
验结果,能否判断40~80℃间甲、乙哪种物质的溶解度变化随温度影响更大 (选填
“能”或“不能”)。
八、简答题(共19分)请根据要求在答题纸相应的位置作答.
24.(8分)实验室以氧化铜、铁粉和稀硫酸为原料制备铜。
方法一:氧化铜 硫酸铜溶液 铜
①I中反应的化学方程式是 ;Ⅱ中反应的基本类型是 。
该方法利用了铁的金属活动性比铜 (选填“强”或“弱”)。
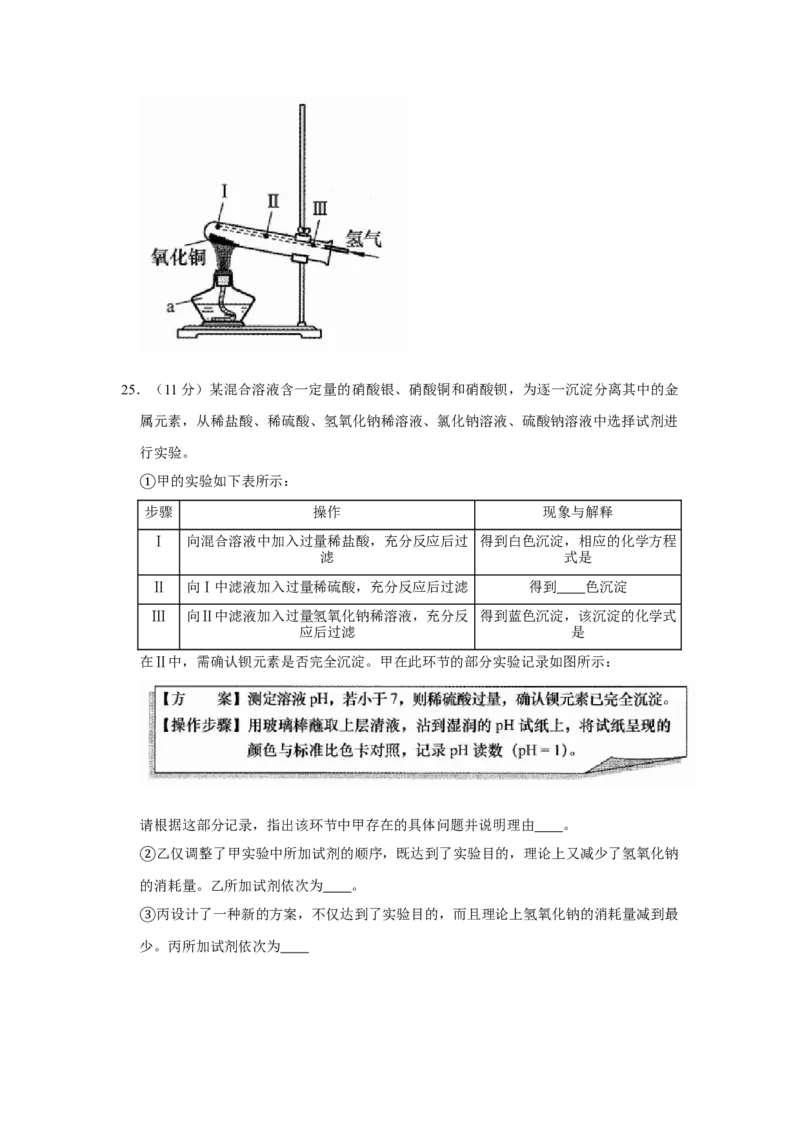
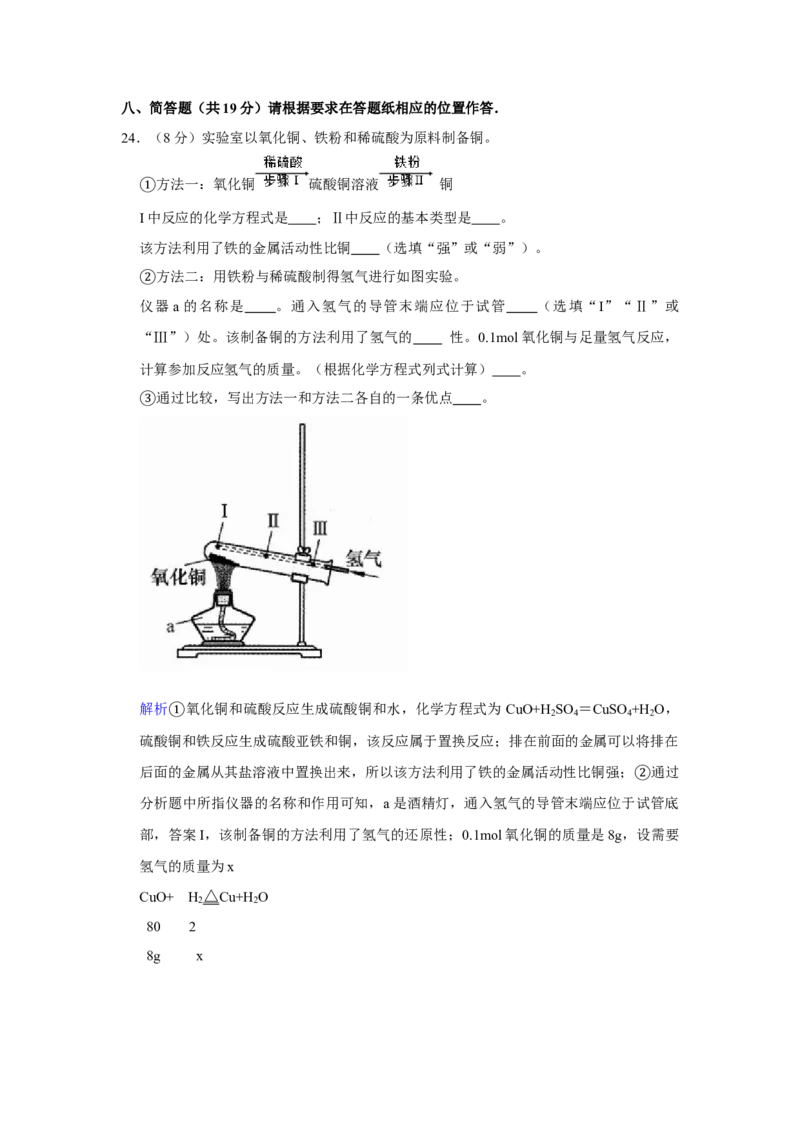
方法二:用铁粉与稀硫酸制得氢气进行如图实验。
②仪器 a 的名称是 。通入氢气的导管末端应位于试管 (选填“I”“Ⅱ”或
“Ⅲ”)处。该制备铜的方法利用了氢气的 性。0.1mol氧化铜与足量氢气反应,
计算参加反应氢气的质量。(根据化学方程式列式计算) 。
通过比较,写出方法一和方法二各自的一条优点 。
③25.(11分)某混合溶液含一定量的硝酸银、硝酸铜和硝酸钡,为逐一沉淀分离其中的金
属元素,从稀盐酸、稀硫酸、氢氧化钠稀溶液、氯化钠溶液、硫酸钠溶液中选择试剂进
行实验。
甲的实验如下表所示:
①步骤 操作 现象与解释
Ⅰ 向混合溶液中加入过量稀盐酸,充分反应后过 得到白色沉淀,相应的化学方程
滤 式是
Ⅱ 向Ⅰ中滤液加入过量稀硫酸,充分反应后过滤 得到 色沉淀
Ⅲ 向Ⅱ中滤液加入过量氢氧化钠稀溶液,充分反 得到蓝色沉淀,该沉淀的化学式
应后过滤 是
在Ⅱ中,需确认钡元素是否完全沉淀。甲在此环节的部分实验记录如图所示:
请根据这部分记录,指出该环节中甲存在的具体问题并说明理由 。
乙仅调整了甲实验中所加试剂的顺序,既达到了实验目的,理论上又减少了氢氧化钠
②的消耗量。乙所加试剂依次为 。
丙设计了一种新的方案,不仅达到了实验目的,而且理论上氢氧化钠的消耗量减到最
③少。丙所加试剂依次为2019 年上海市中考化学试卷解析
一、选择题(共20分)下列各题均只有一个正确选项,请将正确选项的代号用 2B铅笔填
涂在答题纸的相应位置上,更改答案时,用橡皮擦去,重新填涂.
1.属于稀有气体的是( )
A.氮气 B.氦气 C.氢气 D.氧气
解析稀有气体是氦、氖、氩、氪、氙等气体的总称,因此氦气属于稀有气体。
答案B
2.能使紫色石蕊试液变蓝的是( )
A.水 B.石灰水 C.稀硫酸 D.稀盐酸
解析碱性溶液能使紫色石蕊试液变蓝,水呈中性,石灰水显碱性,稀硫酸、稀盐酸显酸
性。
答案B
3.灼烧氯化钠,火焰呈( )
A.黄色 B.红色 C.绿色 D.紫色
解析多种金属或它们的化合物在灼烧时,会使火焰呈现特殊的颜色,化学上叫焰色反应;
氯化钠中含有钠元素,属于钠盐,灼烧氯化钠时火焰的颜色呈黄色。
答案A
4.能提供氮元素的化肥是( )
A.KCl B.K CO C.NH Cl D.Ca(H PO )
2 3 4 2 4 2
解析KCl、K CO 含有钾元素,属于钾肥;NH Cl含有氮元素,属于氮肥;Ca(H PO )
2 3 4 2 4 2
含有磷元素,属于磷肥。
答案C
5.Fe O 中Fe的化合价是( )
2 3
A.﹣3 B.﹣2 C.+2 D.+3
解析 氧元素显﹣2价,设铁元素的化合价是x,根据在化合物中正负化合价代数和为零,
2x+(﹣2)×3=0,x=+3价。
答案D
6.放入一定量水中,充分搅拌后形成乳浊液的是( )
A.蔗糖 B.麻油 C.食盐 D.白醋
解析A、蔗糖、食盐、白醋溶于水,能够形成均一、稳定的混合物,属于溶液;花生油不溶于水,把植物油放到水里是液滴分散到液体中形成的混合物,属于乳浊液。
答案B
7.图示实验操作规范的是( )
A. 取用液体 B. 滴加液体
C. 量筒读数 D. 加热液体
解析取用液体药品时,瓶塞要倒放,标签要对准手心,瓶口紧挨,A错误;使用胶头滴
管滴加少量液体时,注意胶头滴管不能伸入到试管内或接触试管内壁。应垂直悬空在试
管口上方滴加液体,防止污染胶头滴管,B错误;量筒读数时视线要与量筒内液体的凹
液面的最低处保持水平,C正确;给试管中的液体加热时,用酒精灯的外焰加热试管里
的液体,且液体体积不能超过试管容积的1/3,大拇指不能放在短柄上,D错误。
答案C
8.净水过程中可加入的吸附剂是( )
A.活性炭 B.生石灰 C.熟石灰 D.烧碱
解析活性炭具有吸附性,可吸附水中的色素和异味,净水过程中可加入活性炭;生石灰、
熟石灰、烧碱溶于水,使溶液具有强烈的腐蚀性,不能加入。
答案A
9.在氧气中燃烧,产生明亮蓝紫色火焰的是( )
A.硫 B.红磷 C.铁丝 D.氢气
解析硫在氧气中燃烧,发出明亮的蓝紫色火焰,产生一种具有刺激性气味的气体;红磷
在氧气中燃烧,产生大量的白烟;铁丝在氧气中剧烈燃烧,火星四射;氢气在氧气中燃
烧,产生淡蓝色火焰。
答案A
10.瓶中CO气体分子的微观示意图为(“ ”表示C原子,“ ”表示O原子)(
)A. B.
C. D.
解析一氧化碳是由一氧化碳分子构成的,每个一氧化碳分子是由1个碳原子和1个氧原
子构成的,观察四个选项,C符合题意。
答案C
11.有关CuSO 说法正确的是( )
4
A.俗称胆矾 B.可检验水的存在
C.摩尔质量为160 D.不含原子团
解析胆矾是五水合硫酸铜的俗称,无水硫酸铜遇水变蓝色,可检验水的存在,CuSO 的
4
摩尔质量为160g/mol,硫酸铜中含有硫酸根。
答案B
12.一定条件下,能与二氧化碳反应的是( )
A.木炭 B.一氧化碳 C.氧化铜 D.氧气
解析木炭在高温条件下能与二氧化碳反应;一氧化碳、氧化铜、氧气在一定条件下都不
能与二氧化碳反应。
答案A
13.能鉴别氢氧化钠溶液和碳酸钠溶液的是( )
A.酚酞试液 B.盐酸
C.氢氧化钾溶液 D.碳酸钾溶液
解析氢氧化钠溶液和碳酸钠溶液均显碱性,均能使酚酞溶液变红色,不能鉴别;盐酸能
与氢氧化钠溶液反应生成氯化钠和水,与碳酸钠溶液反应生成氯化钠、水和二氧化碳气体,可以鉴别;氢氧化钾溶液与氢氧化钠溶液、碳酸钠溶液均不反应,不能鉴别;碳酸
钾溶液与氢氧化钠溶液、碳酸钠溶液均不反应,不能鉴别。
答案B
14.实验室制氧气的化学方程式书写正确的是( )
A.KClO KCl+O ↑
3 2
B.2KClO
3
→2KC1+3O
2
↑
C.2H O 2H O+O ↑
2 2 2 2
D.H O H ↑+O ↑
2 2 2 2
解析A化学方程式没有配平,B化学方程式缺少反应的条件,正确的化学方程式为
2KClO 2KCl+3O ↑ ;C化学方程式书写正确,D化学方程式生成物写错,也
3 2
没有配平,正确的化学方程式为2H O 2H O+O ↑。
2 2 2 2
答案C
15.能使气体物质溶解度增大的操作是( )
A.增加溶剂 B.振荡溶液 C.增大压强 D.升高温度
解析 气体的溶解度主要受温度和压强的影响,随着温度的升高而增大,随着温度的降
低而减小;随着压强的增大而增大,随着压强的减小而减小。
答案C
16.燃烧前常将汽油(含C H 等)喷成雾状,可以( )
8 18
A.减少O 消耗量
2
B.增大汽油与空气的接触面
C.减少CO 生成量
2
D.使C H 等分子变得更小
8 18
解析 化油器将汽油喷成雾状,进入内燃机气缸可以增大可燃物与氧气的接触面积促进
燃烧。
答案B
17.只含一种分子的物质一定是( )
A.单质 B.化合物 C.纯净物 D.混合物解析单质可能由分子构成,也可能由原子构成,如金属是由原子直接构成的,A错误。
化合物可能由分子直接构成,也可能有离子构成,如绝大多数的盐是离子构成的,B错
误。同一种分子构成的物质是一种物质,则一定是纯净物,C正确。混合物中至少有两
种分子,则只有一种分子的不是混合物,D错误。
答案C
18.25℃时,pH=1的盐酸与pH=13的氢氧化钠溶液混合,立即测定混合液的温度T,然
后测定混合液的pH(25℃时)。有关判断合理的是( )
A.T=25℃pH=7 B.T=25℃1≤pH≤13
C.T>25℃pH=14 D.T>25℃1<pH<13
解析25℃时,pH=1的盐酸与pH=13的氢氧化钠溶液混合,中和反应属于放热反应,
则立即测定混合液的温度T,T>25℃;混合液的pH应大于1,小于13。
答案D
19.含氧元素质量相同的SO 和SO ,具有相同的( )
2 3
A.硫元素质量 B.质量 C.氧原子个数 D.分子个数
解析二氧化硫与三氧化硫分子的构成不同,含氧元素质量相同的SO 和SO ,硫元素的
2 3
质量一定不同。二氧化硫与三氧化硫分子的构成不同,含氧元素质量相同的 SO 和
2
SO ,SO 和SO 的质量一定不同。SO 和SO 中氧元素含量相同,则氧原子个数一定相
3 2 3 2 3
等。
SO 和SO 中氧元素含量相同,由于一个二氧化硫与一个三氧化硫分子中氧原子的个数
2 3
不同,则分子个数一定不相等。
答案C
20.一定量甲烷(CH )在氧气中不完全燃烧,生成一氧化碳、二氧化碳和水的物质的量
4
之比可能为( )
A.1:1:2 B.2:1:4 C.2:3:6 D.3:1:8
解析一定量甲烷在氧气中不完全燃烧,生成一氧化碳、二氧化碳和水,反应前后碳原子
和氢原子的个数不变,设一氧化碳、二氧化碳、水的物质的量之比分别为x、y、z,
(x+y):2z=1:4,则(x+y):z=1:2。
答案D
七、填空题(共21分)请根据要求在答题纸相应的位置作答.
21.(8分)新中国成立70年来,我国化学工业得到长足发展。
积极开发燃料酒精等石油替代品。酒精(C H O)由 种元素组成,属于 (选
2 6
①填“有机物”或“无机物”)。酒精燃烧属于 (选填“物理”或“化学”)变化。
人造金刚石世界闻名。金刚石硬度大,可用于 。金刚石、 (填物质名称)和
②碳60互为同素异形体,其中碳元素以 (选填“游离”或“化合”)态存在。
光伏产品遍及全球。生产中涉及反应:SiO +2C Si+2X↑.X的化学式是 。
2
③
1mol SiO 中约含 个Si原子。
2
解析 酒精由碳、氢、氧三种元素组成,属于有机物。酒精燃烧生成了新物质,属于化
学变①化; 金刚石硬度大,可用于切割玻璃、大理石等。金刚石、石墨和碳 60互为同
素异形体,②都是碳元素组成的单质,所以其中碳元素以游离态存在; 根据质量守恒定
律和工业上制取粗硅的化学方程式可知,R的化学式中应有的Si元素③的原子个数为(1
﹣1)÷2=0,O元素的原子个数为2÷2=1,C元素的原子个数为2÷2=1,则R的化学
式为CO,1mol SiO 中约含个Si原子。
2
答案 (1)三 (2)有机物(3)化学 (4)切割玻璃(合理即可)
(5)石墨 (6)游离(7)CO (8)6.02×1023
22.(6分)实验室制备并收集二氧化碳。
选用药品。按下表进行实验,取等质量的大理石加入足量酸中(杂质不与酸反应),
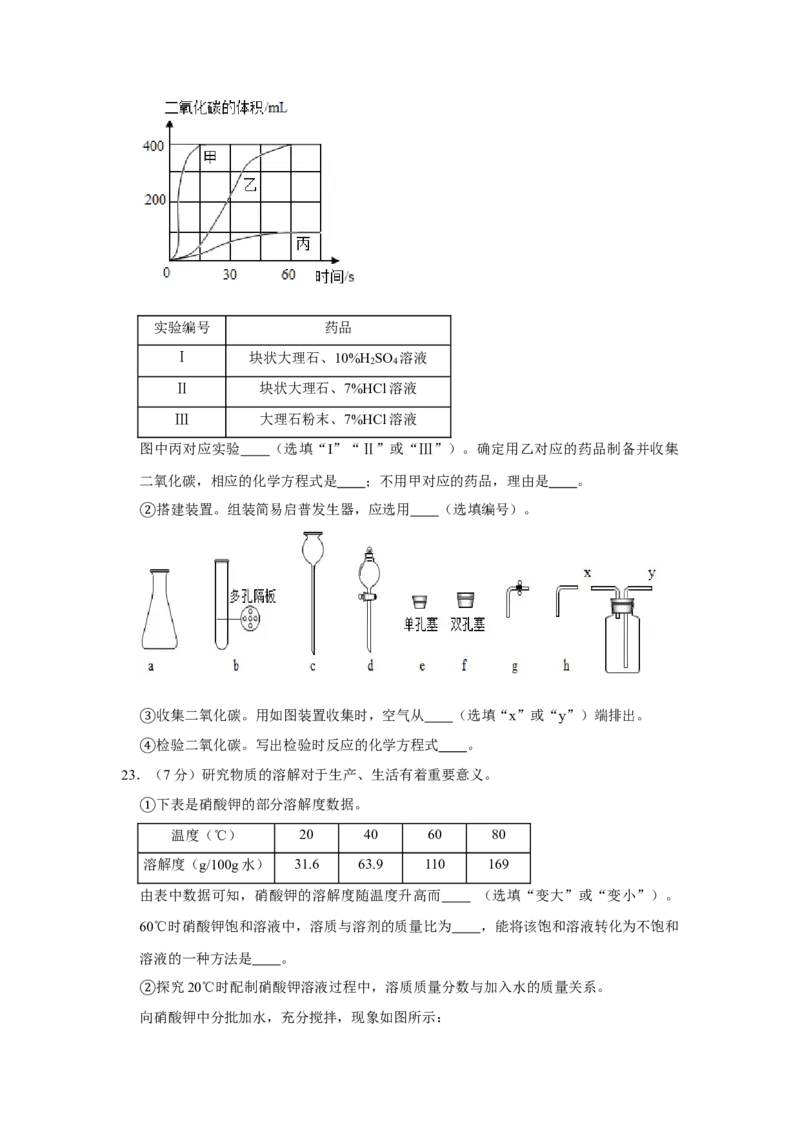
①产生二氧化碳体积随时间变化曲线如图所示:
实验编号 药品
Ⅰ 块状大理石、10%H SO 溶液
2 4
Ⅱ 块状大理石、7%HCl溶液
Ⅲ 大理石粉末、7%HCl溶液
图中丙对应实验 (选填“I”“Ⅱ”或“Ⅲ”)。确定用乙对应的药品制备并收集
二氧化碳,相应的化学方程式是 ;不用甲对应的药品,理由是 。
搭建装置。组装简易启普发生器,应选用 (选填编号)。
②收集二氧化碳。用如图装置收集时,空气从 (选填“x”或“y”)端排出。
③检验二氧化碳。写出检验时反应的化学方程式 。
④解析 根据大理石和稀硫酸反应生成硫酸钙微溶于水,覆盖在大理石表达阻止了反应的
进一①步发生,图中丙对应实验Ⅰ;大理石和稀盐酸反应生成氯化钙、水和二氧化碳,化
学方程式为:CaCO +2HCl=CaCl +H O+CO ↑;不用甲对应的药品,理由是:反应太
3 2 2 2
剧烈,不利于收集二氧化碳;
组装简易启普发生器,应选用b c f g;
②因为二氧化碳的密度经空气大,可用向上排空气法收集,用如图装置收集时,二氧化
③碳应该长进短出,所以二氧化碳从Y端进入,空气从X端排出;
二氧化碳和澄清石灰水反应生成碳酸钙和水,化学方程式为:Ca(OH) +CO =
2 2
④CaCO ↓+H O。
3 2
答案 Ⅰ;CaCO +2HCl=CaCl +H O+CO ↑;反应过于剧烈,不利于收集二氧化碳;
3 2 2 2
b ①c f g x Ca(OH)
2
+CO
2
=CaCO
3
↓+H
2
O
23.②(7分)研③究④物质的溶解对于生产、生活有着重要意义。
下表是硝酸钾的部分溶解度数据。
① 温度(℃) 20 40 60 80
溶解度(g/100g水) 31.6 63.9 110 169
由表中数据可知,硝酸钾的溶解度随温度升高而 (选填“变大”或“变小”)。
60℃时硝酸钾饱和溶液中,溶质与溶剂的质量比为 ,能将该饱和溶液转化为不饱和
溶液的一种方法是 。
探究20℃时配制硝酸钾溶液过程中,溶质质量分数与加入水的质量关系。
②向硝酸钾中分批加水,充分搅拌,现象如图所示:坐标图中,符合实验结果的描点可能是 (选填编号)。
取等质量甲和乙两种物质(均不含结晶水)进行如图所示实验,最终烧杯中析出固体
③的质量乙大于甲。
40℃时,甲的溶解度 (选填“大于”“等于”或“小于”)乙的溶解度。根据本实
验结果,能否判断40~80℃间甲、乙哪种物质的溶解度变化随温度影响更大 (选填
“能”或“不能”)。
解析(1)由表中数据可知,硝酸钾的溶解度随温度升高而变大。60℃时硝酸钾的溶解
度为110g,此温度下的饱和溶液中,溶质与溶剂的质量比为110g:100g=11:10,将
水或升高温度能将该饱和溶液转化为不饱和溶液;故填:变大;11:10;加水(合理即
可);
(2)由图象可知,第一只烧杯和第二只烧杯的底部均有未溶解的硝酸钾晶体,所以二
者均为该温度下的饱和溶液,溶液中溶质的质量分数相等;第三只烧杯中没有晶体存在,
可能恰好是该温度下的饱和溶液,则溶质的质量分数与前二者相等,也可能是该温度下
的不饱和溶液,则溶质的质量分数减小;第四只烧杯中又加入了25g水,溶质的质量分
数比第三只烧杯中的溶质的质量分数又减小了;故填:bd;
(3)取等质量甲和乙两种物质(均不含结晶水)进行如图所示实验,最终烧杯中析出
固体的质量乙大于甲,这一现象说明40℃时,甲的溶解度大于乙的溶解度。根据本实验
结果,并不能判断40~80℃间甲、乙哪种物质的溶解度变化随温度影响更大;故填:大
于;不能。
答案(1)变大;11:10;加水(合理即可)(2)bd(3)大于;不能八、简答题(共19分)请根据要求在答题纸相应的位置作答.
24.(8分)实验室以氧化铜、铁粉和稀硫酸为原料制备铜。
方法一:氧化铜 硫酸铜溶液 铜
①I中反应的化学方程式是 ;Ⅱ中反应的基本类型是 。
该方法利用了铁的金属活动性比铜 (选填“强”或“弱”)。
方法二:用铁粉与稀硫酸制得氢气进行如图实验。
②仪器 a 的名称是 。通入氢气的导管末端应位于试管 (选填“I”“Ⅱ”或
“Ⅲ”)处。该制备铜的方法利用了氢气的 性。0.1mol氧化铜与足量氢气反应,
计算参加反应氢气的质量。(根据化学方程式列式计算) 。
通过比较,写出方法一和方法二各自的一条优点 。
③
解析 氧化铜和硫酸反应生成硫酸铜和水,化学方程式为 CuO+H SO =CuSO +H O,
2 4 4 2
硫酸铜①和铁反应生成硫酸亚铁和铜,该反应属于置换反应;排在前面的金属可以将排在
后面的金属从其盐溶液中置换出来,所以该方法利用了铁的金属活动性比铜强; 通过
分析题中所指仪器的名称和作用可知,a是酒精灯,通入氢气的导管末端应位于②试管底
部,答案I,该制备铜的方法利用了氢气的还原性;0.1mol氧化铜的质量是8g,设需要
氢气的质量为x
CuO+ H △Cu+H O
2 2
80 2
8g x= x=0.2g
,
通过比较,方法一和方法二各自的优点是:方法一节约能源,方法二得到的铜纯净。
③答案 CuO+H
2
SO
4
=CuSO
4
+H
2
O,置换反应;强
酒①精灯,I,还原;0.2g
②方法一:节约能源,方法二:得到的铜纯净。
25.③(11分)某混合溶液含一定量的硝酸银、硝酸铜和硝酸钡,为逐一沉淀分离其中的金
属元素,从稀盐酸、稀硫酸、氢氧化钠稀溶液、氯化钠溶液、硫酸钠溶液中选择试剂进
行实验。
甲的实验如下表所示:
①步骤 操作 现象与解释
Ⅰ 向混合溶液中加入过量稀盐酸,充分反应后过 得到白色沉淀,相应的化学方程
滤 式是
Ⅱ 向Ⅰ中滤液加入过量稀硫酸,充分反应后过滤 得到 色沉淀
Ⅲ 向Ⅱ中滤液加入过量氢氧化钠稀溶液,充分反 得到蓝色沉淀,该沉淀的化学式
应后过滤 是
在Ⅱ中,需确认钡元素是否完全沉淀。甲在此环节的部分实验记录如图所示:
请根据这部分记录,指出该环节中甲存在的具体问题并说明理由 。
乙仅调整了甲实验中所加试剂的顺序,既达到了实验目的,理论上又减少了氢氧化钠
②的消耗量。乙所加试剂依次为 。
丙设计了一种新的方案,不仅达到了实验目的,而且理论上氢氧化钠的消耗量减到最
③少。丙所加试剂依次为 。
解析 向混合溶液中加入过量稀盐酸,稀盐酸和硝酸银反应生成白色沉淀氯化银和硝酸,
反应①的化学方程式为HCl+AgNO ═AgCl↓+HNO ;向Ⅰ中滤液加入过量稀硫酸,稀硫
3 3
酸和硝酸钡反应生成白色沉淀硫酸钡和硝酸;向Ⅱ中滤液加入过量氢氧化钠稀溶液,氢
氧化钠和硝酸铜反应生成蓝色沉淀氢氧化铜和硝酸钠;该环节中甲存在的具体问题:沾
到湿润的pH试纸上;理由:湿润的pH试纸会稀释溶液,会导致测定的酸碱性溶液不正确。
乙所加试剂依次为:过量稀盐酸、过量氢氧化钠溶液、过量稀硫酸,因为这样可以避
②免过量的稀硫酸消耗氢氧化钠。
丙所加试剂依次为:过量氯化钠溶液、过量氢氧化钠溶液、过量稀硫酸,因为这样可
③以避免过量的稀盐酸、稀硫酸消耗氢氧化钠。
答案 HCl+AgNO ═AgCl↓+HNO
3 3
白色①
Cu(OH)
2
问题:沾到湿润的pH试纸上
理由:湿润的pH试纸会稀释溶液。
过量稀盐酸、过量氢氧化钠溶液、过量稀硫酸
②过量氯化钠溶液、过量氢氧化钠溶液、过量稀硫酸
③