文档内容
2019年广东省深圳市中考化学试卷
一、选择题(共10小题,每小题1.5分,共15分.在每小题给出的4个选项中,只有一项符合
题意.)
1.(1.5分)化学与人类的生产、生活密切相关。下列描述正确的是( )
A.引起贫血的主要原因是缺锌
B.不合理施用化肥会造成水体污染
C. 是电池回收标志
D.用水喷淋燃着的酒精以降低着火点
2.(1.5分)下列化学用语表述正确的是( )
A.硫酸钾的化学式:K SO B.1 个氯分子:Cl
2 4
C.2 个硝酸根:2NO D.铜离子:
2
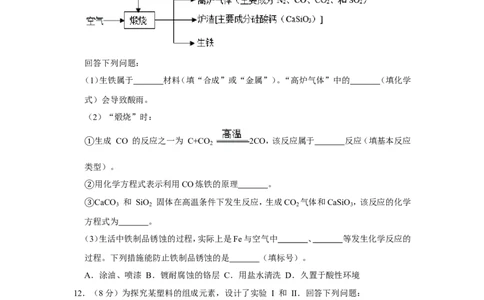
3.(1.5分)下列实验不涉及化学变化的是( )
测定空气中O 的含量 验证浓 比较合金与纯金 判断溶液的酸碱性
2
H SO 的腐 属的硬度
2 4
蚀性
A.A B.B C.C D.D
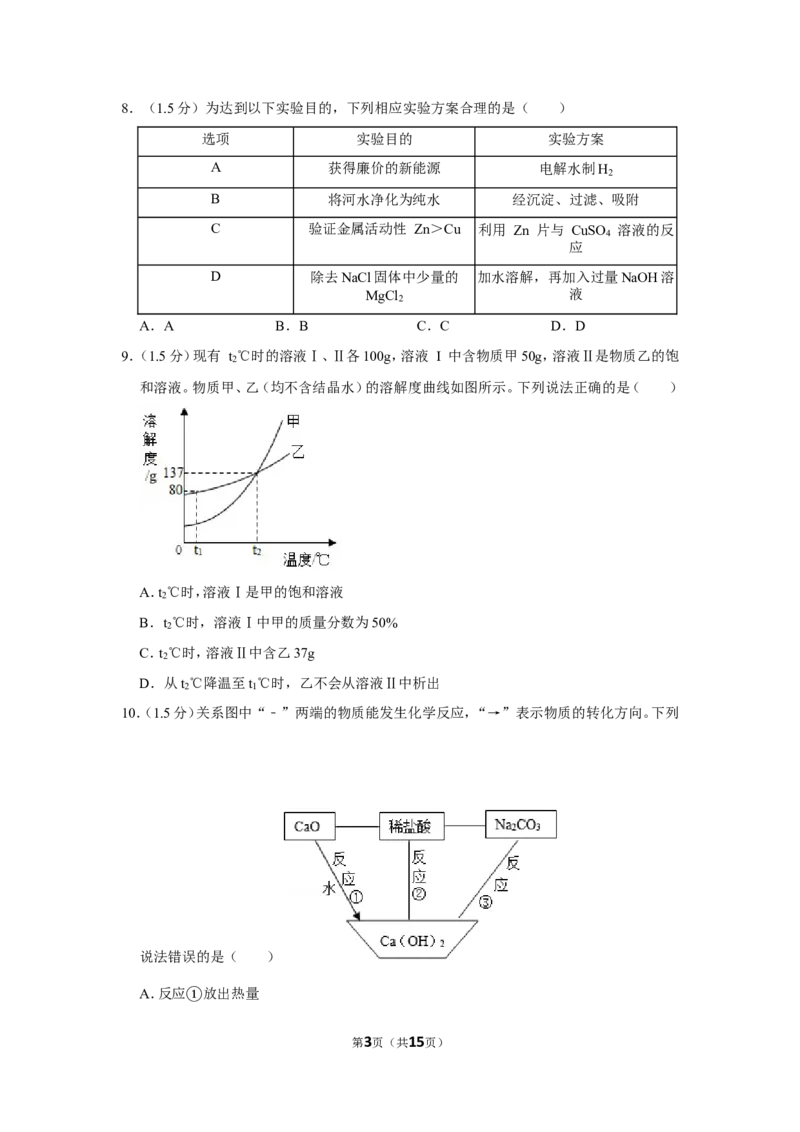
4.(1.5分)钪(Kc)是一种“工业的维生素”。图为钪在元素周期表中的相关信息及其原子
的结构示意图。下列说法正确的是( )
第1页(共15页)A.钪属于非金属元素
B.钪的相对原子质量是 21
C.原子结构示意图中x=10
D.钪原子核外有四个电子层
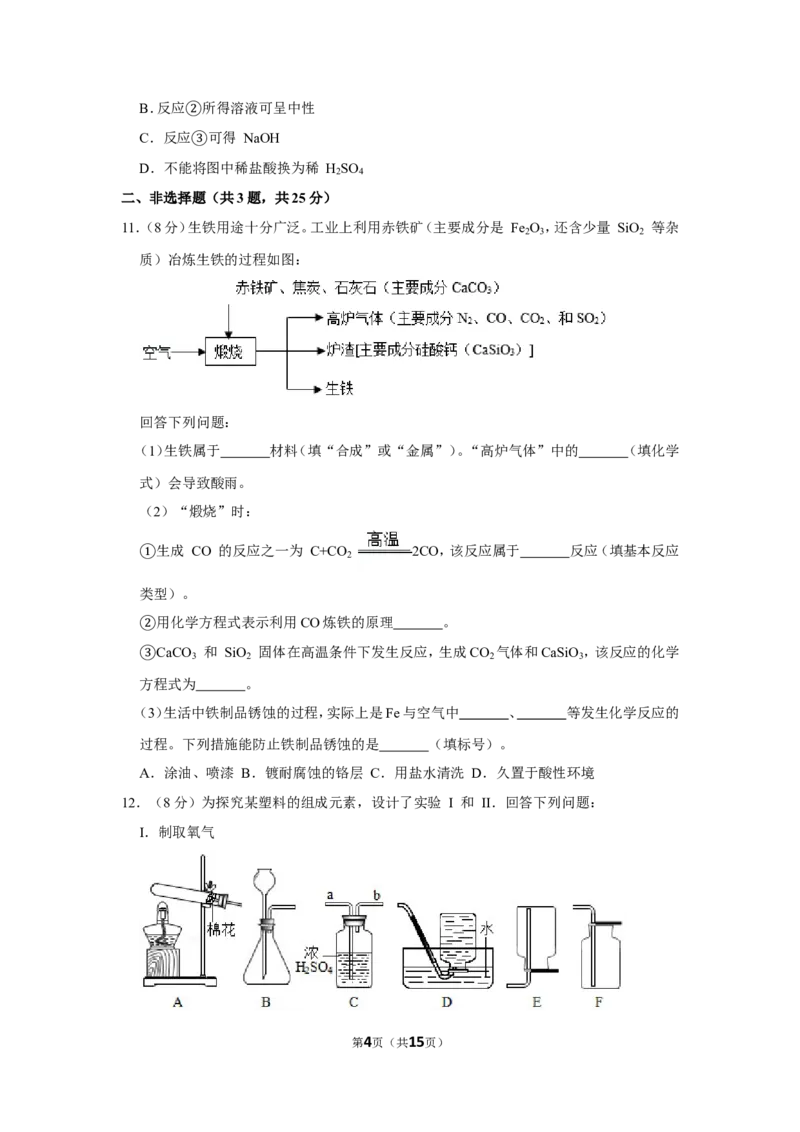
5.(1.5分)科学家研制出一种新型催化剂,可用于去除装修残留的甲醛(化学式为 CH O),
2
该反应过程的微观示意图如图。下列说法正确的是( )
A.物质甲为甲醛,其分子由碳原子和水分子构成
B.物质乙中氧元素的化合价为﹣2 价
C.该反应前后原子种类和数目均发生改变
D.该反应消耗物质甲和生成物质丁的质量比为 5:3
6.(1.5分)CuO 粉末与H 在加热条件下会发生反应。下列说法错误的是( )
2
A.反应所需H 可由Cu与稀H SO 反应制得
2 2 4
B.反应过程可观察到固体粉末由黑色变成红色
C.发生的反应为 CuO+H Cu+H O
2 2
D.该反应说明H 具有还原性
2
7.(1.5分)异烟肼(化学式:C H N O;相对分子质量:137)是治疗肺结核药物的有效成分。下
6 7 3
列说法正确的是( )
A.异烟肼属于氧化物
B.异烟肼分子中 H、O 原子个数比为 7:1
C.异烟肼中 C、H 两种元素的质量比为 36:7
D.异烟肼中 N 元素质量分数的计算式为 ×100%
第2页(共15页)8.(1.5分)为达到以下实验目的,下列相应实验方案合理的是( )
选项 实验目的 实验方案
A 获得廉价的新能源 电解水制H
2
B 将河水净化为纯水 经沉淀、过滤、吸附
C 验证金属活动性 Zn>Cu 利用 Zn 片与 CuSO 溶液的反
4
应
D 除去NaCl固体中少量的 加水溶解,再加入过量NaOH溶
MgCl 液
2
A.A B.B C.C D.D
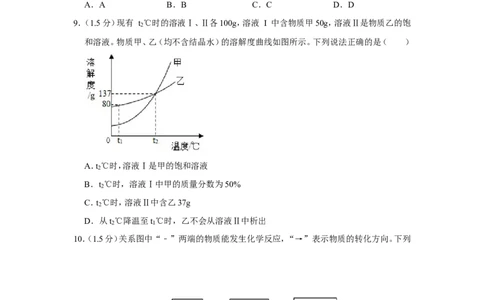
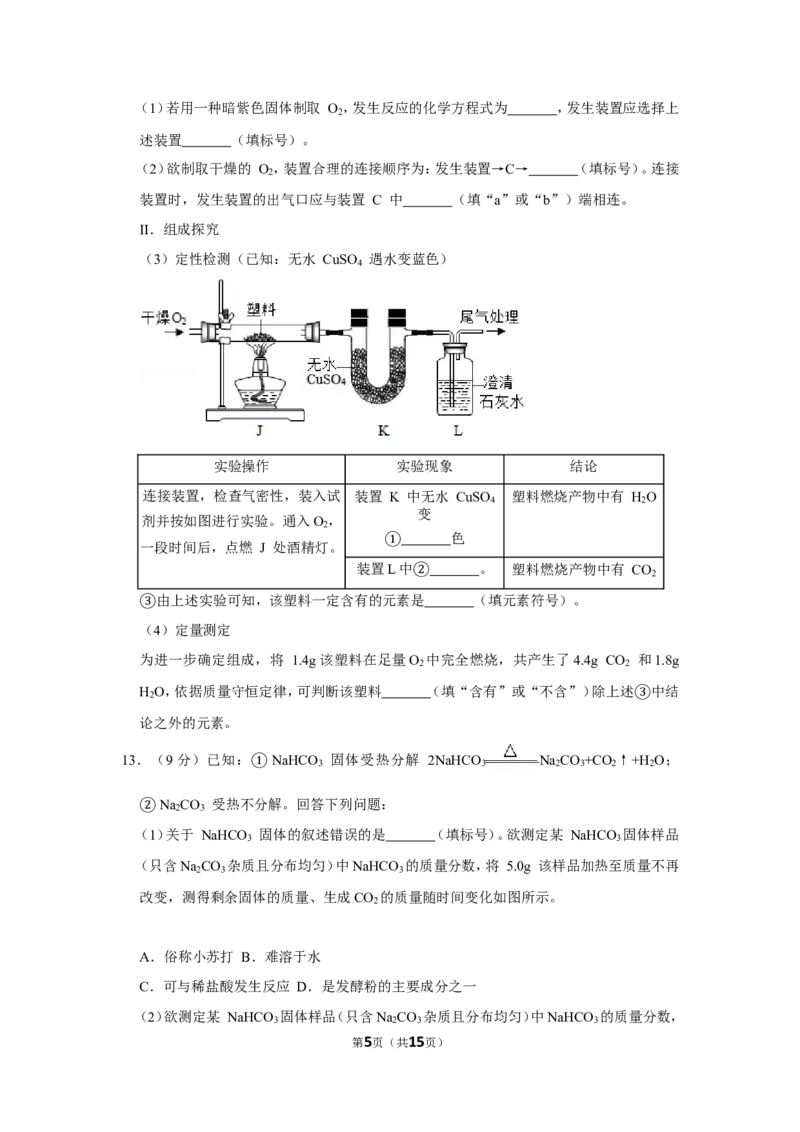
9.(1.5分)现有 t ℃时的溶液Ⅰ、Ⅱ各100g,溶液 I 中含物质甲50g,溶液Ⅱ是物质乙的饱
2
和溶液。物质甲、乙(均不含结晶水)的溶解度曲线如图所示。下列说法正确的是( )
A.t ℃时,溶液Ⅰ是甲的饱和溶液
2
B.t ℃时,溶液Ⅰ中甲的质量分数为50%
2
C.t ℃时,溶液Ⅱ中含乙37g
2
D.从t ℃降温至t ℃时,乙不会从溶液Ⅱ中析出
2 1
10.(1.5分)关系图中“﹣”两端的物质能发生化学反应,“→”表示物质的转化方向。下列
说法错误的是( )
A.反应 放出热量
①
第3页(共15页)B.反应 所得溶液可呈中性
C.反应② 可得 NaOH
D.不能③将图中稀盐酸换为稀 H
2
SO
4
二、非选择题(共3题,共25分)
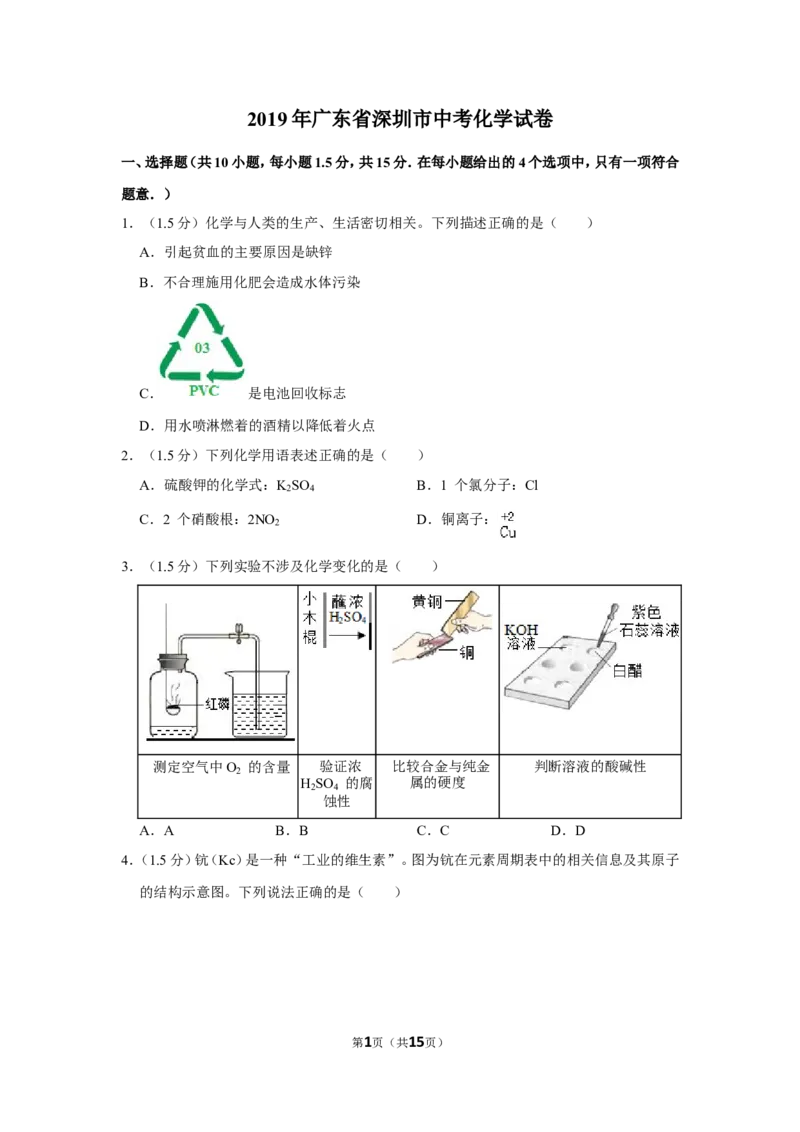
11.(8分)生铁用途十分广泛。工业上利用赤铁矿(主要成分是 Fe O ,还含少量 SiO 等杂
2 3 2
质)冶炼生铁的过程如图:
回答下列问题:
(1)生铁属于 材料(填“合成”或“金属”)。“高炉气体”中的 (填化学
式)会导致酸雨。
(2)“煅烧”时:
生成 CO 的反应之一为 C+CO 2CO,该反应属于 反应(填基本反应
2
①
类型)。
用化学方程式表示利用CO炼铁的原理 。
②CaCO
3
和 SiO
2
固体在高温条件下发生反应,生成CO
2
气体和CaSiO
3
,该反应的化学
③方程式为 。
(3)生活中铁制品锈蚀的过程,实际上是Fe与空气中 、 等发生化学反应的
过程。下列措施能防止铁制品锈蚀的是 (填标号)。
A.涂油、喷漆 B.镀耐腐蚀的铬层 C.用盐水清洗 D.久置于酸性环境
12.(8分)为探究某塑料的组成元素,设计了实验 I 和 II.回答下列问题:
I.制取氧气
第4页(共15页)(1)若用一种暗紫色固体制取 O ,发生反应的化学方程式为 ,发生装置应选择上
2
述装置 (填标号)。
(2)欲制取干燥的 O ,装置合理的连接顺序为:发生装置→C→ (填标号)。连接
2
装置时,发生装置的出气口应与装置 C 中 (填“a”或“b”)端相连。
II.组成探究
(3)定性检测(已知:无水 CuSO 遇水变蓝色)
4
实验操作 实验现象 结论
连接装置,检查气密性,装入试 装置 K 中无水 CuSO 塑料燃烧产物中有 H O
4 2
变
剂并按如图进行实验。通入O ,
2
色
一段时间后,点燃 J 处酒精灯。
装置①L中 。 塑料燃烧产物中有 CO
2
由上述实验可知,该塑料一定含有的元素是② (填元素符号)。
③(4)定量测定
为进一步确定组成,将 1.4g该塑料在足量O 中完全燃烧,共产生了4.4g CO 和1.8g
2 2
H O,依据质量守恒定律,可判断该塑料 (填“含有”或“不含”)除上述 中结
2
论之外的元素。 ③
13.(9分)已知: NaHCO 固体受热分解 2NaHCO Na CO +CO ↑+H O;
3 3 2 3 2 2
①
Na CO 受热不分解。回答下列问题:
2 3
(②1)关于 NaHCO
3
固体的叙述错误的是 (填标号)。欲测定某 NaHCO
3
固体样品
(只含Na CO 杂质且分布均匀)中NaHCO 的质量分数,将 5.0g 该样品加热至质量不再
2 3 3
改变,测得剩余固体的质量、生成CO 的质量随时间变化如图所示。
2
A.俗称小苏打 B.难溶于水
C.可与稀盐酸发生反应 D.是发酵粉的主要成分之一
(2)欲测定某 NaHCO 固体样品(只含Na CO 杂质且分布均匀)中NaHCO 的质量分数,
3 2 3 3
第5页(共15页)将 5.0g 该样品加热至质量不再改变,测得剩余固体的质量、生成CO 的质量随时间变化
2
如图所示。
NaOH溶液的pH 7(填“>”、“=”或“<”),用该溶液将生成的CO 完全
2
①吸收,发生反应的化学方程式为 。
由图中数据可知,上述5.0g NaHCO 样品完全分解产生CO 的质量为 g,产
3 2
②生H O的质量是 g。
2
计算该样品中NaHCO 的质量分数(根据化学方程式写出完整的计算步骤)。
3
③
第6页(共15页)2019 年广东省深圳市中考化学试卷
参考答案与试题解析
一、选择题(共10小题,每小题1.5分,共15分.在每小题给出的4个选项中,只有一项符合
题意.)
1.(1.5分)
【考点】79:水资源的污染与防治;H4:灭火的原理和方法;HH:几种常见的与化学有关的
图标;J1:人体的元素组成与元素对人体健康的重要作用.
【分析】A、根据铁元素的生理功能与缺乏症进行分析;
B、根据不合理施用化肥的危害进行分析;
C、根据标志所表示的含义进行分析;
D、根据灭火的原理进行分析判断。
【解答】解:A、铁是构成血红蛋白的成分,缺铁是引起贫血的主要原因,故错误;
B、农药、化肥的不合理施用,会造成水体污染,故B正确;
C、图中标志为塑料回收标志,故错误;
D、通过降低可燃物的温度至着火点以下可以灭火,可燃物的着火点一般是不变的,不能
降低可燃物的着火点,故错误;
故选:B。
【点评】本题考查的知识点较多,综合性较强,完成此题,可以依据已有的知识进行。
2.(1.5分)
【考点】DF:化学符号及其周围数字的意义.
【分析】A、硫酸钾中钾元素显+1价,硫酸根显﹣2价,进行分析判断。
B、分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其分子符号前加上相
应的数字。
C、根据原子团的表示方法,进行分析判断。
D、离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数
字在前,正负符号在后,带1个电荷时,1要省略。
【解答】解:A、硫酸钾中钾元素显+1价,硫酸根显﹣2价,其化学式为K SO ,故选项化学
2 4
用语书写正确。
B、由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其分子符号前加上
第7页(共15页)相应的数字,则1个氯分子可表示为:Cl ,故选项化学用语书写错误。
2
C、2个硝酸根可表示为2NO ,故选项化学用语书写错误。
3
D、由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,
数字在前,正负符号在后,带1个电荷时,1要省略。铜离子可表示为:Cu2+,故选项化学用
语书写错误。
故选:A。
【点评】本题难度不大,掌握常见化学用语(分子符号、化学式、化合价、离子符号等)的书
写方法、离子符号与化合价表示方法的区别等是正确解答此类题的关键。
3.(1.5分)
【考点】E3:化学变化和物理变化的判别.
【分析】本题考查学生对物理变化和化学变化的确定。判断一个变化是物理变化还是化学
变化,要依据在变化过程中有没有生成其他物质,生成其他物质的是化学变化,没有生成
其他物质的是物理变化。
【解答】解:A、红磷燃烧生成五氧化二磷,属于化学变化,故A错;
B、浓硫酸的腐蚀性,发生的是化学变化,能将物质的氢、氧以水的形式脱出,故B错;
C、比较合金与纯金属的硬度,相互刻画,没有新物质生成,属于物理变化,故C正确;
D、氢氧化钠与石蕊发生反应变色,属于化学变化,故D错。
故选:C。
【点评】搞清楚物理变化和化学变化的本质区别是解答本类习题的关键。判断的标准是看
在变化中有没有生成其他物质。一般地,物理变化有物质的固、液、气三态变化和物质形
状的变化。
4.(1.5分)
【考点】B8:原子结构示意图与离子结构示意图;C5:元素周期表的特点及其应用.
【分析】元素周期表中,方格中左上角是原子序数,右上角是元素符号,中间是元素名称,
下面是相对原子质量;
原子中,核电荷数=核内质子数=核外电子数=原子序数;
除汞外,金属元素的名称都带金字旁,非金属元素的名称不带金字旁;
相对原子质量≈质子数+中子数,单位不是g。
【解答】解:A、钪属于金属元素,该选项说法不正确;
B、钪的相对原子质量是44.96,该选项说法不正确;
C、原子结构示意图中x=8,这是因为第二层电子数最多是8个,该选项说法不正确;
第8页(共15页)D、钪原子核外有四个电子层,该选项说法正确。
故选:D。
【点评】元素周期表反映了元素之间的内在联系,要注意理解和应用。
5.(1.5分)
【考点】B3:微粒观点及模型图的应用;D6:有关元素化合价的计算.
【分析】观察反应的微观示意图,分析反应物生成为及反应的条件写出反应的化学方程式;
根据物质组成、方程式的意义等分析物质的类别、反应的类型等。
【解答】解:据题目信息结合微观示意图可写出反应的方程式为:CH O+O
2 2
CO +H O。
2 2
A.分子是由原子构成的,甲醛分子由碳原子、氢原子和氧原子构成,其中不含水分子,故
错误;
B.物质乙是氧气,是一种单质,单质中元素的化合价为零,故错误;
C.由质量守恒定律可知,化学反应前后原子的种类与数目保持不变,故错误;
D.该反应消耗物质甲和生成物质丁的质量比为(12+1×2+16):(1×2+16)=30:18=5:3,
故正确。
故选:D。
【点评】此题是对化学反应微观示意图问题的考查,根据分子构成判断反应物与生成物的
种类,写出反应的方程式,然后结合相关的知识分析解答即可。
6.(1.5分)
【考点】HK:氢气的化学性质与燃烧实验.
【分析】根据氢气具有还原性,能与氧化铜反应生成铜和水,进行分析判断。
【解答】解:A、Cu与稀H SO 不反应,故选项说法错误。
2 4
B、氢气具有还原性,能与氧化铜反应生成铜和水,可观察到固体粉末由黑色变成红色,故
选项说法正确。
C、发生的反应为 CuO+H Cu+H O,故选项说法正确。
2 2
D、氢气能与氧化铜反应生成铜和水,氢气夺取了氧化铜中的氧,具有还原性,故选项说法
正确。
故选:A。
【点评】本题难度不大,掌握氢气具有还原性、金属的化学性质是正确解答本题的关键。
7.(1.5分)异烟肼(化学式:C H N O;相对分子质量:137)是治疗肺结核药物的有效成分。下
6 7 3
第9页(共15页)列说法正确的是( )
A.异烟肼属于氧化物
B.异烟肼分子中 H、O 原子个数比为 7:1
C.异烟肼中 C、H 两种元素的质量比为 36:7
D.异烟肼中 N 元素质量分数的计算式为 ×100%
【考点】A3:从组成上识别氧化物;D1:化学式的书写及意义;D9:元素质量比的计算;
DA:元素的质量分数计算.
菁优网版权所有
【分析】A.根据氧化物的概念来分析;
B.根据化学式的意义来分析;
C.根据化合物中元素的质量比计算方法来分析;
D.根据化合物中元素质量分数的计算方法来分析。
【解答】解:A.氧化物是由两种元素组成的化合物,而异烟肼是由四种元素组成的,不属于
氧化物,故错误;
B.由化学式可知,异烟肼分子中 H、O 原子个数比为 7:1,故正确;
C.异烟肼中 C、H 两种元素的质量比为(12×6):(1×7)=72:7,故错误;
D.异烟肼中,氮元素质量分数的计算式为 ×100%,故错误。
故选:B。
【点评】本题主要考查化学式的意义和有关计算,难度稍大。
8.(1.5分)
【考点】34:化学实验方案设计与评价;86:金属活动性顺序及其应用;9H:盐的化学性质.
【分析】A、根据电解水的成本较高,进行分析判断。
B、根据水的净化原理,进行分析判断。
C、在金属活动性顺序中,位于前面的金属能把排在它后面的金属从其盐溶液中置换出来,
进行分析判断。
D、除杂质题至少要满足两个条件: 加入的试剂只能与杂质反应,不能与原物质反应;
反应后不能引入新的杂质。 ①
【②解答】解:A、电解水的成本较高,不能获得廉价的新能源,故选项实验方案不合理。
B、经沉淀、过滤、吸附,所得水中仍含有可溶性钙镁化合物等,不能将河水净化为纯水,故
选项实验方案不合理。
C、Zn 片与CuSO 溶液反应,生成硫酸锌溶液和铜,锌片的表面覆盖一层红色物质,可验
4
第10页(共15页)证金属活动性 Zn>Cu,故选项实验方案合理。
D、MgCl 能与过量NaOH溶液反应生成氢氧化镁沉淀和氯化钠,能除去杂质但引入了新
2
的杂质氢氧化钠(过量的),不符合除杂原则,故选项实验方案不合理。
故选:C。
【点评】本题难度不是很大,化学实验方案的设计是考查学生能力的主要类型,同时也是
实验教与学难点,在具体解题时要对其原理透彻理解,可根据物质的物理性质和化学性质
结合实验目的进行分析判断。
9.(1.5分)
【考点】7N:固体溶解度曲线及其作用;7R:溶质的质量分数.
菁优
【分析】根据固体的溶解度曲线可以: 查出某物质在一定温度下的溶解度,从而确定物
质的溶解性, 比较不同物质在同一温①度下的溶解度大小,从而判断饱和溶液中溶质的
质量分数的大小②, 判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶
还是蒸发结晶的方法③达到提纯物质的目的。
【解答】解:A、t ℃时,甲物质的溶解度是137g,所以50g的水中会溶解68.5g,所以I是甲
2
的不饱和溶液,故A错误;
B、t ℃时,甲物质的溶解度是137g,溶液I100g中含物质甲50g,所以溶液I中甲的质量分
2
数为 ×100%=50%,故B正确;
C、t ℃时,乙物质的溶解度是137g,所以溶液II100g中含乙50g,故C错误;
2
D、t ℃时,乙物质的溶解度是80g,溶液乙100g中含物质甲50g,从t ℃降温至t ℃时,50g
1 2 1
的水中会溶解40g的乙,所以乙会从溶液 II 中析出,故D错误。
故选:B。
【点评】本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的
溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力。
10.(1.5分)
【考点】AF:物质的相互转化和制备.
【分析】A、反应 是氧化钙能与水反应,进行分析判断。
B、根据反应 是①稀盐酸与氢氧化钙反应生成氯化钙和水,进行分析判断。
C、反应 是②碳酸钠能与氢氧化钙生成碳酸钙沉淀和氢氧化钠,进行分析判断。
D、根据③酸的化学性质,进行分析判断。
【解答】解:A、反应 是氧化钙能与水反应,放出热量,故选项说法正确。
第11页(共15页)
①B、反应 是稀盐酸与氢氧化钙反应生成氯化钙和水,可能是恰好完全反应,反应 所得
溶液可呈②中性,故选项说法正确。 ②
C、反应 是碳酸钠能与氢氧化钙生成碳酸钙沉淀和氢氧化钠,反应 所得溶液可呈碱性,
故选项说②法正确。 ②
D、硫酸能与氧化钙、碳酸钠、氢氧化钙反应,能将图中稀盐酸换为稀 H SO ,故选项说法
2 4
错误。
故选:D。
【点评】本题难度不大,掌握酸碱盐的化学性质、氧化钙的化学性质是正确解答本题的关
键。
二、非选择题(共3题,共25分)
11.(8分)
【考点】89:金属材料及其应用;8B:铁的冶炼;8G:金属锈蚀的条件及其防护.
【分析】(1)根据金属材料包括纯金属和合金,及产生酸雨的主要原因去分析。
(2)根据反应的特点、炼铁的原料、化学方程式的书写分析;
(3)根据铁生锈的原理分析防锈的方法。
【解答】解:(1)生铁是铁的合金,属于金属材料;二氧化硫气体,会造成酸雨。
(2) C+CO 2CO,反应中由两种物质生成一种物质,属于化合反应;
2
①
CO炼铁的原理是一氧化碳还原氧化铁生成铁和二氧化碳,化学方程式为:3CO+Fe O
2 3
②
2Fe+3CO ;
2
CaCO 和 SiO 固体在高温条件下发生反应,生成CO 气体和CaSiO ,反应的化学方
3 2 2 3
③
程式为CaCO +SiO CaSiO +CO ↑;
3 2 3 2
(3)铁的锈蚀实质是Fe与空气中水、氧气等发生化学反应的过程。防止铁制品锈蚀就是将
铁制品与水、氧气隔离,可用涂油、喷漆、镀耐腐蚀的铬层等方法防锈;用盐水清洗、久置
于酸性环境会加速铁的锈蚀。
故答案为:(1)金属;SO ;
2
(2) 化合;
①
3CO+Fe O 2Fe+3CO ;
2 3 2
②
第12页(共15页)CaCO +SiO CaSiO +CO ↑;
3 2 3 2
③
(3)水、氧气;AB。
【点评】本题主要考查了材料分类、空气污染问题、铁的冶炼、铁的生锈条件和防锈措施等。
能够引起酸雨的是 SO 和氮的氧化物;铁生锈需要与氧气和水同时接触,所以防锈措施
2
包括隔绝水或氧气、保持干燥等方法。
12.(8分)
【考点】2G:实验探究物质的组成成分以及含量;6D:氧气的制取装置;6E:氧气的收集方
法;G1:质量守恒定律及其应用.
【分析】化学反应遵循质量守恒定律,即参加反应的物质的质量之和,等于反应后生成的
物质的质量之和,是因为化学反应前后,元素的种类不变,原子的种类、总个数不变。
【解答】解:(1)若用一种暗紫色固体制取 O ,是利用高锰酸钾制取氧气,发生反应的化学
2
方程式为:2KMnO K MnO +MnO +O ↑,发生装置应选择上述装置A。
4 2 4 2 2
故填:2KMnO K MnO +MnO +O ↑;A。
4 2 4 2 2
(2)欲制取干燥的 O ,装置合理的连接顺序为:发生装置→C→F;
2
连接装置时,发生装置的出气口应与装置 C 中a端相连。
故填:F;a。
(3)装置 K 中无水 CuSO 变蓝色,是因为反应生成了水;
4
装置L中澄清石灰水变浑浊,是因为反应生成了二氧化碳,实验过程如下所示:
实验操作 实验现象 结论
连接装置,检查气密性,装入试 装置 K 中无水 CuSO 变 塑料燃烧产物中有 H O
4 2
蓝色
剂并按如图进行实验。通入O ,
2
一段时间后,点燃 J 处酒精灯。 装置L中澄清石灰水变浑 塑料燃烧产物中有 CO 2
浊
由上述实验可知,该塑料一定含有的元素是H、C。
③故填:H、C。
(4)反应的氧气质量:4.4g+1.8g﹣1.4g=4.8g,
塑料中氧元素质量:4.4g× +1.8g× ﹣4.8g=0,说明塑料中不含有氧元素。
故填:不含。
【点评】化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总
第13页(共15页)个数不变,这是书写化学方程式、判断物质的化学式、判断化学计量数、进行相关方面计
算的基础。
13.(9分)
【考点】9G:常用盐的用途;9H:盐的化学性质;G6:根据化学反应方程式的计算.
【分析】(1)根据碳酸氢钠的性质和用途分析和解答;
(2)根据给出的图以及对应的化学方程式计算和解答;
【解答】解:
(1)
A.NaHCO 俗称小苏打。正确;
3
B.碳酸氢钠属于钠盐,所有的钠盐均可溶。错误;
C.碳酸氢钠可与稀盐酸发生反应生成氯化钠、水和二氧化碳。正确;
D.碳酸氢钠是发酵粉的主要成分之一。正确;
故选:B。
(2)欲测定某 NaHCO 固体样品(只含Na CO 杂质且分布均匀)中NaHCO 的质量分数,
3 2 3 3
将 5.0g 该样品加热至质量不再改变,测得剩余固体的质量、生成CO 的质量随时间变化
2
如图所示。
NaOH溶液为碱,所以pH>7,用该溶液将生成的CO 完全吸收,发生反应是氢氧化钠
2
①和二氧化碳反应生成碳酸钠和水,对应的化学方程式为 CO +2NaOH=Na CO +H O。
2 2 3 2
由图中数据可知,上述5.0g NaHCO 样品完全分解产生CO 的质量为 1.1 g,根据质
3 2
②量守恒定律,产生H O的质量是5.0g﹣3.45g﹣1.1g=0.45 g。
2
设该样品中 NaHCO 的质量分数为 x。
3
③
2NaHCO Na CO +CO ↑+H O
3 2 3 2 2
168 44
5g x 1.1g
=
x=84%
答:该样品中 NaHCO 的质量分数为 84%。
3
故答案为:
(1)B;
(2) >;CO +2NaOH=Na CO +H O;
2 2 3 2
第14页(共15页)
①1.1;0.45;
②84%。
【点③评】根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三
计算过程要完整。
第15页(共15页)