文档内容
责任编辑 黄金国 经上海市中小学教材审查委员会 高级中学课本
高
整体设计 陈 蕾
审查准予试用 准用号 Ⅱ -GB-2006017
级
中
学
课
本
化
学
高
中
一
年
级
第
一
学 高中一年级第一学期
期
) (试用本)
试
用
本
)
高级中学课本
化 学
高中一年级第一学期
(试用本)
上海市中小学(幼儿园)课程改革委员会
上海世纪出版股份有限公司
出版
上 海 科 学 技 术 出 版 社
(上海钦州南路71号,邮政编码200235)
上海中华印刷厂印刷 上海新华书店发行
开本890×1240 1/16 印张6.5
上
2007年8月第1版 2007年8月第1次印刷
海
印数: 1-00 000
科
ISBN 978-7-5323-8923-0 学
技
术
定价:7.35元
出
版
上海市物价局价格审查批准文号:沪价商专(2007)12号 社
此书如有印、装质量问题,请径向本社调换
全国物价举报电话:12358
上海科学技术出版社电话:64089888
上海科学技术出版社高级中学课本
高中一年级第一学期
(试用本)
上海科学技术出版社
化学一(1)目录ok Page 1 2011.4.7, 4:00 AM Adobe PageMaker 6.5C/PPC化学一(1)目录ok Page 2 2011.4.7, 4:00 AM Adobe PageMaker 6.5C/PPC目 录
1
打开原子世界的大门
OPEN THE DOOR OF ATOMIC
STRUCTURE
3◆ 1.1 从葡萄干面包原子模型到原子
结构的行星模型
8◆ 1.2 原子结构和相对原子质量
13◆ 1.3 揭开原子核外电子运动的面纱
2
开发海水中的卤素资源
EXPLOIT HALOGEN RESOURCES
IN SEAWATER
23◆ 2.1 以食盐为原料的化工产品
31◆ 2.2 海水中的氯
39◆ 2.3 从海水中提取溴和碘
目录11
化学一(1)目录ok Page 3 2011.4.7, 4:00 AM Adobe PageMaker 6.5C/PPC3
探索原子构建物质的奥秘
EXPLORE THE MYSTERIES OF CHEMICAL
SUBSTANCES BUILT UP BY ATOMS
57◆ 3.1 原子间的相互作用
60◆ 3.2 离子键
65◆ 3.3 共价键
4
剖析物质变化中的能量变化
ANALYSE THE CHANGES OF ENERGY IN
CHANGES OF SUBSTANCES
73◆ 4.1 物质在溶解过程中有能量变化吗
82◆ 4.2 化学变化中的能量变化
附录
93◆ Ⅰ 元素周期表
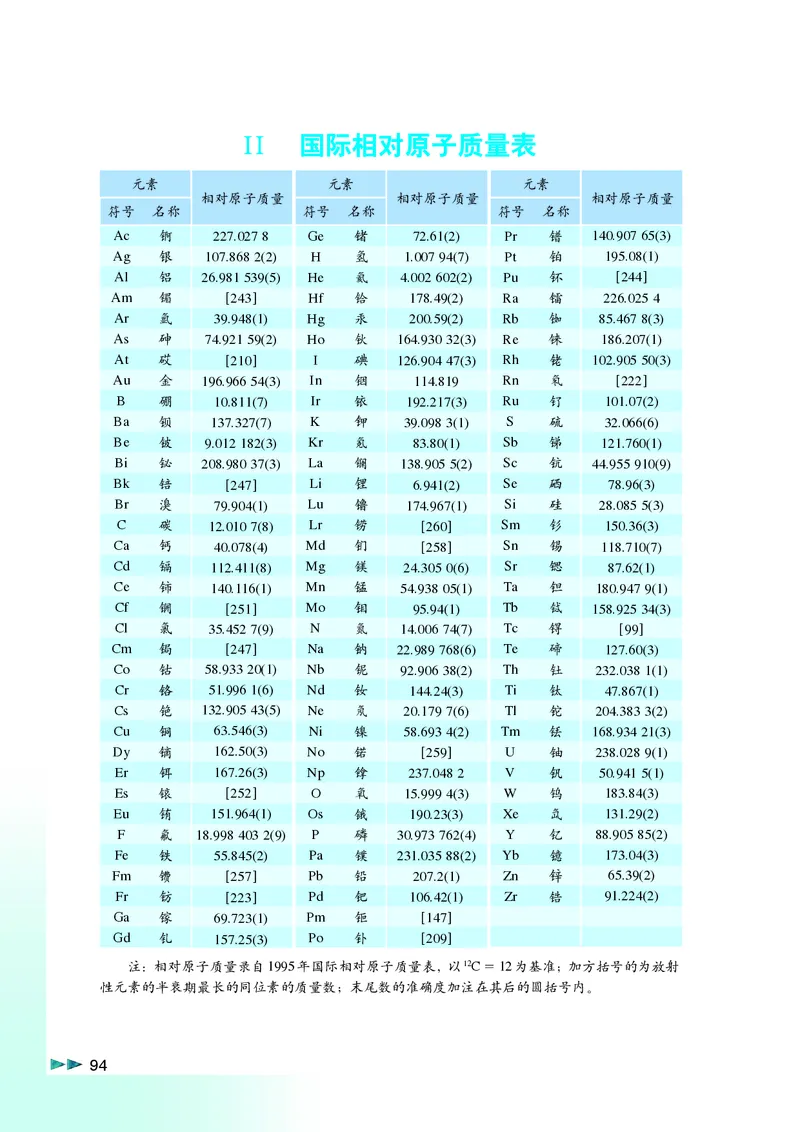
94◆ Ⅱ 国际相对原子质量表
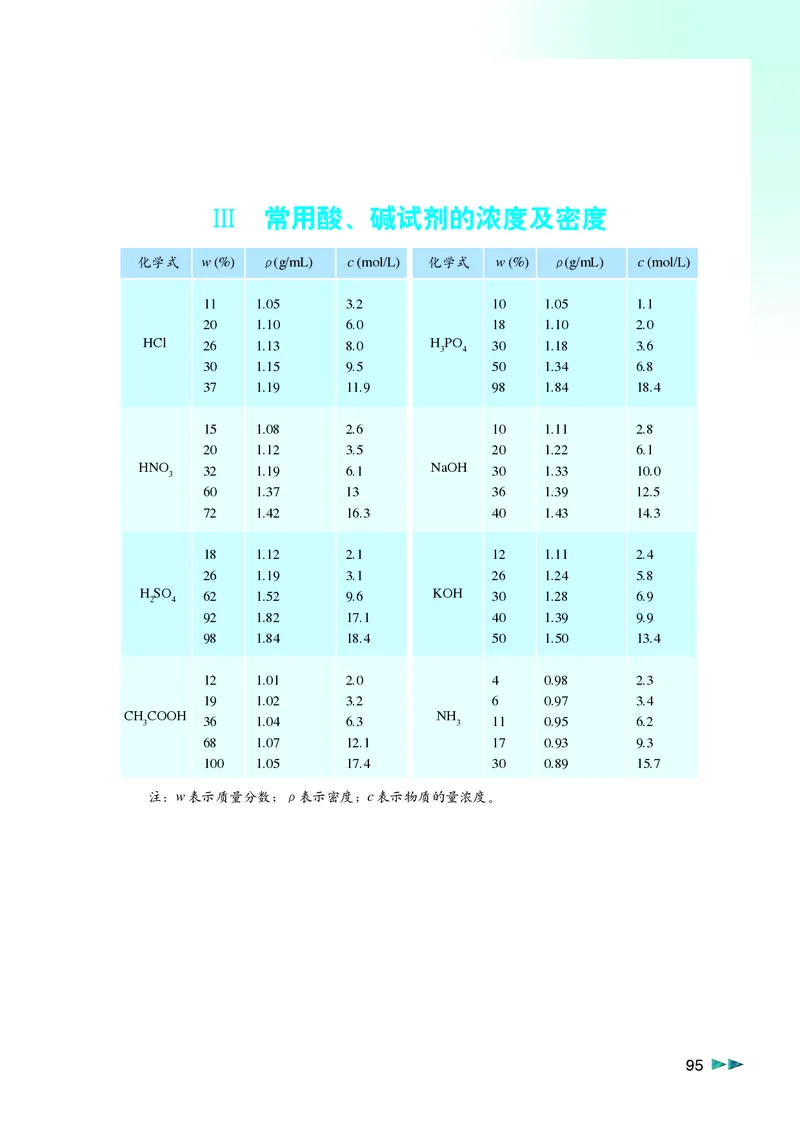
95◆ Ⅲ 常用酸、碱试剂的浓度及密度
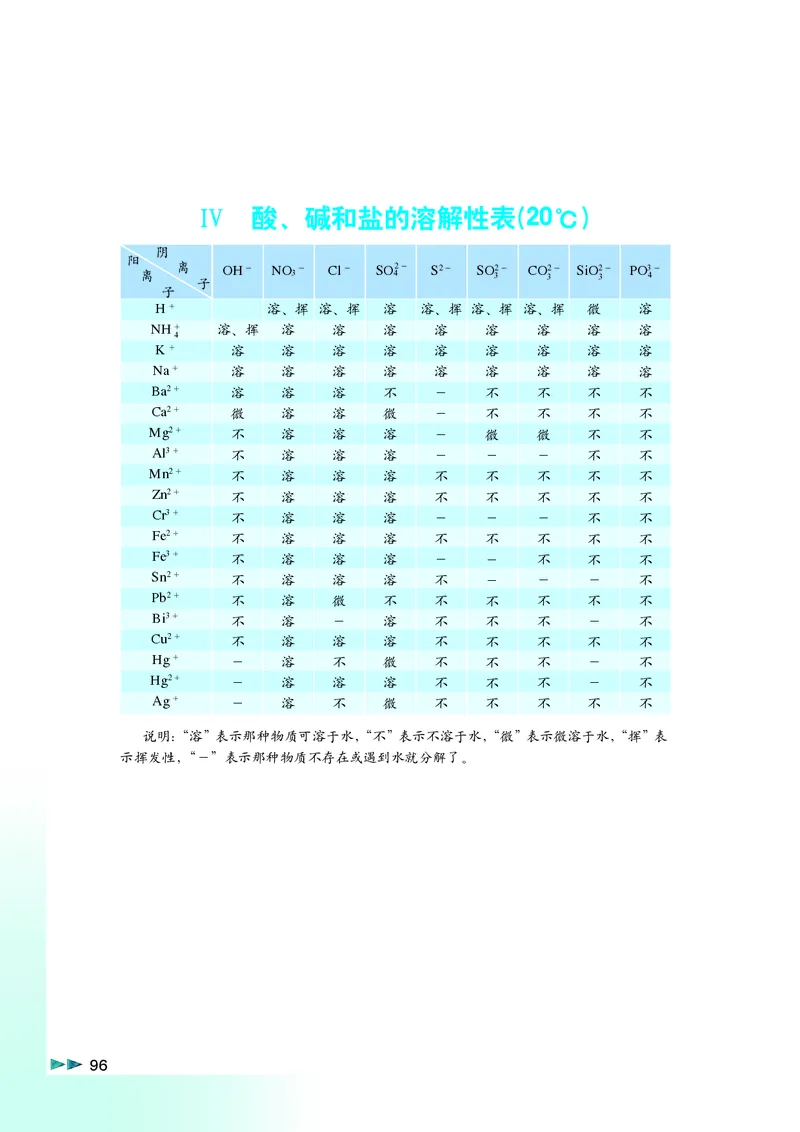
96◆ Ⅳ 酸、碱和盐的溶解性表(20℃)
97◆ Ⅴ 化学词汇英中文对照表
22目录
化学一(1)目录ok Page 4 2011.4.7, 4:00 AM Adobe PageMaker 6.5C/PPC1
打开原子世界的大门
OPEN THE DOOR OF ATOMIC STRUCTURE
◆ 原子的构成 ◆ 元素的相对原子质量
◆ 原子核外电子排布规律 ◆ 离子
◆ 同位素
1
第1章.p65 Page 1 2011.4.7, 3:56 AM Adobe PageMaker 6.5C/PPC随
着科学技术的进步和对原子结构认识的
深化,人们合成的各种各样的物质使我
们所处的物质世界发生着深刻的变化。
而所有的物质和材料都是由百余种元素的原子通过不同
形式组合而形成的。我们只有认识了原子的结构,才能
了解各种化学元素的性质以及它们是如何构建出丰富多
彩的新物质、新材料,以满足各方面日益增长的需要的。
学习化学,首先就要打开原子世界的大门。
2
第1章.p65 Page 2 2011.4.7, 3:56 AM Adobe PageMaker 6.5C/PPC从葡萄干面包原子模型到原子结构的行星模型
1
(FROM RAISIN BREAD ATOMIC MODEL TO PLANET MODEL
.1
OF ATOMIC STRUCTURE)
人们对原子结构的认识经历了几个历史阶段,也因此
留下了人类探究原子结构奥秘的足迹。
从古典原子论到葡萄干面包原子模型
随着人类物质文明的不断发展,特别是制陶、冶金、酿
酒等化学工艺的应用,促使古代的人们思考物质是怎样构
成的,由此形成了不少有关物质构成的观点。
我国战国时期的惠施说过:“一尺之棰,日取其半,万
世不竭。”他认为物质是无限可分的。
战国时期墨子则认为物质被分割是有条件的,如果物
质不存在被分割的条件,物质就不能被分割。这种不能再
被分割的部分,他称其为“端”。
古希腊哲学家德谟克利特(Democritus,约公元前460
—公元前370)则提出古典原子论,认为物质由极小的称为
“原子”(atom)的微粒构成,物质只能分割到原子为止。 图 1.1 德谟克利特
到了19世纪初,英国物理学家和化学家道尔顿(John
Dalton,1766—1844)于1803年提出他的原子论。道尔顿
原子学说为近代化学发展奠定了基础,其要点为:化学元
素均由不可再分的微粒构成,这种微粒称为原子;原子在
一切化学变化中均保持其不可再分性;同一元素的原子在
质量和性质上都相同,不同元素的原子在质量和性质上都
不相同;不同元素化合时,这些元素的原子按简单整数比
结合成化合物。
19世纪末至20世纪初,随着生产力和科技的发展,电
子(electron)被发现了。由于物质在通常情况下显电中性,
而物质中既然存在带负电荷的电子,那么一定还存在带正 图 1.2 道尔顿
电荷的部分。对于原子来说,它所带的正电荷的电荷量必
3
第1章.p65 Page 3 2011.4.7, 3:56 AM Adobe PageMaker 6.5C/PPC然与其电子所带的负电荷的电荷量相等。
英国科学家汤姆孙(Joseph John Thomson,1856—
1940)在1903年提出了葡萄干面包原子模型。他认为,原
子中的正电荷是均匀地分布在整个原子的球形体内,电子
则均匀地分布在这些正电荷之间,就像葡萄干面包一样。
由于人们对原子结构的探索很快进入了新的阶段,汤
姆孙提出的原子模型还未被大多数科学家了解就被弃置一
旁了,但这个模型指出了原子是有结构的。人们对原子结
图 1.3 汤姆孙葡萄干面包
构的探索在发现X射线后才取得新的突破。
原子模型示意图
从X射线到元素放射性的发现
德国物理学家伦琴(Wilhelm Conrad Röntgen, 1845—
1923)在1895年发现了看不见的射线——X射线(X-ray),
这在当时是一个具有重大科学意义和实用价值的发现。
正当不少科学家兴致勃勃地在谈论这种具有巨大穿透
能力的辐射时,法国物理学家贝克勒尔(Antoine Henri
Becquerel, 1852—1908)萌发了一个奇妙的想法,这个想
法就是“哪里还会有看不见的射线?”正是在这种好奇心
的驱动下,贝克勒尔发现了铀的放射性(radioactivity),并
获得了1903年诺贝尔物理学奖。
图 1.4 伦琴
化学史话
1896年贝克勒尔首先想到的是在荧光
中是否也会有看不见的射线。他用被阳光照
射后能发出荧光的铀盐进行实验。
图 1.5 贝克勒尔
4
第1章.p65 Page 4 2011.4.7, 3:56 AM Adobe PageMaker 6.5C/PPCa. 铀盐晶体放置在黑色密封包裹的照 b. 冲洗出的照相底片上出现晶体
相底片上,置于阳光下 感光影像
c. 连日阴雨,实验无法进行,偶然间 d. 几天后冲洗出的照相底片上也出现同
贝克勒尔把铀盐晶体和照相底片一起置 样的晶体感光影像
于抽屉中
图 1.6 贝克勒尔发现铀盐有放射性
这个实验说明底片的曝光不是由阳光照射后的铀盐产生的荧光引起的,而是
铀盐本身发出的看不见的射线引起的。他进一步研究发现纯铀放出射线比铀盐强
好几倍,元素放射性现象由此被发现。
某些元素(element)具有放射性,更进一步说明原
子是具有一定结构的。英国物理学家卢瑟福(Ernest
Rutherford, 1871—1937,1908年诺贝尔化学奖获得者)从
“放出的射线是什么”出发来进一步研究原子结构。他发现
铀能产生两种不同的辐射,一种称之为α辐射,另一种称
之为β辐射。1905年,卢瑟福从α粒子的电荷、质量比值
的实验结果,断定α粒子是氦(helium)原子失去电子后的
正离子(He2+)。此后,人们证实β射线是电子流;另外还
存在一种γ射线,它是波长很短的电磁波。
图 1.7 卢瑟福
5
第1章.p65 Page 5 2011.4.7, 3:56 AM Adobe PageMaker 6.5C/PPC-
+
γ
α
β
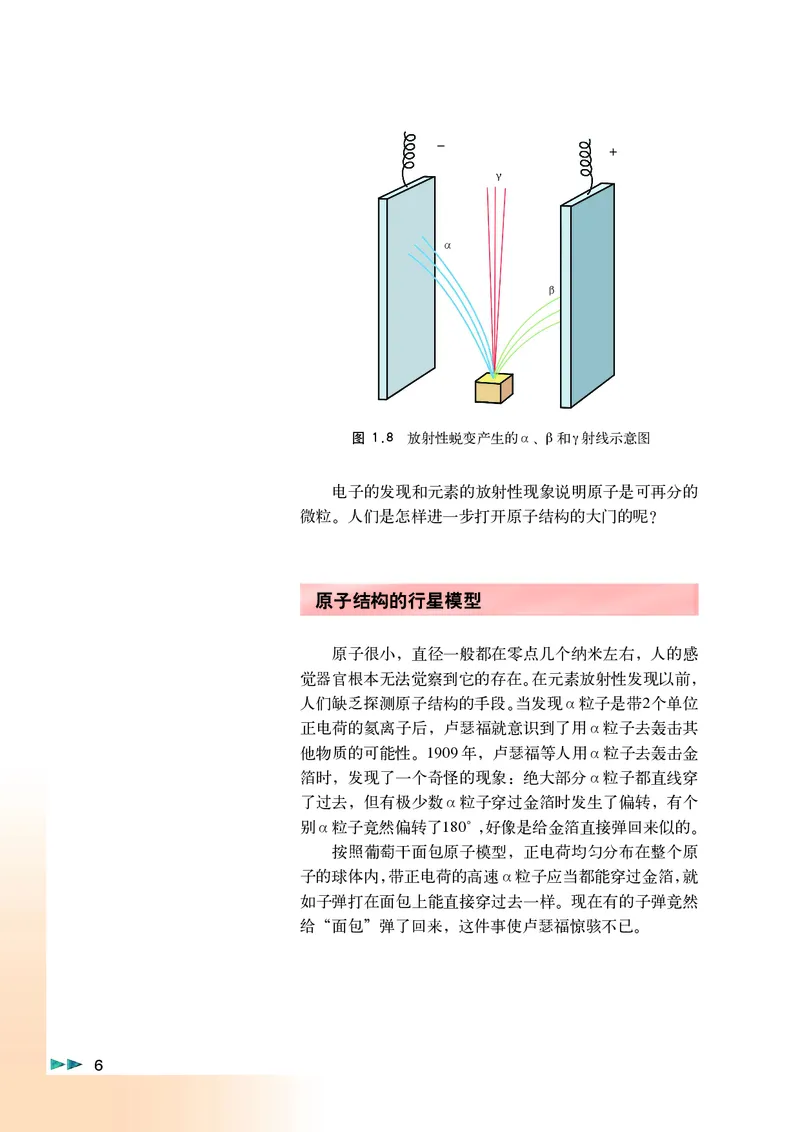
图 1.8 放射性蜕变产生的α、β和γ射线示意图
电子的发现和元素的放射性现象说明原子是可再分的
微粒。人们是怎样进一步打开原子结构的大门的呢?
原子结构的行星模型
原子很小,直径一般都在零点几个纳米左右,人的感
觉器官根本无法觉察到它的存在。在元素放射性发现以前,
人们缺乏探测原子结构的手段。当发现α粒子是带2个单位
正电荷的氦离子后,卢瑟福就意识到了用α粒子去轰击其
他物质的可能性。1909年,卢瑟福等人用α粒子去轰击金
箔时,发现了一个奇怪的现象:绝大部分α粒子都直线穿
了过去,但有极少数α粒子穿过金箔时发生了偏转,有个
别α粒子竟然偏转了180°,好像是给金箔直接弹回来似的。
按照葡萄干面包原子模型,正电荷均匀分布在整个原
子的球体内,带正电荷的高速α粒子应当都能穿过金箔,就
如子弹打在面包上能直接穿过去一样。现在有的子弹竟然
给“面包”弹了回来,这件事使卢瑟福惊骇不已。
6
第1章.p65 Page 6 2011.4.7, 3:56 AM Adobe PageMaker 6.5C/PPC一束α粒子
被散射的α粒子
α粒子源
ZnS荧光屏
金箔 大多数α粒子
没有被散射
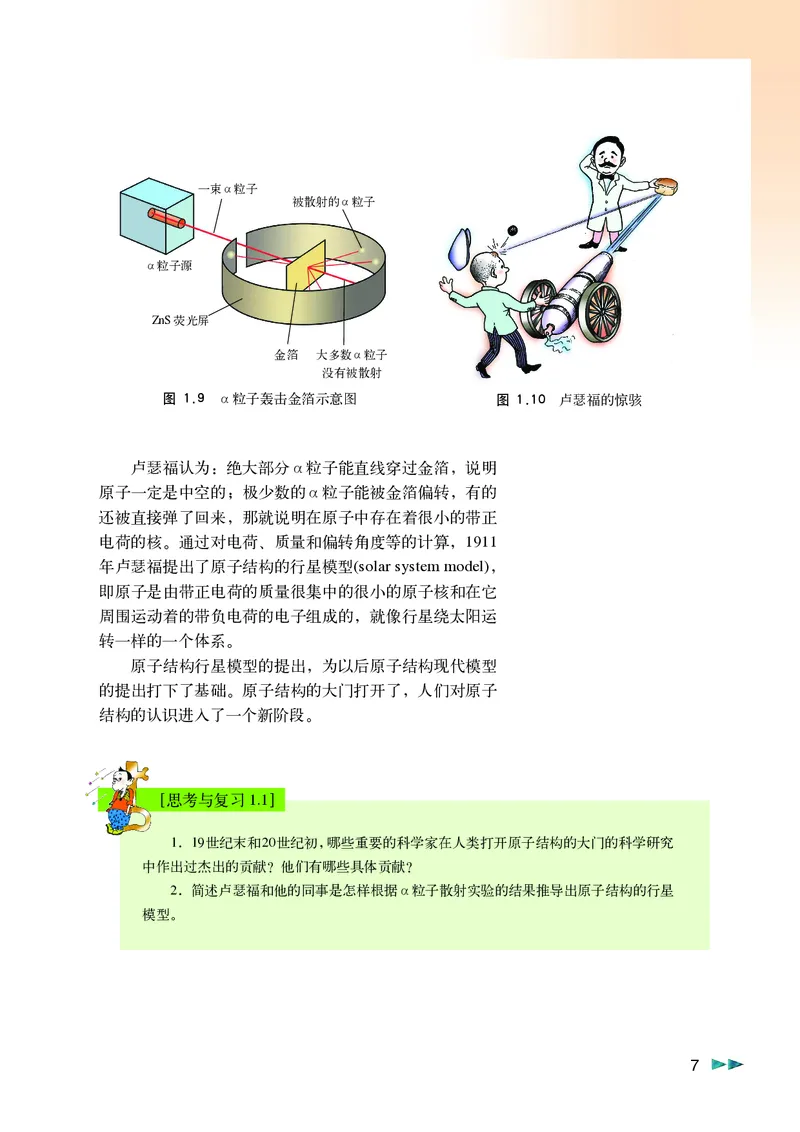
图 1.9 α粒子轰击金箔示意图 图 1.10 卢瑟福的惊骇
卢瑟福认为:绝大部分α粒子能直线穿过金箔,说明
原子一定是中空的;极少数的α粒子能被金箔偏转,有的
还被直接弹了回来,那就说明在原子中存在着很小的带正
电荷的核。通过对电荷、质量和偏转角度等的计算,1911
年卢瑟福提出了原子结构的行星模型(solar system model),
即原子是由带正电荷的质量很集中的很小的原子核和在它
周围运动着的带负电荷的电子组成的,就像行星绕太阳运
转一样的一个体系。
原子结构行星模型的提出,为以后原子结构现代模型
的提出打下了基础。原子结构的大门打开了,人们对原子
结构的认识进入了一个新阶段。
[思考与复习1.1]
1.19世纪末和20世纪初,哪些重要的科学家在人类打开原子结构的大门的科学研究
中作出过杰出的贡献?他们有哪些具体贡献?
2.简述卢瑟福和他的同事是怎样根据α粒子散射实验的结果推导出原子结构的行星
模型。
7
第1章.p65 Page 7 2011.4.7, 3:56 AM Adobe PageMaker 6.5C/PPC1 原子结构和相对原子质量
.2
(ATOMIC STRUCTURE AND RELATIVE ATOMIC MASS)
原子的构成
原子是构成物质的一种微粒。原子又是由哪些微粒构
成的呢?这些微粒有哪些主要性质,它们相互之间有何关
系?
原子是由位于原子中心的原子核和核外电子构成的。
原子很小,原子核更小,它的半径是原子的万分之一,它的
体积只占原子体积的几千亿分之一。原子核是由质子和中
子构成的。表1.1列出了构成原子的微粒和性质。
表1.1 构成原子的微粒和性质
原 子
原子核
构成原子的微粒 电子
质子 中子
质量 9.041×10-31 kg 1.672 6×10-27 kg 1.674 8×10-27 kg
1
相对质量* —— 1.007 1.008
1 836
电性和电荷量 带1个单位负电荷 带1个单位正电荷 不显电性
1
*是指与一种碳原子(原子核内有6个质子和6个中子的碳原子)质量的—相比较所得的数值的近似值。
12
1
电子的质量很小,仅为质子质量的———,原子的质
化合价 1 836
质量数A
±a
b±离子电荷
量主要集中在原子核上。质子(proton)和中子(neutron)的
相对质量分别为1.007和1.008,均取近似整数值为1。如果
忽略电子的质量,将原子核内所有的质子和中子相对质量
质子数Z c原子个数
取近似整数值,加起来所得的数值,叫做质量数,用符号A
图 1.11 元素符号角标的意义 表示。
8
第1章.p65 Page 8 2011.4.7, 3:56 AM Adobe PageMaker 6.5C/PPC构成原子的微粒数之间存在如下关系:
核电荷数(Z)=核内质子数=核外电子数
质量数(A)=质子数(Z)+中子数(N)
构成原子中微粒间的关系可以表示如下:
{质子Z个
{原子核
中子(A-Z)个
原子(X)
核外电子Z个
思考与练习
根据构成原子的各种微粒数之间的关系,求质量数为
40、核外电子数为18的氩原子的核电荷数、质子数和中子数。
同位素
我们知道,具有相同核电荷数(即质子数)的同一类原
子叫做元素。也就是说,同种元素原子的质子数相同,那
么,它们的中子数是否相同呢?科学研究证明,它们不一
定相同。 图 1.12 氕、氘、氚原子
例如,我们发现自然界里有三种不同的氢原子:氕、氘 结构的示意图
(deuterium)、氚(tritium)*(图1.12)。从图中看出,这三种
*氕音pie
-
,氘音da
-
o,氚音chua
-
n。氘
原子的核内都有1个质子,核外都是1个电子,不同的是核 就是重氢,氚就是超重氢。氕、氘、氚
分别用H、D、T来表示。
内所含中子数不一样。氕原子核内只有1个质子,没有中子;
氘原子核内有1个质子和1个中子;氚原子核内有1个质子
和2个中子。因此,氕、氘、氚的质量数也不同,分别为1、
2、3。我们可用化学符号1 H、2 H、3 H来表示氕、氘、氚这
1 1 1
三种不同的氢原子。
氕、氘、氚的原子核所带的核电荷数一样,它们属于同
一种元素——氢元素,它们原子核内的质子数相同,但中
子数不同,原子的质量数也不同,所以不属于一种原子。像
这种具有相同质子数和不同中子数的同一种元素的原子互
称为同位素(isotope)。
大多数天然元素都有同位素。上述1 H、2 H、3 H是氢
1 1 1
的三种同位素,其中2 H、3 H是制造氢弹的材料。铀元素有
1 1
234 U、 235 U、 238U等多种同位素,其中 235 U是制造原子弹的原
92 92 92 92
9
第1章.p65 Page 9 2011.4.7, 3:56 AM Adobe PageMaker 6.5C/PPC料和核反应堆的燃料。碳元素有 12 C、13 C和 14 C等几种同位
6 6 6
素,12 C就是作为相对原子质量基准的那种碳原子,通常也
6
叫碳-12。同一元素的各种同位素虽然质量不同,但它们的
化学性质几乎完全相同。在天然存在的某种元素里,不论
是游离态还是化合态,各种同位素所占的原子百分率一般
是不变的。同位素在现代科学上有很广泛的用途。
拓展视野
放射性同位素的应用
放射性同位素在工农业生产、科学研究、医学等领域有着重要的应用。
探测金属器件缺陷 育种
放射性同位素
研究化学反应机理 保存食物
图 1.13 放射性同位素的应用
人们用放射线对肿瘤进行“放射治
疗”。如医院里常用放射性同位素钴-60进
行“肿瘤照光”。放射治疗作为肿瘤治疗的
重要手段被广泛应用,但也会对人体其他
器官与组织造成难以避免的损伤,如血液
中白细胞减少、免疫功能下降、毛发脱落
等等。
图 1.14 放射线治疗肿瘤
相对原子质量
原子虽小,但还是具有一定的质量。如果用“克”作单
位来称量原子,所得的数值实在太小,给记忆和使用带来不
便。下面是一些原子的质量,它们的数值都很小。
10
第1章.p65 Page 10 2011.4.7, 3:56 AM Adobe PageMaker 6.5C/PPC原子 氢 氧 碳
质量(g) 1.674×10-24 2.656×10-23 1.993×10-23
思考与练习
根据氧原子和氢原子的质量计算一个水分子(H O)的
2
质量和求10 g水中所含的水分子数。
图 1.15 10 g水中含有巨大数目的水分子
这个数目为什么很大,能用什么简便的方法来计算。
在化学计量中,用相对原子质量(relative atomic mass)
来计算很方便。相对原子质量是以一个碳-12原子( 12C)
6
1
质量的—作为标准,任何一个原子的真实质量跟一个碳-12
12 1.按物质中原子的真
1 实质量进行化学计算,其
原子质量的—的比值,称为该原子的相对原子质量。例如,
12
结果和以相对原子质量进
1
一个碳-12原子的质量是1.993×10-23 g,它的—是1.661× 行计算的结果是一样的
12
吗?为什么?
10-24 g,当然很容易理解,碳-12原子的相对原子质量是12。
2.我国古代有个“曹
一个氧原子( 16 O)的质量是2.656×10-23 g,所以,一个氧
8 冲称象”的故事,大象质
原子( 16 O)的相对原子质量是:
8 量太大,古时没有称大象
的量具,曹冲把大象的质
2.656×10-23 g 量,分解成一船石块的质
= 15.990≈16
1.661×10-24 g 量。原子质量太小,“克”作
单位则太大,因此科学家
元素的相对原子质量是它的各种同位素的相对原子质 把称量原子的单位缩小为
1
量,根据其所占的原子百分率计算而得的平均值。 碳 -12原子质量的—。你
12
—
A=A·a %+A·a %+…+A·a % 能体会这两者之间的“异
1 1 2 2 n n
— A是相对原子质量,A ,A …是该元素各种同位素的相 曲同工”之妙吗?
1 2
对原子质量,a %,a %…是各同位素所占的原子百分率。
1 2
11
第1章.p65 Page 11 2011.4.7, 3:56 AM Adobe PageMaker 6.5C/PPC表1.2 国际约定量制基本量和符号单位 【资料库】
单位名称
量的名称 量的符号
及符号
物质的量(amount of substances)是国际约定
长度 l(L) 米 m 量制的7个基本量之一。
时间 t 秒 s 单位名称:摩[尔]。
质量 m 千克 kg 单位符号:mol。
温度 T 开[尔文]K 当物质所包含的微粒数与12 g碳-12(1 6 2C)
的原子数相同时,这些物质就是1 mol。
发光强度 I(I) 坎[德拉]cd
v
1 mol物质所含的微粒数称为阿伏加德罗
电流 I 安[培]A
常数,具体数值约为6.02×1023个(用N 表示)。
物质的量 n 摩[尔]mol A
在使用摩尔时,物质的微粒应予以指明,
例如:原子、分子、离子、电子等。
物质的摩尔质量指1 mol物质的质量,单
位是g/mol,其数值与物质的式量相同。式量
则是物质化学式中各元素的相对原子质量之和。
[思考与复习1.2]
1.填表,并说明编号为(3)、(4)的原子是什么关系?
编号 原子 核电荷数 质子数 中子数
(1) 12C
6
(2) 10 12
(3) 63Cu 29
29
(4) 29 36
2.举例说明为什么原子的种类要远比元素的种类多。
3.国际元素相对原子质量表上查得C是12.01,这是指碳的 ( )。
(A) 质量数 (B) 相对原子质量
(C) 同位素相对原子质量 (D) 平均相对原子质量
4.以下微粒互为同位素的是 ( )。
(A) 2H O和H O (B) 2H 和H (C) 2H和3H (D) O 和O
1 2 2 1 2 2 1 1 2 3
5.1个He原子中含有___________个电子,1 mol He原子中含有___________个质子,
0.5 molα粒子中含有___________mol质子,0.5 molα粒子的质量是___________ g。
12
第1章.p65 Page 12 2011.4.7, 3:56 AM Adobe PageMaker 6.5C/PPC揭开原子核外电子运动的面纱
1
(REVEAL THE VEIL OF MOTION OF ELECTRONS
.3
OUTSIDE ATOMIC NUCLEUS)
原子结构示意图与电子式
原子中的核外电子在核外作高速运动,在含有多个电
子的原子中,通常能量低的电子在靠近原子核处运动,能
量高的电子则在离核较远处运动,即核外电子按能量高低
由内层至外层分层排布的。这种分层排布情况可用原子结
构示意图来表示。
第一电子层称为K层,第二电子层称为L层,第三电
子层称为M层,由近及远的四、五、六、七层,也可依次
把它们称为N、O、P、Q层。
原子的核外电子排布可以用原子结构示意图表示。例
如,铝的原子结构示意图可表示为:
+13
2 8 3
图 1.16 铝的原子结构示意图
元素的化学性质主要由原子的最外层电子数决定,我
们常用小黑点(或×)来表示元素原子的最外层上的电子。
例如:
··
氢 H. 氧· O· 钠 Na.
··
这种图式我们称为电子式(electronic formula)。
13
第1章.p65 Page 13 2011.4.7, 3:56 AM Adobe PageMaker 6.5C/PPC初步认识核外电子排布的规律
你能从表1.3和表1.4
中归纳出原子核外电子排 仔细阅读下面两张表格:
布的一些规律吗?
表1.3 元素原子的电子层排布
核电 元素 元素 各电子层的电子数
荷数 名称 符号 K L M
1 氢 H 1
2 氦 He 2
3 锂 Li 2 1
4 铍 Be 2 2
5 硼 B 2 3
6 碳 C 2 4
7 氮 N 2 5
8 氧 O 2 6
9 氟 F 2 7
10 氖 Ne 2 8
11 钠 Na 2 8 1
12 镁 Mg 2 8 2
13 铝 Al 2 8 3
14 硅 Si 2 8 4
15 磷 P 2 8 5
16 硫 S 2 8 6
17 氯 Cl 2 8 7
18 氩 Ar 2 8 8
表1.4 稀有气体元素原子的电子层排布
核电 元素 元素 各电子层的电子数
荷数 名称 符号 K L M N O P
2 氦 He 2
10 氖 Ne 2 8
18 氩 Ar 2 8 8
36 氪 Kr 2 8 18 8
54 氙 Xe 2 8 18 18 8
86 氡 Rn 2 8 18 32 18 8
从表1.3和表1.4中我们可以归纳出核外电子排布的规
律:
1.各电子层最多可容纳的电子数为2n2(n表示电子层
序数),即K层最多容纳2×12=2个电子,M层最多容纳
2×32=18个电子等。
14
第1章.p65 Page 14 2011.4.7, 3:56 AM Adobe PageMaker 6.5C/PPC2.最外层电子数不超过8个(K层为最外层时则不超过
2个)。当最外层电子数达到8(K层为2)时,就达到了稀有
气体的稳定结构。
3.次外层电子数不超过18,倒数第三层电子数不超过
32。
金属元素原子最外层电子数比较少,
在化学反应中容易失去这些电子使次外层
变为最外层,达到稳定结构;反之非金属
元素原子最外层电子数比较多,反应时容
易得到电子使最外层达到8个电子稳定结
构;而稀有气体(rare gas)原子最外层已
达稳定结构,它们既不易失电子,也不易
图 1.17 不同电子层上的电子能量不同
得电子,所以化学性质很稳定。
离子
原子或原子团得、失电子后形成的带电微粒称为离子
(ion),离子也是构成物质的一种微粒。
离子或原子的结构和带电状况是不同的,如图1.18和
图1.19所示。
+8 +8 思考与练习
2 6 2 8
填表:
离子 结 构
图 1.18 氧原子(O)的结构 图 1.19 氧离子(O2-)的结构 名 称 电子式
符号 示意图
示意图 示意图
钠离子
带正电荷的离子称为阳离子,带负电荷的离子称为 硫离子
阴离子。
下面是一些常见的离子符号:
Na+ Cu2+ Fe2+ Cl- NH+
4
OH- SO2
4
-
比较Na和Na+结构上
钠离子 铜离子 亚铁离子 氯离子 铵根离子 氢氧根离子 硫酸根离子 有何异同?
15
第1章.p65 Page 15 2011.4.7, 3:56 AM Adobe PageMaker 6.5C/PPC[思考与复习1.3]
1.下列微粒结构示意图和电子式写得对吗?如有错,应如何改正?
+9 28 Ca · · [× ·· · · · O· ×] 2- · · · · C · · l× · +4 24
氟原子 钙原子 氧原子 氯离子 碳原子
2.写出下列微粒的结构示意图和电子式:
(1) C (2) Mg2+ (3) S2- (4) Ar
3.下列几种离子中,哪些核外电子排布相同?它们与何种稀有气体元素的原子有相同
的核外电子排布?
F- Ca2+ Cl- Na+ O2- K+
4.填表:
核内质 核外电 微粒结构 是否达到
微 粒 电子式
子数 子数 示意图 稳定结构
C
Al
S
Cl-
Mg2+
Ar
5.某元素离子R2+核外有23个电子,其质量数为55,则R原子核内中子数是___。
6.有四种微粒的结构示意图:+8 2 8 、+9 2 8 、+10 2 8 、+12 2 8 , 下列叙述中错误
的是 ( )。
(A) 它们属于不同的元素
(B) 它们都是离子
(C) 它们都具有稀有气体原子的稳定结构
(D) 它们的核外电子排布均相同
16
第1章.p65 Page 16 2011.4.7, 3:56 AM Adobe PageMaker 6.5C/PPC小结与思考
1.人类认识原子结构的几个探索历程。
(1)历程。
古典原子论 → 近代原子论 → 葡萄干面包模型 → 原子结构的行星模型
墨子、德谟克利特 道尔顿 汤姆孙 卢瑟福
19世纪初,英国物理学家和化学家道尔顿提出的原子论,他认为,“化学元素均由不可
再分的微粒构成,这种微粒称为原子。”
19世纪末至20世纪初,电子被发现了。英国科学家汤姆孙提出了葡萄干面包原子模型。
电子和元素放射性发现后,卢瑟福等人根据α粒子散射实验的结果,提出了原子结构的
行星模型。
从人类探索原子结构的历史过程能感悟科学家的科学精神,能认识科学技术的发展对人
类认识物质世界的重要作用。能认识“模型方法”和“实验方法”在科学研究中的作用,启
迪人们思考“创新”在社会发展与进步中的作用。
(2)卢瑟福的α粒子散射实验。
既然绝大部分α粒子能直线穿过金箔,说明原子一定是中空的;既然极少数的α粒子
能被金箔偏转,有的还被直接弹了回来,那就说明在原子中存在着很小的带正电荷的核。通
过对电荷、质量和偏转角度等的计算,1911年卢瑟福提出了原子结构的行星模型,即原子
是由带正电荷的质量很集中的很小的原子核和在它周围运动着的带负电荷的电子组成的,就
像行星绕太阳运转一样的一个体系。
实验方法是科学研究的重要方法,是检验事实的重要手段。在科学研究中可以通过实验
对假设进行检验,对提出的“模型”进行修正。在实验中会发现新的问题,提出新的思路。
实验方法是科学研究不可缺少的手段和方法。
2.原子结构和相对原子质量。
(1)元素。
具有相同核电荷数(即质子数)的同一类原子叫做元素。
(2)原子的构成。
{质子Z个
原子核
{
中子(A-Z)个
原子
核外电子Z个
17
第1章.p65 Page 17 2011.4.7, 3:56 AM Adobe PageMaker 6.5C/PPC(3)原子的质量数。
① 质量数。
如果忽略电子的质量,将原子核内所有的质子和中子相对质量取近似整数值,加起来所
得的数值,叫做质量数,用符号A表示。
② 构成原子的微粒数之间存在如下关系:
核电荷数(Z)=核内质子数=核外电子数
质量数(A)=质子数(Z)+中子数(N)
(4)同位素。
具有相同质子数和不同中子数的同一种元素的原子互称为同位素。例如,1H、2H、3H
1 1 1
是氢的三种同位素。
(5)原子的相对质子质量。
1
相对原子质量是以一个碳 12 C原子质量的—作为标准,任何一个原子的真实质量跟一
6 12
1
个碳-12原子质量的—的比值,称为该原子的相对原子质量。
12
(6)元素的相对原子质量。
元素的相对原子质量是它的各种同位素的相对原子质量,根据其所占的原子百分率计算
而得的平均值。
-
A=A·a%+A·a %+…+A·a %
1 1 2 2 n n
-
A是相对原子质量,A,A…是该元素各种同位素的相对原子质量,a %,a %…是各种
1 2 1 2
同位素所占的原子百分率。
通常所说的相对原子质量是指元素的相对原子质量。
3.原子核外电子排布。
核外电子按能量由低到高分层排布。每个电子层最多可容纳电子数为2n2,但各电子层
作为最外层时所能容纳的最多电子数为8(K层为2)。最外层8(K层为2)电子结构是稳定结构。
4.离子。
原子或原子团得、失电子后形成的带电微粒称为离子,离子也是构成物质的一种微粒。
例如,钠离子:Na+,氯离子:Cl-。
带正电荷的离子称为阳离子,带负电荷的离子称为阴离子。
5.原子(或离子)的结构示意图及电子式。
可把原子(或离子)的核外电子排布用结构示意图来表示。
例如, 硫原子 +16286 硫离子 +16288
钠原子 +11281 钠离子 +1128
18
第1章.p65 Page 18 2011.4.7, 3:56 AM Adobe PageMaker 6.5C/PPC原子(或离子)的最外层电子数用小黑点(或×)来表示,这种式子叫电子式。
例如,钠原子Na· 镁离子Mg2+ (阳离子的电子式,可用离子符号表示)
··
硫离子[·· S·· ]2-
··
6.思考与复习。
(1)①试写出下列微粒的结构示意图:
钠离子:____________________________
钙原子:____________________________
②写出下列微粒的电子式:
硫原子_______
氟离子(F-)_______
镁离子_______
质量数为17、核内有9个中子的阴离子_______。
③下列表示微粒结构的图式各代表什么微粒?
··
+9 28 ·O· +11 28 +18 288
··
_____ _____ _____ _____
··
④写出两种电子式均为 ·· X·· 的微粒符号。
··
(2)氢元素有氕( 1H)、氘( 2H)和氚( 3H)三种同位素,分别用H、D、T表示,
1 1 1
试说明这三种同位素结构上的相同点与不同点。
(3)填表:
符号 核电荷数(Z) 核内质子数 核外电子数 核内中子数 质量数(A)
(1) 235U
92
(2) AX- 36 45
Z
(4)已知A元素原子核外共有6个电子,B元素原子核外有两个电子层,其外层电子数
为内层电子数的3倍,C元素的原子核内有11个质子和12个中子,试写出:
①B元素的原子结构示意图:_______________
②C元素的离子符号:_______________
③由三种元素组成的化合物的化学式:_______________
19
第1章.p65 Page 19 2011.4.7, 3:56 AM Adobe PageMaker 6.5C/PPC(5)在人类认识原子结构的过程中,科学家曾使用过不少科学研究方法。其中有一种方
法是模型方法,如葡萄干面包模型、行星模型等。在科学研究中,人们根据实验事实和已知
的科学原理,对研究对象的结构、性能和运动规律进行理性分析,设想出其大致框架,即提
出未知事物的“模型”,然后再进行推理与计算,对未知事物作出解释和预测,并对模型加
以检验、修正乃至抛弃。还有一种是实验方法,如卢瑟福的α粒子散射实验,即通过改变外
部条件来给事物一个刺激,这种刺激要足够有力以便引起事物的某种变化,然后根据这种变
化进而推知未知事物的内部结构与功能。学习本章后,你怎样理解这两种方法对科学研究的
意义?
(6)阅读下列短文:
The electrons may be represented graphically as arranged in a number of successive“ shells”;
2 in the first, 8 in the second, 18 in the third, and 32 in the forth. If the outermost shell is complete,
the element is inert, like neon or argon. If the outermost shell is incomplete, this element enters into
chemical reaction. Atoms of metals have comparatively few electrons in the outermost shell (1, 2 or
3). Such atoms tend to lose electrons in chemical reaction. Atoms of non-metals have a comparatively
large number of electrons in the outermost shell (5, 6 or 7), and tend to gain electrons in chemical
reaction.
20
第1章.p65 Page 20 2011.4.7, 3:56 AM Adobe PageMaker 6.5C/PPC2
开发海水中的卤素资源
EXPLOIT HALOGEN RESOURCES IN SEAWATER
◆ 氯的单质和化合物性质 ◆ 电离方程式和离子方程式
◆ 氯、溴、碘的原子结构、性质 ◆ 氧化还原反应中的化合价变化
递变规律和用途 与电子得失的关系
◆ 气体摩尔体积 ◆ 有关化学反应的计算
21
第2章.p65 Page 21 2011.4.7, 3:57 AM Adobe PageMaker 6.5C/PPC浩
瀚的大海覆盖了约70%的地球表面。一
望无垠的蔚蓝色的海洋不仅集中了地球
上绝大部分的水,而且蕴藏着丰富的化
学资源。随着人口的增多和社会的进步,人们对化学资
源的需求不断增长,开发海洋、开发海水中丰富的化学
资源,已日益受到人们的重视。
让我们从最常见的海水中卤素资源的开发入手,进
入这一个有着诱人前景的领域吧。
22
第2章.p65 Page 22 2011.4.7, 3:57 AM Adobe PageMaker 6.5C/PPC以食盐为原料的化工产品
2
(CHEMICAL PRODUCTS FROM SALT AS THE RAW
.1
MATERIAL)
海洋是资源的宝库。若问你海水中含量最高的是哪种
物质,你肯定会说出“食盐”。海水中所含食盐(氯化钠)高
达4×1016 t,是海洋资源的重要组成部分,也是化学工业
的重要原料。
海水晒盐
古代我国的沿海居民就在海滩晒盐,汉末许慎(约公
元58—147)在《说文解字》中记载:“古宿沙初作,煮海
为盐。”说的就是传说中和神农氏同时代的宿沙氏首先用海
图 2.1 《天工开物》中制
水制食盐。把海水引入盐田,利用日光、风力蒸发浓缩海
海盐图
水,使其达到饱和,并进一步使食盐结晶出来,这种方法称
明朝末年,宋应星的《天
为太阳能蒸发法,又称为盐田法。目前,我国海盐的年产量 工开物》中设篇目“海水盐”,
已超过1×107 t,位居世界之首。 详细记载了海盐的生产过程。
a. 盐池 b. 用铲盐机收集盐层
c. 挖掘机挖出盐后将它放在传送带上 d. 盐通过传送带被装上船
图 2.2 现代盐田生产的一些情景
23
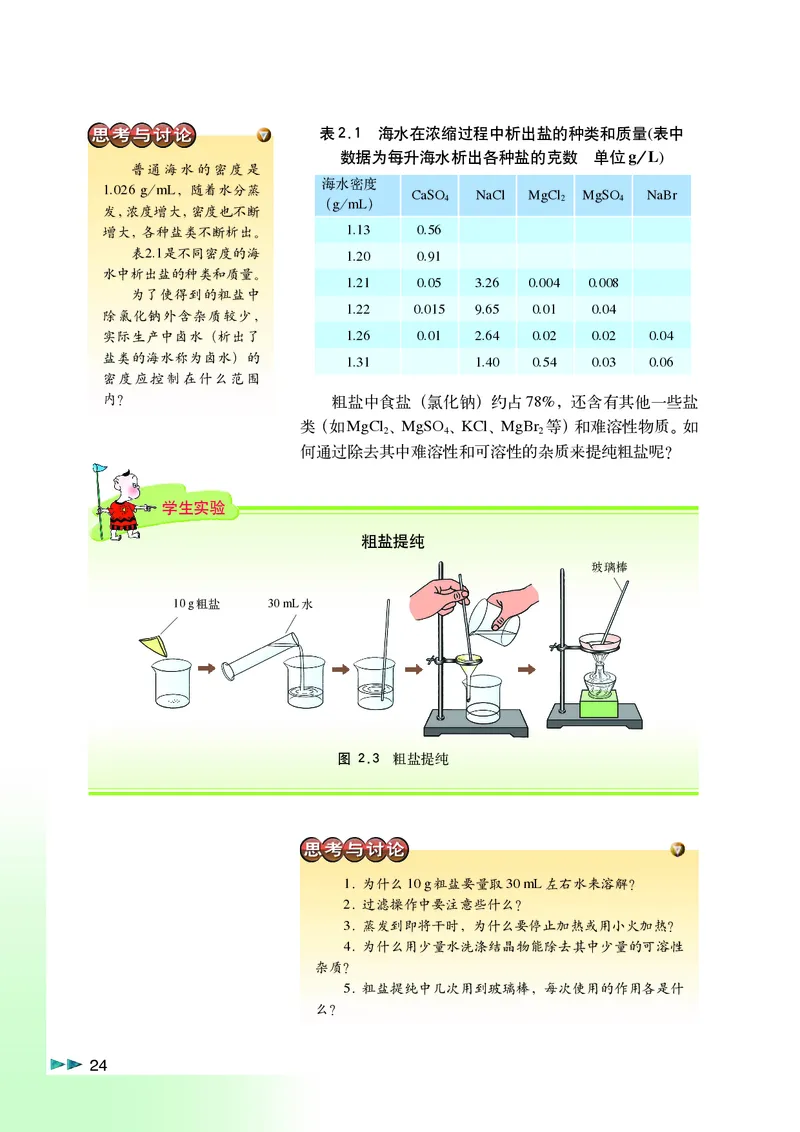
第2章.p65 Page 23 2011.4.7, 3:57 AM Adobe PageMaker 6.5C/PPC表2.1 海水在浓缩过程中析出盐的种类和质量(表中
数据为每升海水析出各种盐的克数 单位g/////L)
普通海水的密度是
海水密度
1.026 g/mL,随着水分蒸
CaSO NaCl MgCl MgSO NaBr
(g/mL) 4 2 4
发,浓度增大,密度也不断
增大,各种盐类不断析出。 1.13 0.56
表2.1是不同密度的海
1.20 0.91
水中析出盐的种类和质量。
1.21 0.05 3.26 0.004 0.008
为了使得到的粗盐中
1.22 0.015 9.65 0.01 0.04
除氯化钠外含杂质较少,
实际生产中卤水(析出了 1.26 0.01 2.64 0.02 0.02 0.04
盐类的海水称为卤水)的
1.31 1.40 0.54 0.03 0.06
密度应控制在什么范围
内? 粗盐中食盐(氯化钠)约占78%,还含有其他一些盐
类(如MgCl 、MgSO 、KCl、MgBr 等)和难溶性物质。如
2 4 2
何通过除去其中难溶性和可溶性的杂质来提纯粗盐呢?
学生实验
粗盐提纯
玻璃棒
10 g粗盐 30 mL水
图 2.3 粗盐提纯
1.为什么10 g粗盐要量取30 mL左右水来溶解?
2.过滤操作中要注意些什么?
3.蒸发到即将干时,为什么要停止加热或用小火加热?
4.为什么用少量水洗涤结晶物能除去其中少量的可溶性
杂质?
5.粗盐提纯中几次用到玻璃棒,每次使用的作用各是什
么?
24
第2章.p65 Page 24 2011.4.7, 3:57 AM Adobe PageMaker 6.5C/PPC【资料库】
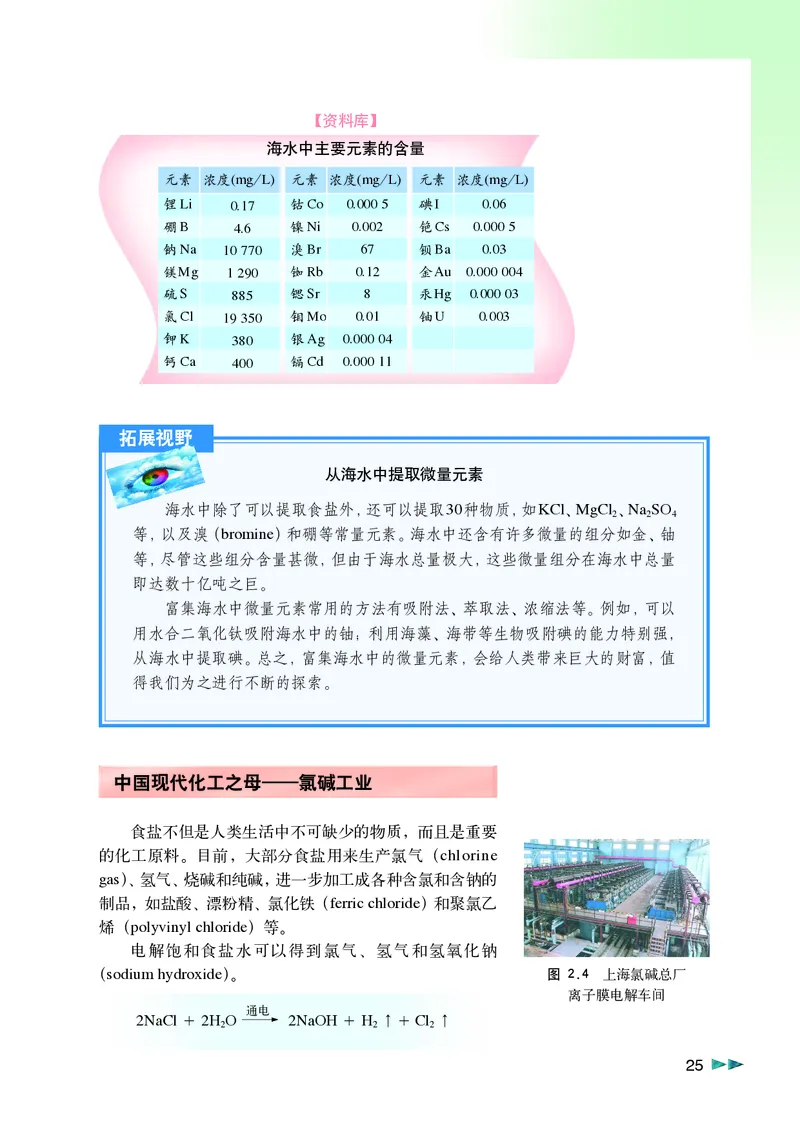
海水中主要元素的含量
元素 浓度(mg/L) 元素 浓度(mg/L) 元素 浓度(mg/L)
锂Li 0.17 钴Co 0.000 5 碘I 0.06
硼B 4.6 镍Ni 0.002 铯Cs 0.000 5
钠Na 10 770 溴Br 67 钡Ba 0.03
镁Mg 1 290 铷Rb 0.12 金Au 0.000 004
硫S 885 锶Sr 8 汞Hg 0.000 03
氯Cl 19 350 钼Mo 0.01 铀U 0.003
钾K 380 银Ag 0.000 04
钙Ca 400 镉Cd 0.000 11
拓展视野
从海水中提取微量元素
海水中除了可以提取食盐外,还可以提取30种物质,如KCl、MgCl 、Na SO
2 2 4
等,以及溴(bromine)和硼等常量元素。海水中还含有许多微量的组分如金、铀
等,尽管这些组分含量甚微,但由于海水总量极大,这些微量组分在海水中总量
即达数十亿吨之巨。
富集海水中微量元素常用的方法有吸附法、萃取法、浓缩法等。例如,可以
用水合二氧化钛吸附海水中的铀;利用海藻、海带等生物吸附碘的能力特别强,
从海水中提取碘。总之,富集海水中的微量元素,会给人类带来巨大的财富,值
得我们为之进行不断的探索。
中国现代化工之母——氯碱工业
食盐不但是人类生活中不可缺少的物质,而且是重要
的化工原料。目前,大部分食盐用来生产氯气(chlorine
gas)、氢气、烧碱和纯碱,进一步加工成各种含氯和含钠的
制品,如盐酸、漂粉精、氯化铁(ferric chloride)和聚氯乙
烯(polyvinyl chloride)等。
电解饱和食盐水可以得到氯气、氢气和氢氧化钠
(sodium hydroxide)。 图 2.4 上海氯碱总厂
离子膜电解车间
通电
2NaCl + 2H O 2NaOH + H ↑+Cl ↑
2 2 2
25
第2章.p65 Page 25 2011.4.7, 3:57 AM Adobe PageMaker 6.5C/PPC课堂实验
电解饱和食盐水
如图2.5所示,在电化学实验平台里加入提纯后的饱和食盐水,在两边的集
气管中各加入几滴酚酞(phenolphthalein)试液,接通直流电源。
请观察阴极(铁棒)、阳极(炭棒)和溶液中产生的现象,并记录。
请分别抽取集气管中气体继续以下实验:
1.用湿润的淀粉碘化钾试纸检验阳极生成的气体。
2. 抽取阴极生成的气体,作点燃试验。
阳极 阴极
饱和食盐水
图 2.5 电解饱和食盐水
化学史话
近代著名实业家——吴蕴初先生
我国近代著名的实业家吴蕴初先生于1923年创办天厨味精厂,因此,吴蕴
初先生有“味精大王”之美称。为了振兴民族工业,吴蕴初先生于1929年在上
海创建天原电化厂(后改名为天原化工厂)。中国最早的氯碱企业从此矗立在苏
州河畔。
此外,吴蕴初先生还创办了天盛陶瓷厂、天利氮气厂、天诚玻璃厂等,为振
兴民族工业作出了很大的贡献。
现在,天原化工厂主要生产烧碱、聚氯乙烯树脂、液氯、漂粉精、盐酸等18
个产品,广泛用于纺织、造纸、化纤、塑料、医药、建筑等行业。
26
第2章.p65 Page 26 2011.4.7, 3:57 AM Adobe PageMaker 6.5C/PPC重要的化工基本原料——盐酸和烧碱
电解食盐水可以得到烧碱溶液;将另两种产物氯气和
氢气化合,生成氯化氢(hydrogen chloride),溶于水后得到
盐酸。烧碱和盐酸都是重要的化工原料。 【资料库】
电离方程式
→HCl
电离方程式
散热铁片 (ionization equation)
是表示电解质如酸、
碱、盐在溶液中或
视孔 视孔 受热熔化时电离成
自由移动离子的式
H2→ 合成塔里的燃烧器
Cl2→ 子。在电离方程式
图 2.6 氯化氢合成塔
中,阳离子带的正
电荷总数和阴离子
带的负电荷总数的
盐酸(hydrochloric acid)是易挥发的一元强酸,在盐
绝对值相等。
酸中氯化氢全部电离成氢离子和氯离子。
NaOH Na++OH-
H SO 2H++SO2-
2 4 4
HCl H+ + Cl-
课堂实验
氯化氢的物理性质
1.观察一瓶氯化氢气体的颜色和状态。
2.打开集气瓶上玻璃盖,小心嗅闻它的气味,并观察瓶口有什么现象发
生。
记录:_____________________________
__________________________________
___________________。
3.用一条湿润的蓝色石蕊(litmus)试纸接近瓶口,观察现象。
记录:_____________________________
__________________________________
___________________。
27
第2章.p65 Page 27 2011.4.7, 3:57 AM Adobe PageMaker 6.5C/PPC4.如图2.7所示,在圆底烧瓶中充满氯化氢气体,挤压预先吸有水的胶头
滴管,使水射入烧瓶中,观察现象,并进行解释。
________________________________
______________________________。
【资料库】
氯化氢在水里的溶解度
t (℃) V(HCl)*
0 507
10 471
20 442
30 412
40 386
*V(HCl)是总压强为101 kPa时溶
于1体积水中的氯化氢的体积数。
图 2.7 氯化氢的溶解性
探究与实践
实验室制氯化氢气体
在实验室通常用加热食盐和浓硫酸的方法来制取氯化氢气体。
微热
NaCl + H SO(浓) NaHSO + HCl↑
2 4 4
初中化学中,我们学习过实验室制取氧气和二氧化碳的方法,请将实验室制
取氯化氢的方法与它们进行比较。
反应物状态 反应条件
实验室制O
2
实验室制CO
2
实验室制HCl
28
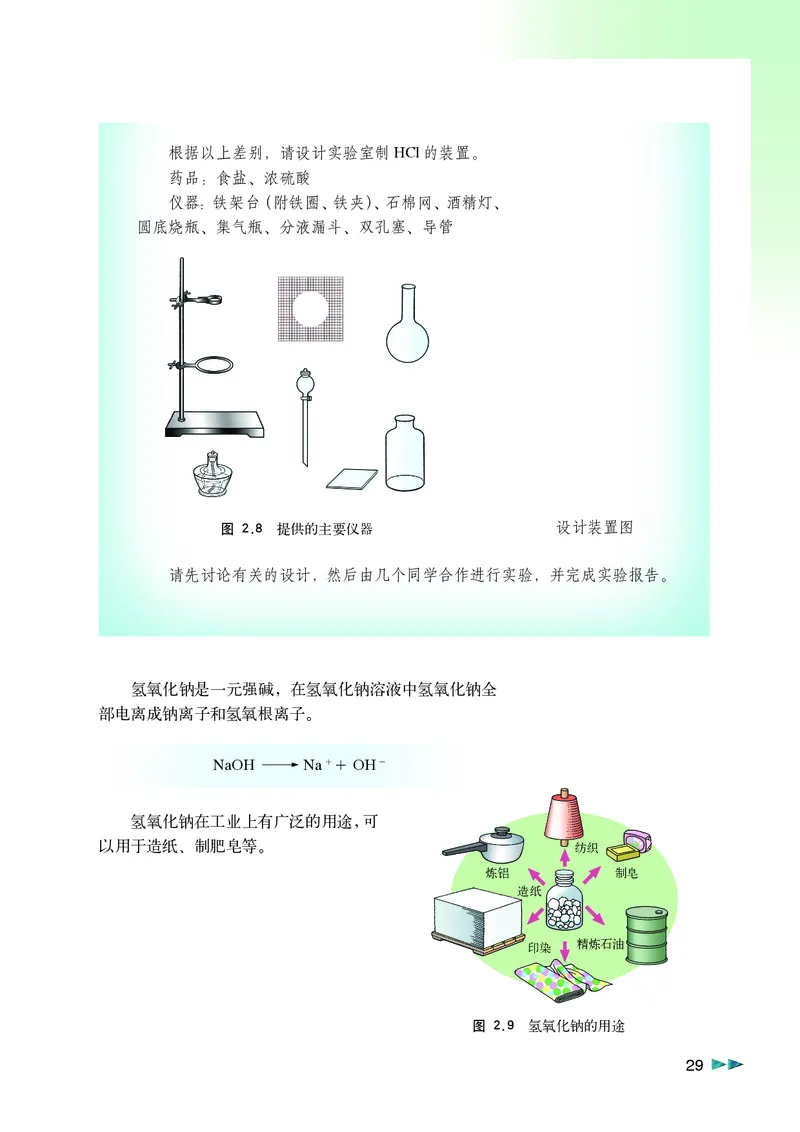
第2章.p65 Page 28 2011.4.7, 3:57 AM Adobe PageMaker 6.5C/PPC根据以上差别,请设计实验室制HCl的装置。
药品:食盐、浓硫酸
仪器:铁架台(附铁圈、铁夹)、石棉网、酒精灯、
圆底烧瓶、集气瓶、分液漏斗、双孔塞、导管
图 2.8 提供的主要仪器 设计装置图
请先讨论有关的设计,然后由几个同学合作进行实验,并完成实验报告。
氢氧化钠是一元强碱,在氢氧化钠溶液中氢氧化钠全
部电离成钠离子和氢氧根离子。
NaOH Na++ OH-
氢氧化钠在工业上有广泛的用途,可
以用于造纸、制肥皂等。 纺织
炼铝 制皂
造纸
精炼石油
印染
图 2.9 氢氧化钠的用途
29
第2章.p65 Page 29 2011.4.7, 3:57 AM Adobe PageMaker 6.5C/PPC[思考与复习2.1]
1.请你到图书馆或上网收集有关海水资源的资料,完成一个有关的专题报告,如海水
淡化、海水的综合利用、海水“淘”金、海水中的核燃料等。
2.在提纯粗盐时,通常在溶液中依次加入BaCl 、NaOH和Na CO ,以除去SO2-
2 2 3 4
(Na SO )、Mg2+(MgCl)和Ca2+(CaCl ),写出有关反应的化学方程式。
2 4 2 2
3.如果要将实验室制得的氯化氢用水吸收制得盐酸,请设计有关的实验装置(注意HCl
气体在水中的溶解性)。
4.分析电解饱和食盐水反应中各元素化合价的变化情况。
5.以盐酸和烧碱为例,归纳整理酸和碱有哪些通性。
6.现有无标签的MgSO、NaCl、NaOH和HCl四瓶无色溶液,而实验桌上只有一瓶酚
4
酞试液,请设计鉴别上述溶液的实验方案。
7.查找有关胃液中盐酸及有关消化的资料,写一篇题为“人体里的盐酸”的短文。
30
第2章.p65 Page 30 2011.4.7, 3:57 AM Adobe PageMaker 6.5C/PPC海水中的氯
2
.2
(CHLORINE IN SEAWATER)
海水中除了氢、氧元素之外,含量最多的就是氯元素,
海水中的氯元素主要以氯化钠形式存在,工业上电解饱和
食盐水可以得到氯气。
氯气性质的研究
我们知道,自来水生产过程中常用氯气来消毒杀菌。氯
气又是一种有毒的气体,在第一次世界大战期间,德军曾向
英法联军施放氯气,造成伤亡达2万人之多。某化工厂曾因
氯气泄漏而造成环境污染和人员中毒事件。你想知道氯气是
怎样一种气体吗?让我们通过实验和观察来逐步认识它。
课堂实验
氯气的性质
实验1:观察氯气的颜色和状态。
记录:_____________________________。
实验2:试验氯气在水中的溶解性。
常温下1 体积水中可以溶解氯
氯气 氯气 氯气
气的体积:__________ 氯水
水
______________。
结论:__________
______________。
图 2.10 氯气的溶解性
31
第2章.p65 Page 31 2011.4.7, 3:57 AM Adobe PageMaker 6.5C/PPC实验3:铁丝在氯气中的燃烧。
把细铁丝绕成螺旋状,一端系在一
根粗铁丝上,另一端系上一段火柴梗。点
燃火柴,待火柴即将燃尽立即把细铁丝伸
氯气
入盛有氯气的集气瓶里。
铁丝
可以看到:___________
_______________。
结论:_____________ 图 2.11 铁丝在氯气中燃烧
_______________。
点燃
2Fe+3Cl 2FeCl
2 3
氢气
实验4:氢气在氯气中燃烧。
点燃从导管中逸出的氢气,然后
氯气
把导管伸入满盛氯气的瓶里。
可以看到:_________
_______________。
图 2.12 氢气在氯气中燃烧
点燃
H +Cl 2HCl
2 2
氯化钠和次氯
酸钠混合液
氯气
实验5:氯气跟氢氧化钠溶液的反
应。
用100 mL针筒抽取50 mL氯气,然
后再抽取10 mL 15%的氢氧化钠溶液,
振荡。
可以看到:__________
氢氧化钠溶液
_______________。
实验现象说明:________ 图 2.13 氯气跟氢氧化钠的反应
_______________。
工业上用氯气和消石灰作原料来制
Cl + 2NaOH NaCl + NaClO + H O
2 2
造漂粉精,其反应跟上述反应很类似, 次氯酸钠
试写出有关反应的化学方程式:___ (sodium hypochlorite)
________________。
32
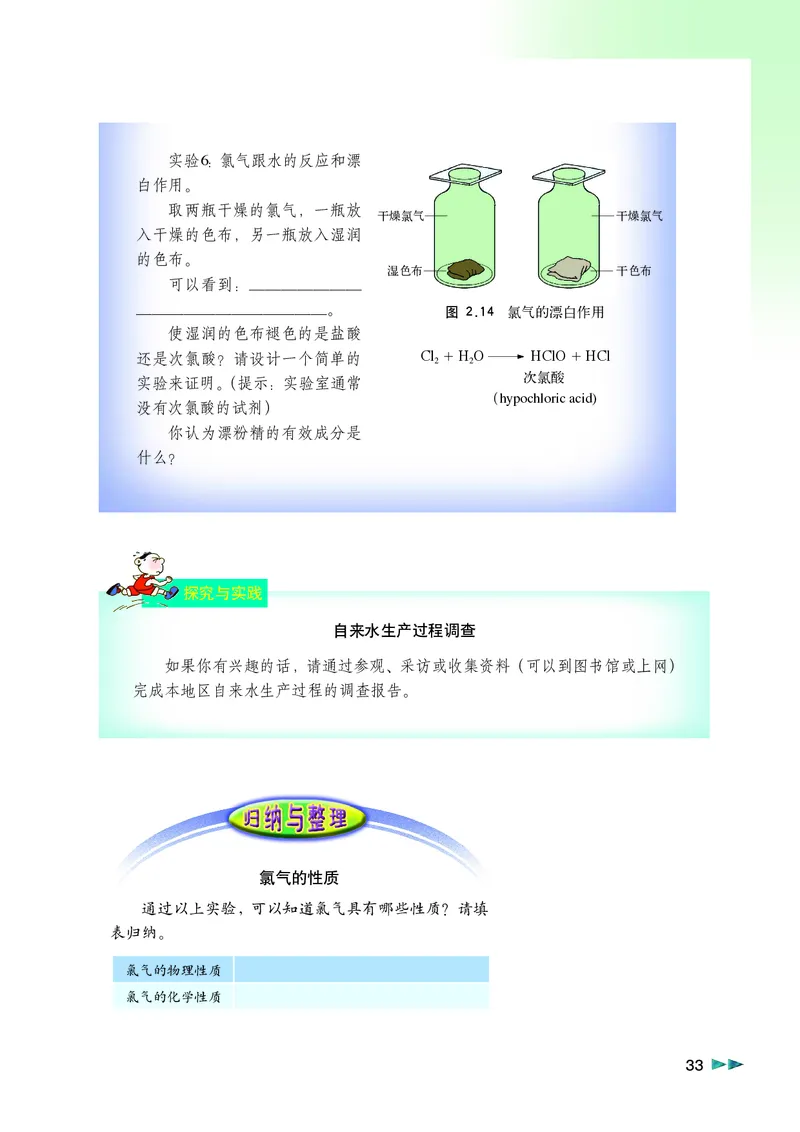
第2章.p65 Page 32 2011.4.7, 3:57 AM Adobe PageMaker 6.5C/PPC实验6:氯气跟水的反应和漂
白作用。
取两瓶干燥的氯气,一瓶放
干燥氯气 干燥氯气
入干燥的色布,另一瓶放入湿润
的色布。
湿色布 干色布
可以看到:_______
____________。 图 2.14 氯气的漂白作用
使湿润的色布褪色的是盐酸
还是次氯酸?请设计一个简单的 Cl +H O HClO+HCl
2 2
次氯酸
实验来证明。(提示:实验室通常
(hypochloric acid)
没有次氯酸的试剂)
你认为漂粉精的有效成分是
什么?
探究与实践
自来水生产过程调查
如果你有兴趣的话,请通过参观、采访或收集资料(可以到图书馆或上网)
完成本地区自来水生产过程的调查报告。
氯气的性质
通过以上实验,可以知道氯气具有哪些性质?请填
表归纳。
氯气的物理性质
氯气的化学性质
33
第2章.p65 Page 33 2011.4.7, 3:57 AM Adobe PageMaker 6.5C/PPC漂粉精和水的消毒
从氯气性质的研究中,我们知道电解食盐水得到的氯
气可以用来制得聚氯乙烯、塑料、盐酸等多种含氯产品,还
可以用来制漂粉精和消毒水。
聚氯乙烯
漂粉精 盐酸
氯气
医药 氯仿
图 2.15 氯气的用途
次氯酸(HClO)能使许多有机色质褪色,还能杀灭水
为什么工业上通常用 中的细菌。生产自来水时可用液氯来消毒杀菌,但氯气的
消石灰跟氯气反应制消毒
贮存、运输都不方便。人们发现次氯酸盐溶于水中,并吸收
剂,而不用烧碱跟氯气反
空气中的二氧化碳也能生成次氯酸,因此就用氯气跟熟石
应呢?
灰或烧碱反应,生产次氯酸盐作消毒剂和漂白剂。工业上
用氯气和消石灰作原料来制造漂粉精。
【资料库】
水的其他消毒方法
2Cl +2Ca(OH) CaCl +Ca(ClO) +2H O
2 2 2 2 2
除了用氯气和
漂粉精的有效成分是次氯酸钙,同时还含有少量的氯
漂粉精消毒外,还
可以用臭氧和二氧 化钙等杂质。次氯酸钙在酸性溶液中,生成具有消毒作用
化氯等作消毒剂。 的次氯酸。
臭氧很不稳
定,容易分解。
Ca(ClO) +2HCl CaCl +2HClO
2 2
O O +[O]
3 2
[O]表示游离
Ca(ClO) +2CO +2H O Ca(HCO ) +2HClO
氧原子,具有很强 2 2 2 3 2
的杀菌作用。
另外,用物理
的方法,如紫外线、
超声波、加热等方
法,也可以消毒水。
34
第2章.p65 Page 34 2011.4.7, 3:57 AM Adobe PageMaker 6.5C/PPC次氯酸钙
N.WT.40kg
中国上海
图 2.16 游泳池中的水用漂粉精来消毒
拓展视野
一些重要的卤化物
我们知道,海水中除含有大量的氯化钠外,还含有较多的氯化镁和氯化钾。
一些重要的盐在生活、生产中都有广泛的用途。
氯化钾是白色固体,易溶于水,可用作钾肥。
氯化铁可作净水剂,热的氯化铁可以跟金属铜反应,生成氯化铜和氯化亚
铁,所以它常用作制印刷电路板的腐蚀剂。
2FeCl +Cu 2FeCl +CuCl
3 2 2
溴化银是既不溶于水又不溶于酸的难溶性盐,见光易分解,常用于制作印相
纸。照相暗房里的废定影液中含有大量的银离子,可以加入氯离子(如氯化钠溶
液),使银离子变成氯化银沉淀进行回收。
光
2AgBr 2Ag+Br ↑
2
Ag+ + Cl- AgCl↓
35
第2章.p65 Page 35 2011.4.7, 3:57 AM Adobe PageMaker 6.5C/PPC探究与实践
自制褪色灵
褪色灵有很多配方,现介绍用漂白粉为主要成分的两种配制方法。这两种自
制褪色灵可以用来褪去蓝黑墨水写的字迹(不能褪黑墨水字迹)。
配制方法一:
使用方法:褪字迹时,
玻璃棒 先用毛笔蘸取少量漂白粉
60 mL水 40 mL水 清液(A)涂于字上,片刻字
迹逐渐消褪,但有时留有
取上层
20 g漂白粉 清液 10 g草酸 黄色斑迹,然后用干毛笔
或吸水纸将上述余液吸干,
(A) (B) 再用少量草酸溶液(B)涂
于斑迹处,可将字迹消去。
配制方法二:
1份漂白粉 使用方法:褪字迹时,
2份碳酸钠
用毛笔蘸取少量配制溶液
0.5份硼酸
10份水 涂于字上即可。该褪色灵
对衣服上的墨水迹,褪色
效果较好。
图 2.17 自制褪色灵
探究气体体积的规律
氯气在通常情况下贮存和运输都不方便,因此常将它
压缩成液氯装在绿色钢瓶中。气态物质的体积大小与哪些
因素有关,是否存在某些规律呢?
物质体积的大小取决于构成这种物质的微粒数目、微
粒大小和微粒之间的距离这三个因素。对于气体来说,分
子间的距离主要跟温度(temperature)和压强(pressure)有
关。当温度升高(压强不变)或压强减小(温度不变)时,
36
第2章.p65 Page 36 2011.4.7, 3:57 AM Adobe PageMaker 6.5C/PPC气体分子之间的距离增大;当温度降低(压强不变)或压强
增大(温度不变)时,气体分子之间的距离缩小。我们通常
为什么标准状况下1 mol
将温度为0℃、压强为101 kPa时的状况称为标准状况。
任何气体的体积会相同?
1 mol不同的气态物质在相同状况下体积是否相同呢? (提示:从前面所述影响气
让我们先来计算一下1 mol氯气在标准状况下的体积。 体体积大小的三个因素进
经测定知道氯气在标准状况下的密度为3.17 g/L,则1 mol 行分析。一般来说,气体分
子直径为0.4 nm,分子间距
氯气在标准状况下的体积为:
为4 nm)
71 g/mol
在标准状况下,如果
≈ 22.4 L/mol
3.17 g/L
是1 mol固体或液体物质是
否有类似的规律呢?
我们先来分析微粒大
思考与练习
小、微粒间距离和体积大
小的关系。
计算1 mol氢气、氧气、二氧化碳在标准状况下的体积。
当微粒间距较小时,
标准状况 1 mol气体标准
气体 摩尔质量 微粒大小对体积大小有明
下的密度 状况下的体积
显的影响;而当微粒间距
H 2 0.089 9 g/L 2.016 g/mol 离变大时,则微粒大小对
O 1.429 g/L 32 g/mol 体积大小的影响变小。当
2
微粒间的距离比微粒直径
CO 1.977 g/L 44 g/mol
2
大得多时,情况会怎样
呢?
大量的科学实验表明,在标准状况下,1 mol任何气体
所占的体积都约为22.4 L。
我们把单位物质的量气体所占的体积叫做气体摩尔体
V
积(molar volume of gas),用符号V 表示。即V =—,常
m m n
在相同的温度和压强
用的单位为L/mol。22.4 L/mol是指标准状况下的气体
下,不同气体分子间平均
摩尔体积,在室温和101 kPa,1 mol任何气体的体积约
距离是相等的,那么相同
为24 L。
体积的不同气体中含有的
分子数是否相等?
思考与练习
1. 在标准状况下,0.05 mol氯气的体积是多少?
2. 计算标准状况下,1 L氯化氢气体的物质的量是多少?
37
第2章.p65 Page 37 2011.4.7, 3:57 AM Adobe PageMaker 6.5C/PPC[思考与复习2.2]
1.完成下列物质间转化的化学方程式,并指出其中哪些反应属于四类基本反应类型。
HCl Cl Ca(ClO)
2 2
HClO NaClO
38
→
—
—→ —
→
→
—→ → —
NaCl FeCl
3
2.某学生做了以下关于氯水的实验:
(1)向氯水中滴入几滴硝酸银溶液。
(2)在蓝色石蕊试纸上滴氯水。请推测实验现象并加以说明。
3.氯气有毒,为什么又可用来消毒?
4.某纺织厂用次氯酸钠在稀盐酸存在下进行布匹的漂白,写出次氯酸钠和稀盐酸反应
的化学方程式。
5.下列说法中正确的是( )。
(A)1 mol任何气体的体积都是22.4 L
(B)1 mol任何物质在标准状况下所占体积都约是22.4 L
(C)1 mol氯气、水、碘(I)在标准状况下所含分子数相等
2
(D)在同温同压下,相同质量的氯气和氢气体积相同
6.分别计算n mol氯气的质量、标准状况下的体积和所包含的分子数。想一想,能否
计算标准状况下,一定体积(V L)的氯气的质量和所包含的分子数。
7.在相同状况(同温同压)下,相同体积的任何气体里有相同数目的分子,这称为阿
伏加德罗定律。根据以上定律,是否可以认为同温同压下气体的体积之比等于它的物质的量
之比,为什么?
*8.阅读下列短文,写出有关反应的化学方程式。
Chlorine is manufactured by the electrolysis of sodium chloride. It is a greenish-yellow,
poisonous gas with a pungent smell. Chlorine is somewhat soluble in water, forming chlorine water.
Chlorine water contains dissolved chlorine and hydrochloric and hypochlorie acids.
Hypochloric acid is unstable, and can break down into hydrochloric acid and oxygen. So
hypochloric acid is a powerful oxidizing agent.Sodium hypochlorite is made by passing chlorine into
cold sodium hydroxide solution. Bleaching powder is made by the action of chlorine on slaked lime.
The hypochlorites and hypochlorous acid are excellent bleaching agents.
第2章.p65 Page 38 2011.4.7, 3:57 AM Adobe PageMaker 6.5C/PPC2 从海水中提取溴和碘
.3
(EXTRACT BROMINE AND IODINE FROM SEAWATER)
虽然在海水中几乎存在所有的常见元素,但除了氯和
钠之外,大多数元素的浓度很低,提取的成本或技术要求
很高。目前,从海水中提取的两类物质已形成产业。一类是
海水中含量较高,提取比较容易,而且成本也不很高的物
质,如镁(magnesium)和钾(potassium)等;另一类是陆
上含量极少,只能从海水中提取的物质,如溴和碘(iodine)
等。
从海水中提取的元素——溴和碘
汽油中
占地球上储量99%的溴分布在海洋中,从海水中提取 镇静剂 的防燥剂
溴,一般要经过浓缩、氧化和提取三个步骤。
溴钨灯 红药水
溴在海水中的浓度很低,必须先进行浓缩。我国目前
溴
是从食盐化工的尾料中提取溴。要将海水中的溴离子氧化
相纸 抗生素
成单质溴,常用的氧化剂是氯气。
胶卷 杀虫剂
Cl + 2Br- 2Cl-+Br
2 2 图 2.18 溴的主要用途
这时生成的单质溴仍然溶解在海水中,怎样才能把溴
提取出来呢?根据溴的沸点比水低的性质,可以鼓入热空
气或水蒸气,使它和水蒸气一起挥发出来,冷凝后得到粗
溴,再将粗溴精制就可以得到高纯度的溴了。目前,我国
溴的年产量仅数千吨,远不能满足需求,因此大力开展海
水提溴的研究和开发具有广阔的前景。
溴是深红棕色、密度比水大的液体,很容易挥发,具
有强烈的腐蚀性,所以把溴存放在试剂瓶里时应密闭保存,
同时需要在瓶中加一些水,以减少挥发。
碘是紫黑色固体,几乎不溶于水,但能溶于酒精,形
39
第2章.p65 Page 39 2011.4.7, 3:57 AM Adobe PageMaker 6.5C/PPC成碘酊(碘酒)。碘加热时,不经熔化就直接变成紫色蒸气,
蒸气遇冷,重新凝聚成固体。这种固体物质不经液态而直
接变成气态的现象,叫做升华。碘的另一个特性就是能使
淀粉(starch)溶液变蓝色。
溴、碘在有机溶剂中的溶解度比它们在水中的溶解度
大得多。利用这一性质,我们可以用有机溶剂把溴或碘从
水溶液中提取出来。
利用溶质在互不相溶的溶剂里溶解度不同的性质,用
一种溶剂把溶质从它与另一种溶剂所组成的溶液里提取出
图 2.19 碘的升华
来的方法,叫做萃取。在生产和科学研究上、萃取是一种常
用的分离物质的方法。
学生实验
从海带中提取碘
海带具有从海水中富集碘的能力,灼烧干的海带能使其中的有机物烧成二氧
化碳和水,留下无机物,同时使碘的有机化合物变成无机的碘化物,最后用氯水
将其氧化成单质碘。试设计从海带中提取碘的实验,并加以检验。
探究与实践
化 学 密 信
1935年,当时在狱中的方志敏同志避开狱警的严密监视,用米汤(其主要成
分是淀粉溶液)在白纸上写下密信,通过地下工作的同志送给鲁迅先生。鲁迅先
生在干净的碗里盛上一碗清水,在清水里滴入少量碘酒,然后将上述白纸浸入碘
水中,马上呈现出蓝色的字迹。请你在家里用同样的方法来完成以上实验。
40
第2章.p65 Page 40 2011.4.7, 3:57 AM Adobe PageMaker 6.5C/PPC化学史话
无意的发现和不懈的追求
氯在自然界中以化合态存在。单质氯是由瑞典化
学家舍勒(Karl Wilhelm Scheele,1742 — 1786)首先
发现并制得的。在1773年的某一天,他在研究软锰矿
(MnO )时,将这种矿石与盐酸放在曲颈甑中,并将曲
2
颈甑放置在沙浴上加热,甑颈处所冒出的气泡里很快
充满了一种黄绿色的气体。这种气体具有刺激性气味,
吸入后使肺部极为难受。
1810年,有人证明了这种气体是由一种化学元素
构成,并定名为氯(chlorine)。
图 2.20 舍勒
过了100多年,到19世纪80年代,天然存在的化
学元素大部分已经被发现,并且获得了游离态的元素,但氟是一个例外。许多科
学家都为此努力过,但都没有成功。爱尔兰的R·诺克斯还为此献出了宝贵的生
命。
法国化学家莫瓦桑(H.Moissan,1852—1907)从他的导师弗雷密手中接过这
未完成的实验,通过几年的不懈努力,终于在1886年通过低温(-25℃)电解氟
化钾的氢氟酸溶液获得了游离态的氟,并进而研究了这个极为活泼的游离态氟的
性质,解决了前人70多年没有解决的难题,从而在1906年荣获诺贝尔化学奖。
莫瓦桑谦虚地说:“我是踏着先驱失败的台阶而登上成功的顶点的。”
人类的历史就是在不断实践的基础上有所发现和不断前进的。科学家不畏艰
险努力进取的精神,激励着我们每一个人去努力实践探索,不断创新。
拓展视野
卤素的应用
在希腊文中卤素原意是成盐元素。
因为氯、溴、碘的单质都是典型的非金
属,都能跟典型的金属化合生成盐而
得名。在生活中卤素有着广泛的应用。
例如,含氟牙膏、胶卷、碘钨灯、聚四
氟乙烯涂层、生理盐水、含碘食品等。
图 2.21 卤素的用途
41
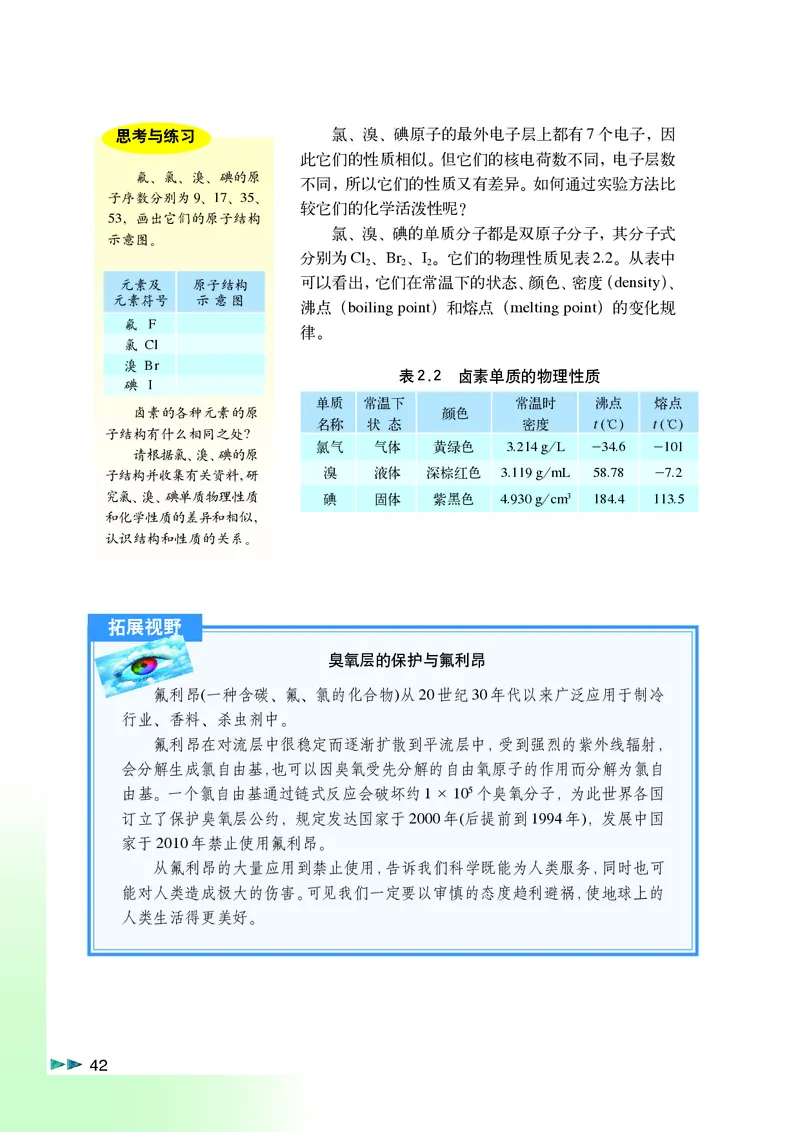
第2章.p65 Page 41 2011.4.7, 3:57 AM Adobe PageMaker 6.5C/PPC思考与练习 氯、溴、碘原子的最外电子层上都有7个电子,因
此它们的性质相似。但它们的核电荷数不同,电子层数
氟、氯、溴、碘的原
不同,所以它们的性质又有差异。如何通过实验方法比
子序数分别为9、17、35、
较它们的化学活泼性呢?
53,画出它们的原子结构
氯、溴、碘的单质分子都是双原子分子,其分子式
示意图。
分别为Cl 、Br 、I 。它们的物理性质见表2.2。从表中
2 2 2
元素及 原子结构 可以看出,它们在常温下的状态、颜色、密度(density)、
元素符号 示 意 图
沸点(boiling point)和熔点(melting point)的变化规
氟 F
律。
氯 Cl
溴 Br
表2.2 卤素单质的物理性质
碘 I
单质 常温下 常温时 沸点 熔点
卤素的各种元素的原 颜色
名称 状 态 密度 t (℃) t (℃)
子结构有什么相同之处?
氯气 气体 黄绿色 3.214 g/L -34.6 -101
请根据氯、溴、碘的原
子结构并收集有关资料,研 溴 液体 深棕红色 3.119 g/mL 58.78 -7.2
究氯、溴、碘单质物理性质 碘 固体 紫黑色 4.930 g/cm3 184.4 113.5
和化学性质的差异和相似,
认识结构和性质的关系。
拓展视野
臭氧层的保护与氟利昂
氟利昂(一种含碳、氟、氯的化合物)从20世纪30年代以来广泛应用于制冷
行业、香料、杀虫剂中。
氟利昂在对流层中很稳定而逐渐扩散到平流层中,受到强烈的紫外线辐射,
会分解生成氯自由基,也可以因臭氧受先分解的自由氧原子的作用而分解为氯自
由基。一个氯自由基通过链式反应会破坏约1×105个臭氧分子,为此世界各国
订立了保护臭氧层公约,规定发达国家于2000年(后提前到1994年),发展中国
家于2010年禁止使用氟利昂。
从氟利昂的大量应用到禁止使用,告诉我们科学既能为人类服务,同时也可
能对人类造成极大的伤害。可见我们一定要以审慎的态度趋利避祸,使地球上的
人类生活得更美好。
42
第2章.p65 Page 42 2011.4.7, 3:57 AM Adobe PageMaker 6.5C/PPC探究与实践
比较氯、溴、碘的化学活泼性
要比较物质的化学活泼性有哪些基本方法?在初中化学中我们根据金属的活
动性可以判断相关的置换反应能否发生,所以我们也可以通过一种元素的单质能
否把另一种元素从它的化合物中置换出来,推断它们的化学活泼性。
现有氯水、溴水、碘水、氯化钠溶液、溴化钠溶液、碘化钾溶液和四氯化碳,
根据实验1,再设计其他实验。
同样,我们还可以通过在相同的条件下,氯、溴、碘的单质跟某些物质能否
反应、反应的条件、吸收或放出热量的大小,以及生成物的热稳定性等,来判断
卤素活泼性的递变规律。根据氯、溴、碘单质跟氢气化合的化学方程式,分析化
学反应的情况,也可以得出它们的活泼性顺序。
实验序号 实 验 过 程 实验现象以及发生反应的化学方程式
2 mL新制氯水 1 mL四氯化碳
1
振荡 振荡
2 mLNaBr溶液
2
43
第2章.p65 Page 43 2011.4.7, 3:57 AM Adobe PageMaker 6.5C/PPC(续表)
实验序号 实 验 过 程 实验现象以及发生反应的化学方程式
3
4
5
结论
思考与练习
【资料库】
请寻找其他有关资
料,如氯、溴、碘单质跟
氯、溴、碘的单质跟氢气的化合
水反应的情况进行比较
分析。 H (g) + Cl (g) 2HCl(g) +92.3 kJ
2 2
点燃或光照条件下剧烈化合,放出大量的热,并
【资料库】
发生爆炸。
溴和碘在不同情况下的 500℃
H (g)+Br (g) 2HBr(g) +36.4 kJ
2 2
颜色 在500℃才能缓慢反应。
饱和溴水 橙色
△
H (g)+I (g) 2HI(g) - 26.5 kJ
2 2
稀溴水 黄色
在不断加热条件下才能缓慢反应,且生成的HI不
溴在苯、四氯化
稳定,同时发生分解。
红棕色
碳等有机溶剂中
黄色到
碘的水溶液
浅棕色
碘的酒精溶液 棕色
碘的四氯化碳溶液 紫色
碘的苯溶液 紫红色
44
第2章.p65 Page 44 2011.4.7, 3:57 AM Adobe PageMaker 6.5C/PPC化合价升高,被氧化
→
2Fe + 3Cl 2FeCl
2 3
45
→
在初中化学里,我们曾学过从不同的角度对化学反应
进行分类。例如,根据反应物和生成物的类别以及反应前
后物质种类的多少,把化学反应分为化合反应、分解反应、
置换反应和复分解反应四种基本类型的反应。但这种分类
方法不能包括所有的化学反应(如前面讲述的电解食盐
水)。
我们还从得氧和失氧的角度学习了氧化还原反应
(redox reaction)。
现在,让我们从元素的化合价入手,进一步探究元素
化合价的升降与氧化还原反应的关系。
化合价升高,被氧化
得到氧,被氧化 →
→ +2 0 0 +1
△ △
CuO + H Cu+H O CuO +H Cu + H O
2 2 2 2
物质所含元素化合价升高的反应是氧化反应(oxidation
reaction),物质所含元素化合价降低的反应是还原反应
(reduction reaction),有元素化合价升降的化学反应是氧化
还原反应。
0 0 + 3-1
化合价降低,被还原
→
失去氧,被还原
→
进一步认识氧化还原反应
四种基本类型的反应
反应类型 表达式
化合反应 A+B—→AB
分解反应 AB—→A+B
置换反应 A+BC—→AC+B
复分解反应 AB+CD—→AD+CB
化合价降低,被还原
点燃
虽然上述反应中没有得氧和失氧,但元素的化合价发
生升降。铁的化合价升高,发生了氧化反应;氯的化合价降
低,发生了还原反应。可见氧化还原反应的概念扩大了。在
反应中,铁是还原剂(reducing agent),氯气是氧化剂
(oxidizing agent)。
第2章.p65 Page 45 2011.4.7, 3:57 AM Adobe PageMaker 6.5C/PPC思考与练习
请用化合价升降来分析下列反应:
2Na +Br 2NaBr
2
Cl +H O HCl + HClO
2 2
通直流电
2NaCl + 2H O 2NaOH+H ↑+Cl ↑
2 2 2
我们知道,元素化合价的升降与电子得失(或偏移)有
密切的关系。例如:
Na - e Na+
Cl + 2e 2Cl-
2
失去2e
→
点燃
2Na+Cl 2NaCl
2
也可以用箭头表示反应物中不同元素间电子转移的情况。
在氧化还原反应里,有元素失去电子,必然有元素同时
得到电子,而且失去电子的总数必定等于得到电子的总数。
因此,从本质上来看,有电子转移的反应都属于氧化
还原反应;而没有电子转移的反应,则属于非氧化还原反
应。失去电子的物质称为还原剂,元素的原子失去电子(化
46
→
得到2e
2e
→
点燃
2Na + Cl 2NaCl
2
化合价降低 得电子
被还原
化合价升高 被氧化
失电子
图 2.22 氧化还原反应中元素电子得失和化合价变化关系图
第2章.p65 Page 46 2011.4.7, 3:57 AM Adobe PageMaker 6.5C/PPC合价升高)的反应是氧化反应;得到电子的物质称为氧化
剂,元素的原子得到电子(化合价降低)的反应是还原反应。
怎样检验Cl-、Br-、I-
硝酸银(silver nitrate)溶液中的Ag+与自来水中含有
的Cl-结合, 生成难溶的白色氯化银沉淀。
用什么化学方法来检
验一瓶水是蒸馏水还是自
Ag++Cl- AgCl↓
来水?
这种用实际参加反应的离子符号来表示离子反应的式
子,称为离子方程式,它更能体现反应的实质。
课堂实验
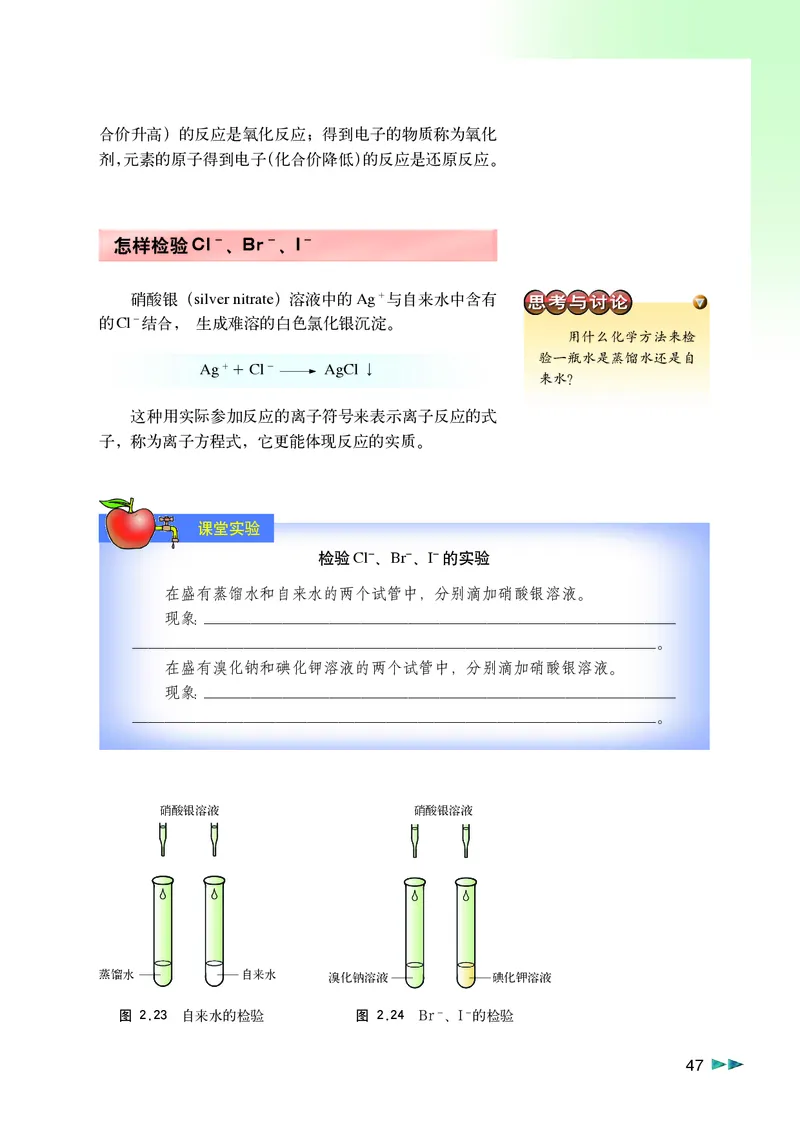
检验Cl-、Br-、I-的实验
在盛有蒸馏水和自来水的两个试管中,分别滴加硝酸银溶液。
现象:______________________________
_________________________________。
在盛有溴化钠和碘化钾溶液的两个试管中,分别滴加硝酸银溶液。
现象:______________________________
_________________________________。
硝酸银溶液 硝酸银溶液
蒸馏水 自来水 溴化钠溶液 碘化钾溶液
图 2.23 自来水的检验 图 2.24 Br-、I-的检验
47
第2章.p65 Page 47 2011.4.7, 3:57 AM Adobe PageMaker 6.5C/PPC反应的化学方程式分别为:
NaBr + AgNO AgBr↓+ NaNO
3 3
淡黄色沉淀
KI + AgNO AgI↓+ KNO
3 3
黄色沉淀
写成离子方程式分别为:
Br-+Ag+ AgBr↓
I-+Ag+ AgI↓
拓展视野
检验Cl-时如何排除CO 2-的干扰
3
如果溶液中有CO2-存在,用AgNO 溶液检验Cl-就会受到干扰:
3 3
CO2-+2Ag+ Ag CO ↓(白色* )
3 2 3
Ag CO 溶于稀硝酸:
2 3
Ag CO +2H+ 2Ag++H O+CO ↑
2 3 2 2
因此,在用AgNO 溶液检验Cl-时,可先在被检验的溶液中滴入少量稀硝
3
酸,将其酸化,以排除CO2-等的干扰。然后再滴入AgNO 溶液,如产生白色沉
3 3
淀,就可判断该溶液中含有Cl-。
*AgCO 固体为浅黄色,只有在水溶液中出现少量沉淀时呈白色。
2 3
氯化银(silver chloride)、溴化银(silver bromide)和碘
化银(silver iodide)都不溶于水,也不溶于酸,加入稀硝
酸,沉淀不溶解,因此可以用硝酸银溶液及稀硝酸来检验
Cl-、Br- 和I- 的存在。
氯化银、溴化银和碘化银的沉淀见光后都会逐渐变黑,
这是由于卤化银在光的作用下,都能分解出银(极微小的
银粒呈黑色)的缘故。利用这个性质,卤化银常用来制摄影
胶卷和感光纸等。常用的变色镜里含有卤化银、少量的氧
化铜和稀土元素。
48
第2章.p65 Page 48 2011.4.7, 3:57 AM Adobe PageMaker 6.5C/PPC有关化学反应的计算
我们知道,物质是由原子、分子或离子等微粒组成,物
质之间的化学反应是按一定的数量关系进行的。化学方程式
可以明确表示出这些微粒之间的数量关系。例如:
Mg+2HCl MgCl +H ↑
2 2
在化学方程式中,化学式前的化学计量数之比,也就
是反应物和生成物之间的物质的量之比。因此,将物质的
量、摩尔质量、气体摩尔体积等概念应用于化学方程式进
行计算时,对于定量研究化学反应中各物质之间的量的关
系,会更加方便。
[例题1] 在实验室里用0.12 g镁带和足量的盐酸反
应,能生成氢气多少毫升(标准状况下)?
解:0.12 g镁带的物质的量:
0.12 g
n(Mg)=—————=0.005 mol
24 g/mol
Mg+2HCl MgCl +H ↑
2 2
根据化学方程式可知生成氢气的物质的量等于镁的物
质的量。
在标准状况下,生成氢气的体积:
V(H )=0.005 mol×22.4 L/mol
2
=0.112 L=112 mL
答:0.12 g镁带和足量的盐酸反应,能生成氢气112 mL
(标准状况)。
工业上常用氯气和氢气化合的方法来制取氯化氢气体。
氯化氢气体冷却后被水吸收成为盐酸。氯气和氢气反应时,
有毒的氯气被过量的氢气所包围,使氯气充分反应,防止
了对空气的污染(参见图2.6)。在生产上,往往采取使用一
种过量的原料而使有害的或价格较昂贵的原料充分反应。
在实际生产中,这类反应的原料和产品的量应该怎样
计算呢?
[例题2] 某化工厂生产盐酸,每天耗用氯气42.6 t,氢
气1.45 t,问该厂理论上每天最多能生产31%的盐酸多少吨?
49
第2章.p65 Page 49 2011.4.7, 3:57 AM Adobe PageMaker 6.5C/PPC分析:本题已知两种反应物的量,根据化学反应中量
的关系来分析,可能有两种情况。如果两者的量符合反应
比例,则两种反应物都恰好完全反应;如果其中之一超过
了反应需要的量,那么,过量的反应物就不会参加反应。如
何判断哪一种反应物过量了呢?
解:(1) 反应物过量判断
已知消耗氯气:
思考与练习
42.6 t×106 g/t
在启普发生器中放
n (Cl )=————————=6.00×105 mol
2 71 g/mol
入12 g锌粒和11%(ρ =
1.05 g/mL) 30 mL盐酸,
消耗氢气:
理论上最多能产生多少 1.45 t×106 g/t
n (H )=———————=7.25×105 mol
升氢气(标准状况下)? 2 2 g/mol
点燃
H +Cl 2HCl
2 2
根据化学方程式,氢气和氯气完全反应时,物质的量
之比为1∶1。
当氯气完全反应时,需要氢气的量为:
n′(H )=6.00×105 mol×1=6.00×105 mol
2
因为n (H )>n′(H ),所以氢气过量。
2 2
过量的氢气不参加反应,生成物的量必须根据完全参
加反应的氯气的量来进行计算。
(2) 求盐酸的产量
n (HCl)=6.00×105 mol×2=1.20×106 mol
M (HCl)=36.5 g/mol
1.20×106 mol×36.5 g/mol
m (HCl)=—————————————=43.8 t
1×106 g/t
每天能生产31%的盐酸的质量:
m[HCl(aq)]=43.8 t÷0.31=141 t
答:每天生产31%的盐酸141 t。
50
第2章.p65 Page 50 2011.4.7, 3:57 AM Adobe PageMaker 6.5C/PPC[思考与复习2.3]
1.试从原子结构角度,解释为何碘的非金属性比氯、溴弱。
2.甲状腺肿等碘缺乏病是世界上分布最广、发病人数最多的一种地区性疾病。为了防
止碘缺乏病,你认为应采取哪些有效措施?
3.臭氧(O)是一种有点腥味的淡蓝色气体,它具有比氧气更强的氧化性。已知臭氧
3
能使湿润的淀粉碘化钾试纸变蓝,反应中有氧气生成,则反应的化学方程式为
__________________________。反应中的还原剂是_______________。
4.填表:
从得氧失氧 从化合价升降 从电子得失
观点分析 观点分析 观点分析
氧化反应
还原反应
氧化还原反应
氧化剂
还原剂
5.判断下列反应是不是氧化还原反应;是氧化还原反应的,指出氧化剂和还原剂。
(1) NaCl+AgNO AgCl↓+NaNO
3 3
点燃
(2) 2Fe+3Cl 2FeCl
2 3
(3) 2F +2HO 4HF+O
2 2 2
△
(4) 4HCl(浓)+MnO MnCl +2H O+Cl ↑
2 2 2 2
6.试管中的黄色溶液可能是碘水,试用两种方法加以验证。
7.三瓶失去标签的瓶中,分别盛有氯化钠、溴化钠和碘化钠溶液,怎样用两种不同的
实验方法来鉴别,写出有关反应的化学方程式。
8.用铁粉处理废定影液后,得到的银中还含有过量的铁粉。怎样除去过量的铁粉而得
到较纯净的银?
9.1.5 mL密度为1.028 g/cm3的盐酸(质量分数为6%)跟足量的硝酸银溶液起反应,计
算生成氯化银的质量。在实验室,用5.85 g食盐和98%浓硫酸100 g在微热条件下充分反
应,能生成氯化氢气体多少升(标准状况下)?
*10.阅读下列短文,请举例加以说明,写出有关反应的化学方程式。
If we pass through chlorine into a solution of a bromide or an iodide, we find that free bromine
or iodine respectively is liberated and a chloride formed. Bromine will also liberate iodine from the
iodide. They are the replacement reactions. But iodine will liberate neither bromine nor chlorine from
their salts.
51
第2章.p65 Page 51 2011.4.7, 3:57 AM Adobe PageMaker 6.5C/PPC小结与思考
1.海水中各类化学资源。
含量最多的食盐资源
核反应堆燃料铀资源
轻金属镁资源
用途广泛的溴、碘资源
海水化学资源 重要的钾肥资源
多种重金属资源
潜力巨大的重水能源
海洋淡水资源
其他资源
2.氯、溴、碘的原子结构和性质。
(1)氯、溴、碘的原子结构。(根据本章有关内容填空)
元素名称 氯 溴 碘
元素符号
核电荷数
最外层电子数
核外电子层数
原子半径的变化 逐渐增大——————————→
(2)氯、溴、碘的化学性质及其变化规律。
氯、溴、碘的单质都具有较强的氧化性,氯、溴、碘随着其原子半径的增大,氧化性逐
渐减弱。(根据本章有关内容并查找有关资料填空)
化 学 式 Cl Br I
2 2 2
颜色变化
物
状态变化
理
性 密度变化
质
熔、沸点变化
化 与H 反应的情况
2
学
与H O反应的情况
性 2
质 氧化性强弱比较
52
第2章.p65 Page 52 2011.4.7, 3:57 AM Adobe PageMaker 6.5C/PPC3.物质的量与标准状况下气体体积、物质的质量以及对应微粒数之间的关系。
÷M g/mol ×6.02×1023 mol-1
物质的质量(g) 物质的量(mol) 微粒数
×M g/mol ÷6.02×1023 mol-1
÷22.4 L/mol
×22.4 L/mol
气体体积(L,标准状况)
4.氧化还原反应。
氧化反应和还原反应同时发生。氧化剂得电子,元素化合价降低,被还原;还原剂失电
子,元素化合价升高,被氧化。
矛盾对立面的统一:
氧 化 剂 — 还 原 剂
得 电 子 — 失 电 子
还原反应 — 氧化反应
化合价降低 — 化合价升高
5.电离方程式和离子方程式。
电离方程式是用来表示电解质在溶液中(或受热熔化时)电离成自由移动离子的式子。
离子方程式是用实际参加反应的离子符号来表示离子反应的式子。
要注意区别电离方程式和离子方程式。电离方程式表示电解质电离的过程;离子方程
式表示离子反应的过程。
6.思考与复习。
(* 1)请在生活中寻找含氯、溴、碘物质的说明书,进行分类汇总,体会其在社会生活
中的作用。
(2)我国晋朝炼丹术士葛洪所著的《肘后备急》卷五《食肉方》(腐蚀皮肤的药方)中
有一段记载:“取白炭灰、荻灰等分,煎合如膏。此不宜预作,十日即歇。关可去黑子,此
大毒。”其中“白炭灰”是石灰,“荻灰”是草木灰,“煎”即加水后加热。写出有关反应的
化学方程式,并加以说明。
(3)氯气通入水中形成的氯水有以下变化:(“ ”表示在相同条件下,正向和逆向
反应同时进行)
Cl +H O HCl + HClO
2 2
HCl H++ Cl-
HClO H+ + ClO-
HO H++OH-
2
请分析一下新制的氯水中有哪些分子,有哪些离子?
向氯水中滴加硝酸银溶液有什么现象?是氯水中的哪些成分跟硝酸银溶液发生反应?
53
第2章.p65 Page 53 2011.4.7, 3:57 AM Adobe PageMaker 6.5C/PPC将氯水滴在蓝色石蕊试纸上,有什么现象?是氯水中的哪种成分跟石蕊发生作用,起漂
白作用的又是氯水中的哪种成分?
上述氯水的各种反应说明了什么?
(4)利用碘的一些性质,如受热会升华成碘蒸气,碘蒸气能溶解在手指上的油脂等分泌
物中,设计实验使在白纸上现出你的指纹。实验用品:蒸发皿、铁架台(附铁圈)、酒精灯、
碘、白纸。
(5)变色眼镜的变色镜片是特制的。在熔制普通光学玻璃时,加入微量的溴化银及氧化
铜,就能得到能变色的光学玻璃。试猜测和分析溴化银和氧化铜的作用,并查阅有关资料加
以证实。
(6)实验室用浓盐酸跟二氧化锰在加热条件下制取氯气。
△
MnO + 4HCl(浓) MnCl +Cl ↑+ 2H O
2 2 2 2
①指出反应中的氧化剂、还原剂和电子转移的情况。
②实验室制备氯气的装置与下列哪种气体的装置相类似?
(A)O(B)CO(C)HCl
2 2
③多余的氯气用什么来吸收?
④8.7 g二氧化锰和37%浓盐酸100 mL(密度为1.19 g/mL)充分反应,生成的氯气在标
准状况下的体积为多少毫升?
(7)现有氧化铜、炭粉、二氧化锰三种黑色固体试剂,请设计实验把它们一一鉴别出来。
(8)在碘化钾溶液中通入一定量的氯气,然后提取其中的碘。要得到碘0.254 g,问至
少需要通入氯气多少升(标准状况)?
54
第2章.p65 Page 54 2011.4.7, 3:57 AM Adobe PageMaker 6.5C/PPC3
探索原子构建物质的奥秘
EXPLORE THE MYSTERIES OF CHEMICAL
SUBSTANCES BUILT UP BY ATOMS
◆ 原子间的相互作用
◆ 离子键和离子化合物
◆ 共价键和共价分子
55
第3章.p65 Page 55 2011.4.7, 3:58 AM Adobe PageMaker 6.5C/PPC近
几十年来,由于社会的需要和化学的突
飞猛进,人类新发现和合成的物质正
以每年数十万、上百万种的数量急剧增
加,现在人们已经认识到了3 000多万种物质。然而数
量如此庞大的物质,却仅是由百余种元素的原子通过不
同的组合、排列构建而成的。
揭开物质构建的奥秘,了解物质中原子之间的相互
作用,能使我们更清楚地认识、了解物质世界,从而能
够创造出更多更新的物质为人类服务。
在本章中,我们将对原子构建物质的奥秘作初步的
探索。
56
第3章.p65 Page 56 2011.4.7, 3:58 AM Adobe PageMaker 6.5C/PPC原子间的相互作用
3
.1
(INTERACTION BETWEEN ATOMS)
性能各异的物质
我们知道,构成物质世界的元素只有100多种,那么这
100多种元素的原子是怎么构成3 000多万种物质的呢?
碳元素组成的金刚石(diamond)和石墨(graphite)都
是由碳元素组成的,但金刚石十分坚硬,石墨却很柔软。在
常态下二氧化碳是气体,而组成与二氧化碳相近的二氧化
硅,像水晶、砂子等却是坚硬的固体。同是氢原子可以与
氯、氧、氮分别形成HCl、H O、NH 等原子数比例不同的
2 3
分子。而碳、氢两种元素的原子能形成大小不等、性能各
异、数量庞大的碳氢化合物(hydrocarbon)……
总之,各种元素的原子可能通过不同的途径、不同的
方式构建成性能各异的物质。下面我们将在学习原子结构
的基础上,探索原子构建物质过程的奥秘。
a. 二氧化硅晶体 b. 宝石 c. 翡翠
d. 单质硫 e. 各种形状的金属
图 3.1 性能各异的物质
57
第3章.p65 Page 57 2011.4.7, 3:58 AM Adobe PageMaker 6.5C/PPC拓展视野
化学为人类创造了无数的新材料
随着人类社会的发展,天然的材料已远远满足不了人们的需求。砍伐森林获
得的木材是有限的,性能也很难满足多方面的要求。今天人们已能合成出性能比
木材更优良的材料。化学为人类创造了无数优良的材料。
埋在地底下2 000多年的越王剑,依然光彩照人,锋利异常。已有5 000多
年历史的玻璃,从无色到彩色,从电光到声光,从微孔到纤维,犹如繁花异卉,
争奇斗艳。天文望远镜、显微镜、内窥镜、荧光屏、光导纤维、光学仪器等都离
不开玻璃,玻璃为现代科学技术作出了巨大的贡献。陶瓷是永不凋谢的材料之
花,从考古专家挖掘出的瓷片,发展到今天,出现了神通广大的压电陶瓷、具有
生理功能的生物陶瓷等。
“羊毛”不一定出在羊身上,金属居然有了记忆,飞机隐去了庞大的身影,头
发丝粗细的玻璃纤维能成为信息高速公路。化学正在为人类的材料世界创造着奇
迹。
化学键
自19世纪中叶起,科学家对原子如何结合成分子、分
子的形状、空间结构等作了深入的研究。以后,科学家又研
究了原子是如何直接构成物质的。
研究表明,分子内存在着使各原子结合成一个比较稳
定的整体的相互作用,其中相邻的原子之间的作用是原子
形成分子的主要因素。破坏它要消耗比较大的能量。原子
在构建物质的过程中,也可直接形成一定几何形状的固体
(晶体),构成这些固体(晶体)的微粒间也存在着强烈的相
互作用。
这种物质中相邻原子之间的强烈相互作用称为化学键
(chemical bond)。化学键的种类有离子键(ionic bond)、共
图 3.2 原子间的吸引、
排斥作用 价键(covalent bond)和金属键(metallic bond)等。
58
第3章.p65 Page 58 2011.4.7, 3:58 AM Adobe PageMaker 6.5C/PPC[思考与复习3.1]
1.原子结合成分子时,原子间( )。
(A) 只存在吸引力 (B) 没有排斥力
(C) 吸引力大于排斥力 (D) 吸引力与排斥力达到平衡
2.化学键是一种相互作用,它存在于( )。
(A) 分子或原子团中相邻的原子之间 (B) 构成物质的所有微粒之间
(C) 物质中的原子之间 ( D) 分子之间
59
第3章.p65 Page 59 2011.4.7, 3:58 AM Adobe PageMaker 6.5C/PPC离子键
3
.2
(IONIC BOND)
原子间强烈的相互作用是怎样产生的?化学键的本质
是什么?
原子趋向稳定的途径
稀有气体(rare gas)都是很稳定的物质,这是因为它
们的原子最外电子层的电子排布(氦只有一个电子层为2个
电子,其余最外层均为8个电子)是稳定结构的缘故,除稀
有气体元素外,其他元素的原子最外电子层都没有达到稳
定结构。当原子之间相互作用时,大多有使其最外电子层
达到稳定结构的趋势。
原子相互作用时,原子达到稳定结构的途径有哪些?
活泼的金属元素原子最外层电子数较少,倾向于失去
电子;活泼的非金属元素原子最外层电子数较多,倾向于
得到电子。因此,它们之间反应时是通过得失电子达到最
外层8个电子的稳定结构。而非金属元素的原子间进行反应
时,因它们都不易失去电子,只有通过电子的共用来达到
稳定结构。
离子键的形成
让我们从氯与钠化合生成氯化钠为例进行探讨。
60
第3章.p65 Page 60 2011.4.7, 3:58 AM Adobe PageMaker 6.5C/PPC课堂实验
钠在氯气中燃烧
金属钠在氯气中点燃时可发生剧烈反应,生成氯化钠。
点燃
2Na+Cl 2NaCl
2
在这个反应中,钠和氯的原子结构发生了什么变化
Na
Cl
呢?
从原子结构看,钠原子的最外电子层上有1个电子, +11 +17
容易失去,氯原子最外电子层上有7个电子,容易得到
1个电子。所以,在钠原子与氯原子相互作用时,氯原
子得到钠原子失去的1个电子,都成了最外层是8个电子
Na+ Cl-
的稳定结构,并且分别变成了带正电荷的钠离子(Na+)
和带负电荷的氯离子(Cl-),钠离子和氯离子之间产生 +11 +17
了强烈的静电作用。这种阴、阳离子间通过静电作用形
成的化学键称为离子键。
Na+离子和Cl-离子之间除了有静电吸引作用外,
还有电子与电子、原子核与原子核之间的相互排斥作
用。当两种离子接近到一定距离时,吸引和排斥作用达 +11 +17
到了平衡,于是阴、阳离子之间就形成了稳定的离子键。
氯化钠的电子式表示为 NaCl
··
Na+[· · C l · · ]- 图 3.3 氯化钠形成的示意图
··
活泼的金属(如钾、钠、钙等)与活泼的非金属(如
氯、溴、氧等)结合时都能形成离子键。
例如,溴化钙、氧化钠都是由离子键形成的物质。它
离子键的相互作用只
们的电子式分别为:
·· ·· ·· 是阴、阳离子间的静电吸
[· · B r · · ]-Ca2+[· · B · · r ]-、 Na+[· · O · · ]2-Na+
·· ·· ·· 引力,这样的理解正确
吗?
离子的结构特征
离子是带电荷的原子或原子团。离子所带电荷与原子
形成离子键时的得失电子有关。例如,钙和溴形成溴化钙
61
第3章.p65 Page 61 2011.4.7, 3:58 AM Adobe PageMaker 6.5C/PPC时,每个钙原子失去2个电子形成钙离子Ca2+,每个溴原
子得到1个电子形成溴离子Br-。
F-、 Na+、 Mg2+、 Al3+
某些元素所形成的离子的电子层是饱和的。例如,
的电子层结构与何种原子
相同?写出与Ar原子电子 Li+、 Be2+等离子最外层是2个电子, Na+、 K+、 Mg2+、
层结构相同的离子符号 Ca2+、 O2-、 F-、 S2-、 Cl-等离子最外层是8个电子。
(阴、阳离子各一种)。 离子的结构特征还有离子半径等。离子的结构特征是
影响由离子键形成的物质性质的主要因素。
拓展视野
由于阳离子由原子失去电子而形成的,所以阳离子的半径比相应的原子半径
小。例如:
原子半径(10-10m) Li Na K Rb
1.52 1.86 2.31 2.44
Li+ Na+ K+ Rb+
离子半径(10-10m)
0.68 0.97 1.33 1.47
碱金属阳离子半径随原子序数增加而增大。
由于阴离子的外层电子数比相应的原子多,而核电荷数没有变化,所以,阴
离子的半径比相应的原子半径大。例如:
原子半径(10-10m) F Cl Br I
0.64 0.99 1.15 1.33
离子半径(10-10m) F- Cl- Br- I-
1.33 1.81 1.96 2.20
卤素阴离子半径随核电荷数增加而增大。
对于电子层结构相同的离子,如F-、 Na+、 Mg2+、 Al3+,随着核电荷数的
增加,离子半径逐渐减小。
62
第3章.p65 Page 62 2011.4.7, 3:58 AM Adobe PageMaker 6.5C/PPCF- Na+ Mg2+ Al3+
1.33 0.97 0.65 0.50
离子半径对离子化合物的性质有重要影响。例如氯化钠的熔点比溴化钠高,
就是因为Cl-的半径比Br-的半径小,NaCl中的静电作用比NaBr中强烈的缘故。
离子化合物
【资料库】
以离子键结合的化合物叫离子化合物(ionic compound)。
NaCl、 KCl、 CaBr 、 Na O等都是离子化合物。 NHCl的电子式为
2 2 4
铵离子NH +及OH-、SO 2 - 、 NO -、 CO 2- 等也能形成离
4 4 3 3 H
·· ··
子化合物。例如, NaOH、NH Cl、 Na SO 、 Na CO 、 NH NO [H · · N · · H ]+[· · C · ·l ]-
4 2 4 2 3 4 3 ·· ··
等也都是离子化合物。 H
在常温、常压下,离子化合物一般都是晶体。在离子化 NaOH的电子式为
··
· ·
合物的晶体中,阴、阳离子按一定规律作空间排列。图3.4 N a +[·
·
O
·
· H]-
所示是氯化钠的晶体结构模型。从图中可以看出,每个Na+
离子同时吸引有6个Cl-离子,每个Cl-离子也同时吸引有
6个Na+离子。因此,在氯化钠晶体中不存在单个氯化钠分
子。又因Na+和Cl-的个数比是1∶1,所以, 氯化钠的化
学式是NaCl。其他离子化合物的化学式也只表示组成阴、阳
离子的个数之比。
在离子化合物中,离子间存在强烈的静电作用(即离
子键),因此,离子化合物有较高的熔点和沸点,硬度也较
大。高温下,由于离子键受热被破坏,离子可以自由运动,
故离子化合物受热熔化时可以导电。当离子化合物溶于水
后,由于水分子作用,离子键也被破坏而形成自由移动的
离子,故离子化合物溶于水也能导电。
图 3.4 食盐的实物照片
和结构模型
63
第3章.p65 Page 63 2011.4.7, 3:58 AM Adobe PageMaker 6.5C/PPC化学史话
研究化学键的功臣——鲍林
1922年鲍林(Linus Carl Pauling,1901—1994)毕业于俄勒冈州立农学院
化学工程系;1925年获加利福尼亚理工学院哲学博士学位;鲍林从小胸怀大志,
虚心好学,刻苦钻研,在读书时就勇于探索,收集有关化学键的资料,开始进行
研究。
1931年起,他用量子力学理论研究了分子和原子的结构及化学键的本质,
提出了原子的电负性,创立了杂化轨道理论。
1938年他出版了《化学键的本质兼论分子与晶体的
结构: 现代结构化学导论》,并进一步把分子结构理论应用
到了生命科学的研究中,根据化学键和X射线衍射数据提
出了血红蛋白的α-螺旋结构。
1954年,他因化学键本质和血红蛋白α-螺旋结构
的贡献而获得了诺贝尔化学奖。从20世纪50年代起,鲍林
不惧压力,提出禁止核武器扩散及大气层试验的主张,致
力于人类和平事业,1962年又获得诺贝尔和平奖。
图 3.5 鲍林
[思考与复习3.2]
1.什么叫离子键?怎样的原子之间会形成离子键?举例说明。
2.下列元素的原子,哪些能以离子键两两相互结合?写出结合后生成离子化合物的化
学式。
钠、镁、氯、氧。
3.下列离子化合物的电子式错误的是( )。
·· ··
(A)Na+[· · S · · ]2-Na+ (B)K · ·C · ·l
·· ··
·· ·· ··
(C)Mg2+[· · · · O · · ]2- (D)[· · · C · · · l ]-Ca2+[ · · · C · · · l ]-
4.氯化镁是离子化合物。为什么固体氯化镁不能导电,而氯化镁水溶液或加热到熔化
时便能导电?
64
第3章.p65 Page 64 2011.4.7, 3:58 AM Adobe PageMaker 6.5C/PPC共价键
3
.3
(COVALENT BOND)
活泼金属与活泼非金属原子之间易形成离子键,那么
非金属元素原子之间又会产生怎样的作用呢?
共价键的形成
让我们以氯气与氢气化合生成氯化氢为例进行探讨。
课堂实验
氢气与氯气的反应
我们已经做过氢气在氯气中安静燃烧的实验。那么,若把氢气与氯气充分
混合后进行光照,又会有怎样的现象呢?
将氢气和氯气按1∶1的体积之比混合于集气瓶中,瓶口盖上一层薄塑料片。
在集气瓶附近点亮闪光灯。(可用漂粉精片半粒与几粒锌粒装在同一试管中,
加入浓盐酸,产生氢、氯混合气体)
观察到的现象:________________。
反应的化学方程式:______________。
氢气与氯气是怎样化合生成氯化氢的呢?
分析氢原子和氯原子的结构特点,讨论它们是通过什么方
式使原子最外层电子达到稳定结构的。
氯化氢分子形成过程中,电子不是从氢原子转移到氯
原子上,而在氢、氯原子间形成共用的电子对,使氢、氯原
65
第3章.p65 Page 65 2011.4.7, 3:58 AM Adobe PageMaker 6.5C/PPCCl
H
+1 +17 +1 +17
HCl
图 3.6 氯化氢分子形成的示意图
子都达到了稳定结构。
像氯化氢分子那样,原子间通过共用电子对而形成的
化学键称为共价键。
··
氯化氢分子的电子式表示为H· · C · ·l (注意:氢原子和氯
··
原子之间的共用电子对稍偏向于Cl原子)。
由共价键形成的化合物是共价化合物。共价化合物中
原子间全部是共价键。相对于离子化合物,共价化合物的
数量十分庞大。人们迄今已知的几千万种物质,绝大部分
是共价化合物。HCl、 H O、 CO 、 H SO 、 HNO 以及大多数
2 2 2 4 3
有机物都是共价化合物。
氯化氢、水、氨和甲烷的分子构成分别是HCl、 H O、
2
NH 和CH ,为什么共价化合物中原子间按一定的数目比互
3 4
相结合呢?
课题:根据共价键知
识探究氯化氢、水、氨和甲 根据氯、氧、氮、碳和氢原子的最外层电子数,1个氯
烷的化学式为什么是HCl、 原子与1个氢原子形成1对共用电子对,1个氧原子与2个
H O、 NH 和CH 。
2 3 4 氢原子形成2对共用电子对,而氮原子和碳原子各与3个、
提示:从H、 Cl、 O、 N、
4个氢原子分别形成3对和4对共用电子对。HCl、H O、NH
C的原子结构,研究相关原 2 3
和CH 分子的电子式为:
子形成共价键时,要达到 4
饱和电子层结构,各需要
H
多少数目的共用电子对。 H · · · C · · · l H · · · · O · · H H · · · · N · · H H · · · · C · · H
·· ·· ·· ··
H H
化学上常用一根短线表示一对共用电子对,因此它们
的结构式:
H
H—Cl H—O—H H—N—H H— C—H
H H
共价分子
非金属元素的原子之间一般都是通过共用电子对形成
共价键而结合在一起的。
66
第3章.p65 Page 66 2011.4.7, 3:58 AM Adobe PageMaker 6.5C/PPC分子中原子之间全部是共价键的叫做共价分子。HCl、
H O、NH 和CH 等都是共价分子。 为什么离子化合物的
2 3 4
在H 、 Cl 等同种原子形成的单质分子中,氢原子与氢 化学式不能看作分子式?
2 2
原子之间,氯原子与氯原子之间形成的都是共价键。H 和 而共价分子的化学式就是
2
···· 分子式?各举一例说明。
Cl 2 也是共价分子,它们的电子式分别表示为H∶H和· · · C · · ·l · C · · ·l ,
结构式是H—H和Cl—Cl。
共价分子构成的物质,不论是单质还是化合物,其最
小组成单元是分子,因此,与离子化合物不同,共价分子的
化学式就是分子式。
在共价分子中,除了原子间存在着强烈的共价键作用
外,分子之间还存在比化学键弱得多的相互作用。正是这
种分子间相互作用,大量分子聚集成气、液或固态。所以共
价分子构成的物质熔、沸点较低,硬度较小。
拓展视野
用电子式表示物质的形成
在元素符号的周围用小黑点或×表示该原子最外层上的电子,称为原子的电
子式。例如, 、 、 和 等。离子的电子式除了在元素符号周围标出最外
层电子外,还需标出所带的电荷。例如:Na+、Mg2+、[ ]-和[ ]2-等。
我们可以用电子式表示氯化钠的形成: + Na+[ ]-用电子式
表示氯化氢分子的形成: + H
氯化钙和水分子是如何形成的?其化学键的类型有什么不同?
钙原子最外层上有2个电子,需失去2个电子方能成为稳定结构,而氯原子
最外层上有7个电子,只需得到1个电子便可成为稳定结构,所以钙原子失去的
电子需由2个氯原子来得到,形成的是离子键。
+ + [ ]- Ca2+[ ]-
氢原子最外层上有1个电子,因只有一个电子层,只需得到1个电子便成为
稳定结构,而氧原子最外层上有6个电子,需得到2个电子才能成为稳定结构,
所以一个氧原子要与2个氢原子形成共用电子对,才都能成为稳定结构,形成的
是共价键。
+ + H H
这样,我们对H S、MgO、MgCl ,甚至CO 、Na S、CH 等中的化学键的
2 2 2 2 4
形成都可以进行探究了。当然还有很多分子中的化学键需要我们掌握了更多的理
论知识后,才能去研究和分析。
67
第3章.p65 Page 67 2011.4.7, 3:58 AM Adobe PageMaker 6.5C/PPC原子以共价键直接构成物质
原子可以通过共价键结合成分子,分子再聚集成气态、
液态或固态物质。此外,原子还可以通过共价键直接构成
固体(晶体),金刚石就是碳原子直接以共价键结合而成。
图3.7是金刚石结构示意图,从图中可看出,每个碳原
子以4根共价键与其他4个碳原子连接,全部碳原子均以C
—C键构成一个庞大的立体结构。由于共价键强烈的相互
图3.7 金刚石的结构示意图 作用,以及结构高度对称性,因此金刚石熔点高而坚硬,是
自然界最硬的物质。
查阅石墨和C 的结
60
构的有关资料,分析其中
碳原子间的化学键种类,
并说明石墨为什么熔点高 C 分子 金刚石 石墨
60
而质地柔软。
图3.8 碳的三种同素异形体的结构示意图
不同种原子也可以通过共价键直接构成化合物,二氧
化硅就是硅、氧原子以共价键形成的固体(晶体)。因结构
与金刚石十分类似,所以二氧化硅也是高熔点、高硬度物
质。
思考:为什么二氧化硅的化学式(SiO )仅表示硅、氧
2
原子个数之比?
拓展视野
形形式式的晶体
氯化钠、金刚石和干冰等都是晶体。晶体具有整齐规则的几何外形和固定的
熔点等性质。
离子化合物形成的晶体是离子晶体,它们是由阴、阳离子通过离子键结合而
成的。离子晶体具有较大的硬度和较高的熔、沸点。
金刚石与二氧化硅等固体硬度很大,熔、沸点很高,它们都是由原子通过共
价键结合而成的具有空间网状结构的原子晶体。
68
第3章.p65 Page 68 2011.4.7, 3:58 AM Adobe PageMaker 6.5C/PPC图 3.9 二氧化硅晶体实物和结构模型 图 3.10 干冰的结构示意图
固体二氧化碳称为干冰。当二氧化碳分子间充分接近时,产生分子间作用
力,也称范德华力。由于这种作用力较弱,因此分子之间通过范德华力结合而成
的分子晶体,熔、沸点较低,硬度较小。干冰、固体碘、冰等都是分子晶体。
[思考与复习3.3]
1.氯气分别与下列物质反应时,原子间通过什么途径形成稳定结构?形成什么样的化
学键?产生的化合物是离子化合物还是共价化合物?
镁 碳 钾 氢气
2.以下表示上述生成物的电子式正确的是( )。
Cl
(A)[ ]- Mg2+[ ]- (B)Cl Cl
Cl
(C)K (D)H+[ ]-
3.根据你的认识,从形成条件和形成过程看离子键和共价键有什么不同?离子化合物和
共价化合物的性质有哪些主要区别?
4.下列化合物各属于哪一类物质(酸、碱、盐、氧化物)?哪些是离子化合物,哪些
是共价化合物?
HBr NaOH KI MgO CO
2
5.下列各种单质中是否存在化学键?若存在,则是哪一种类型的化学键?
氩气 金刚石 氮气 氢气
69
第3章.p65 Page 69 2011.4.7, 3:58 AM Adobe PageMaker 6.5C/PPC小结与思考
1.一百零几种元素的原子却构成了目前人类已知的3 000多万种物质。探索这神秘而
浩渺的物质世界,就要去研究物质是怎样由原子构建成的。物质之所以具有不同的性质,是
因为物质具有不同的组成和结构。
2.探索物质构建的奥秘,主要是了解原子是怎样构成物质的,其主要内容就是化学键。
化学键是物质(分子或晶体)中相邻原子间的强烈的相互作用。化学键有离子键、共价键和
金属键等(金属键以后学习)。原子形成离子后,通过离子键形成离子化合物。原子通过共价
键形成分子,分子聚集成各种状态的物质;原子也可以直接通过共价键直接形成物质(晶体)。
3.对离子键和共价键作归纳对比,填写下表:
名 称 定 义 例举形成的物质
4.思考与复习。
(1)原子在相互结合时会趋向稳定结构。所谓稳定结构,是原子的最外电子层具
有________ 个电子。形成这种稳定结构的常见途径有________和________等。
(2)镁原子与氯原子结合生成氯化镁过程:镁原子________成为________,而氯原
子________成为________。它们之间产生的化学键称为________,氯化镁是________化
合物。氯化镁的电子式为________。
(3)氢原子与氧原子结合成水的过程:氢原子与氧原子之间通过____________而结合。
原子间通过这种_____________而形成的化学键称为_____________。水是___________化
合物,水分子的电子式为___________。
70
第3章.p65 Page 70 2011.4.7, 3:58 AM Adobe PageMaker 6.5C/PPC4
剖析物质变化中的能量变化
ANALYSE THE CHANGES OF ENERGY IN CHANGES
OF SUBSTANCES
◆ 物质的溶解、结晶和热现象
◆ 化学反应中的热现象和热化学
方程式
◆ 铜-锌原电池
71
第4章.p65 Page 71 2011.4.9, 10:41 PM Adobe PageMaker 6.5C/PPC人
类社会的发展史是和人类利用物质变化
产生的能量变化的进步密切相关的。最
早的火的利用,就是通过燃烧植物,把
植物内部的化学能转化成了热,使人类结束了茹毛饮血
的原始生活。蒸汽机的发明,则是把煤的化学能转化为
热能,再转化为机械能,引来了工业革命。100多年来
电能的利用,使几千年来人们向往的神话奇迹开始出
现,这种神奇的背后包含有许许多多的化学变化。让我
们剖析物质变化中的能量变化,准备将来进一步创造新
的奇迹吧。
72
第4章.p65 Page 72 2011.4.9, 10:41 PM Adobe PageMaker 6.5C/PPC物质在溶解过程中有能量变化吗
4
(ARE THERE ANY CHANGES OF ENERGY IN
.1
DISSOLVED PROCESS OF SUBSTANCES)
能量的守恒和转化
世界是物质的。物质都在不断地运动着,没有不运动
的物质,也没有无物质的运动。运动是物质的固有属性,物
质的运动形式又是多种多样的,如机械运动、分子热运动、
电磁运动等。
能量则是物质运动的一种度量。自然界一切物质都具
有能量,能量具有各种不同的形式,并且能够从一种形式
转化为另一种形式,从一个物体传递给另一个物体,在转
换和传递的过程中,各种形式能量的总量保持不变。这就
是能量守恒定律。
人们在日常生活和生产中,需要各种各样形式的能。例
如,使用电子计算机需要电能,绿色植物的生长需要光能,
烹调美味佳肴需要热能。你是否想过这些能量是从哪里来
的吗?
图 4.1 能量从哪里来
73
第4章.p65 Page 73 2011.4.9, 10:41 PM Adobe PageMaker 6.5C/PPC能量的转化常常伴随着物质的变化。太阳具有巨大的
能量,它每时每刻都在辐射能量,每秒辐射到地球的太阳
能达1.7×1014 kJ。绿色植物吸收太阳能经过光合作用,提
供了人和动物所需的食物和燃料。古代生物吸收了太阳能,
经过漫长的地质变化,形成了煤、石油、天然气等矿物燃
料。人类常利用的煤、石油、天然气和食物的能量,归根到
底都是由太阳能转化而来的,并以化学能的形式储存下来。
当煤、石油、天然气和食物在转化为其他物质的过程中,给
人类提供了各种各样的能量。例如,食物在人体新陈代谢
的过程中发生了能量的转化,由化学能转变为能使人保持
体温的热能,转化为使肌肉和骨骼运动的动能,转化为使
神经纤维用以传递信息的电能。
食物中产生能量的营养物质主要是糖类、脂肪和蛋白
质,它们是人体所需能量的主要来源。
表 4.1 100g牛奶能提供的能量
营养素 100 g牛奶中的含量 提供的能量
糖类 4.7 g 80 kJ
脂肪 3.9 g 140 kJ
蛋白质 3.3 g 56 kJ
我们知道,固态冰在受热后会变成液态的水,液态的
1. 比较每克糖类、脂 水继续加热会变为水蒸气。相反,要使水蒸气变成液态的
肪和蛋白质所提供能量的 水时就会放出能量,水变成冰时也会放出能量。在物质三
大小。
态变化中,均存在着能量的变化:
2. 据测算,1个成年人
每天约需12 000~13 000 kJ
吸收能量 吸收能量
的能量。估算一下,你的能
固态 液态 气态
量摄入是否恰当? 放出能量 放出能量
图 4.2 物质三态变化中能量的变化
人们在生活中运用这一变化规律来调节环境的温度,
营造舒适的居住环境。在工业生产中,运用这一规律制造
热交换器,用于对原料的预热或产品的降温。
74
第4章.p65 Page 74 2011.4.9, 10:41 PM Adobe PageMaker 6.5C/PPC拓展视野
能源的种类和储量
能源是指能产生机械能、光能、热能、电磁能、化学能等各种能量的自然资
源。从能源的形成和来源角度看,可把能源分为来自太阳(如生物质能、风能、
煤、石油、天然气等)、来自地球内部(如地热能等)、来自核反应(如裂变能和
聚变能等)和来自天体间引力(如潮汐能等)等4种。
从能源利用状况角度看,煤、石油、天然气、水能以及生物能等是多年来大
规模使用的能源,称为常规能源,核能、地热能、海洋能等称为新能源。
从能源的原有形态是否改变的角度看,可把能源分为自然界现存的一次能源
(如煤炭、石油、天然气等)和由一次能源加工转换而成的二次能源(如电能、氢
能、汽油等)。
从能源是否能循环再生角度看,可将能源分为可再生能源(水力、沼气等)
和不可再生能源(煤、石油等)。
石油是世界上分布最不均衡的资源之一,全世界已勘探可开发的石油储量约
1.4×1011 t,95%仅分布在20个国家里,前五位国家分别是沙特阿拉伯、伊拉
克、阿联酋、科威特和伊朗。目前,天然气是消费量增长最快的矿物燃料。天然
气现在占全球商业能源的23%,其生产在过去的20年里增长约70%。虽然全球
天然气估计储量正在迅速地增长,但已发现的天然气储量仍比石油少。相对而言
固体燃料煤较为丰富,是世界能源的一个重要组成部分。
溶解的过程和溶解热现象
溶液(solution)是由一种或一种以上的物质[溶质
(solute)]分散到另一种物质[溶剂(solvent)]里,形成的
均匀、稳定的混合物。均匀是指溶液中溶质的分散程度达
到分子(或离子)水平。那么,溶质是如何被分散到溶剂
中,又如何形成均一、稳定的混合物呢?
请观察高锰酸钾晶体在水中的溶解(dissolve)情况。
75
第4章.p65 Page 75 2011.4.9, 10:41 PM Adobe PageMaker 6.5C/PPC课堂实验
高锰酸钾溶于水的现象
在盛有水的小烧杯中,轻轻地放入一小粒高锰酸钾晶
体,记录观察到的现象:______________
________________。
图 4.3 高锰酸钾微
粒在水中的扩散
在水中放入紫黑色的高锰酸钾晶体后,可以清楚地看
到,溶液中紫红色范围逐渐扩大,最后,溶液都变成紫红
色。这是由于高锰酸钾晶体在水溶液中电离出钾离子(无
色)和高锰酸根离子(紫红色),钾离子和高锰酸根离子受
到水分子的作用,克服了离子间的引力,逐渐向水中扩散,
分布于整个溶液中,因而使溶液变成了紫红色。
KMnO K++MnO-
4 4
那么,物质的溶解过程是否伴随能量的变化呢?
课堂实验
物质溶解过程的能量变化
在三只小烧杯中分别加入25 mL蒸馏水,并用数字测温仪(见图4.4)测出
水的温度,然后分别加入10 g氯化铵、氢氧化钠和氯化钠固体,用玻璃棒搅拌
使固体溶解,再分别测出溶液的温度。
实验记录:水温 ____________。
溶解氯化铵固体后溶液的温度 ______。
溶解氢氧化钠固体后溶液的温度 _____。
溶解氯化钠固体后溶液的温度 ______。
实验结论:______________。
图 4.4 数字测温仪
76
第4章.p65 Page 76 2011.4.9, 10:41 PM Adobe PageMaker 6.5C/PPC为什么不同溶质在溶解时所表现出的热现象不相同
呢?
用溶质溶解过程来解
原来,物质的溶解通常有两个过程:一个是溶质的分
释,氢氧化钠固体和氯化
子或离子受到水分子的作用,向水中扩散的过程,在这个 钠固体溶于水后的能量变
过程中,溶质分子或离子要克服分子或离子之间的引力,需 化。
要向外界吸收热量,这是一个物理过程;另一个是溶质分
子或离子和水分子结合成水合分子(hydrated molecule)或
水合离子(hydrated ion)的过程,这一过程放出热量,是
一个化学过程。
物质溶解时,溶液的温度是升高还是降低,取决于溶
质微粒扩散过程所吸收的热量和水合过程所放出热量的相
对大小。氯化铵溶解在水中时,扩散过程吸收的热量大于
水合过程放出的热量,所以溶液的温度降低。反之,氢氧化
钠溶解在水中时,扩散过程吸收的热量小于水合过程放出
的热量,所以溶液的温度升高。
综上所说,物质在溶解过程中总是伴随着能量的变化。
而表现出来的放热或者吸热现象,则是溶质微粒在扩散过
程和水合过程中能量变化的总效应。
溶解和结晶
将固体溶质的水溶液放在敞口的容器中让水慢慢地蒸
发,或改变溶液的温度,都可能使晶态溶质从溶液中析出,
这个过程称为结晶(crystallize)。
结晶和溶解是同时进行的相反的两个过程。当溶质溶
解在溶剂中,一方面溶质的微粒不断地克服微粒间的引力,
离开溶质表面扩散到溶剂中;另一方面,溶解在溶剂中的
溶质微粒碰撞固体表面时,又受到固体表面微粒对它的吸
引,不断地在未溶解的溶质表面聚集成晶体。所以,在溶解
过程的同时,也进行着结晶的过程,这两个同时进行的相
反过程是可逆的,通常用“ ”表示。
溶解
固体溶质 溶液中的溶质
结晶
77
第4章.p65 Page 77 2011.4.9, 10:41 PM Adobe PageMaker 6.5C/PPC图 4.5 溶解与结晶的示意图
当溶质开始溶解时,在单位时间内从固体溶质表面扩
散到溶剂里的溶质微粒的数目,比回到固体溶质表面的溶
质微粒的数目多,这时溶液处于不饱和状态,所以从表面
看来,固体溶质在不断地溶解(减少)。随着溶液里溶质微
粒的逐渐增加,由溶液里回到固体溶质表面的微粒数目也
随之增加,这时溶质溶解的量逐渐减少,同时溶质结晶的
量逐渐增大。直到在单位时间内扩散到溶液里的溶质微粒
数目,与回到固体溶质表面的溶质微粒数目相等时,也就
是溶质溶解的速率等于结晶的速率,这时从表面看,固体
溶质不再减少,也不再增加,我们称之为达到了溶解平衡
(solution equilibrium)状态。这时的溶液是饱和溶液。
在工业生产中常常要从溶液中提取溶解的固体物质。
例如,从海水中提取食盐,通常利用风吹、日晒,让海水蒸
发。随着水分的减少,氯化钠溶液的浓度逐渐提高,并达到
饱和。进一步蒸发水分,氯化钠便从溶液中结晶析出。随着
温度的变化而溶解度变化不大的物质,一般可以用蒸发溶
剂的方法从溶液中提取。溶解度受温度的改变变化较大的
固体物质,一般用冷却热的饱和溶液的方法来使溶质结晶
析出。
78
第4章.p65 Page 78 2011.4.9, 10:41 PM Adobe PageMaker 6.5C/PPC课堂实验
硫酸铜和明矾的溶解和结晶
在两支试管中各注入10 mL蒸馏水,分别加入少量硫酸铜和明矾。振荡试
管,使它们完全溶解。然后,加热溶液,再分别继续加入硫酸铜和明矾,制成饱
和溶液。把试管放在冷水中冷却,请记录所看到的实验现象: _______
___________________________________
_________________________________。
硫酸铜
明矾
图 4.6 溶解度与温度的关系
食盐、硫酸铜晶体和明矾晶体,都有一定的几何形
状。这种自发形成且具有规则几何形状的固体叫做晶体。
有些晶体在溶液中析出形成晶体时会结合一定数目的水分 结晶水合物是混合物
还是纯净物?
子,含有水分子的晶体叫结晶水合物(crystalline hydrate),
例如,胆矾(CuSO·5H O)、绿矾(FeSO·7H O)、明矾
4 2 4 2
[KAl(SO )·12H O]、石膏(CaSO ·2H O)等。也有的
4 2 2 4 2
物质的晶体不含结晶水,像食盐、硝酸钾等。
图 4.7 晶体的形状
79
第4章.p65 Page 79 2011.4.9, 10:41 PM Adobe PageMaker 6.5C/PPC课堂实验
硫酸铜晶体的变化
(1) 取5 g研碎的蓝色硫酸铜晶体放入试
管中,加热,观察现象。
(2)待上述实验生成白色粉末冷却后,滴加
几滴水,观察固体颜色的变化。
记录现象:_____________
____________________
__________________。
图 4.8 硫酸铜晶体的变化
有些结晶水合物中的结晶水不太稳定,在室温下和干
燥的空气里会失去一部分或全部结晶水,这种现象叫做风
上述两个实验的变化
化(efflorescence)。例如,在室温下,石碱(Na CO·10H O)
过程属于物理变化还是化 2 3 2
学变化? 放在干燥的空气里会逐渐失去结晶水而成为粉末状的碳酸
钠。有些晶体能吸收空气中的水蒸气,在晶体的表面逐渐
形成溶液,这种现象叫做潮解(deliquescence)。例如,氯化
钙、氢氧化钠固体在空气里很容易潮解。
[思考与复习4.1]
1.氯化钠晶体属于离子晶体,根据溶解过程分析氯化钠溶液中存在几种微粒?
2.下列说法是否正确?为什么?
(1)浓硫酸溶于水放出大量的热量,说明浓硫酸只有溶质的水合过程。
(2)物质在溶解时,若溶解速率等于结晶速率,物质就不再溶解了。
(3)加热胆矾晶体时,胆矾会失去结晶水成为白色粉末,这一现象称风化。
3.试分析氯化钙固体常被用作干燥剂的原因。
4.芒硝是硫酸钠的结晶水合物,实验测得其中硫酸钠和结晶水的质量之比为1∶1.267 6。
试写出芒硝的化学式。
80
第4章.p65 Page 80 2011.4.9, 10:41 PM Adobe PageMaker 6.5C/PPC5.阅读下面短文。
One important use of food is to serve as a source of energy, permitting work to be done, and of
heat, keeping the body warm. Foods serve in this way through their oxidation within the body by
oxygen which is extracted from the air in the lungs and is carried to the tissues by the hemoglobin
of the blood. The ultimate products of oxidation of most of the hydrogen and carbon in foods are water
and carbon dioxide. The nitrogen is for the most part converted into urea, CO(NH ) , which is
2 2
eliminated in the urine.
Heats of combustion of foods and their relation to dietary requirements have been thoroughly
studied. The food ingested daily by a healthy man of average size doing a moderate amount of
muscular work should have a total heat of combustion of about 12 500 kJ; about 90% of this is made
available as work and heat by digestion and metabolism of the food.
81
第4章.p65 Page 81 2011.4.9, 10:41 PM Adobe PageMaker 6.5C/PPC化学变化中的能量变化
4
.2
(THE CHANGES OF ENERGY IN CHEMICAL REACTIONS)
在化学反应中,物质发生了变化,同时还伴随着能量
的变化。人们利用化学反应,有时是为了制取所需的物质,
有时却主要是为了利用化学反应所释放的能量。例如,人
们利用燃烧煤所产生的能量使机器运转、火车开动;利用
氢气和氧气化合时所放出的能量来焊接金属。人类的祖先
从学会用火起,就已经在利用化学反应所放出的能量了。
化学反应过程中释放的能量有多种形式。例如,镁带
燃烧时产生强光;煤气燃烧时,放出大量的热能;干电池中
的化学变化,释放出的主要是电能。化学反应可以释放出
光能、热能、电能等多种形式的能量,但大多数是热能。
化学反应中的热效应
化学反应中的能量变化,通常表现为热量的变化。反
应时所放出或吸收的热量,叫做反应的热效应。化学中把
有热量放出的化学反应叫做放热反应(exothermic reaction),
把吸收热量的化学反应叫做吸热反应(endothermic reaction)。
炭的燃烧,氢气和氧气的化合,都是放热反应。
点燃
C +O CO +Q
2 2
点燃
2H +O 2H O+Q
2 2 2
碳酸钙的分解,红热的炭与二氧化碳反应生成一氧化
碳,都是要吸收足够的热量才能发生反应,它们都是吸热
反应。
82
第4章.p65 Page 82 2011.4.9, 10:41 PM Adobe PageMaker 6.5C/PPC△
CaCO CaO+CO ↑-Q
3 2
高温
C+CO 2CO -Q
2
“Q”是热量的符号,热量的单位是焦耳(J)。放出热
量,在反应式右方用“+Q”表示;吸收热量,在反应式右
方用“-Q”表示。
课堂实验
中和反应的热效应
用两只50 mL量筒分别量取2 mol/L盐酸和2 mol/L氢氧化钠溶液各50 mL,
用数字测温仪测出这两种溶液的温度(每次使用之后,数字测温仪探头必须用蒸
馏水洗净),并作好记录。将两种溶液倒入同一个烧杯里,用玻璃棒轻轻搅动,混
匀后,测量该溶液的温度。观察混合前后温度的变化。
记录:混合前溶液温度________,混合后溶液的温度________________。
结论:_________________________________________________________。
化学方程式:____________________________________________________。
反应物的总能量高
为什么有的化学反应会放出热量,而有的化学反应却
需要吸收热量呢?我们知道,各种物质内部都储存着能量,
这种潜藏在物质内部、只有在化学反应时才释放出来的能 放热反应
量,称为化学能(chemical energy)。反应物和生成物能量的
相对高低程度决定该反应是放热反应还是吸热反应。如果
反应物所具有的总能量高于生成物所具有的总能量,那么 生成物的总能量低
在发生化学反应时,有一部分能量就会转变成热量等形式 a. 放热反应
释放出来(见图4.9a),这就是放热反应。如果反应物所具 生成物的总能量高
有的总能量低于生成物所具有的总能量,那么在发生化学
反应时,反应物就需要吸收能量才能转化为生成物(见
图4.9b),这就是吸热反应。由此可见,化学反应的过程,也 吸热反应
可看成是储存在物质内部的能量转化为热能等释放出来,
或者是热能等转化为物质内部的能量而被储存起来的过程。
当化学反应过程释放出或吸收的能量表现为热量时, 反应物的总能量低
b. 吸热反应
反应物具有的能量总和与生成物具有能量总和的差值,即
图 4.9 化学反应中能量
为反应热。大量事实表明,物质化合时,放出能量越多,生
变化示意图
83
第4章.p65 Page 83 2011.4.9, 10:41 PM Adobe PageMaker 6.5C/PPC成物的热稳定性越大。例如,氢气和氧气化合生成1 mol水
蒸气时,放出241.8 kJ热量,而氢气与硫蒸气化合生成1 mol
硫化氢时,只放出20.1 kJ热量,所以水的热稳定性比硫化
氢的热稳定性大,硫化氢受热容易分解。因此,在化合反应
中生成相等物质的量的生成物时,放出或吸收热量的大小
是生成物热稳定性的有效标志。
热化学方程式
为了简明地表达反应过程的热量变化,把反应中放出
或吸收的热量写入化学方程式。例如,通过实验,测得1 mol
无定形碳在氧气中充分燃烧时,放出393.5 kJ的热量;1 mol
氢气和0.5 mol氧气化合生成1 mol液态水时,放出285.8 kJ
的热量。这些反应过程可以分别用下面的表明反应热的化
学方程式来表示。
C(s)+ O (g) CO (g)+393.5 kJ
2 2
1
H (g) +—O (g) H O ( l )+285.8 kJ
2 2 2 2
这种表示化学反应所放出或吸收热量的化学方程式,
叫做热化学方程式(thermo chemical equation)。热化学方程
式不仅表明了一个反应中的反应物和生成物,还表明了一
定量物质在反应中所放出或吸收的热量。例如,1 mol红热
的炭和1 mol水蒸气反应生成水煤气,要吸收131.3 kJ的热
量,它的热化学方程式如下:
C(s)+H O(g) CO(g) +H (g) -131.3 kJ
2 2
在化学方程式中,化学式前的化学计量数表示反应物
和生成物之间的微粒的个数之比;而在热化学方程式中,化
学式前的化学计量数是表示物质的量,因反应热效应与反
1
应物的物质的量有关。例如,—O 表示0.5 mol的氧气,约
2 2
3.01×1023个氧分子。因此,在热化学方程式中,化学式前
的化学计量数可以是分数。
84
第4章.p65 Page 84 2011.4.9, 10:41 PM Adobe PageMaker 6.5C/PPC热化学方程式中反应物和生成物都必须注明状态,因
为化学反应放出或吸收的热量的多少是和反应物、生成物
呈现哪一种聚集状态有关。
例如,氢气燃烧生成水蒸气时,其热化学方程式如下:
1
H (g)+—O (g) H O(g)+241.8 kJ
2 2 2 2
由于生成水的状态不同,这一反应热同氢气跟氧气化
合生成1 mol液态水时的反应热相差44 kJ。
根据热化学方程式可以计算一定量某纯净物在化学反
应中放出或吸收的热量。例如,甲烷燃烧的热化学方程式
如下:
CH (g)+2O (g) CO (g)+2H O(l)+ 890.3 kJ
4 2 2 2
从热化学方程式中可知,1 mol甲烷完全燃烧放出890.3 kJ
热量,则1 m3甲烷(1 000 L)在标准状况时燃烧所放出的
热量为:
1 000 L
Q = —————×890.3 kJ/mol=3.975×104 kJ
22.4 L/mol
物质名称 分子式 物质状态 燃烧产生的热量(kJ/mol)
甲烷 CH 气态 890.3
4
乙炔 CH 气态 1 230
2 2
丁烷 CH 气态 2 876
4 10
酒精 CH OH 液态 1 365
2 5
分别讨论在等物质的量和等质量两种情况下,上述四种
物质充分燃烧时放出热量的大小。
85
第4章.p65 Page 85 2011.4.9, 10:41 PM Adobe PageMaker 6.5C/PPC【资料库】
比较常见的燃料的热值
我们实际使用的各种燃料,例如,煤气、液化气、
汽油、柴油等都是混合物,很难用热化学方程式来比
较它们燃烧时放出的热量,而是用单位质量或单位体
积燃料的热值来比较。热值是燃料质量的重要指数。
热值越大,燃料作为提供热量的能源的价值越高。
燃 料 热 值
城市煤气(H 48%、
2
15.6 MJ/m3
CO15%、CH 13%)
4
液化气 109.2 MJ/m3、47.3 MJ/kg
氢气 10.8 MJ/m3、120.8 MJ/kg
汽油 46 MJ/kg
柴油 42.6 MJ/kg
标准煤 29.26 MJ/kg
煤气和液化气都是城市民用燃料,液化气的热值
比煤气高,1 kg液化气汽化后的体积约是0.4 m3,而
它的发热量相当于2.8 m3的煤气。因此,液化气是一
种高热值的民用燃料。
燃料的充分利用
世界各国所需的燃料几乎全部来自化石燃料,然而,在
自然界经历几百万年才形成的化石燃料,极有可能在几百
年内全部被人类耗尽。因此,如何控制燃烧反应,使燃料充
分燃烧,这对于节约能源非常重要。
总体来讲,使燃料充分利用,通常需要考虑两点:一是
燃料的充分燃烧;二是热能的充分利用。
可燃物跟空气里的氧气是以一定的比例反应的,如果
空气不足,燃料燃烧得不完全,可燃物会随烟气或废渣排
出,造成燃料的浪费和空气的污染。所以,燃烧过程要有足
量的空气。但空气也不是越多越好,因为通入过多的空气
会带走一部分热量,造成热量损失。
86
第4章.p65 Page 86 2011.4.9, 10:41 PM Adobe PageMaker 6.5C/PPC由于大块的固体燃料和液体燃料与空气接触面有限,
燃烧往往不够充分。因此,工业上常常把固体燃料粉碎,把
液体燃料喷成雾状,增加燃料跟空气的接触面,使燃料的
不完全燃烧降到最低程度。例如,我国已开发出新型煤粉
尘燃烧器,煤的燃烧效率可达95%以上。
煤直接燃烧不仅热值不高,而且会产生大量的烟尘。我
国多产高硫煤,煤在燃烧过程中产生的SO 是导致酸雨的主
2
要原因之一。因此,发展洁净煤技术、减少污染物的排放、
提高煤炭的利用率,已成为世界各国研究的重要课题。目
前,煤的气化和液化是高效、清洁地利用煤的重要途径。将
焦炭在高温下与水蒸气反应,能得到CO和H :
2
高温
C(s)+H O(g) CO(g)+ H (g)-131.3 kJ
2 2
制得的CO和H 的混合物称为水煤气,燃烧水煤气不 温度较高
2
的气体
仅污染少,而且燃烧效率高。
为了充分利用燃料的能量,除了要使燃料完全燃烧外,
还要提高热能的利用率。一般通过改进设备、利用余热、防 热气体
止热损失。
热交换是工业上利用反应热的常用方法。它通过热交
冷气体
换器来实现。图4.10是常用的热交换器的示意图。它的内
部装有许多平行管道或蛇形管,以扩大传热面积。当一种
流体在管道内流动,另一种流体在管道外逆向流动时,它
们通过管壁进行热交换,使热的流体得到降温,冷的流体 温度较低的气体
得到预热。在化工厂里,利用热交换的原理,使一种反应物 图 4.10 热交换器示意图
放出的热量,用于加热另一种反应物。此外,人们常利用化
学反应中放出的热能来加热生活用水,满足企业内的热水
供应。
目前,在一些发达国家,第一代能源薪柴几乎已被淘
汰,第二代能源煤炭也已逐渐被第三代能源石油所取代。而
在我国的能源构成中,却仍以煤炭为主。据最新统计表明,
中国矿物能源资源探明的可采储量中煤炭占94%,石油、天
然气则不到6%。在今后50年以至更长的时间内,中国的能
源结构不会有大的改变,而且在未来的能源构成中,煤炭
的地位将显得更加重要。
87
第4章.p65 Page 87 2011.4.9, 10:41 PM Adobe PageMaker 6.5C/PPC探究与实践
反应热的充分利用
1.设计一个隔热、保温的容器,用于测定含1 mol氢氧化钠的溶液和含1 mol
氯化氢的盐酸反应的反应热,并分析产生误差的原因。
2.设计实验,测定普通酒精灯中燃料乙醇热值的利用率。若使用挡风罩,其
热值的利用率提高多少?
铜-锌原电池及其原理
化学能可以转变为热能,还可以转变为其他形式的能
量。把化学能转变为电能的装置,我们称为化学电源
(electrochemical power sources),习惯上称为电池。化学电
源大体上可分为原电池(primary battery)、蓄电池(storage
battery)和燃料电池(fuel cell)三大类。常见的干电池(中
性锌、二氧化锰电池)就是一种原电池。
在学习原电池的原理之前,先让我们来看一个实验。
图 4.11 形形色色的化学电池
课堂实验
在两个250 mL的烧杯中各盛有100 mL稀硫酸,在其中的一只烧杯中分别
放入一根铁丝和一根铜丝,在另一只烧杯中放入上端连接在一起的铁丝和铜丝,
观察现象。
记录观察到的现象:________________________
________________________________。
88
第4章.p65 Page 88 2011.4.9, 10:41 PM Adobe PageMaker 6.5C/PPC这是一个有趣的实验,我们知道铜与稀硫酸是不发生
反应的,但当上端连接在一起的铁丝和铜丝,同时放入稀
硫酸时,铜丝的表面会出现气泡,这是为什么呢?原来,上
端连接在一起的铁丝和铜丝与稀硫酸已构成了一个小电池,
在金属丝中有电子流动。
课堂实验
铜-锌原电池
e e
Zn
把一块锌片和一块铜片平行地插入盛有稀硫酸溶液 Cu
的烧杯中,观察现象。再用导线把锌片和铜片连接起来,
在导线中间接入灵敏电流计,观察锌片、铜片和灵敏电
H+
流计发生的变化。
H
2
记录观察到的现象:_____________ Zn2+
________________________ H S + O 2- SO 2 4 -
4
______________________。
图 4.12 铜-锌原电池
实验结果表明,浸在稀硫酸溶液里的锌片和铜片用导
线连接后,由于锌比铜活泼,容易失去电子,锌被氧化成
Zn2+而进入溶液,锌原子失去的电子通过导线流向铜片,溶
液里的H+从铜片上获得电子,被还原成氢原子,氢原子再
两两结合成氢分子从铜片上放出。
以上现象可用离子方程式表示为:
Zn+2H+ Zn2++H ↑
2
在原电池中,电子流出的电极(electrode)是负极
(cathode),如锌片,电极材料被氧化,发生氧化反应;电子
流入的电极是正极(anode),如铜片,H+在电极上被还原,发 组成铜-锌原电池的
生还原反应。人们就是利用原电池的原理制作了多种电池。 必要条件是什么?
89
第4章.p65 Page 89 2011.4.9, 10:41 PM Adobe PageMaker 6.5C/PPC探究与实践
小实验——番茄电池 导线
灵敏电流计
G
番茄汁显酸性,当在番茄里平行
地插入铜片和锌片时,形成原电池。 铜片 锌片
实验步骤为:取2个半熟的番茄,相
番茄
隔一定距离,分别平行插入铜片和锌
片。按图4.13所示,用导线将铜片与
锌片及灵敏电流计相连,观察现象。 图 4.13 番茄电池
历史上第一个提供稳定连续电流的电源装置伏打电池
诞生于1800年。伏打电池的发明归功于两位意大利科学家。
一位是解剖学家和医学教授伽伐尼,一位是物理学家和化
学家伏打。
拓展视野
电池的发明
1780年,伽伐尼(Luigi Galvani 1737—1798)在一次解剖青蛙时有一个偶
然的发现。一只已解剖的青蛙放在一个潮湿的铁案上,当解剖刀无意中触及蛙腿
上外露的神经时,死蛙的腿猛烈地抽搐了一下。伽伐尼立即重复了这个实验,又
观察到同样的现象。作为解剖学家的伽伐尼脑子里总是想着肌肉和神经等,他想
用动物体内有某种电来解释,但这种“动物电”的解释是含糊不清的。1789年他
写成了《关于电对肌肉运动的作用》的论文,于1791年发表。
伏打(Alessandro Volta 1745—1827)读到了这篇论文后,多次重复了伽伐
尼的实验。作为物理学家,他的注意点主要集中在那把金属的解剖刀和铁案上,
而不在青蛙的神经上。他想这可能与电有关,他用自己设计的精密验电器,对各
种金属进行了许多实验。这些实验证明,只要在两种金属片中间隔以用盐水或碱
水浸过的(甚至只要是湿的)硬纸、麻布、皮革或其他海绵状的东西,并用金属
线把两个金属片连接起来,都会有电流通过。这就说明电并不是从蛙的组织中产
生的,蛙腿的作用只不过相当于一个非常灵敏的验电器而已。于是,世界上的第
一个可以提供持续、恒定电流的实用铜-锌电池(简称伏打电池)诞生了。
90
第4章.p65 Page 90 2011.4.9, 10:41 PM Adobe PageMaker 6.5C/PPC[思考与复习4.2]
1.下面关于反应热的叙述中,错误的是( )。
(A)放热反应中,反应热数值是反应物能量的总和与生成物能量的总和的差值
(B)反应热之大小与反应物的物质的量无关
(C)放热反应的逆反应一定是吸热反应
(D)反应热是指反应过程中放出的热量
2.在下列反应中,生成物能量总和高于反应物能量总和的是( )。
(A)Zn(s)+CuSO (aq) ZnSO (aq) +Cu(s) + 216 kJ
4 4
(B)CaCO (s) CaO(s)+CO (g)-1 185 kJ
3 2
1 1
(C)—H (g)+—I (s) HI(g)-26.5 kJ
2 2 2 2
1 1
(D)NaOH(aq)+—HSO (aq) —Na SO (aq)+H O(l)+66.48 kJ
2 2 4 2 2 4 2
3.1 mol 氨气分解成氮气和氢气要吸收46.19 kJ 的热,下列热化学方程式中正确的
是( )。
(A)2NH N + 3H -46.19 kJ
3 2 2
(B) 2NH (g) N (g) + 3H (g)-46.19 kJ
3 2 2
1 3
(C)NH —N +— H +46.19 kJ
3 2 2 2 2
1 3
(D)NH (g) —N (g)+—H (g)-46.19 kJ
3 2 2 2 2
4.雾化油燃烧是工业上一项节能措施,它是采用在油里掺水加压的方法,油水从油管
喷出以形成雾状。为什么把油雾化后燃烧能达到节能的效果?
5.化学电池中发生的主要反应是否必须是氧化还原
反应,氧化还原反应发生在何处,为什么?
6.某学生将一块镁片和一块锌片插进一只柠檬内,
并用导线将两块金属连接,试问这样是否组成了原电
池?若是原电池,那么镁片和锌片各是什么极?
7.普通的钢铁是铁碳合金,请你分析一下,为什么
钢铁在干燥的环境中不易腐蚀,而在潮湿的环境中很容
易腐蚀?
(第6题)
91
第4章.p65 Page 91 2011.4.9, 10:41 PM Adobe PageMaker 6.5C/PPC小结与思考
1.溶质溶解过程的能量变化。
溶解的两 两个过程的 两个过程的 溶液温度
个过程 能量变化 能量关系 的变化
溶质溶 扩散过程
于水 水合过程
2.用自己的语言阐述下列化学概念。
(1)溶解平衡 (2)结晶、结晶水合物 (3)风化、潮解 (4)放热反应、吸热反应
(5)反应热、燃烧产生的热量 (6)热化学方程式 (7)原电池、化学电池
3.热化学方程式的书写注意点。
(1)热化学方程式中各化学式前的化学计量数代表该物质的物质的量。
(2)热化学方程式后面的热量表示这些物质的量的物质反应或生成时,放出或吸收的
热量。“+”表示放出的热量,“-”表示吸收的热量。
(3)物质的状态不同,反应释放或吸收的热量也不同,所以必须在各物质的化学式的
后面注明它的状态。
4.原电池的构成。
(1)电极:它通常由两种活动性不同的金属(或石墨),其中活动性强的金属作负极,
它较容易失去电子,活动性较弱的金属作正极。
(2)电解质溶液:电解质溶液中的某种阳离子,在正极获得电子。
(3)导线:构成闭合电路。
5.思考与复习。
(1)把纯碱和烧碱置于空气中,一段时间后,能看到什么现象?说明理由。
(2)某种城市煤气的组成是:50%氢气、30%甲烷、10%一氧化碳、6%氮气和4%的
二氧化碳。已知:
1
H (g)+—O (g) H O(l)+285.8 kJ
2 2 2 2
1
CO(g)+—O (g) CO (g)+ 282.6 kJ
2 2 2
CH (g)+ 2O (g) CO (g)+ 2HO(l)+ 890.3 kJ
4 2 2 2
计算在标准状况下1 m3煤气燃烧时放出的能量。
(3)实验室用锌与稀硫酸反应制取氢气,某学校实验员为了提高制氢的速度,在此溶液
中,加入少量硫酸铜溶液,你认为此举可行吗?
(4)现有下列仪器:一个烧杯、一块铜片、一块镁片、硫酸铜溶液、一个灵敏电流计和
一些电线。试画一示意图,表示如何用上述仪器组成一个化学电池,并标出正、负极。
92
第4章.p65 Page 92 2011.4.9, 10:41 PM Adobe PageMaker 6.5C/PPC表
期
周
素
元
Ⅰ
录
附
93
第4章.p65 Page 93 2011.4.9, 10:41 PM Adobe PageMaker 6.5C/PPCⅡ 国际相对原子质量表
元素 元素 元素
相对原子质量 相对原子质量 相对原子质量
符号 名称 符号 名称 符号 名称
Ac 锕 227.027 8 Ge 锗 72.61(2) Pr 镨 140.907 65(3)
Ag 银 107.868 2(2) H 氢 1.007 94(7) Pt 铂 195.08(1)
Al 铝 26.981 539(5) He 氦 4.002 602(2) Pu 钚 [244]
Am 镅 [243] Hf 铪 178.49(2) Ra 镭 226.025 4
Ar 氩 39.948(1) Hg 汞 200.59(2) Rb 铷 85.467 8(3)
As 砷 74.921 59(2) Ho 钬 164.930 32(3) Re 铼 186.207(1)
At 砹 [210] I 碘 126.904 47(3) Rh 铑 102.905 50(3)
Au 金 196.966 54(3) In 铟 114.819 Rn 氡 [222]
B 硼 10.811(7) Ir 铱 192.217(3) Ru 钌 101.07(2)
Ba 钡 137.327(7) K 钾 39.098 3(1) S 硫 32.066(6)
Be 铍 9.012 182(3) Kr 氪 83.80(1) Sb 锑 121.760(1)
Bi 铋 208.980 37(3) La 镧 138.905 5(2) Sc 钪 44.955 910(9)
Bk 锫 [247] Li 锂 6.941(2) Se 硒 78.96(3)
Br 溴 79.904(1) Lu 镥 174.967(1) Si 硅 28.085 5(3)
C 碳 12.010 7(8) Lr 铹 [260] Sm 钐 150.36(3)
Ca 钙 40.078(4) Md 钔 [258] Sn 锡 118.710(7)
Cd 镉 112.411(8) Mg 镁 24.305 0(6) Sr 锶 87.62(1)
Ce 铈 140.116(1) Mn 锰 54.938 05(1) Ta 钽 180.947 9(1)
Cf 锎 [251] Mo 钼 95.94(1) Tb 铽 158.925 34(3)
Cl 氯 35.452 7(9) N 氮 14.006 74(7) Tc 锝 [99]
Cm 锔 [247] Na 钠 22.989 768(6) Te 碲 127.60(3)
Co 钴 58.933 20(1) Nb 铌 92.906 38(2) Th 钍 232.038 1(1)
Cr 铬 51.996 1(6) Nd 钕 144.24(3) Ti 钛 47.867(1)
Cs 铯 132.905 43(5) Ne 氖 20.179 7(6) Tl 铊 204.383 3(2)
Cu 铜 63.546(3) Ni 镍 58.693 4(2) Tm 铥 168.934 21(3)
Dy 镝 162.50(3) No 锘 [259] U 铀 238.028 9(1)
Er 铒 167.26(3) Np 镎 237.048 2 V 钒 50.941 5(1)
Es 锿 [252] O 氧 15.999 4(3) W 钨 183.84(3)
Eu 铕 151.964(1) Os 锇 190.23(3) Xe 氙 131.29(2)
F 氟 18.998 403 2(9) P 磷 30.973 762(4) Y 钇 88.905 85(2)
Fe 铁 55.845(2) Pa 镤 231.035 88(2) Yb 镱 173.04(3)
Fm 镄 [257] Pb 铅 207.2(1) Zn 锌 65.39(2)
Fr 钫 [223] Pd 钯 106.42(1) Zr 锆 91.224(2)
Ga 镓 69.723(1) Pm 钷 [147]
Gd 钆 157.25(3) Po 钋 [209]
注:相对原子质量录自1995年国际相对原子质量表,以12C=12为基准;加方括号的为放射
性元素的半衰期最长的同位素的质量数;末尾数的准确度加注在其后的圆括号内。
94
第4章.p65 Page 94 2011.4.9, 10:41 PM Adobe PageMaker 6.5C/PPCⅢ 常用酸、碱试剂的浓度及密度
化学式 w (%) ρ (g/mL) c (mol/L) 化学式 w (%) ρ (g/mL) c (mol/L)
11 1.05 3.2 10 1.05 1.1
20 1.10 6.0 18 1.10 2.0
HCl 26 1.13 8.0 H PO 30 1.18 3.6
3 4
30 1.15 9.5 50 1.34 6.8
37 1.19 11.9 98 1.84 18.4
15 1.08 2.6 10 1.11 2.8
20 1.12 3.5 20 1.22 6.1
HNO 32 1.19 6.1 NaOH 30 1.33 10.0
3
60 1.37 13 36 1.39 12.5
72 1.42 16.3 40 1.43 14.3
18 1.12 2.1 12 1.11 2.4
26 1.19 3.1 26 1.24 5.8
H SO 62 1.52 9.6 KOH 30 1.28 6.9
2 4
92 1.82 17.1 40 1.39 9.9
98 1.84 18.4 50 1.50 13.4
12 1.01 2.0 4 0.98 2.3
19 1.02 3.2 6 0.97 3.4
CH COOH NH
3 36 1.04 6.3 3 11 0.95 6.2
68 1.07 12.1 17 0.93 9.3
100 1.05 17.4 30 0.89 15.7
注:w表示质量分数;ρ表示密度;c表示物质的量浓度。
95
第4章.p65 Page 95 2011.4.9, 10:41 PM Adobe PageMaker 6.5C/PPCⅣ 酸、碱和盐的溶解性表(20℃)
阴
阳
离 OH- NO - Cl- SO2- S2- SO2- CO2- SiO2- PO3-
离 子 3 4 3 3 3 4
子
H+ 溶、挥 溶、挥 溶 溶、挥 溶、挥 溶、挥 微 溶
NH+ 溶、挥 溶 溶 溶 溶 溶 溶 溶 溶
4
K+ 溶 溶 溶 溶 溶 溶 溶 溶 溶
Na+ 溶 溶 溶 溶 溶 溶 溶 溶 溶
Ba2+ 溶 溶 溶 不 - 不 不 不 不
Ca2+ 微 溶 溶 微 - 不 不 不 不
Mg2+ 不 溶 溶 溶 - 微 微 不 不
Al3+ 不 溶 溶 溶 - - - 不 不
Mn2+ 不 溶 溶 溶 不 不 不 不 不
Zn2+ 不 溶 溶 溶 不 不 不 不 不
Cr3+ 不 溶 溶 溶 - - - 不 不
Fe2+ 不 溶 溶 溶 不 不 不 不 不
Fe3+ 不 溶 溶 溶 - - 不 不 不
Sn2+ 不 溶 溶 溶 不 - - - 不
Pb2+ 不 溶 微 不 不 不 不 不 不
Bi3+ 不 溶 - 溶 不 不 不 - 不
Cu2+ 不 溶 溶 溶 不 不 不 不 不
Hg+ - 溶 不 微 不 不 不 - 不
Hg2+ - 溶 溶 溶 不 不 不 - 不
Ag+ - 溶 不 微 不 不 不 不 不
说明:“溶”表示那种物质可溶于水,“不”表示不溶于水,“微”表示微溶于水,“挥”表
示挥发性,“-”表示那种物质不存在或遇到水就分解了。
96
第4章.p65 Page 96 2011.4.9, 10:41 PM Adobe PageMaker 6.5C/PPCⅤ 化学词汇英中文对照表
amount of substances 物质的量 isotope 同位素
anode 正极(阳极) litmus 石蕊
atom 原子 magnesium 镁
boiling point 沸点 melting point 熔点
bromine 溴 metallic bond 金属键
cathode 负极(阴极) molar volume of gas 气体摩尔体积
chemical bond 化学键 mole 摩尔
chemical energy 化学能 neutron 中子
chlorine 氯 oxidation reaction 氧化反应
covalent bond 共价键 oxidizing agent 氧化剂
crystalline hydrate 结晶水合物 phenolphthalein 酚酞
crystallize 结晶 polyvinyl chloride 聚氯乙烯
deliquescence 潮解 potassium 钾
density 密度 pressure 压强
deuterium 氘 primary battery 原电池
diamond 金刚石 proton 质子
dissolve 溶解 radioactivity 放射性
efflorescence 风化 rare gas 稀有气体
electrochemical power sources 化学电源 redox reaction 氧化还原反应
electrode 电极 reducing agent 还原剂
electron 电子 reduction reaction 还原反应
electronic formula 电子式 relative atomic mass 相对原子质量
element 元素、单质 silver bromide 溴化银
endothermic reaction 吸热反应 silver chloride 氯化银
exothermic reaction 放热反应 silver iodide 碘化银
ferric chloride 氯化铁 silver nitrate 硝酸银
fuel cell 燃料电池 sodium hydroxide 氢氧化钠
graphite 石墨 sodium hypochlorite 次氯酸钠
helium 氦 solar system model 行星模型
hydrated ion 水合离子 solute 溶质
hydrated molecule 水合分子 solution 溶液
hydrocarbon 碳氢化合物 solution equilibrium 溶解平衡
hydrochloric acid 盐酸 solvent 溶剂
hydrogen chloride 氯化氢 starch 淀粉
hypochloric acid 次氯酸 storage battery 蓄电池
iodine 碘 temperature 温度
ion 离子 thermo chemical equation 热化学方程式
ionic bond 离子键 tritium 氚
ionic compound 离子化合物 X-ray X射线
97
第4章.p65 Page 97 2011.4.9, 10:41 PM Adobe PageMaker 6.5C/PPC说 明
本册教材根据上海市中小学(幼儿园)课程改革委员会制定的课程
方案和《上海市中学化学课程标准(试行稿)》编写,供高中一年级第
一学期试用。
本教材由上海市长宁区教育局主持编写,经上海市中小学教材审查
委员会审查准予试用。
本册教材的编写人员有:
主编:姚子鹏 副主编:陈基福 洪东府
特约撰稿人:(按姓氏笔划为序)施永新 徐晓燕 高 清 解守宗
本教材经过四年试验后作重新修改。参加教材最后修订的除主编、
副主编外,还有陆惊帆、阮锦莲等。
欢迎广大师生来电来函指出教材的差错和不足,提出宝贵意见。上
海市中小学(幼儿园)课程改革委员会办公室地址:上海市陕西北路500
号(邮政编码:200041),联系电话:62560016(总机转)、52136338;出
版社电话:64089888。
声明 按照《中华人民共和国著作权法》第二十三条,关于“为
实施九年制义务教育和国家教育规划而编写出版教科书,除作者事先声
明不许使用的外,可以不经著作权人许可,在教科书中汇编已经发表的
作品片段或者短小的文字作品、音乐作品或单幅的美术作品、摄影作
品,但应当按照规定支付报酬,指明作者姓名、作品名称”的有关规定,
我们已尽量寻找原作者支付报酬。原作者如有关于支付报酬事宜可及时
与出版社联系。
99
第4章.p65 Page 99 2011.4.9, 10:41 PM Adobe PageMaker 6.5C/PPC责任编辑 黄金国
经上海市中小学教材审查委员会
整体设计 陈 蕾
审查准予试用 准用号 Ⅱ -GB-2006017
高级中学课本
化 学
高中一年级第一学期
(试用本)
上海市中小学(幼儿园)课程改革委员会
上海世纪出版股份有限公司
出版
上 海 科 学 技 术 出 版 社
(上海钦州南路71号,邮政编码200235)
上海新华书店发行 苏州望电印刷有限公司印刷
开本890×1240 1/16 印张6.5 字数 140 000
2007年7月第1版 2011年5月第5次印刷
ISBN 978-7-5323-8923-0/G.1945
定价:7.35元
上海市物价局价格审查批准文号:沪价商专(2007)12号
全国物价举报电话:12358 此书如有印、装质量问题,请径向本社调换
上海科学技术出版社电话:64089888