文档内容
绝密★考试结束前
2024 学年第二学期温州新力量联盟期末联考
高二化学学科 试题
命题学校:洞头一中 池景 崔广瑞 审题学校:六十一中 陈梦蕾
考生须知:
1.本卷共8页满分100分,考试时间90分钟。
2.答题前,在答题卷指定区域填写班级、姓名、考场号、座位号及准考证号并填涂相应数字。
3.所有答案必须写在答题纸上,写在试卷上无效。
4.考试结束后,只需上交答题纸。
5.可能用到的相对原子质量:H-1C-12N-14O-16F-19Na-23Si-28S-32Cl-35.5K-39Ca-40
Fe-56Cu-64I-127Ag-108
选择题部分
一、选择题(本大题共16小题,每小题3分,共48分,每小题列出的四个备选项中只有一个是
符合题目要求的,不选、多选、错选均不得分)
1.下列属于非极性分子的是
A.HCl B.NH C.CH D.H O
3 4 2 2
2.下列化学用语表示正确的是
A.基态S原子的电子排布式:2s22p4 B.H O中的中心原子的杂化轨道类型:sp3
2
C.乙醛的结构简式:CH COH D.CO 2-的空间结构:正四面体型
3 3
3. 化学与生产生活密切相关,下列说法不
.
正
.
确
.
的是
A.BaSO 不溶于水和酸,且不容易被X射线透过,医疗上可用于“钡餐”
4
B.Fe O 是一种红棕色粉末,可用作红色颜料
2 3
C.维生素C具有还原性,常用作食品中的防腐剂
D.聚丙烯酸钠具有大量亲水基团,是一种高吸水性树脂
4. 下列说法不
.
正
.
确
.
的是
A.第一电离能:N>O>C B.离子半径:Na+>Mg2+>Cl-
C.酸性:HClO >H SO D.化合物中离子键百分数:MgO>Al O
4 2 4 2 3
5. 下列说法不
.
正
.
确
.
的是
A.若苯酚不慎沾到皮肤上,先用NaOH溶液清洗,后用水清洗
B.中学实验室中可以将未用完的钠、钾、白磷等放回原试剂瓶
C.分液漏斗和容量瓶在使用前都要检查是否漏水
D.不慎误服重金属盐溶液,可立即大量食用蛋清或牛奶解毒
△
6. 金属铜与浓盐酸共热时可得到亚铜合三氯酸[H (CuCl )]: 2Cu+6HCl 2H (CuCl )+H ↑。下
2 3 ==== 2 3 2
列说法不正确的是
...
A.H (CuCl )中Cu的化合价+1
2 3
B.H 既是氧化产物,又是还原产物
2
C.HCl在反应中表现了氧化性和酸性
D.生成1molH (CuCl )转移电子的数目为1N
2 3 A
高二化学学科 试题 第1页(共8页)7.下列结构或性质内容不
.
能
.
说明对应用途的是
A.SO 有漂白性,工业上常用来漂白纸浆、毛、丝等
2
B.具有网状结构的交联橡胶弹性好、强度高,故可用作汽车轮胎
C.单晶硅为空间网状结构,可用作信息工业的半导体材料
D.聚四氟乙烯具有耐热、耐酸碱腐蚀的性能,故可用作家用不粘锅内侧涂层
8.下列方程式不
.
正
.
确
.
的是
A.向苯酚钠溶液中通入少量CO 气体:
2
B.NO 与H O反应:3NO +H O=2H++2NO -+NO
2 2 2 2 3
C.鸡蛋壳浸泡在醋酸溶液中:CaCO +2H+=Ca2++CO ↑+H O
3 2 2
D.将SO 通入酸性KMnO 溶液:5SO +2MnO -+2H O=5SO 2-+2Mn2++4H+
2 4 2 4 2 4
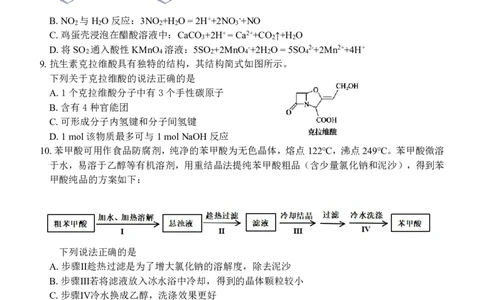
9.抗生素克拉维酸具有独特的结构,其结构简式如图所示。
下列关于克拉维酸的说法正确的是
A.1个克拉维酸分子中有3个手性碳原子
B.含有4种官能团
C.可形成分子内氢键和分子间氢键
D.1mol该物质最多可与1molNaOH反应
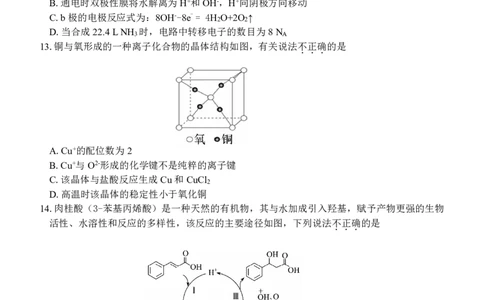
10.苯甲酸可用作食品防腐剂,纯净的苯甲酸为无色晶体,熔点122℃,沸点249℃。苯甲酸微溶
于水,易溶于乙醇等有机溶剂,用重结晶法提纯苯甲酸粗品(含少量氯化钠和泥沙),得到苯
甲酸纯品的方案如下:
下列说法正确的是
A.步骤Ⅱ趁热过滤是为了增大氯化钠的溶解度,除去泥沙
B.步骤Ⅲ若将滤液放入冰水浴中冷却,得到的晶体颗粒较小
C.步骤Ⅳ冷水换成乙醇,洗涤效果更好
D.步骤Ⅳ洗涤的时候需要用玻璃棒不断搅拌
11.下列说法正确的是
A.能够自发进行的反应一定是熵增的过程
B.2SO (g)+O (g) 2SO (g),压缩容器体积,平衡正移,则反应的平衡常数增大
2 2 3
C.CO(g)+H (g) C(s)+H O(g)△H<0,则正反应的活化能大于逆反应的活化能
2 2
D.[Cu(NH ) ]+(aq)+CO(g)+NH (g) [Cu(NH ) CO]+(aq),高压可提高CO的吸收率
3 2 3 3 3
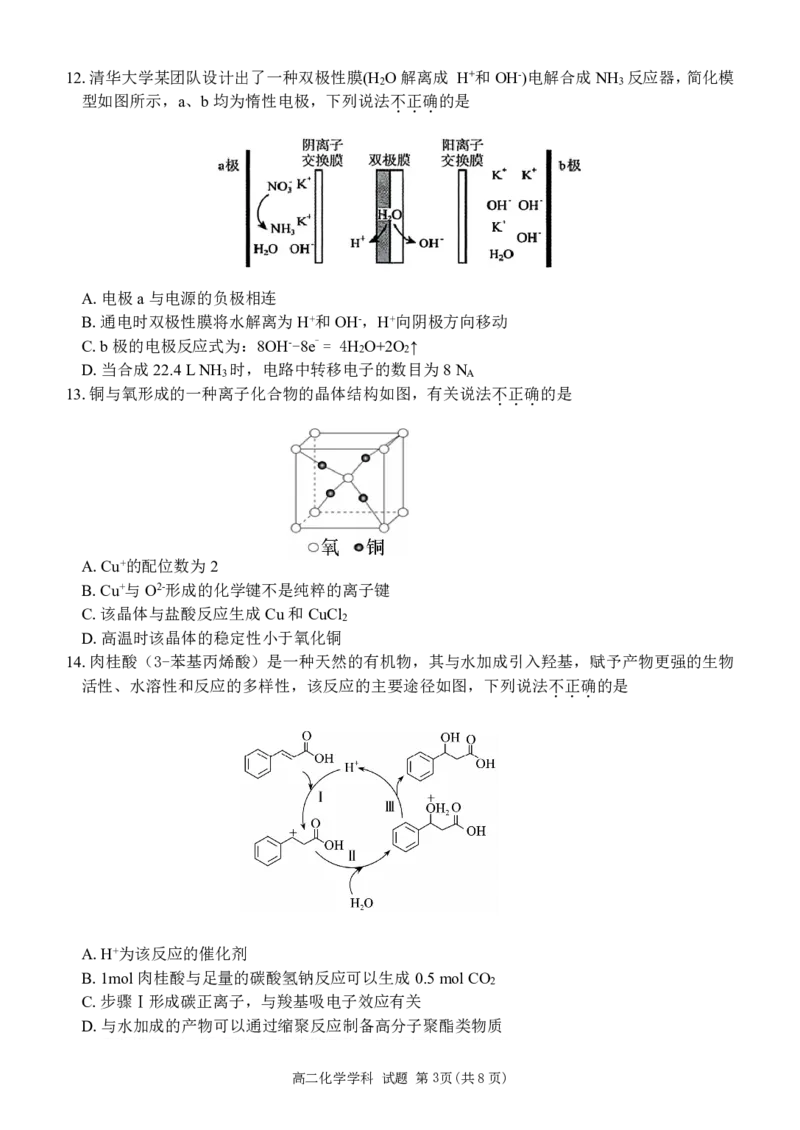
高二化学学科 试题 第2页(共8页)12.清华大学某团队设计出了一种双极性膜(H O解离成 H+和OH-)电解合成NH 反应器,简化模
2 3
型如图所示,a、b均为惰性电极,下列说法不
.
正
.
确
.
的是
A.电极a与电源的负极相连
B.通电时双极性膜将水解离为H+和OH-,H+向阴极方向移动
C.b极的电极反应式为:8OH--8e-= 4H O+2O ↑
2 2
D.当合成22.4LNH 时,电路中转移电子的数目为8N
3 A
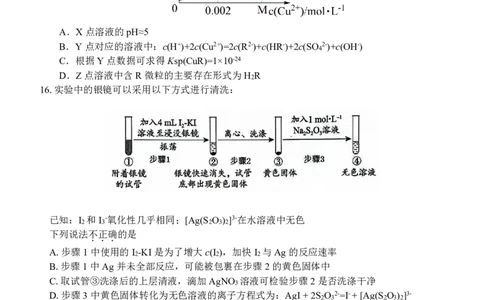
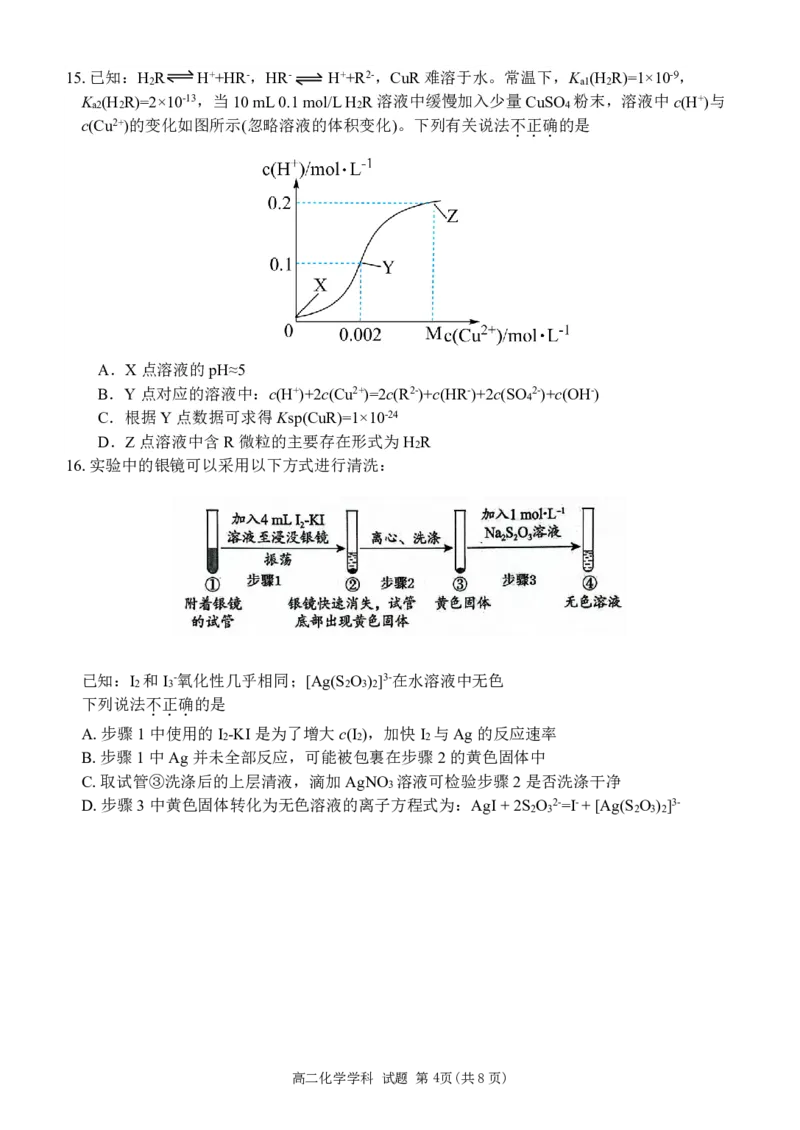
13.铜与氧形成的一种离子化合物的晶体结构如图,有关说法不
.
正
.
确
.
的是
A.Cu+的配位数为2
B.Cu+与O2-形成的化学键不是纯粹的离子键
C.该晶体与盐酸反应生成Cu和CuCl
2
D.高温时该晶体的稳定性小于氧化铜
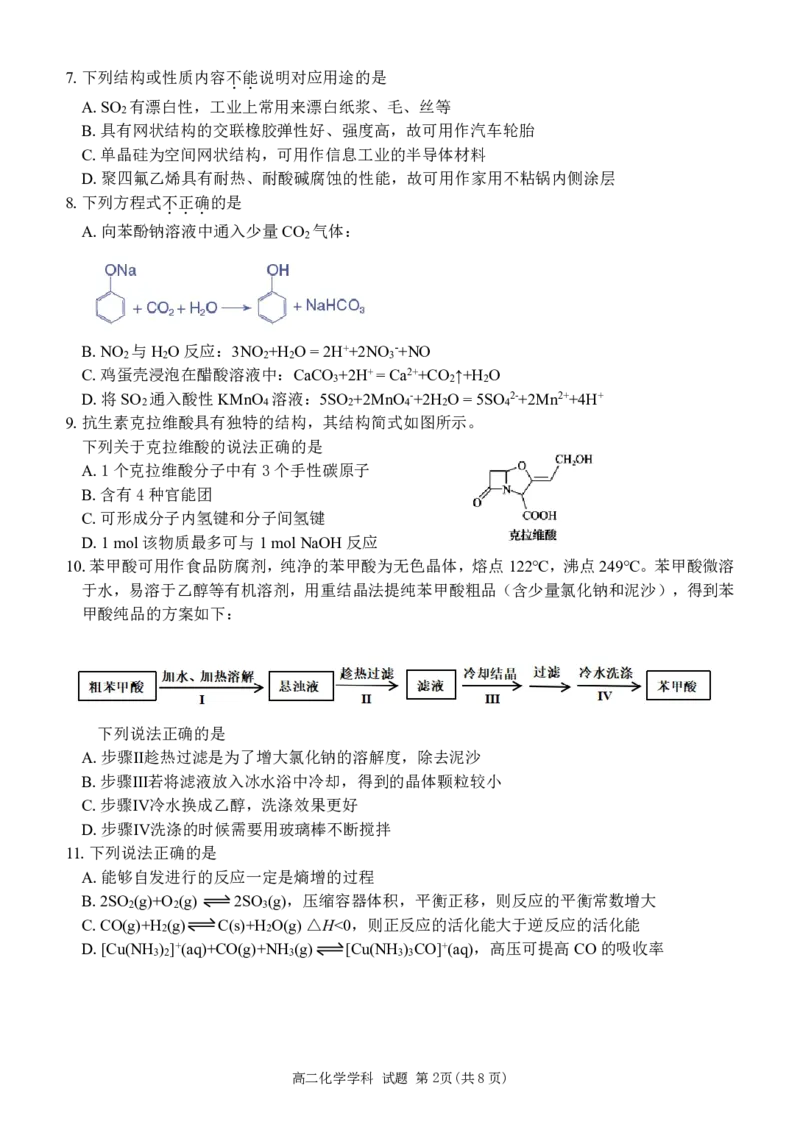
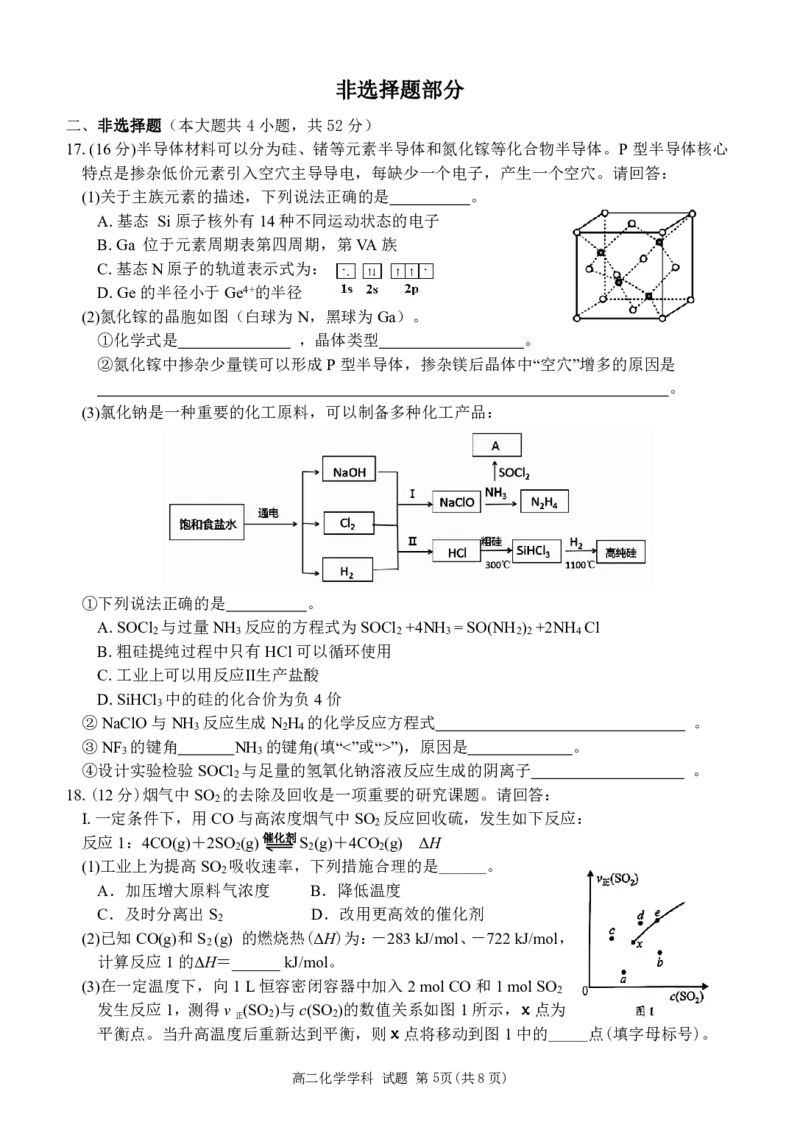
14.肉桂酸(3-苯基丙烯酸)是一种天然的有机物,其与水加成引入羟基,赋予产物更强的生物
活性、水溶性和反应的多样性,该反应的主要途径如图,下列说法不正确的是
...
A.H+为该反应的催化剂
B.1mol肉桂酸与足量的碳酸氢钠反应可以生成0.5molCO
2
C.步骤Ⅰ形成碳正离子,与羧基吸电子效应有关
D.与水加成的产物可以通过缩聚反应制备高分子聚酯类物质
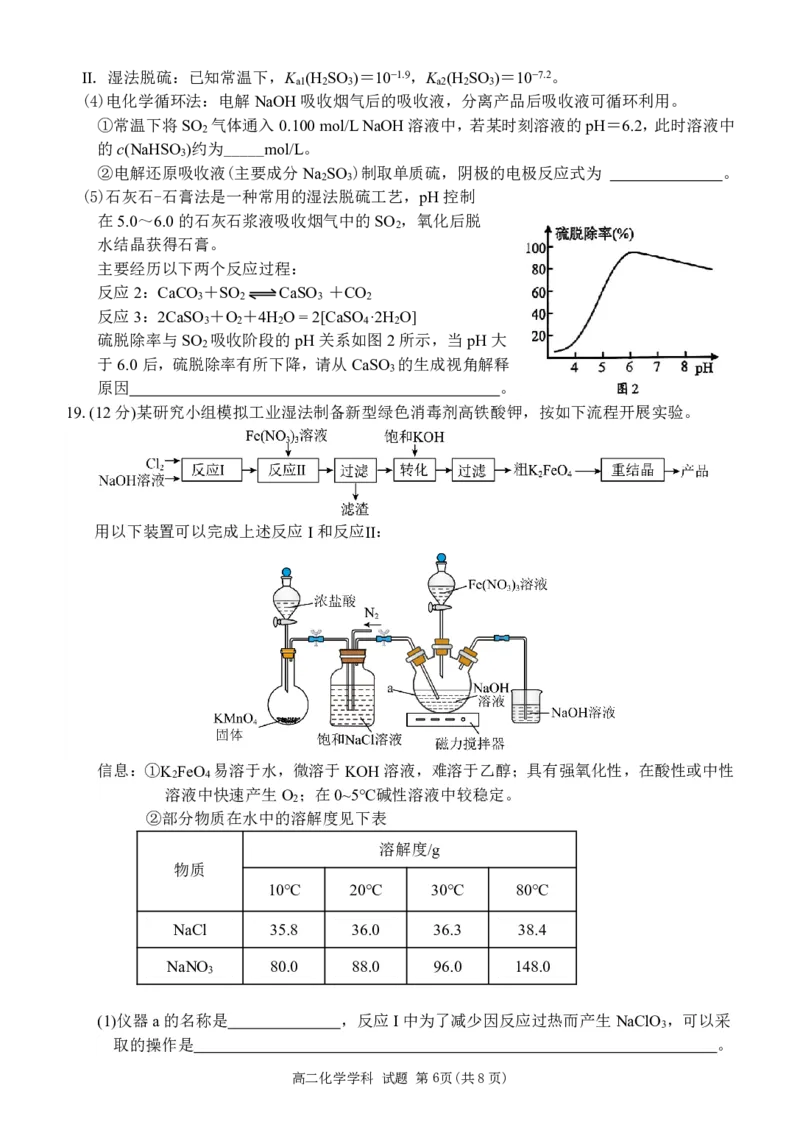
高二化学学科 试题 第3页(共8页)15.已知:H R H++HR-,HR- H++R2-,CuR难溶于水。常温下,K (H R)=1×10-9,
2 a1 2
K (H R)=2×10-13,当10mL0.1mol/LH R溶液中缓慢加入少量CuSO 粉末,溶液中c(H+)与
a2 2 2 4
c(Cu2+)的变化如图所示(忽略溶液的体积变化)。下列有关说法不
.
正
.
确
.
的是
A.X点溶液的pH≈5
B.Y点对应的溶液中:c(H+)+2c(Cu2+)=2c(R2-)+c(HR-)+2c(SO 2-)+c(OH-)
4
C.根据Y点数据可求得Ksp(CuR)=1×10-24
D.Z点溶液中含R微粒的主要存在形式为H R
2
16.实验中的银镜可以采用以下方式进行清洗:
已知:I 和I -氧化性几乎相同;[Ag(S O ) ]3-在水溶液中无色
2 3 2 3 2
下列说法不正确的是
...
A.步骤1中使用的I -KI是为了增大c(I ),加快I 与Ag的反应速率
2 2 2
B.步骤1中Ag并未全部反应,可能被包裏在步骤2的黄色固体中
C.取试管③洗涤后的上层清液,滴加AgNO 溶液可检验步骤2是否洗涤干净
3
D.步骤3中黄色固体转化为无色溶液的离子方程式为:AgI+2S O 2-=I-+[Ag(S O ) ]3-
2 3 2 3 2
高二化学学科 试题 第4页(共8页)非选择题部分
二、非选择题(本大题共4小题,共52分)
17.(16分)半导体材料可以分为硅、锗等元素半导体和氮化镓等化合物半导体。P型半导体核心
特点是掺杂低价元素引入空穴主导导电,每缺少一个电子,产生一个空穴。请回答:
(1)关于主族元素的描述,下列说法正确的是 。
A.基态 Si原子核外有14种不同运动状态的电子
B.Ga 位于元素周期表第四周期,第VA族
C.基态N原子的轨道表示式为:
D.Ge的半径小于Ge4+的半径
(2)氮化镓的晶胞如图(白球为N,黑球为Ga)。
①化学式是 ,晶体类型 。
②氮化镓中掺杂少量镁可以形成P型半导体,掺杂镁后晶体中“空穴”增多的原因是
。
(3)氯化钠是一种重要的化工原料,可以制备多种化工产品:
①下列说法正确的是 。
A.SOCl 与过量NH 反应的方程式为SOCl +4NH =SO(NH ) +2NH Cl
2 3 2 3 2 2 4
B.粗硅提纯过程中只有HCl可以循环使用
C.工业上可以用反应Ⅱ生产盐酸
D.SiHCl 中的硅的化合价为负4价
3
②NaClO与NH 反应生成N H 的化学反应方程式 。
3 2 4
③NF 的键角 NH 的键角(填“<”或“>”),原因是 。
3 3
④设计实验检验SOCl 与足量的氢氧化钠溶液反应生成的阴离子 。
2
18.(12分)烟气中SO 的去除及回收是一项重要的研究课题。请回答:
2
Ⅰ.一定条件下,用CO与高浓度烟气中SO 反应回收硫,发生如下反应:
2
反应1:4CO(g)+2SO (g) 催化剂 S (g)+4CO (g) ΔH
2 2 2
(1)工业上为提高SO 吸收速率,下列措施合理的是______。
2
A.加压增大原料气浓度 B.降低温度
C.及时分离出S D.改用更高效的催化剂
2
(2)已知CO(g)和S (g) 的燃烧热(ΔH)为:-283kJ/mol、-722kJ/mol,
2
计算反应1的ΔH=______kJ/mol。
(3)在一定温度下,向1L恒容密闭容器中加入2molCO和1molSO
2
发生反应1,测得v (SO )与c(SO )的数值关系如图1所示,χ点为
正 2 2
平衡点。当升高温度后重新达到平衡,则χ点将移动到图1中的_____点(填字母标号)。
高二化学学科 试题 第5页(共8页)Ⅱ.湿法脱硫:已知常温下,K (H SO )=10−1.9,K (H SO )=10−7.2。
a1 2 3 a2 2 3
(4)电化学循环法:电解NaOH吸收烟气后的吸收液,分离产品后吸收液可循环利用。
①常温下将SO 气体通入0.100mol/LNaOH溶液中,若某时刻溶液的pH=6.2,此时溶液中
2
的c(NaHSO )约为_____mol/L。
3
②电解还原吸收液(主要成分Na SO )制取单质硫,阴极的电极反应式为 。
2 3
(5)石灰石-石膏法是一种常用的湿法脱硫工艺,pH控制
在5.0~6.0的石灰石浆液吸收烟气中的SO ,氧化后脱
2
水结晶获得石膏。
主要经历以下两个反应过程:
反应2:CaCO +SO CaSO +CO
3 2 3 2
反应3:2CaSO +O +4H O=2[CaSO ·2H O]
3 2 2 4 2
硫脱除率与SO 吸收阶段的pH关系如图2所示,当pH大
2
于6.0后,硫脱除率有所下降,请从CaSO 的生成视角解释
3
原因 。
19.(12分)某研究小组模拟工业湿法制备新型绿色消毒剂高铁酸钾,按如下流程开展实验。
用以下装置可以完成上述反应I和反应Ⅱ:
信息:①K FeO 易溶于水,微溶于KOH溶液,难溶于乙醇;具有强氧化性,在酸性或中性
2 4
溶液中快速产生O ;在0~5℃碱性溶液中较稳定。
2
②部分物质在水中的溶解度见下表
溶解度/g
物质
10℃ 20℃ 30℃ 80℃
NaCl 35.8 36.0 36.3 38.4
NaNO 80.0 88.0 96.0 148.0
3
(1)仪器a的名称是 ,反应I中为了减少因反应过热而产生NaClO ,可以采
3
取的操作是 。
高二化学学科 试题 第6页(共8页)(2)下列说法正确的是___________。
A.反应Ⅱ中为了加快反应速率,可进行搅拌与加热
B.反应Ⅱ结束后应通一段时间氮气,然后再拆下装置进行后续实验
C.加入饱和KOH溶液发生的是复分解反应
D.若用FeCl 溶液代替Fe(NO ) 溶液作铁源,K FeO 的产率和纯度都会降低
3 3 3 2 4
(3)为了提高纯度需要对粗产品进行重结晶操作,从下列选项中选出合理的操作并排
序: 。
( )→( )→( )→置于冰水浴中→( )→用乙醇洗涤→干燥→得产品
a.将粗产品溶于水 b.将粗产品溶于冷的稀KOH溶液 c.过滤取沉淀
d.过滤取滤液 e.蒸发浓缩,趁热过滤 f.加入饱和KOH溶液 g.冷却结晶
(4)测定产品的纯度(K FeO 的摩尔质量为Mg/mol)
2 4
称取ag左右碘化钾于碘量瓶中,加入100mL6molL1NaOH溶液和bg左右的固体氟化
钠,待溶解完毕;准确称取mg样品于碘量瓶中,待样品充分溶解后,加硫酸酸化至反应
完全;淀粉作指示剂,用cmol·L-1Na S O 标准溶液进行滴定,消耗标准液体积为VmL。
2 2 3
已知:FeO2IF FeF3I ,I S O2 IS O2(方程式未配平)
4 6 2 2 2 3 4 6
①本次实验测得K FeO 纯度为 ,然后重复上述过程,平行测试3次。
2 4
②实验过程中往往需要加入过量且比理论计算所需量过量2~3倍左右的KI,理由是(请写
出两点) 。
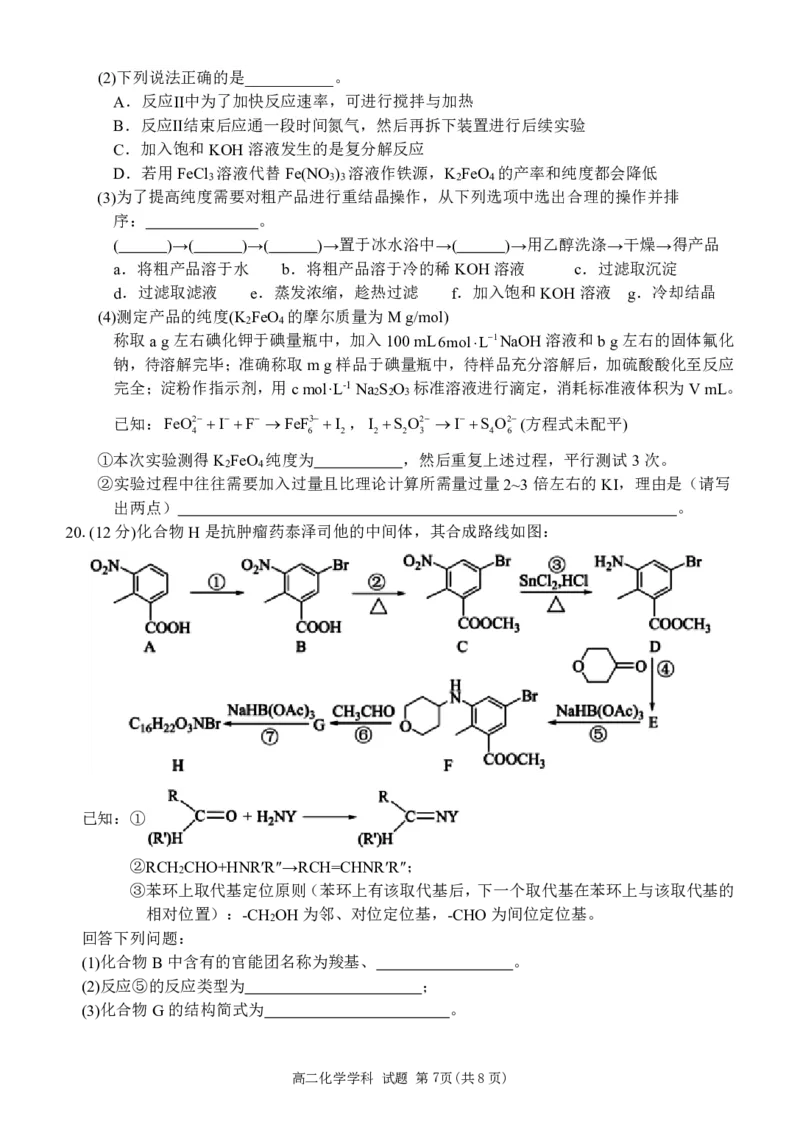
20.(12分)化合物H是抗肿瘤药泰泽司他的中间体,其合成路线如图:
已知:①
②RCH CHO+HNR′R″→RCH=CHNR′R″;
2
③苯环上取代基定位原则(苯环上有该取代基后,下一个取代基在苯环上与该取代基的
相对位置):-CH OH为邻、对位定位基,-CHO为间位定位基。
2
回答下列问题:
(1)化合物B中含有的官能团名称为羧基、 。
(2)反应⑤的反应类型为 ;
(3)化合物G的结构简式为 。
高二化学学科 试题 第7页(共8页)(4)满足下列条件的A的同分异构体的结构简式为 。
①含有苯环,且苯环上有5个取代基;②可发生银镜反应;③可与氯化铁溶液发生显色反应;
④核磁共振氢谱有4组峰,峰面积之比为1:2:2:2 。
(5)已知酯可以水解生成醇,也可以氨解生成醇,RCOOR′+NH →RCONH +R′OH。化合物 D
3 2
通过聚合反应可形成一种高分子,该反应的化学方程式为 。
(6)参照题干中的合成路线,设计以苯甲醇为主要原料,制备 的合成路线
(无机试剂任选)。
高二化学学科 试题 第8页(共8页)