文档内容
丽水市 2024 学年第二学期普通高中教学质量监控
高二化学试题卷
2025.06
本试题卷分选择题和非选择题两部分,共8页,满分100分,考试时间90分钟。
考生须知:
1.答题前,请务必将自己的姓名、准考证号用黑色字迹的签字笔或钢笔填写在答题纸规
定的位置上。
2.答题时,请按照答题纸上“注意事项”的要求,在答题纸相应的位置上规范作答,写在
本试题卷上的答案一律无效。
3.非选择题的答案必须用黑色字迹的签字笔或钢笔写在答题纸上相应区域内,作图时可先使用
2B铅笔,确定后必须使用黑色字迹的签字笔或钢笔描黑,答案写在本试题卷上无效。
4.可能用到的相对原子质量:H1 C12 N14 O16 Na23 S32 Cu64
选择题部分
一、选择题(本题包括20小题,1-10每小题2分,11-20每小题3分,共50分。每小题
只有一个选项符合题意)
1.材料是人类赖以生存和发展的物质基础,下列材料主要成分属于有机物的是
A. 生铁 B. 聚酰胺纤维 C. 光导纤维 D. 碳纤维
2.硫酸钡在医学上可被用作消化系统X射线检查的内服药剂,下列说法不
.
正
.
确
.
的是
A.BaSO 属于强电解质 B. 基态S原子最高能级的原子轨道形状为哑铃形
4
C.Ba元素位于p区 D.SO 2-的空间结构是正四面体形
4
3.下列表示不
.
正
.
确
.
的是
A.CO 的电子式: B. HCl中共价键的电子云图:
2
C.NH 的VSEPR模型: D. 的名称:2,4-二甲基己烷
3
4.下列物质的结构或性质比较不
.
正
.
确
.
的是
A. 水中的溶解度:SO >O >O B. 熔点:MgO>CaO>Ca(H PO )
2 3 2 2 4 2
C. 共价键的键能:F-F>Cl-Cl>Br-Br D. 键角:NO −>H O>H S
2 2 2
5.以乙烯为原料合成六元环状化合物D(C H O ),反应如下所示(部分试剂、产物及反应
4 8 2
条件略去),下列说法正确的是
A.B的密度小于水 B.1molC与足量Na反应可生成0.5molH
2
C.C→D的反应类型是消去反应 D.D的结构简式为
高二化学试题卷 第1页 共8页
{#{QQABSQy04wgQgEYACC4bQQEOCkmQkIGQLQoORUCYOAxLSIFABIA=}#}6.下列说法正确的是
A.16O 和18O 互为同素异形体
2 2
B.CHCHOOCCH 和CHCOOCH 是同一种物质
3 2 3 3 2 5
C. 甲酸与草酸互为同系物
D. 淀粉和纤维素互为同分异构体
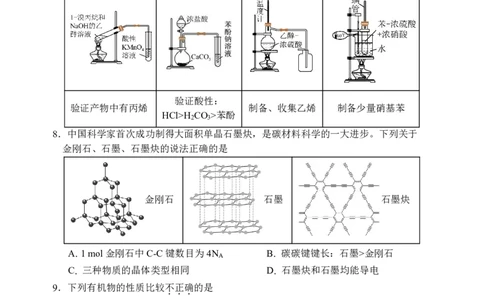
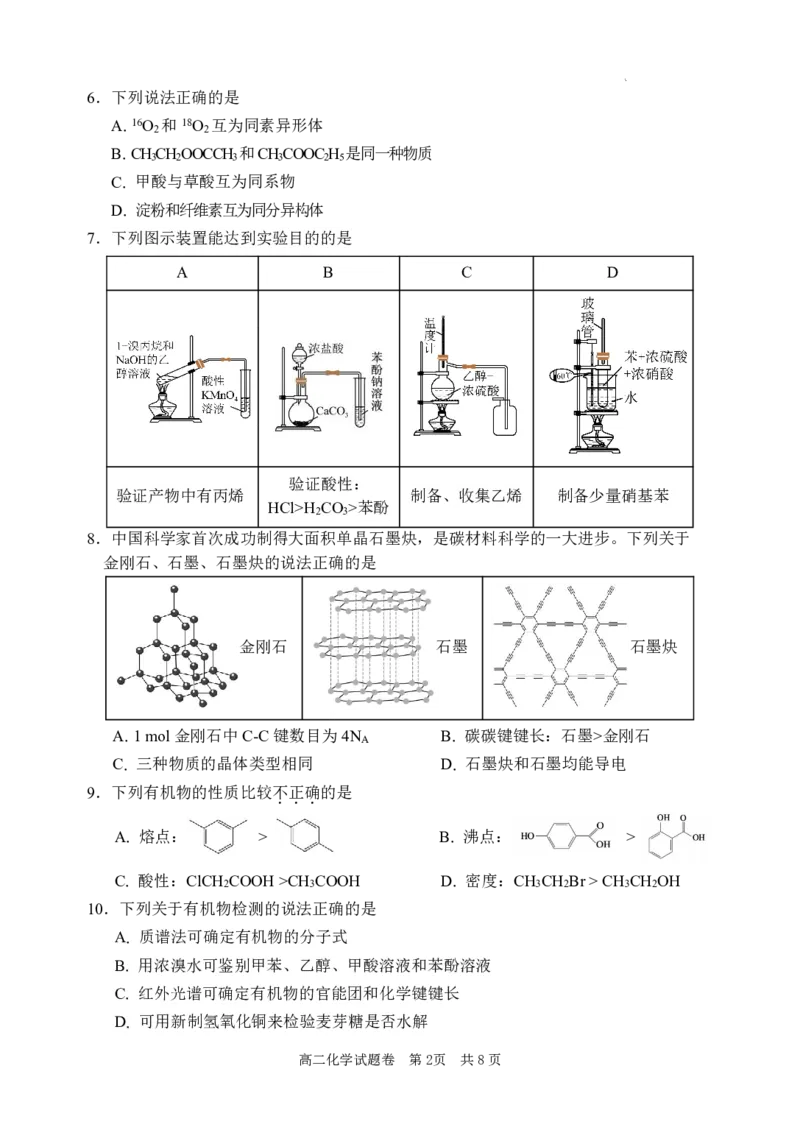
7.下列图示装置能达到实验目的的是
A B C D
验证酸性:
验证产物中有丙烯 制备、收集乙烯 制备少量硝基苯
HCl>H CO >苯酚
2 3
8.中国科学家首次成功制得大面积单晶石墨炔,是碳材料科学的一大进步。下列关于
金刚石、石墨、石墨炔的说法正确的是
金刚石 石墨 石墨炔
A.1mol金刚石中C-C键数目为4N B. 碳碳键键长:石墨>金刚石
A
C. 三种物质的晶体类型相同 D. 石墨炔和石墨均能导电
9.下列有机物的性质比较不
.
正
.
确
.
的是
A. 熔点: > B. 沸点: >
C. 酸性:ClCH COOH>CH COOH D. 密度:CH CH Br>CH CH OH
2 3 3 2 3 2
10.下列关于有机物检测的说法正确的是
A. 质谱法可确定有机物的分子式
B. 用浓溴水可鉴别甲苯、乙醇、甲酸溶液和苯酚溶液
C. 红外光谱可确定有机物的官能团和化学键键长
D. 可用新制氢氧化铜来检验麦芽糖是否水解
高二化学试题卷 第2页 共8页
{#{QQABSQy04wgQgEYACC4bQQEOCkmQkIGQLQoORUCYOAxLSIFABIA=}#}11.桂皮中的肉桂醛( )是一种食用香料,一种合成路线如下:
下列说法正确的是
A. 实验室制取CHCH时可用饱和NaCl溶液代替纯水以减小其反应速率
B. 物质M可发生银镜反应,向氨水中逐滴加入硝酸银溶液中即可配得银氨溶液
C. 肉桂醛分子中所有原子一定共平面
D. 向肉桂醛中滴加酸性高锰酸钾溶液,褪色则证明肉桂醛分子中含有碳碳双键
12.X、Y、Z、M四种短周期主族元素,原子序数依次增大,X原子半径最小,基态Y
原子最高能级的不同轨道都有电子且自旋方向相同,基态Z原子的s能级与p能级的
电子数相等,M原子有2个价电子。下列说法正确的是
A. 第一电离能:Z>Y
B. 简单离子的半径:M>Z
C.X、Y、Z元素形成的化合物均为共价化合物
D. 化学键中离子键成分的百分数:MZ>MX
2
13.下列说法正确的是
A. 酸性条件下,苯酚与甲醛反应生成网状结构的酚醛树脂
B. 油酸甘油酯属于高分子化合物,与碱反应称为皂化反应
C. 纤维素在一定条件下可与乙酸发生酯化反应得到醋酸纤维
D. 向鸡蛋清溶液中加入硝酸银溶液产生沉淀,加水后沉淀可溶解
14.有关脂肪烃的结构或性质说法正确的是
A. 乙炔、丙炔和2-丁炔分子中的碳原子均在同一条直线上,均能发生加成反应
B.2-甲基-2-丁烯存在顺反异构体,它们的化学性质和物理性质基本相同
C. 丙烯能使酸性KMnO 溶液、溴水褪色,反应类型相同
4
D. 直链烷烃分子中的碳原子在一条直线上,既含有极性键又含有非极性键
15.某实验小组提取青蒿素的实验流程如图。青蒿素为无色针状晶体,熔点156~157℃,
易溶于丙酮、氯仿和乙醚,在水中几乎不溶。
下列说法不正确的是
...
A. 粉碎的目的是增大青蒿与乙醚的接触面积,提高浸取率
B. 操作Ⅰ加入乙醚,操作Ⅱ分离出乙醚,乙醚起催化剂作用
C. 操作Ⅱ中提取液经过蒸馏后可得青蒿素粗品
D. 操作Ⅲ中提高固体青蒿素的纯度一般采用重结晶法
高二化学试题卷 第3页 共8页
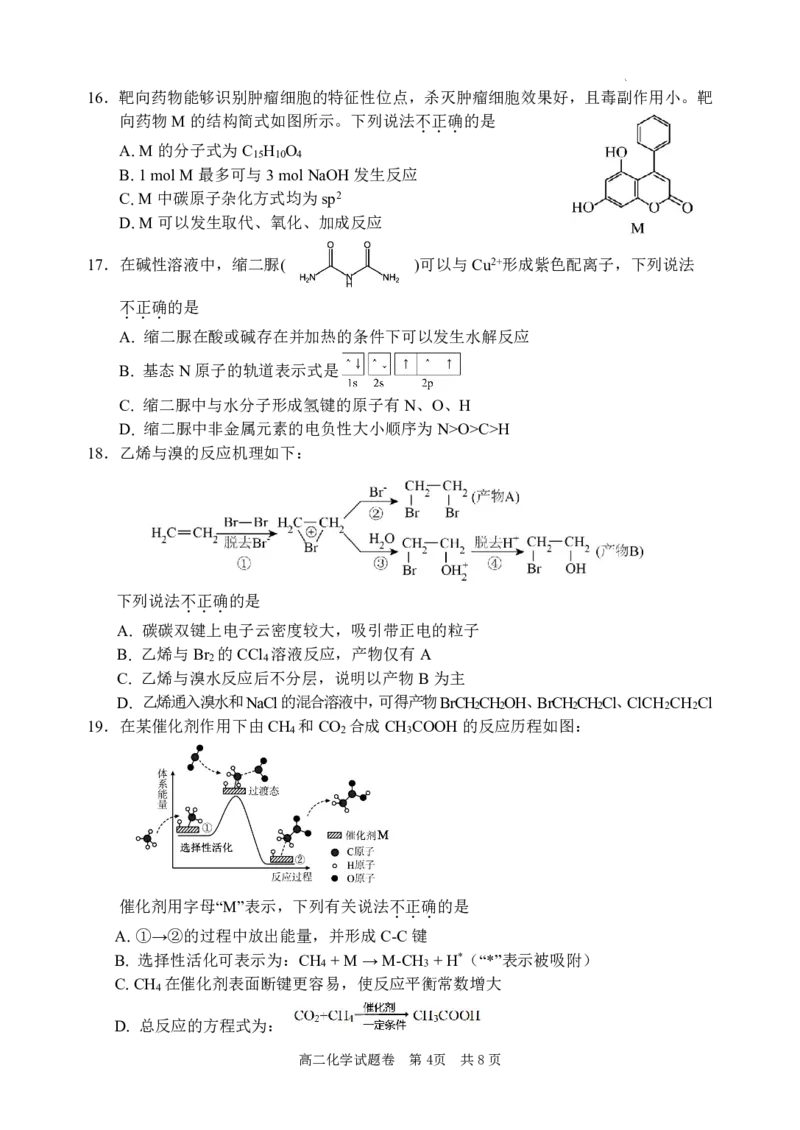
{#{QQABSQy04wgQgEYACC4bQQEOCkmQkIGQLQoORUCYOAxLSIFABIA=}#}16.靶向药物能够识别肿瘤细胞的特征性位点,杀灭肿瘤细胞效果好,且毒副作用小。靶
向药物M的结构简式如图所示。下列说法不
.
正
.
确
.
的是
A.M的分子式为C H O
15 10 4
B.1molM最多可与3molNaOH发生反应
C.M中碳原子杂化方式均为sp2
D.M可以发生取代、氧化、加成反应
17.在碱性溶液中,缩二脲( )可以与Cu2+形成紫色配离子,下列说法
不正确的是
...
A. 缩二脲在酸或碱存在并加热的条件下可以发生水解反应
B. 基态N原子的轨道表示式是
C. 缩二脲中与水分子形成氢键的原子有N、O、H
D. 缩二脲中非金属元素的电负性大小顺序为N>O>C>H
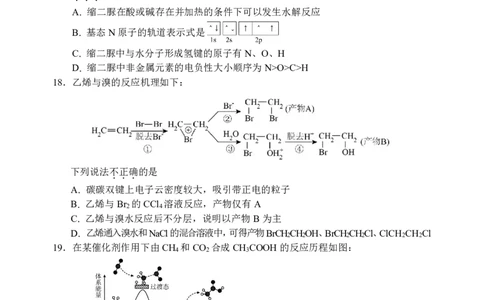
18.乙烯与溴的反应机理如下:
下列说法不正确的是
...
A. 碳碳双键上电子云密度较大,吸引带正电的粒子
B. 乙烯与Br 的CCl 溶液反应,产物仅有A
2 4
C. 乙烯与溴水反应后不分层,说明以产物B为主
D. 乙烯通入溴水和NaCl的混合溶液中,可得产物BrCHCHOH、BrCHCHCl、ClCH CH Cl
2 2 2 2 2 2
19.在某催化剂作用下由CH 和CO 合成CH COOH的反应历程如图:
4 2 3
催化剂用字母“M”表示,下列有关说法不
.
正
.
确
.
的是
A.①→②的过程中放出能量,并形成C-C键
B. 选择性活化可表示为:CH +M→M-CH +H*(“*”表示被吸附)
4 3
C.CH 在催化剂表面断键更容易,使反应平衡常数增大
4
D. 总反应的方程式为:
高二化学试题卷 第4页 共8页
{#{QQABSQy04wgQgEYACC4bQQEOCkmQkIGQLQoORUCYOAxLSIFABIA=}#}20.下列实验探究方案不能达到探究目的的是
探究方案 探究目的
向2支分别盛有2mL苯和2mL甲苯的试管中各加入几滴酸 探究有机物中基团
A
性高锰酸钾溶液,用力振荡,观察现象 间的相互作用
用pH计测0.1mol/LCH COONa溶液与0.1mol/LNaCN溶液,K (CH COOH)>
3 a 3
B
得pH分别为8.9、11.1 K (HCN)
a
向试管中滴入几滴1﹣溴丁烷,再加入2mL5%NaOH溶液, 检验1﹣溴丁烷中
C 振荡后加热,反应一段时间后停止加热,静置。取数滴水层 的溴元素
溶液于试管中,加入几滴2%AgNO 溶液,观察现象
3
以Zn、Fe为电极,以酸化的3%NaCl溶液作电解质溶液,连探究牺牲阳极的阴
D 接成原电池装置。过一段时间,从Fe电极区域取少量溶液于 极保护法
试管中,再向试管中滴入2滴K [Fe(CN) ]溶液,观察现象
3 6
非选择题部分
二、非选择题(本题包括5小题,共50分)
21.(8分)某粗品CCl 中溶有一定量的CS ,试剂a为KOH、H O和CH CH OH混合液,
4 2 2 3 2
用于除去CS 。制备干燥纯净的CCl 的流程如图所示:
2 4
(1)从分子结构角度解释CS 能溶于CCl 的原因是 ▲ 。
2 4
(2)步骤ⅱ的目的是除去CCl 中的大量乙醇,该步骤用到的分离提纯方法是 ▲ 。
4
(3)步骤ⅲ中,CaCl 中的Ca2+可以与H O、乙醇形成配位键,其中配原子是 ▲ 。
2 2
(4)常温下CCl 与H O几乎不反应,SiCl 遇H O迅速反应生成H SiO 和HCl,请从原
4 2 4 2 4 4
子结构和化学键的角度解释SiCl 易水解的原因 ▲ 。
4
22.(10分)元素周期表中的四种元素A、B、E、F,原子序数依次增大。A的基态原子价
层电子排布为nsnnpn;B的基态原子2p能级有3个单电子;E2+的3d轨道中有10个电
子;F单质在金属活动性顺序中排在最末位。
(1)写出基态E原子的价层电子排布式 ▲ 。
(2)AB形成的AB-常作为配位化合物中的配体,下列说法不 . 正 . 确 . 的是 ▲ 。
A.AB-与F+形成配位键时,A原子的配位能力强于B原子
B.E(AB) 2-中E的配位数为4,1mol该离子中σ键与π键的数目之比为1:1
4
C.A单质的熔点一定大于同族其他元素的单质
D.A与氧元素1:1形成的化合物,其在水中的溶解度大于B的单质B
2
(3)B元素的两种氢化物BH 和B H ,碱性更弱的是 ▲
3 2 4
(写化学式),理由是 ▲ 。
(4)A元素的某种氧化物的晶胞如图所示。
该氧化物在晶胞中的配位数为 ▲ ;
冰的配位数小于该晶体,试解释原因 ▲
高二化学试题卷 第5页 共8页
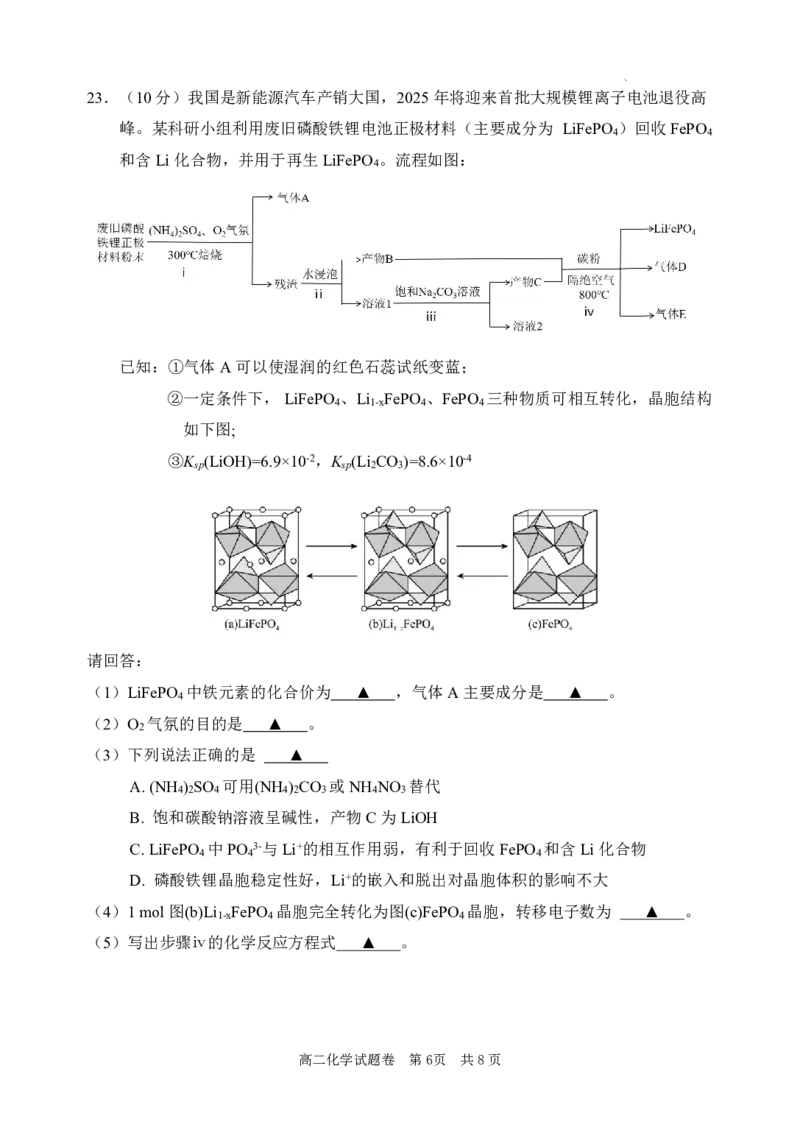
{#{QQABSQy04wgQgEYACC4bQQEOCkmQkIGQLQoORUCYOAxLSIFABIA=}#}23.(10分)我国是新能源汽车产销大国,2025年将迎来首批大规模锂离子电池退役高
峰。某科研小组利用废旧磷酸铁锂电池正极材料(主要成分为 LiFePO )回收FePO
4 4
和含Li化合物,并用于再生LiFePO 。流程如图:
4
已知:①气体A可以使湿润的红色石蕊试纸变蓝;
②一定条件下,LiFePO 、Li FePO 、FePO 三种物质可相互转化,晶胞结构
4 1-x 4 4
如下图;
③K (LiOH)=6.9×10-2,K (Li CO )=8.6×10-4
sp sp 2 3
请回答:
(1)LiFePO 中铁元素的化合价为 ▲ ,气体A主要成分是 ▲ 。
4
(2)O 气氛的目的是 ▲ 。
2
(3)下列说法正确的是 ▲
A.(NH ) SO 可用(NH ) CO 或NH NO 替代
4 2 4 4 2 3 4 3
B. 饱和碳酸钠溶液呈碱性,产物C为LiOH
C.LiFePO 中PO 3-与Li+的相互作用弱,有利于回收FePO 和含Li化合物
4 4 4
D. 磷酸铁锂晶胞稳定性好,Li+的嵌入和脱出对晶胞体积的影响不大
(4)1mol图(b)Li FePO 晶胞完全转化为图(c)FePO 晶胞,转移电子数为 ▲ 。
1-x 4 4
(5)写出步骤ⅳ的化学反应方程式 ▲ 。
高二化学试题卷 第6页 共8页
{#{QQABSQy04wgQgEYACC4bQQEOCkmQkIGQLQoORUCYOAxLSIFABIA=}#}24.(10分)为探究铜片在不同试剂中的“溶解”,某小组进行如下4组实验:
实验 铜片
试剂及用量 现象
编号 质量/g
30%H O 50mL、 10h后,溶液变为浅蓝色,铜片表面附着蓝
1号 0.5 2 2
蒸馏水8mL 色沉淀
开始铜片表面有气泡生成(先慢后快),40min
30%H O 50mL、
2号 0.5 2 2 后,形成明显的蓝色CuSO 溶液,铜片表面
4
5mol·L-1H SO 8mL
2 4 光亮
30%H O 50mL、 立即产生大量气泡,形成深蓝色溶液,铜片
3号 0.5 2 2
5mol·L-1氨水8mL 表面附着少量蓝色沉淀
30%H O 50mL、
2 2 立即产生大量气泡,形成深蓝色溶液,铜片
4号 0.5 5mol·L-1氨水8mL
表面仍光亮
和适量试剂X
请回答:
(1)1号实验和3号实验中蓝色沉淀成分的化学式可能是 ▲ 。
(2)下列有关说法正确的是 ▲ 。
A.2号实验相比1号实验反应快,是因为H SO 溶液溶解了蓝色沉淀
2 4
B.2号实验中产生气泡先慢后快,可推测生成物Cu2+可以催化H O 分解产生O
2 2 2
C. 往深蓝色溶液中滴加适量蒸馏水,并用玻璃棒摩擦试管内壁,能得到深蓝色的晶体
D.4号实验相比3号实验反应快,是因为加入了试剂X,它可能是(NH ) SO 固体
4 2 4
(3)相比 2 号实验,3 号和 4 号实验铜片“溶解”更快且均得到深蓝色溶液,原因是
▲ (用化学方程式表示)
(4)为测定铜氨溶液中铜元素的含量,可采用如下方法:
i.移取500mL铜氨溶液于锥形瓶中,滴加稀H SO ,调节溶液的pH为3-4
2 4
ⅱ.加入适当过量的KI溶液,并加入3mL0.5%淀粉溶液(2Cu2++4I-=2CuI+I );
2
ⅲ.用0.1000mol·L-1Na S O 标准溶液滴定至终点,消耗标准液体积为5.80mL
2 2 3
(I +2S O 2-=2I-+S O 2-)。
2 2 3 4 6
①iii中滴定至终点时,溶液的颜色变化为 ▲ 。
②该铜氨溶液中铜元素的含量为 ▲ g·mL-1(保留两位有效数字)。
高二化学试题卷 第7页 共8页
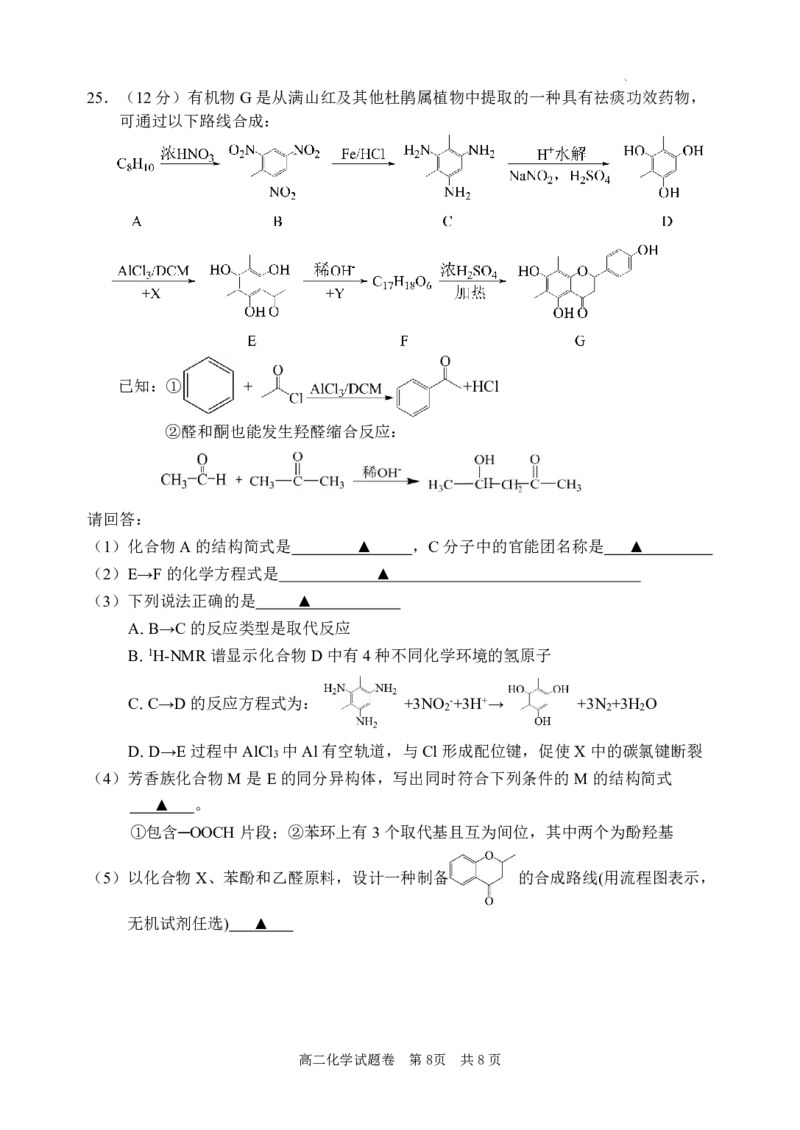
{#{QQABSQy04wgQgEYACC4bQQEOCkmQkIGQLQoORUCYOAxLSIFABIA=}#}25.(12分)有机物G是从满山红及其他杜鹃属植物中提取的一种具有祛痰功效药物,
可通过以下路线合成:
已知:① + +HCl
②醛和酮也能发生羟醛缩合反应:
请回答:
(1)化合物A的结构简式是 ▲ ,C分子中的官能团名称是 ▲
(2)E→F的化学方程式是 ▲
(3)下列说法正确的是 ▲
A.B→C的反应类型是取代反应
B.1H-NMR谱显示化合物D中有4种不同化学环境的氢原子
C.C→D的反应方程式为: +3NO -+3H+→ +3N +3H O
2 2 2
D.D→E过程中AlCl 中Al有空轨道,与Cl形成配位键,促使X中的碳氯键断裂
3
(4)芳香族化合物M是E的同分异构体,写出同时符合下列条件的M的结构简式
▲ 。
①包含─OOCH片段;②苯环上有3个取代基且互为间位,其中两个为酚羟基
(5)以化合物X、苯酚和乙醛原料,设计一种制备 的合成路线(用流程图表示,
无机试剂任选) ▲
高二化学试题卷 第8页 共8页
{#{QQABSQy04wgQgEYACC4bQQEOCkmQkIGQLQoORUCYOAxLSIFABIA=}#}