文档内容
2025年5月高三适应性训练 (一)
化 学 试 卷
(本试卷满分100分,考试时间75分钟)
注意事项:
1.答卷前,考生务必将自己的姓名、 准考证号填写清楚,将条形码准确粘贴在条形码区域内。
2.选择题必须使用2B铅笔填涂; 非选择题必须使用0.5毫米黑色字迹的签字笔书写,字体工整、 笔迹清楚。
3.请按照题号顺序在各题目的答题区域内作答,超出答题区书写的答案无效; 在草稿纸、 试题卷上答题无效 。
4.保持卡面清洁,不要折叠、 不要弄破、 弄皱,不准使用涂改液、 修正带、 刮纸刀 。
可能用到的相对原子质量:H-1 C-12 O-16 N-14 Na-23 Cl-35.5 Fe-56 Ru-101
一、 选择题: 本题共14小题,每小题3分,共42分。 在每小题给出的四个选项中,只有一项是符合题目要求的。
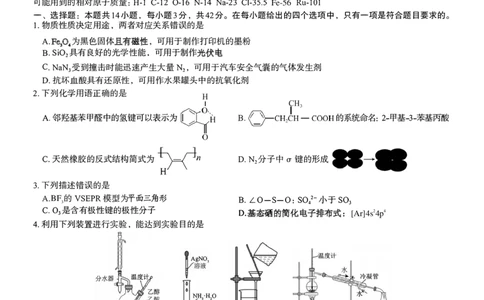
1.物质性质决定用途,两者对应关系错误的是
A.FeO为黑色固体且有磁性,可用于制作打印机的墨粉
3 4
B.SiO₂具有良好的光学性能,可用于制作光伏电
C.NaN₃受到撞击时能迅速产生大量N₂,可用于汽车安全气囊的气体发生剂
D.抗坏血酸具有还原性,可用作水果罐头中的抗氧化剂
2.下列化学用语正确的是
A.邻羟基苯甲醛中的氢键可以表示为 B. 的系统命名: 2-甲基-3-苯基丙酸
C.天然橡胶的反式结构简式为 D.N₂分子中σ键的形成
3.下列描述错误的是
A.BF的VSEPR模型为平面三角形 B.∠O-S-O:SO²-小于SO₃
3
C.O₃是含有极性键的极性分子
D.基态硒的简化电子排布式: [Ar]4s24p4
4.利用下列装置进行实验,能达到实验目的是
另
AgNO 温度计
溶液₃
水
分水器 温度i计p 冷凝管
乙醇 NH HO 水
乙酸
₃
浓硫酸
⑤
电磁加热搅拌器
① ② ③ ④
A.①制备乙酸乙酯并提高产率 B.②配制银氨溶液
C.③分离乙酸乙酯中的乙酸、 乙醇 D.④分离苯和硝基苯的混合物
5.一种药物的重要中间体的合成方法如图。 下列说法正确的是
第 1 页 共6页A.Y分子中碳原子的杂化类型有sp²、 sp³两种
B.X与稀硫酸反应只有一个官能团发生变化
C.Y分子中所有原子可能共面
D.X和氢气完全加成后的分子中有3个手性碳
6.已知:碳酸的Ka=4.5×10-7,Ka=4.7×10-11;次氯酸的Ka=4.0×10-8。下列指定反应的离子方程式正确的是
1 2 1
A.CO 通入足量的NaClIO溶液中 : CO +2CIO+H O=2HClO+CO 3
₂ ₂ ₂
B.用惰性电极电解CuCl₂水溶液:
C.用Na,SO,溶液吸收少量Cl₂: 3SO³+Cl₂+H₂O=2HSO3+2Cr+
D.用高锰酸钾标准溶液滴定草酸: 2MnO7+5C₂O}+16H'=2Mn²+10CO₂↑+8H,O
7.华为最新研发了一种高效含硫化合物固态电池,充电快速又安全。 该含硫化合物的结构如下图所示, 已知X、
Y、 Z、 L、 M、 R为短周期主族元素,原子序数依次递增,X的
单质保存在固态石蜡中,L与R同族。 下列说法正确的是
A.氢化物的沸点:Y H L
₂ ₂
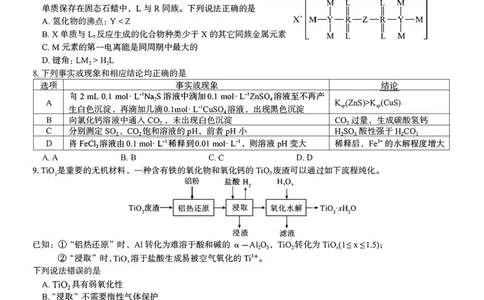
8.下列事实或现象和相应结论均正确的是
选项 事实或现象 结论
向2 mL0.1 mol·L Na.S溶液中滴加0.1 mol·L'ZnSO₂溶液至不再产 n
A K ( Z S)>K (CuS)
生白色沉淀,再滴加几滴0.1mol:L-CuSO,溶液,出现黑色沉淀
₉ ₉
B 向氯化钙溶液中通入CO₂,未出现白色沉淀 CO₂过量,生成碳酸氢钙
C 分别测定SO₂、CO₂饱和溶液的pH,前者pH小 H SO 酸性强于H CO
D 将FeCl,溶液由0.1 mol·L¹稀释到0.01 mol·L',则溶液pH变大 稀 ₂ 释后 ₃ ,Fe*的水 ₂ 解程 ₃ 度增大
A.A B.B c.C D.D
9.TiO是重要的无机材料,一种含有铁的氧化物和氧化钙的TiO₂废渣可以通过如下流程纯化。
2
铝粉 盐酸且, H O
₂ ₂
o
Ti 废渣一 铝热还原 浸取 氧化水解 →TiO xH O
₂ ₂ ₂
浸渣 滤液
已知: ① “铝热还原”时,Al转化为难溶于酸和碱的 α-Al₂O₃,TiO₂转化为TiO,(1≤x≤1.5);
②“浸取”时,TiO,溶于盐酸生成易被空气氧化的T²+。
下列说法错误的是
A.TiO₂具有弱氧化性
B.“浸取”不需要惰性气体保护
C.“氧化水解”过程中为加快反应速率并使氧化完全,应快速加入过量的H₂O₂
D.H₂可能来自 Fe、 过量铝粉及Ti2+与盐酸的反应
10.段镶锋教授深入研究了锂硫电池中复杂的硫还原反应进程,研究结果表明Li-S电池中涉及的多硫化物转化反
应,下图展示了电池中硫还原反应的示意图(左侧为嵌入S₆的碳纳米管,右侧为Li), 涉及从S6分子到Li,s
固体的复杂的16电子转化过程。
已知: ①S6为淡黄色固体;多硫化物溶液的颜色随着S²中x的增多,颜色由黄色变深直至红色;
②Li₂S的水溶性较差。 下列说法错误的是
A.图示电池总反应为 : 16Li+S =8Li,s
₈
B.Li₂S₄是控制整体硫还原反应过程的关键电化学中间体
C.选择合适的溶剂能让电池保持稳定的电流输出
D.充电时,正极附近颜色由红色变到黄色最后变成无色
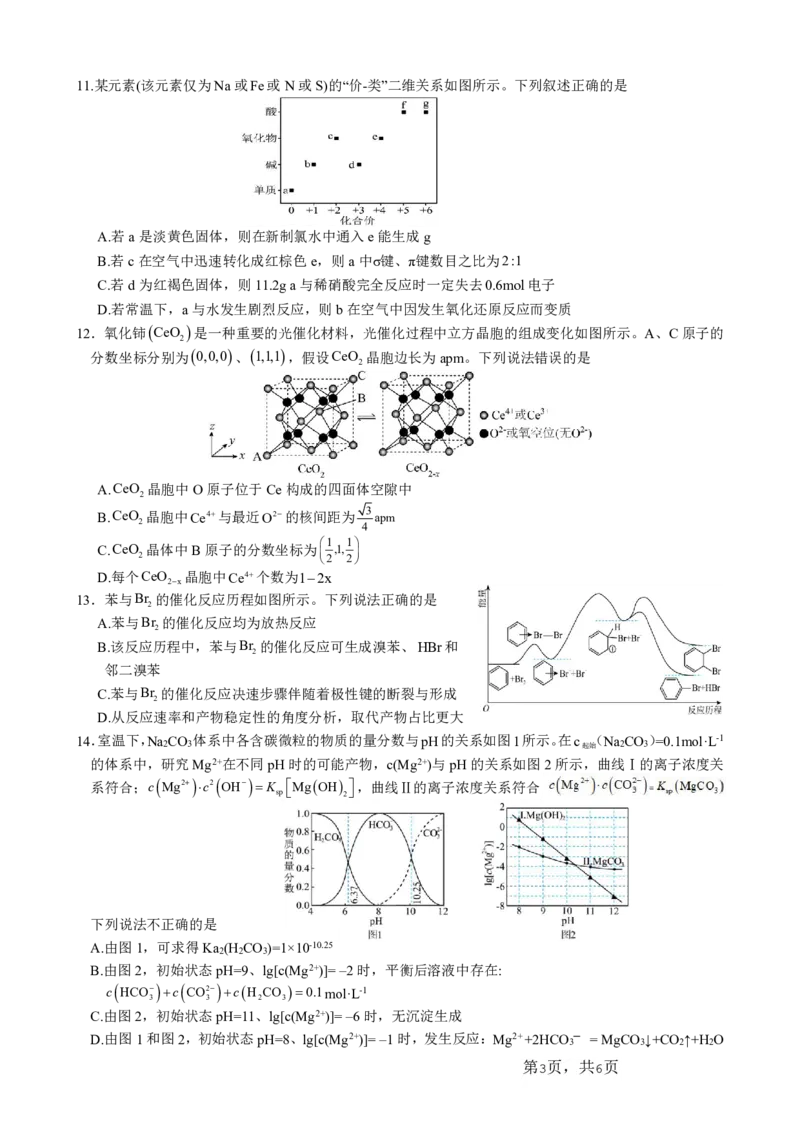
第 2页 共 6页11.某元素(该元素仅为Na或Fe或N或S)的“价-类”二维关系如图所示。下列叙述正确的是
A.若a是淡黄色固体,则在新制氯水中通入e能生成g
B.若c在空气中迅速转化成红棕色e,则a中σ键、π键数目之比为2:1
C.若d为红褐色固体,则11.2ga与稀硝酸完全反应时一定失去0.6mol电子
D.若常温下,a与水发生剧烈反应,则b在空气中因发生氧化还原反应而变质
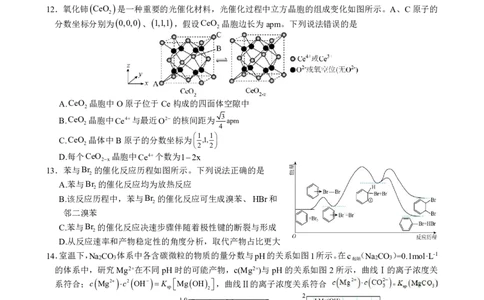
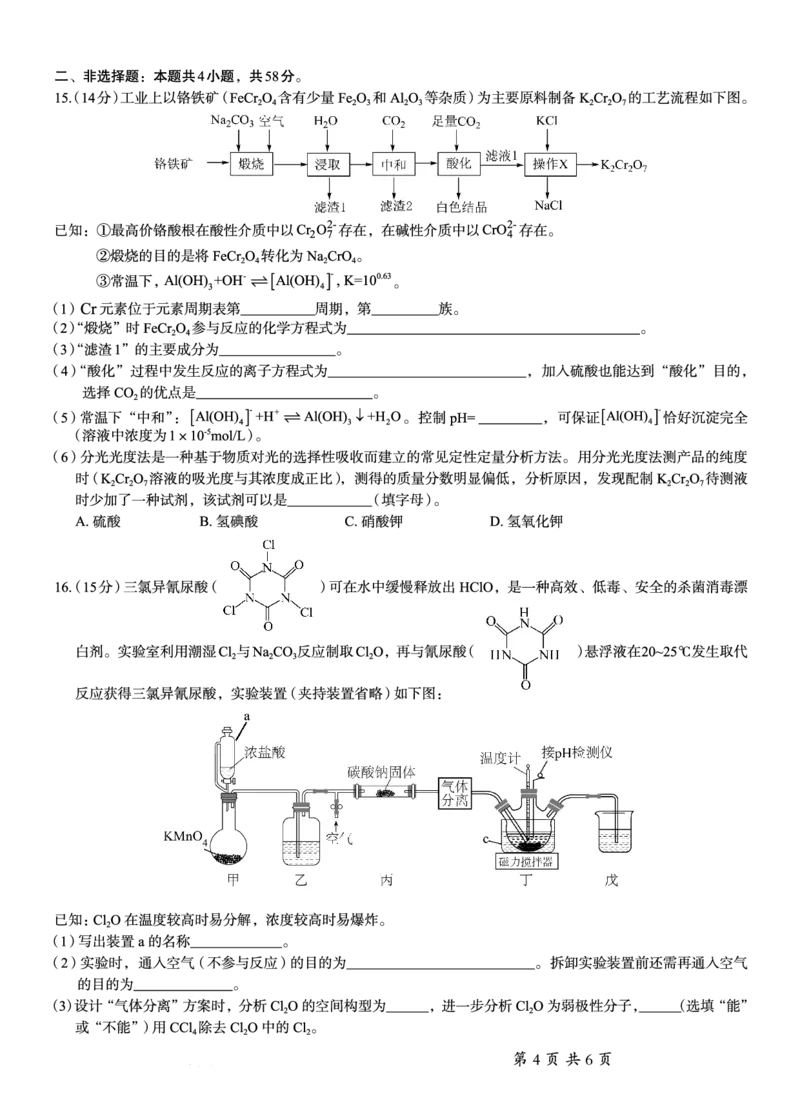
12.氧化铈CeO 是一种重要的光催化材料,光催化过程中立方晶胞的组成变化如图所示。A、C原子的
2
分数坐标分别为0,0,0、1,1,1,假设CeO 晶胞边长为apm。下列说法错误的是
2
A.CeO 晶胞中O原子位于Ce构成的四面体空隙中
2
B.CeO 晶胞中Ce4与最近O2的核间距为 3 apm
2
4
1 1
C.CeO 晶体中B原子的分数坐标为 ,1,
2 2 2
D.每个CeO 晶胞中Ce4个数为12x
2x
13.苯与Br 的催化反应历程如图所示。下列说法正确的是
2
A.苯与Br 的催化反应均为放热反应
2
B.该反应历程中,苯与Br 的催化反应可生成溴苯、HBr和
2
邻二溴苯
C.苯与Br 的催化反应决速步骤伴随着极性键的断裂与形成
2
D.从反应速率和产物稳定性的角度分析,取代产物占比更大
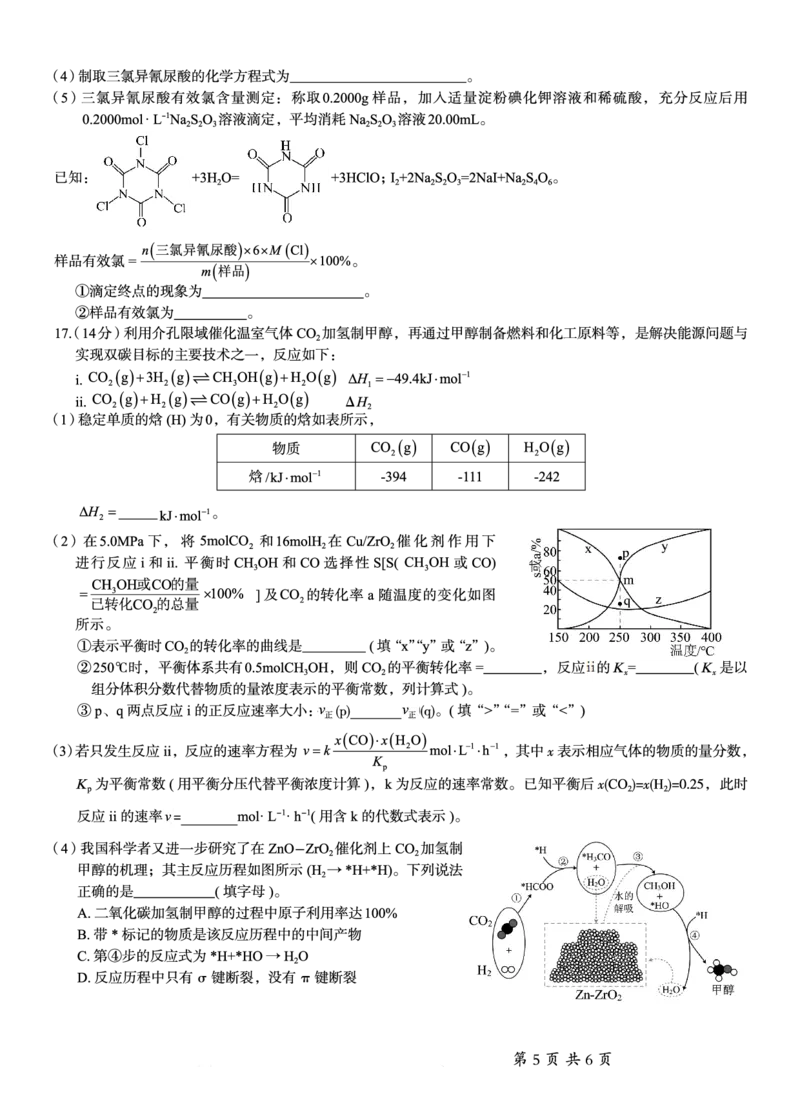
14.室温下,Na CO 体系中各含碳微粒的物质的量分数与pH的关系如图1所示。在c (Na CO )=0.1mol·L-1
2 3 起始 2 3
的体系中,研究Mg2+在不同pH时的可能产物,c(Mg2+)与pH的关系如图2所示,曲线Ⅰ的离子浓度关
系符合;c Mg2 c2 OH K sp MgOH 2 ,曲线Ⅱ的离子浓度关系符合: =
下列说法不正确的是
A.由图1,可求得Ka (H CO )=1×10-10.25
2 2 3
B.由图2,初始状态pH=9、lg[c(Mg2+)]=–2时,平衡后溶液中存在:
c HCO c CO2 cH CO 0.1mol·L-1
3 3 2 3
C.由图2,初始状态pH=11、lg[c(Mg2+)]=–6时,无沉淀生成
D.由图1和图2,初始状态pH=8、lg[c(Mg2+)]=–1时,发生反应:Mg2++2HCO ─ =MgCO ↓+CO ↑+H O
3 3 2 2