文档内容
石家庄实验中学 2026 届高三年级第一学期期中考试
化 学
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需
改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。
写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
4.可能用到的相对原子质量:H 1 C 12 O 16 F 19 Fe 56 Cu 64 Zn 65 Ag 108
一、选择题:本题共 14 小题,每小题3分,共 42分。每小题只有一个选项符合题目要求。
1.化学与生产生活密切相关,下列说法错误的是( )
A.中国航母003“福建舰”母船海水浸泡区的铝基可保障船体不易腐蚀利用了牺牲阳极
的保护法
B.“梨花院落溶溶月,柳絮池塘淡淡风”,柳絮的主要成份是糖类
C.加酶洗衣粉不宜洗涤羊毛衫,会使羊毛衫的蛋白质变性
D.碲化镉是冬奥会用作发电玻璃的新材料,其中碲元素的基态原子核外有3个未成对
电子
❑
2.已知:I +2Na S O ,下列化学用语表达正确的是( )
2 2 2 3 ¿
A. I 2 分子的σ 键轮廓图:
B. 硫原子的结构示意图:
C. 碘化钠的电子式:
O
D. 基态 原子的核外电子轨道表示式:
3.化学与生产、生活和社会息息相关。下列有关说法错误的是( )
A.菏泽特产牡丹籽油属于高分子化合物
B.燃煤中加入CaO可以减少酸雨的形成
C.亚硝酸钠可用于一些肉制品的加工,发挥防腐作用
D.煤炭经气化和液化等过程,可获得清洁能源和重要的化工原料
4.在给定条件下,下列选项所示的物质间转化均能实现的是( )
A.N NO HNO
2 3
B.MnO Cl 漂白粉
2 2
C.黄铁矿 SO 硫酸
3
D.CuSO (aq) Cu(OH) Cu O
4 2 2
5.下列实验方法及所选硅酸盐仪器(其他材质仪器任选)均正确的是A.除去苯中混有的少量苯酚:加入溴水,然后过滤,仪器为①⑦⑨
B.分离CCl 和Br 的混合液体,可用分液法,仪器为⑦⑧
4 2
C.使用酸性高锰酸钾标准溶液通过滴定法测定某未知浓度的 FeSO 溶液的浓度,仪器为
4
④⑥
D.蒸馏法淡化海水,仪器为②③⑤⑥
6.有研究称金粉溶于过氧化氢 浓盐酸也可以安全环保地制备氯金酸 ,其化学
方程式为 ,下列有关说法错误的是
A. 有强氧化性,其中 与4个氯离子形成4个σ键
B.该反应中, 的作用是与 配合,使其更易被氧化
C.当反应中溶解 时,有 过氧化氢发生还原反应
D.该反应的氧化产物和还原产物的物质的量之比为
7.下列反应的离子方程式表示不正确的是
A.明矾溶液中滴入 溶液使 恰好完全沉淀:
B.向 溶液通入少量的 :
C.用 溶液吸收少量的 :
D.向 溶液通入足量的 :
8.设 为阿伏加德罗常数,下列叙述正确的有( )
① 与 ( )的混合物中所含共价键数目为
② 溶液中含 离子数为
③ 与 的混合物中所含中子数为
④常温下电解饱和食盐水,当溶液 由7变为13时,电路中转移的电子数为
⑤常温常压下, 所含的氧原子数为
⑥标准状况下, 乙醇完全燃烧后生成 的分子数为
A.二个 B.三个 C.四个 D.五个
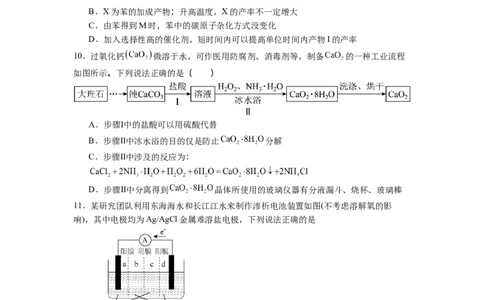
9.在浓 和浓 混合溶液中加入苯,反应过程中能量变化示意图如下。下列说法
错误的是( )A.浓 导致反应③的活化能比反应②低
B.X为苯的加成产物;升高温度,X的产率不一定增大
C.由苯得到M时,苯中的碳原子杂化方式没变化
D.加入选择性高的催化剂,短时间内可以提高单位时间内产物I的产率
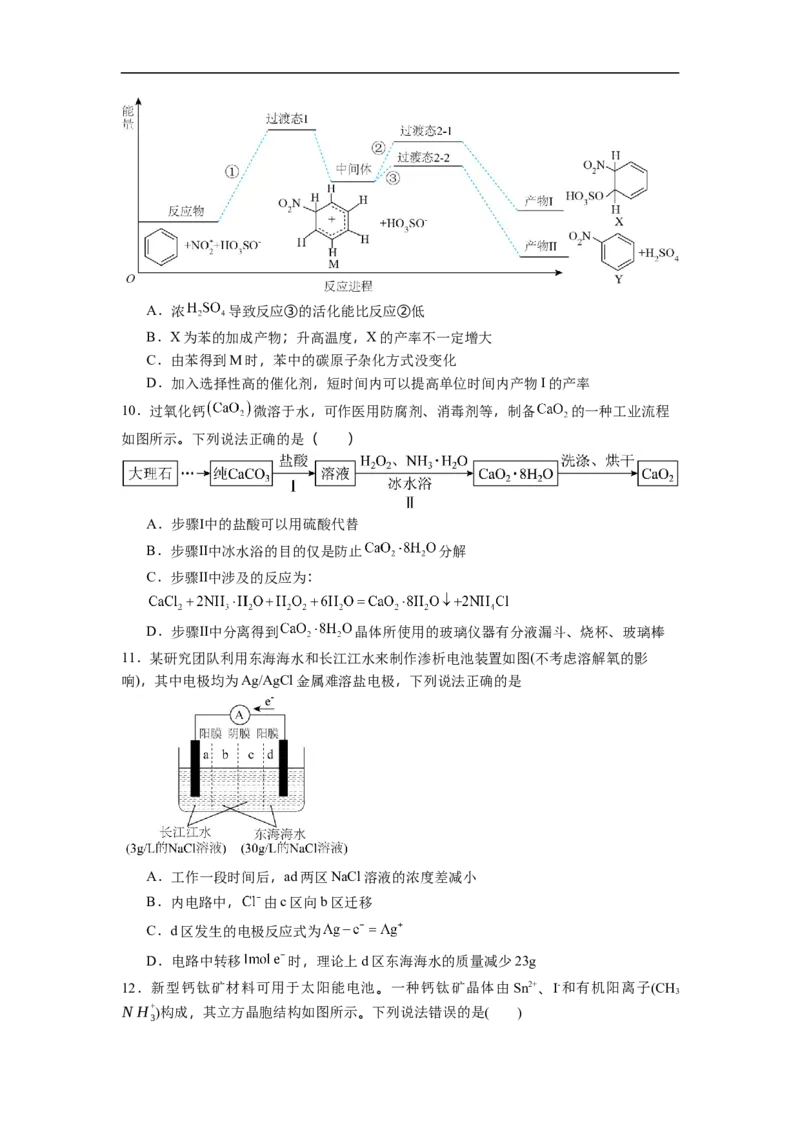
10.过氧化钙 微溶于水,可作医用防腐剂、消毒剂等,制备 的一种工业流程
如图所示。下列说法正确的是( )
A.步骤Ⅰ中的盐酸可以用硫酸代替
B.步骤Ⅱ中冰水浴的目的仅是防止 分解
C.步骤Ⅱ中涉及的反应为:
D.步骤Ⅱ中分离得到 晶体所使用的玻璃仪器有分液漏斗、烧杯、玻璃棒
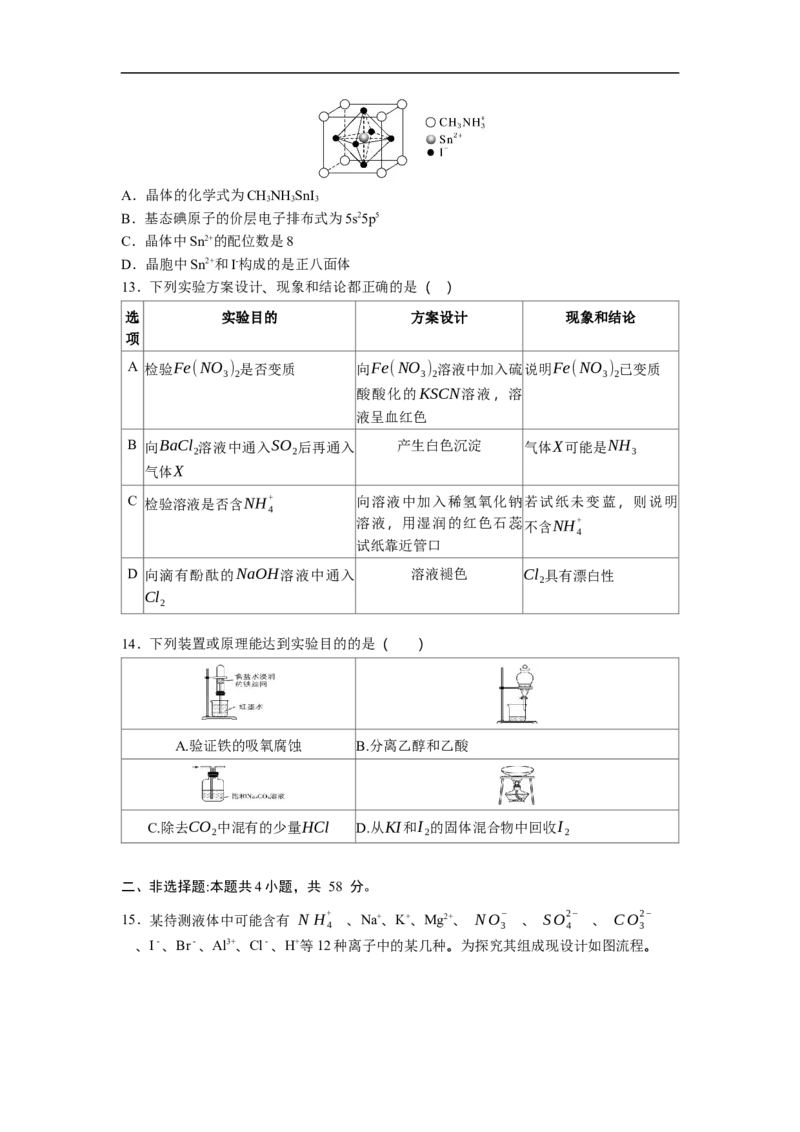
11.某研究团队利用东海海水和长江江水来制作渗析电池装置如图(不考虑溶解氧的影
响),其中电极均为Ag/AgCl金属难溶盐电极,下列说法正确的是
A.工作一段时间后,ad两区NaCl溶液的浓度差减小
B.内电路中, 由c区向b区迁移
C.d区发生的电极反应式为
D.电路中转移 时,理论上d区东海海水的质量减少23g
12.新型钙钛矿材料可用于太阳能电池。一种钙钛矿晶体由Sn2+、I-和有机阳离子(CH
3
N H+ )构成,其立方晶胞结构如图所示。下列说法错误的是( )
3A.晶体的化学式为CHNH SnI
3 3 3
B.基态碘原子的价层电子排布式为5s25p5
C.晶体中Sn2+的配位数是8
D.晶胞中Sn2+和I-构成的是正八面体
13.下列实验方案设计、现象和结论都正确的是( )
选 实验目的 方案设计 现象和结论
项
A 检验Fe(NO ) 是否变质 向Fe(NO ) 溶液中加入硫说明Fe(NO ) 已变质
3 2 3 2 3 2
酸酸化的KSCN溶液,溶
液呈血红色
B 向BaCl 溶液中通入SO 后再通入 产生白色沉淀 气体X可能是NH
2 2 3
气体X
C 检验溶液是否含NH+ 向溶液中加入稀氢氧化钠若试纸未变蓝,则说明
4
溶液,用湿润的红色石蕊 不含NH+
4
试纸靠近管口
D 向滴有酚酞的NaOH溶液中通入 溶液褪色 Cl 具有漂白性
2
Cl
2
14.下列装置或原理能达到实验目的的是( )
A.验证铁的吸氧腐蚀 B.分离乙醇和乙酸
C.除去CO 中混有的少量HCl D.从KI和I 的固体混合物中回收I
2 2 2
二、非选择题:本题共4小题,共 58 分。
15.某待测液体中可能含有 N H+ 、Na+、K+、Mg2+、 NO− 、 SO2− 、 CO2−
4 3 4 3
、I-、Br-、Al3+、Cl-、H+等12种离子中的某几种。为探究其组成现设计如图流程。已知该待测液中所有离子的浓度均相等。
(1)待测液中 c(SO2−)= __________mol·L-1。
4
(2)生成不溶物I的离子方程式为__________。
(3)不溶物Ⅱ和不溶物Ⅲ的化学式分别为__________、__________。
(4)若向溶液I中加入过量的稀盐酸,观察到的现象为__________;若向溶液Ⅱ中加入过量的
稀盐酸,再通入标准状况下112 mL Cl ,观察到的现象为__________。
2
(5)待测液中一定不含的离子是__________。
16.镓(Ga)被誉为“电子工业脊梁”,性质与铝相似。氮化镓(GaN)在5G基站和互联网系统
建设等方面用途广泛。以砷化镓废料(主要成分是GaAs,含Fe O、Al O 和CaCO 等杂质)
2 3 2 3 3
制备GaN和NaAsO ∙12H O的流程如下:
3 4 2
请回答下列问题:
(1)滤渣2的主要成分是 (填化学式)。
(2)“碱浸”中发生主要反应的化学方程式为 ,在该反应中氧化剂和还原剂的物质的量之
比为 。
(3)“调pH2”时通入过量CO,写出离子方程式: 。操作a包括蒸发浓缩、降温结晶、
2
过滤、洗涤、低温干燥,“低温干燥”的目的是 。
(4)制备氮化镓时生成一种气体,它是 (填化学式)。
(5)制备氮化镓需要纯氨气,实验室制备氨气宜选择的装置是 (填字母)。
(6)设计简单实验证明滤液1是否含Fe3+: 。
17.叠氮化钠( )常用作汽车安全气囊中的药剂。实验室制取叠氮化钠的原理、实验装
置及实验步骤如下:
①打开装置D导管上的旋塞,加热制取氨气。
②再加热装置A中的金属钠,使其熔化并充分反应后,再停止加热装置D并关闭旋塞。③向装置A中b容器内充入加热介质并加热到210~220℃,然后通入 。
④冷却,向产物中加入乙醇(降低 的溶解度),减压浓缩结晶后,再过滤,并用乙醚洗
涤,晾干。
已知:Ⅰ. 是易溶于水的白色晶体,微溶于乙醇,不溶于乙醚;
Ⅱ. 熔点210℃,沸点400℃,在水溶液中易水解。
请回答下列问题:
(1)实验室若采用固体加热方式制取氨气的化学方程式为 。
(2)步骤①中先加热通氨气的目的是 ;步骤②氨气与熔化的钠反应生成 的化
学方程式为 ;步骤③中最适宜的加热方式为 (填“水浴加热”,“油浴加热”)
(3)图中仪器a用的材料是铁质而不用玻璃,其主要原因是 。
(4)汽车经撞击后30毫秒内,会引发叠氮化钠迅速分解为两种单质,其中氧化产物和还原
产物的质量之比为 。
(5)步骤④中用乙醚洗涤的主要原因除因其易挥发,有利于产品快速干燥外,还因为
。
(6)实验室用滴定法测定叠氮化钠样品中 的质量分数:
①将2.500g试样配成500.00mL溶液。
②取50.00mL溶液置于锥形瓶中,加入50.00mL 溶液。
③充分反应后,将溶液稍稀释,向溶液中加入8mL浓硫酸,滴入3滴邻菲啰啉指示液,用
标准溶液滴定过量的 ,消耗溶液体
29.00mL。测定过程的反应方程式为:
;
;
试样中 的质量分数为 (保留小数点后一位)。
18.CH 与CO 的干法重整(DRM)反应可制备CO和H。体系内发生的反应如下:
4 2 2
反应Ⅰ:CH
4
(g)+CO
2
(g)⇌2CO(g)+2H
2
(g)
ΔH
1反应Ⅱ:CH
4
(g)+3CO
2
(g)⇌ 4CO(g)+2H
2
O(g)
ΔH=+329 kJ·mol-1
2
反应Ⅲ:CO(g)+H
2
O(g)⇌CO
2
(g)+H
2
(g)
ΔH=-41 kJ·mol-1
3
(1)ΔH= (填含ΔH、ΔH 的表达式)。
1 2 3
(2)向密闭容器中通入3 mol CO (g)和1 mol CH (g),若仅考虑发生上述三个反应,
2 4
平衡时CO (g)、CH (g)、CO(g)、H (g)的物质的量随温度T的变化如图甲所
2 4 2
示。
①曲线X、Z分别表示 、 (填化学式)的物质的量变化。
②900 K时,CH 的物质的量分数为 (填含a的表达式,下同),反应Ⅲ的平衡常
4
数K= 。
c
(3)使用CaO/Fe O/Ni复合催化剂,可显著提高二氧化碳的转化率,实现碳氢分离,并
3 4
得到富含CO的产物,催化机理如图乙所示。
乙
某化学兴趣小组用化学方程式解释碳氢分离的原理:4CO+Fe O 3Fe
3 4
+4CO 、4H +Fe O 3Fe+4HO、 、 (补齐另外两
2 2 3 4 2
个化学方程式)。