文档内容
福州一中 2025—2026 学年第一学期第一学段模块考试
高三化学学科试卷
(完卷时间:75 分钟; 满分:100分)
班级__________座号____________姓名____________
可能用到的相对原子质量:H1 C12 N14 O16 Na23 Cl35.5 Fe56
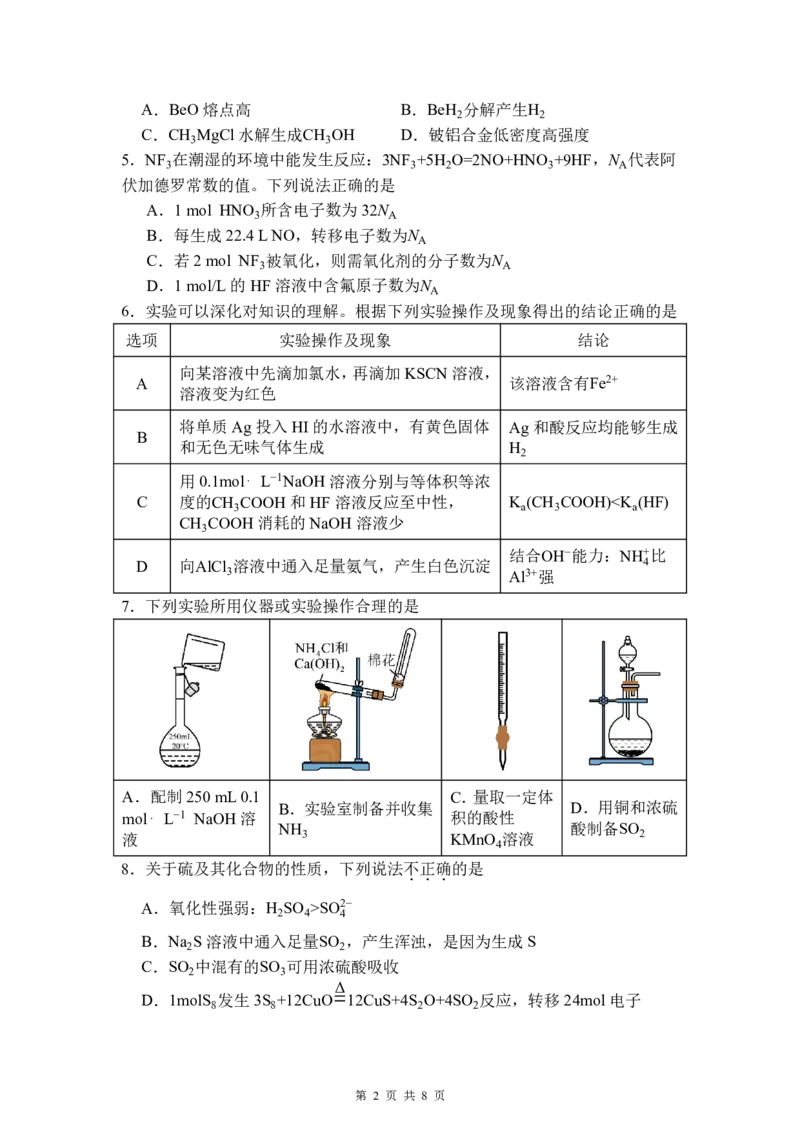
一、选择题(每小题 3分,共 48分;每题的四个选项中,只有一项符合要求)
1.化学与生产生活密切相关,下列说法不
.
正
.
确
.
的是
A.利用硝酸铵和水合碳酸钠的反应可制冷敷袋,该反应能发生的原理是熵增
B.二氧化硅可用作牙膏的摩擦剂,说明它难溶于水
C.La-Ni 合金在一定条件下能吸放氢气,故可用作储氢合金
D.氢氟酸呈酸性,故可用于刻蚀玻璃器皿
阅读下列材料,完成 2、3、4三个小题:
铍及其化合物具有重要应用。铍与铝性质相似,铍铝合金可用作航空材料,BeH
2
是很好的储氢材料;BeO 可用于制造耐火陶炎,晶胞结构如图所示;NH BeF
4 2 4
固体加热至280℃得BeF 分子和两种气态氢化物;气态BeCl 主要以二聚体
2 2
( )形式存在,可与CH MgCl 在乙醚中制备 Be CH ;Be NO
3 3 2 3 2
在125℃分解为N O 和Be O NO 等。
2 4 4 3 6
2.下列说法正确的是
A.NH 键角大于NH+ B.BeF 为离子化合物
3 4 2
C.BeO 晶胞中O2−配位数为4 D.1mol Be Cl 气体含4mol σ键
2 4
3.下列化学反应表示不
.
正
.
确
.
的是
A.Be 溶于NaOH 溶液:Be+2OH−=BeO2− +H ↑
2 2
280℃
B.BeF 的制备: NH BeF BeF +2NH ↑+2HF↑
2 4 2 4 2 3
125℃
C.Be NO 的受热分解:8Be NO 2Be O NO +2N O ↑+O ↑
3 2 3 2 4 3 6 2 4 2
D.电解BeCl 、NaCl混合熔融盐阴极反应:2Cl−−2e−=Cl ↑
2 2
4.下列说法不
.
正
.
确
.
的是
第 1 页 共 8 页
{#{QQABBQEgwwiQgIQACC7LAUUSCkgYkJOzLIgsgVCaqAwCgRNABCA=}#}A.BeO熔点高 B.BeH 分解产生H
2 2
C.CH MgCl 水解生成CH OH D.铍铝合金低密度高强度
3 3
5.NF 在潮湿的环境中能发生反应:3NF +5H O=2NO+HNO +9HF,N 代表阿
3 3 2 3 A
伏加德罗常数的值。下列说法正确的是
A.1mol HNO 所含电子数为 32N
3 A
B.每生成22.4LNO,转移电子数为N
A
C.若2mol NF 被氧化,则需氧化剂的分子数为N
3 A
D.1mol/L 的HF溶液中含氟原子数为N
A
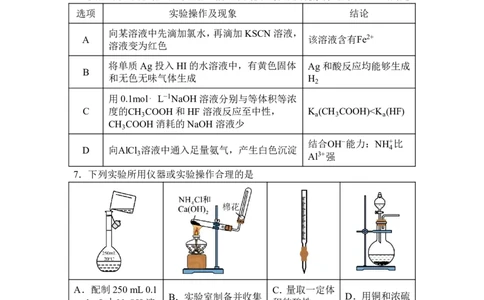
6.实验可以深化对知识的理解。根据下列实验操作及现象得出的结论正确的是
选项 实验操作及现象 结论
向某溶液中先滴加氯水,再滴加KSCN溶液,
A 该溶液含有Fe2+
溶液变为红色
将单质Ag投入HI的水溶液中,有黄色固体 Ag和酸反应均能够生成
B
和无色无味气体生成 H
2
用0.1mol⋅ L−1NaOH 溶液分别与等体积等浓
C 度的CH COOH和HF 溶液反应至中性, K (CH COOH)SO2−
2 4 4
B.Na S溶液中通入足量SO ,产生浑浊,是因为生成 S
2 2
C.SO 中混有的SO 可用浓硫酸吸收
2 3
Δ
D.1molS 发生3S +12CuO 12CuS+4S O+4SO 反应,转移24mol电子
8 8 2 2
第 2 页 共 8 页
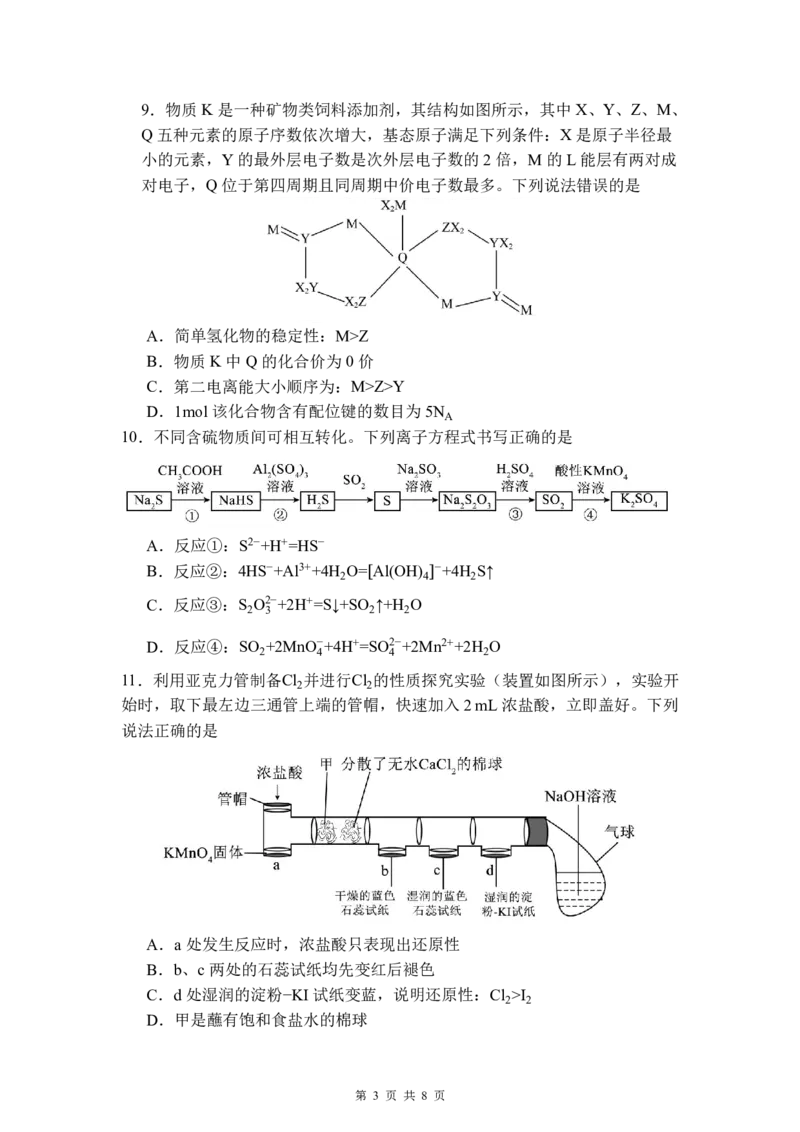
{#{QQABBQEgwwiQgIQACC7LAUUSCkgYkJOzLIgsgVCaqAwCgRNABCA=}#}9.物质K是一种矿物类饲料添加剂,其结构如图所示,其中 X、Y、Z、M、
Q五种元素的原子序数依次增大,基态原子满足下列条件:X是原子半径最
小的元素,Y的最外层电子数是次外层电子数的2倍,M 的L能层有两对成
对电子,Q位于第四周期且同周期中价电子数最多。下列说法错误的是
A.简单氢化物的稳定性:M>Z
B.物质K中Q的化合价为0价
C.第二电离能大小顺序为:M>Z>Y
D.1mol 该化合物含有配位键的数目为 5N
A
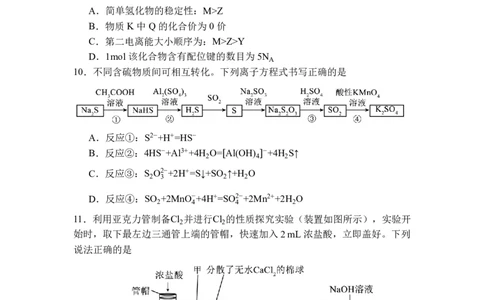
10.不同含硫物质间可相互转化。下列离子方程式书写正确的是
A.反应①:S2−+H+=HS−
B.反应②:4HS−+Al3++4H O= Al(OH) −+4H S↑
2 4 2
C.反应③:S O2−+2H+=S↓+SO ↑+H O
2 3 2 2
D.反应④:SO +2MnO−+4H+=SO2−+2Mn2++2H O
2 4 4 2
11.利用亚克力管制备Cl 并进行Cl 的性质探究实验(装置如图所示),实验开
2 2
始时,取下最左边三通管上端的管帽,快速加入2 mL 浓盐酸,立即盖好。下列
说法正确的是
A.a 处发生反应时,浓盐酸只表现出还原性
B.b、c两处的石蕊试纸均先变红后褪色
C.d处湿润的淀粉−KI 试纸变蓝,说明还原性:Cl >I
2 2
D.甲是蘸有饱和食盐水的棉球
第 3 页 共 8 页
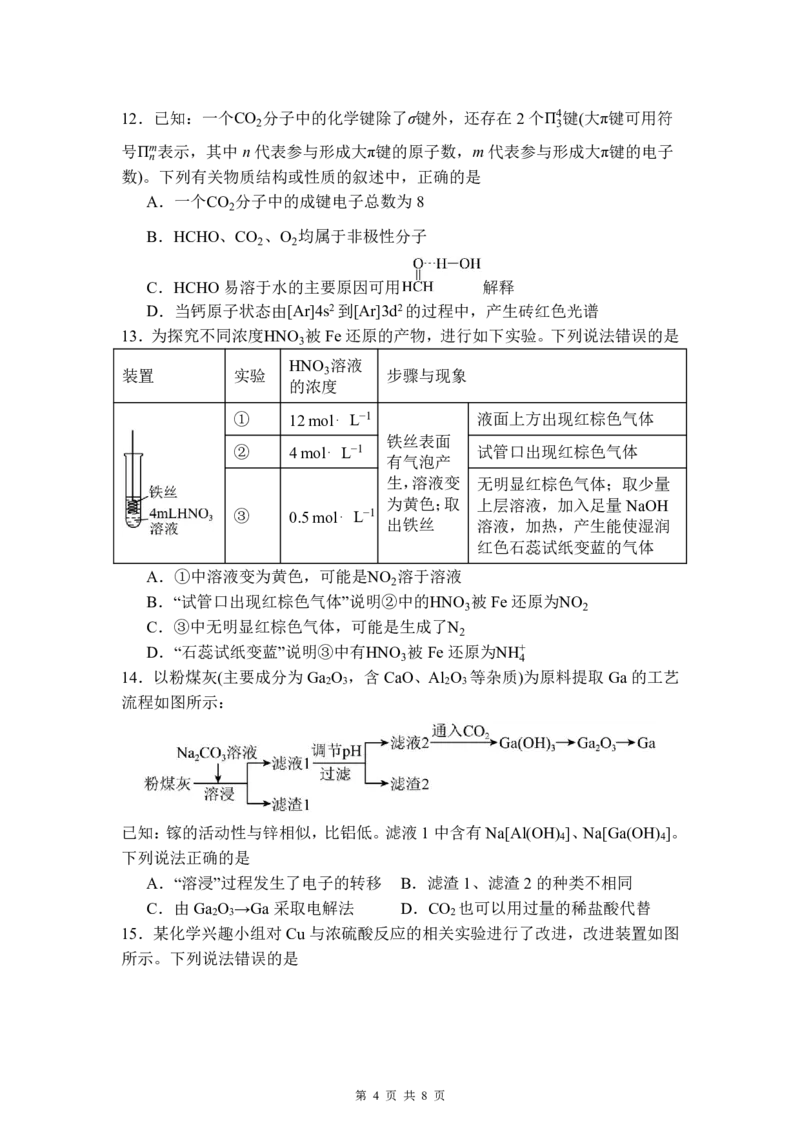
{#{QQABBQEgwwiQgIQACC7LAUUSCkgYkJOzLIgsgVCaqAwCgRNABCA=}#}12.已知:一个CO 分子中的化学键除了σ键外,还存在2个Π4键(大π键可用符
2 3
号Πm表示,其中n代表参与形成大π键的原子数,m代表参与形成大π键的电子
n
数)。下列有关物质结构或性质的叙述中,正确的是
A.一个CO 分子中的成键电子总数为 8
2
B.HCHO、CO 、O 均属于非极性分子
2 2
C.HCHO易溶于水的主要原因可用 解释
D.当钙原子状态由[Ar]4s2到[Ar]3d2的过程中,产生砖红色光谱
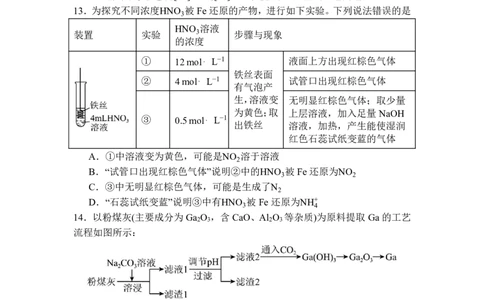
13.为探究不同浓度HNO 被Fe 还原的产物,进行如下实验。下列说法错误的是
3
HNO 溶液
装置 实验 3 步骤与现象
的浓度
① 12 mol⋅ L−1 液面上方出现红棕色气体
铁丝表面
② 4 mol⋅ L−1 试管口出现红棕色气体
有气泡产
生,溶液变 无明显红棕色气体;取少量
为黄色;取 上层溶液,加入足量NaOH
③ 0.5 mol⋅ L−1
出铁丝 溶液,加热,产生能使湿润
红色石蕊试纸变蓝的气体
A.①中溶液变为黄色,可能是NO 溶于溶液
2
B.“试管口出现红棕色气体”说明②中的HNO 被Fe 还原为NO
3 2
C.③中无明显红棕色气体,可能是生成了N
2
D.“石蕊试纸变蓝”说明③中有HNO 被Fe 还原为NH+
3 4
14.以粉煤灰(主要成分为Ga O ,含 CaO、Al O 等杂质)为原料提取Ga的工艺
2 3 2 3
流程如图所示:
已知:镓的活动性与锌相似,比铝低。滤液1中含有Na[Al(OH) ]、Na[Ga(OH) ]。
4 4
下列说法正确的是
A.“溶浸”过程发生了电子的转移 B.滤渣1、滤渣2的种类不相同
C.由Ga O →Ga 采取电解法 D.CO 也可以用过量的稀盐酸代替
2 3 2
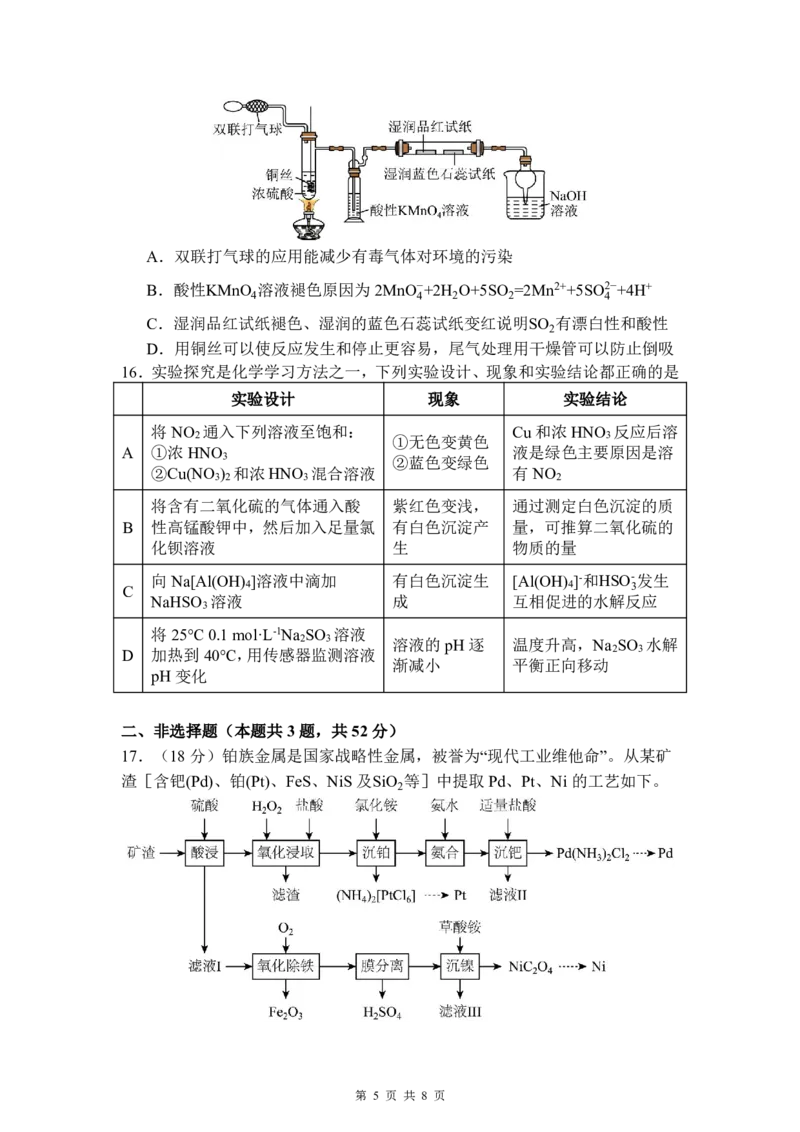
15.某化学兴趣小组对Cu 与浓硫酸反应的相关实验进行了改进,改进装置如图
所示。下列说法错误的是
第 4 页 共 8 页
{#{QQABBQEgwwiQgIQACC7LAUUSCkgYkJOzLIgsgVCaqAwCgRNABCA=}#}A.双联打气球的应用能减少有毒气体对环境的污染
B.酸性KMnO 溶液褪色原因为2MnO−+2H O+5SO =2Mn2++5SO2−+4H+
4 4 2 2 4
C.湿润品红试纸褪色、湿润的蓝色石蕊试纸变红说明SO 有漂白性和酸性
2
D.用铜丝可以使反应发生和停止更容易,尾气处理用干燥管可以防止倒吸
16.实验探究是化学学习方法之一,下列实验设计、现象和实验结论都正确的是
实验设计 现象 实验结论
将NO 通入下列溶液至饱和: Cu和浓HNO 反应后溶
2 ①无色变黄色 3
A ①浓HNO 液是绿色主要原因是溶
3 ②蓝色变绿色
②Cu(NO ) 和浓HNO 混合溶液 有 NO
3 2 3 2
将含有二氧化硫的气体通入酸 紫红色变浅, 通过测定白色沉淀的质
B 性高锰酸钾中,然后加入足量氯 有白色沉淀产 量,可推算二氧化硫的
化钡溶液 生 物质的量
向Na[Al(OH) ]溶液中滴加 有白色沉淀生 [Al(OH) ]-和HSO-发生
C 4 4 3
NaHSO 溶液 成 互相促进的水解反应
3
将25℃ 0.1mol·L-1Na SO 溶液
2 3 溶液的pH逐 温度升高,Na SO 水解
D 加热到 40℃,用传感器监测溶液 2 3
渐减小 平衡正向移动
pH 变化
二、非选择题(本题共 3题,共 52分)
17.(18分)铂族金属是国家战略性金属,被誉为“现代工业维他命”。从某矿
渣[含钯(Pd)、铂(Pt)、FeS、NiS 及SiO 等]中提取Pd、Pt、Ni 的工艺如下。
2
第 5 页 共 8 页
{#{QQABBQEgwwiQgIQACC7LAUUSCkgYkJOzLIgsgVCaqAwCgRNABCA=}#}已知:Pd、Pt 经“氧化浸取”转化为H PdCl 、H PtCl ;“氨合”后,Pd(Ⅱ)主要
2 4 2 6
以 Pd NH 2+的形式存在;常温下,H C O 的K =5.6×10−2,K =1.5×10−4。
3 4 2 2 4 a1 a2
(1)Pt、Pd与Fe 为同族元素,位于元素周期表的 区。
(2)“氧化浸取”时,Pd 发生反应的化学方程式为 。
(3)“滤液Ⅱ”中的溶质可在 工序中循环利用。
(4)“氧化除铁”时,温度为180℃,该过程主要发生两步反应:
(ⅰ)4Fe2++O +4H+=4Fe3++2H O
2 2
(ⅱ) (填离子方程式)。
(5)常温下,“沉镍”时,需调节溶液pH=2,此时
c C2O2
4
−
= 。
c H2C2O4
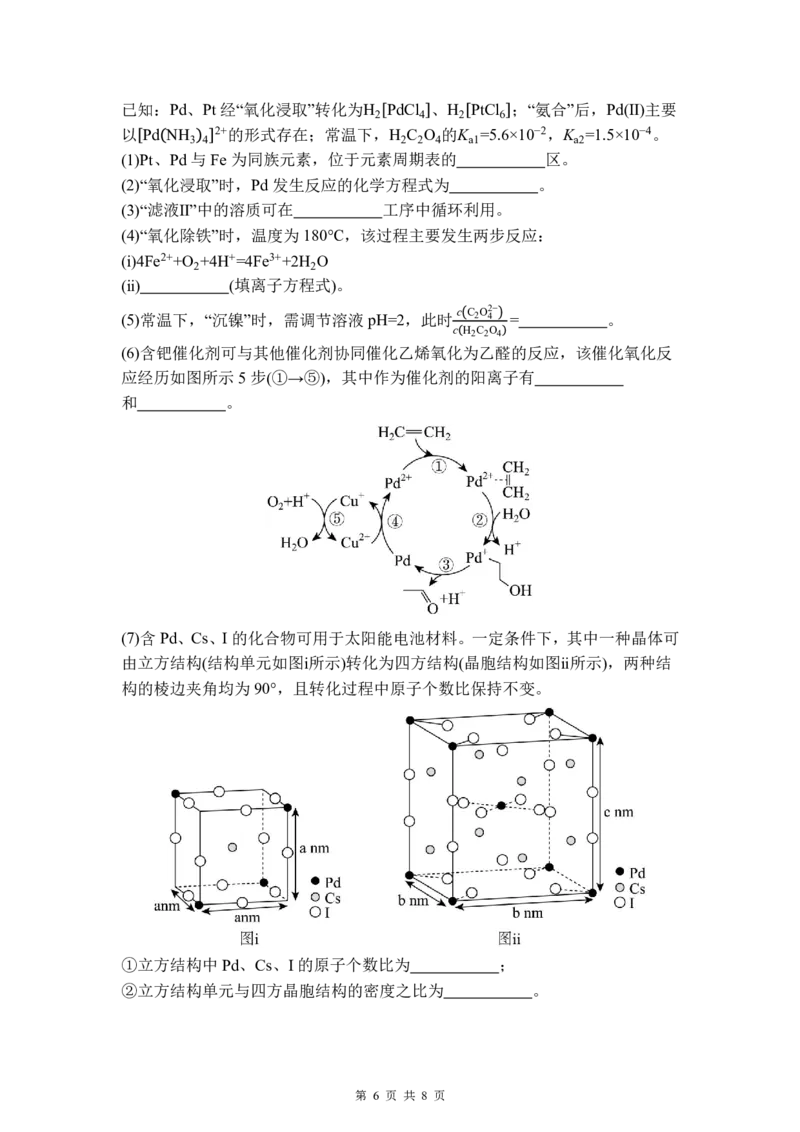
(6)含钯催化剂可与其他催化剂协同催化乙烯氧化为乙醛的反应,该催化氧化反
应经历如图所示5步(①→⑤),其中作为催化剂的阳离子有
和 。
(7)含Pd、Cs、I 的化合物可用于太阳能电池材料。一定条件下,其中一种晶体可
由立方结构(结构单元如图ⅰ所示)转化为四方结构(晶胞结构如图ⅱ所示),两种结
构的棱边夹角均为90°,且转化过程中原子个数比保持不变。
①立方结构中Pd、Cs、I的原子个数比为 ;
②立方结构单元与四方晶胞结构的密度之比为 。
第 6 页 共 8 页
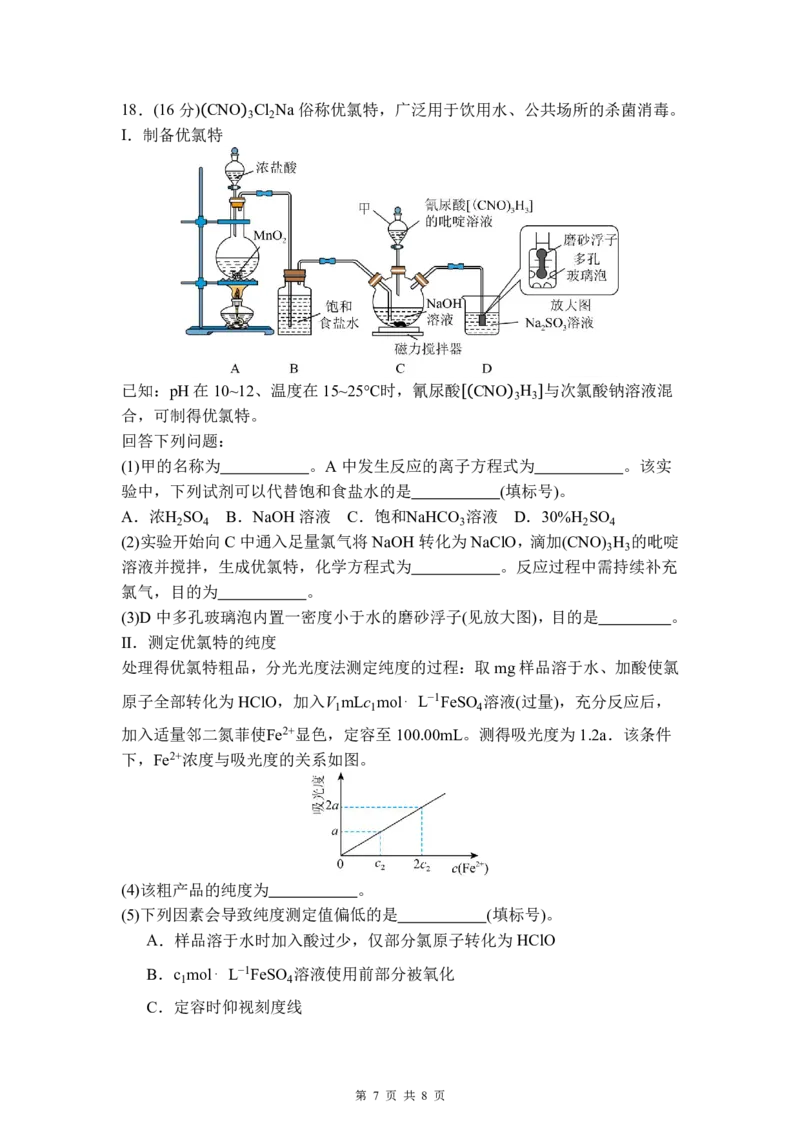
{#{QQABBQEgwwiQgIQACC7LAUUSCkgYkJOzLIgsgVCaqAwCgRNABCA=}#}18.(16分) CNO Cl Na 俗称优氯特,广泛用于饮用水、公共场所的杀菌消毒。
3 2
Ⅰ.制备优氯特
已知:pH在10~12、温度在15~25℃时,氰尿酸 CNO H 与次氯酸钠溶液混
3 3
合,可制得优氯特。
回答下列问题:
(1)甲的名称为 。A 中发生反应的离子方程式为 。该实
验中,下列试剂可以代替饱和食盐水的是 (填标号)。
A.浓H SO B.NaOH溶液 C.饱和NaHCO 溶液 D.30%H SO
2 4 3 2 4
(2)实验开始向C 中通入足量氯气将NaOH 转化为NaClO,滴加(CNO) H 的吡啶
3 3
溶液并搅拌,生成优氯特,化学方程式为 。反应过程中需持续补充
氯气,目的为 。
(3)D 中多孔玻璃泡内置一密度小于水的磨砂浮子(见放大图),目的是 。
Ⅱ.测定优氯特的纯度
处理得优氯特粗品,分光光度法测定纯度的过程:取mg 样品溶于水、加酸使氯
原子全部转化为 HClO,加入V mLc mol⋅ L−1FeSO 溶液(过量),充分反应后,
1 1 4
加入适量邻二氮菲使Fe2+显色,定容至100.00mL。测得吸光度为1.2a.该条件
下,Fe2+浓度与吸光度的关系如图。
(4)该粗产品的纯度为 。
(5)下列因素会导致纯度测定值偏低的是 (填标号)。
A.样品溶于水时加入酸过少,仅部分氯原子转化为HClO
B.c mol⋅ L−1FeSO 溶液使用前部分被氧化
1 4
C.定容时仰视刻度线
第 7 页 共 8 页
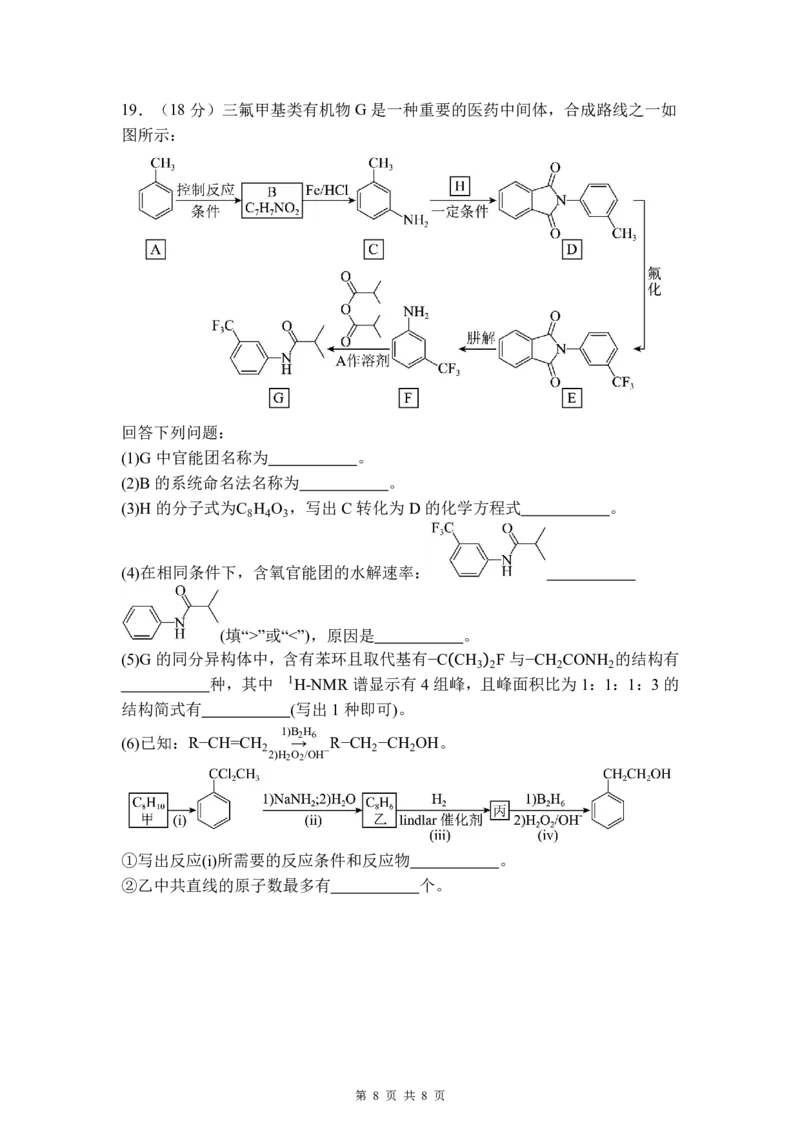
{#{QQABBQEgwwiQgIQACC7LAUUSCkgYkJOzLIgsgVCaqAwCgRNABCA=}#}19.(18分)三氟甲基类有机物G是一种重要的医药中间体,合成路线之一如
图所示:
回答下列问题:
(1)G 中官能团名称为 。
(2)B 的系统命名法名称为 。
(3)H 的分子式为C H O ,写出C 转化为D的化学方程式 。
8 4 3
(4)在相同条件下,含氧官能团的水解速率:
(填“>”或“<”),原因是 。
(5)G 的同分异构体中,含有苯环且取代基有−C CH F 与−CH CONH 的结构有
3 2 2 2
种,其中 1H-NMR 谱显示有4组峰,且峰面积比为1:1:1:3的
结构简式有 (写出1种即可)。
(6)已知:R−CH=CH
1)B
→
2H6
R−CH −CH OH。
2 2)H2O2/OH− 2 2
①写出反应(i)所需要的反应条件和反应物 。
②乙中共直线的原子数最多有 个。
第 8 页 共 8 页
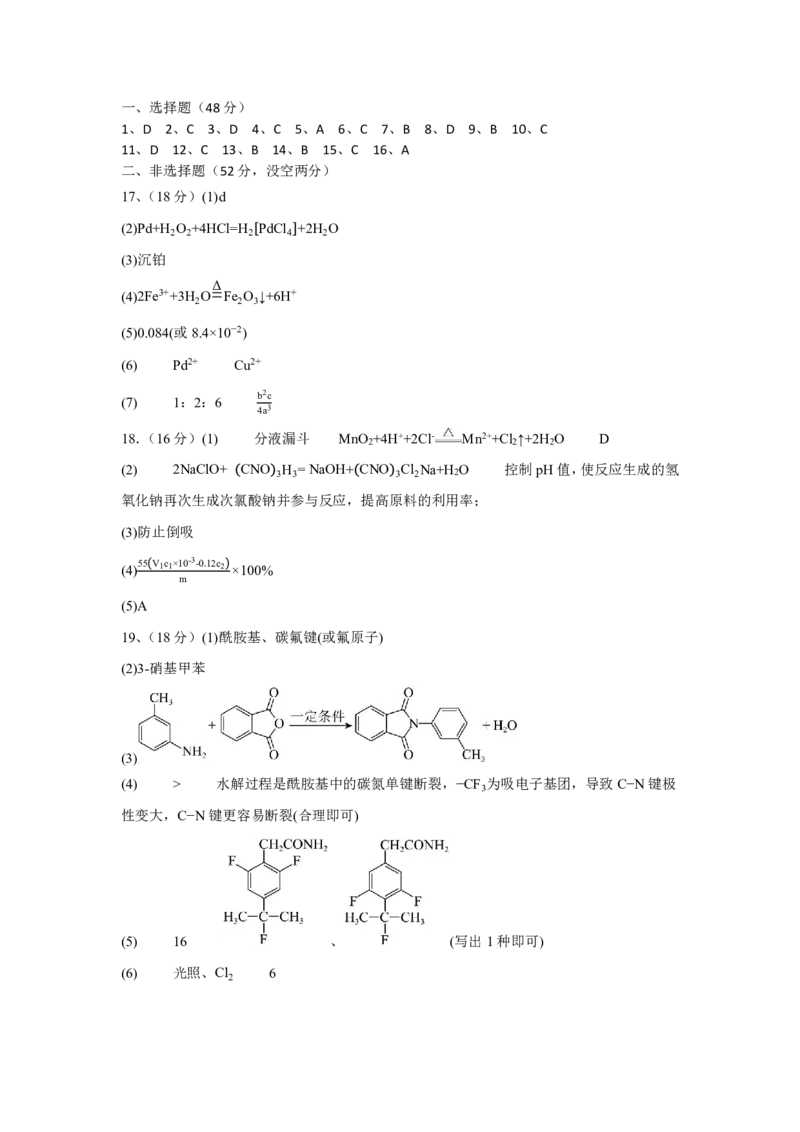
{#{QQABBQEgwwiQgIQACC7LAUUSCkgYkJOzLIgsgVCaqAwCgRNABCA=}#}一、选择题(48分)
1、D 2、C 3、D 4、C 5、A 6、C 7、B 8、D 9、B 10、C
11、D 12、C 13、B 14、B 15、C 16、A
二、非选择题(52分,没空两分)
17、(18分)(1)d
(2)Pd+H O +4HCl=H PdCl +2H O
2 2 2 4 2
(3)沉铂
Δ
(4)2Fe3++3H O Fe O ↓+6H+
2 2 3
(5)0.084(或8.4×10−2)
(6) Pd2+ Cu2+
(7) 1:2:6
b2c
4a3
18.(16分)(1) 分液漏斗 MnO +4H++2Cl- Mn2++Cl ↑+2H O D
2 2 2
(2) 2NaClO+ CNO H =NaOH+ CNO Cl Na+H O 控制pH值,使反应生成的氢
3 3 3 2 2
氧化钠再次生成次氯酸钠并参与反应,提高原料的利用率;
(3)防止倒吸
(4)
55 V1c1×10-3-0.12c2
×100%
m
(5)A
19、(18分)(1)酰胺基、碳氟键(或氟原子)
(2)3-硝基甲苯
(3)
(4) > 水解过程是酰胺基中的碳氮单键断裂,−CF 为吸电子基团,导致C−N键极
3
性变大,C−N键更容易断裂(合理即可)
(5) 16 、 (写出1种即可)
(6) 光照、Cl 6
2
{#{QQABBQEgwwiQgIQACC7LAUUSCkgYkJOzLIgsgVCaqAwCgRNABCA=}#}