文档内容
微信公众号:文采学社
2 0 2 5 年 上 教 师 资 格 · 化 学 学 科 笔 试
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微
主讲老师 岳筱涵
粉笔教师教育 粉笔教师微信公众号:文采学社
镁、铝及其化合物
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
P45
四、铝的其他化合物及铝合金
(一)明矾
化学式:KAl(SO ) ·12H O
4 2 2
属类:复盐(由两种不同的金属阳离子和一种酸根阴离子构成的化合物)。
社
学
采
道
明矾净水原理: 渠 文
:
新
号
更
众
一
KAl(SO ) ·12H O溶解于水后发唯生反公应
信
4 2 2
微
Al3++3H O Al(OH) (胶体)+3H+,
2 3
形成的Al(OH) 胶体吸附能力强。
3微信公众号:文采学社
P45
(二)铝合金及其制品
1. 合金指的是由两种或两种以上的金属(或金属与非金属)熔合
而成的具有金属特性的物质。
2. 合金有比它的成分金属更优良的性质。
社
学
如:①合金的熔点一般比它的各成分金属的低;
采
道
文
渠
:
新
号
更
②合金的硬度一般比它的各成分一金属众的大;
公
唯
信
微
③合金的化学性质也因成分金属的不同而不同。微信公众号:文采学社
P45
3.金属铝与镁、铜、硅等金属或非金属熔合形成铝合金。铝合金
具有密度小、强度高、塑性好、易于成型、制造工艺简单、成本低廉
等特点,并且有一定的抗腐蚀能力。铝合金可用于建筑业、容器、包
装业、交通运输、电子行业,并广泛用于制造飞机构件等。
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
P46
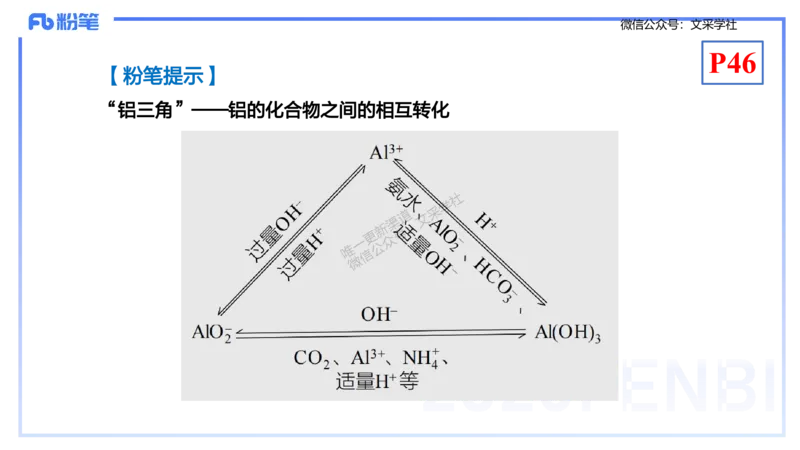
【粉笔提示】
“铝三角”——铝的化合物之间的相互转化
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
P46
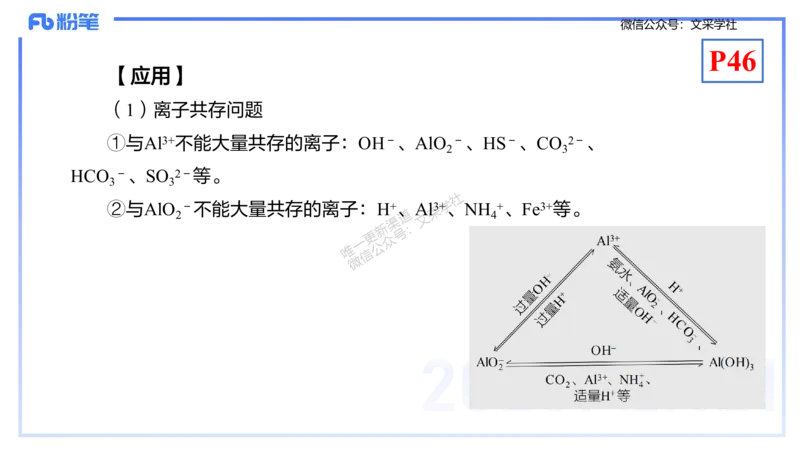
【应用】
(1)离子共存问题
①与Al3+不能大量共存的离子:OH-、AlO -、HS-、CO 2-、
2 3
HCO -、SO 2-等。
3 3
社
学
②与AlO -不能大量共存的离子:H+、Al3+、NH +、Fe3+等。
采
2 道 文 4
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
P46
(2)鉴别(利用滴加顺序不同,现象不同)
①AlCl 溶液中滴加NaOH溶液现象为:先产生白色沉淀,后沉淀溶解。
3
Al3+ + 3OH- Al(OH) ↓
3
Al(OH) + OH - AlO - + 2H O
3 2 2
社
学
采
道
文
渠
:
新
号
②NaOH溶液中滴加AlCl 溶液现更象众为:开始无明显现象,后产生白色沉
一
3 公
唯
信
微
淀,沉淀不溶解。
Al3+ + 4OH - AlO - + 2H O
2 2
Al3+ + 3AlO - + 6H O 4Al(OH) ↓
2 2 3微信公众号:文采学社
P46
(3)分离提纯
①利用Al能溶于强碱溶液,分离Al与其他金属的混合物。
②利用Al O 能与强碱溶液反应,分离Al O 与其他金属氧化物。
2 3 2 3
③利用Al(OH) 能与强碱溶液反应,分离Al3+与其他金属阳离子。
3
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
P47
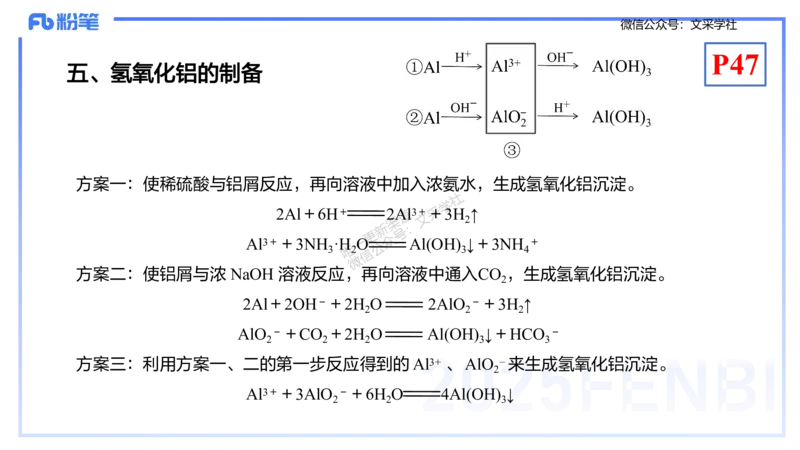
五、氢氧化铝的制备
方案一:使稀硫酸与铝屑反应,再向溶液中加入浓氨水,生成氢氧化铝沉淀。
社
学
2Al+6H+ 2A道l3+采+3H ↑
文
渠 2
:
新
号
更
众
Al3++3NH ·H一O Al(OH) ↓+3NH +
公
3 唯2信 3 4
微
方案二:使铝屑与浓 NaOH 溶液反应,再向溶液中通入CO ,生成氢氧化铝沉淀。
2
2Al+2OH-+2H O 2AlO -+3H ↑
2 2 2
AlO -+CO +2H O Al(OH) ↓+HCO -
2 2 2 3 3
方案三:利用方案一、二的第一步反应得到的 Al3+ 、 AlO − 来生成氢氧化铝沉淀。
2
Al3++3AlO -+6H O 4Al(OH) ↓
2 2 3微信公众号:文采学社
P47
1. 某白色粉末由两种物质组成,为鉴别其成分进行如下实验:①取少
量样品加入足量水,仍有部分固体未溶解;再加入足量稀盐酸,有气泡产
生,固体全部溶解。②取少量样品加入足量稀硫酸,有气泡产生,振荡后
仍有固体存在。该白色粉末为( )。 社
学
采
道
文
渠
:
新
号
更
众
A. NaHCO 、Al(OH) B.一 A公gCl、NaHCO
唯
3 3 信 3
微
C. Na SO 、BaCO D. Na CO 、CuSO
2 3 3 2 3 4微信公众号:文采学社
P47
2. 下列叙述正确的是( )。
A. 将稀盐酸滴入部分变质的氢氧化钠溶液,立刻产生气泡
B. 将氯化铝溶液滴入浓氢氧化钠溶液,立刻产生大量白色沉淀
社
学
采
道
文
渠
C. 将草酸溶液逐滴滴入酸性高锰酸钾溶:液,高锰酸钾溶液逐渐褪色
新
号
更
众
一
公
唯
信
微
D. 将打磨过的铁钉放入冷浓硫酸,产生大量刺激性气味气体微信公众号:文采学社
铁、铜及其化合物
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
P48
一、铁和铜的物理性质
铁元素在周期表中位于第四周期 第Ⅷ族,属于过渡金属。
铁的粉末为黑色,纯净的铁块是银白色金属,不仅有金属的通性
(良好的导热性、延展性),而且易被磁铁吸引,也可被磁化。
社
学
采
道
文
渠
:
新
号
更
众
一
铜元素在周期表中的位置是第四公周期 第IB族,属于过渡金属。
唯
信
微
铜是一种有金属光泽的紫红色金属,质软,具有良好的导电导热
性(仅次于银)、延展性。铜属于重金属、有色金属、常见金属、不
能被磁铁吸引。微信公众号:文采学社
P48
二、铁和铜的化学性质
(一)铁的化学性质
当铁与弱氧化剂(如盐酸、硫酸铜溶液等)反应时,只能失去2个电子
形成Fe2+,当铁与强氧化剂(如氯气、硝酸等)反应时,失去3个电子而形
社
学
成Fe3+。 道 采
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
P48
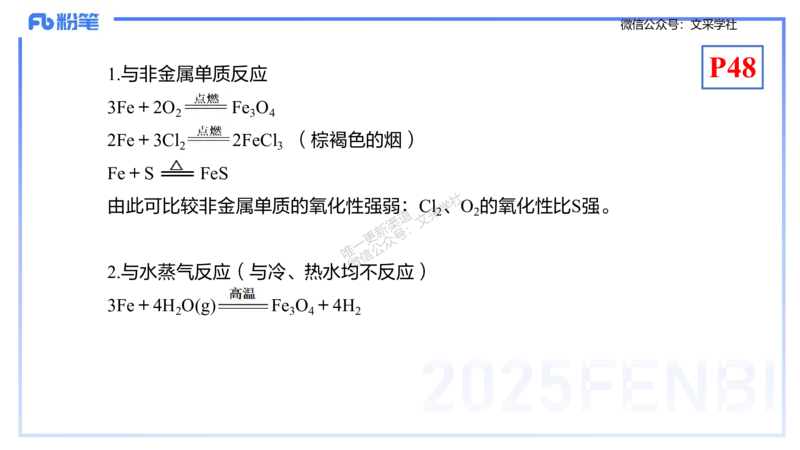
1.与非金属单质反应
3Fe+2O Fe O
2 3 4
2Fe+3Cl 2FeCl (棕褐色的烟)
2 3
Fe+S FeS
社
由此可比较非金属单质的氧化性强弱:Cl学、O 的氧化性比S强。
道 采2 2
文
渠
:
新
号
更
众
一
公
唯
信
微
2.与水蒸气反应(与冷、热水均不反应)
3Fe+4H O(g) Fe O +4H
2 3 4 2微信公众号:文采学社
P48
3.与酸反应
与非氧化性酸:Fe+2H+ Fe2++H ↑
2
与氧化性酸:
(1)在冷的浓HNO 或浓H SO 中钝化。
3 2 4
社
(2)反应时,酸过量的产物为Fe3+: 学
采
道
文
渠
:
新
号
Fe+4HNO (稀) Fe(NO ) +更 N众O↑+2H O
一
3 3 3 公 2
唯
信
微
4.与盐反应
Fe与CuSO 溶液反应的离子方程式:Fe+Cu2+ Cu+Fe2+
4
Fe与FeCl 溶液反应的离子方程式:Fe+2Fe3+ 3Fe2+
3微信公众号:文采学社
P49
(二)铜的化学性质
1.与非金属单质反应
2Cu+O 2CuO
2
铜在干燥的空气中很稳定,但在潮湿的空气中易被腐蚀。
社
学
2Cu+CO +H O+O Cu (OH) CO (铜绿)
采
2 2 2 2 2 道 文3
渠
:
新
号
更
Cu+Cl CuCl (棕黄色的一烟)众
公
2 2 唯
信
微
2Cu+S Cu S(黑色固体)
2
2.通入O 时,能与盐酸、硫酸反应
2
2Cu+O +4HCl 2CuCl +2H O
2 2 2微信公众号:文采学社
P49
3.与强氧化性酸(浓H SO 、硝酸)反应
2 4
Cu+2H SO (浓) CuSO +SO ↑+2H O
2 4 4 2 2
Cu+4HNO (浓) Cu(NO ) +2NO ↑+2H O
3 3 2 2 2
3Cu+8HNO (稀) 3Cu(NO ) +2NO↑+4H O
3 3 2 2
社
4.与盐溶液反应 学
采
道
文
渠
:
新
号
Cu+2Fe3+ Cu2++2Fe2+ 更 众
一
公
唯
信
微
Cu+2Ag+ Cu2++2Ag微信公众号:文采学社
P50
三、铁和铜的重要实验
(一)铁的氢氧化物的制备
1.实验原理
由相应的可溶性盐和碱溶液反应制得。
社
学
FeCl +3NaOH Fe(OH) ↓+3NaC道l 采
文
3 3 渠
:
新
号
更
众
一
FeSO +2NaOH Fe(OH) ↓唯 +N公a SO
4 2 信 2 4
微
2.实验步骤
在两支试管中分别加入少量的FeCl 溶液和FeSO 溶液,然后滴入
3 4
NaOH溶液。微信公众号:文采学社
P50
3.实验现象:
试管1中立即产生红褐色沉淀;
试管2中先生成白色絮状沉淀,随后变成灰绿色沉淀,最后变成
红褐色沉淀。
社
两支试管内分别发生反应: 学
采
道
文
渠
:
新
号
试管 1:FeCl +3NaOH Fe(O 更 H)众↓+3NaCl
一
3 公3
唯
信
微
试管 2:FeSO +2NaOH Fe(OH) ↓+Na SO 、
4 2 2 4
4Fe(OH) +O +2H O 4Fe(OH)
2 2 2 3微信公众号:文采学社
P50
4.制备Fe(OH) 时的注意事项
2
(1)所用亚铁盐溶液必须是新制的,NaOH溶液必须煮沸。
(2)滴管必须插入液面以下。
(3)往往在液面上加一层油膜,如苯或植物油等(以防止氧气
社
的氧化)。 学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
P50
(二)硫酸亚铁的制备
1.实验原理
Fe +H SO FeSO +H ↑
2 4 4 2
Fe O +3H SO Fe (SO ) +3H O
2 3 2 4 2 4 3 2
社
学
Fe+Fe (SO ) 3FeSO 采
2 4 3 4 道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
P50
2.实验步骤
在烧杯中加入稀H SO 和足量的铁屑。水浴加热,不要煮沸,到只有
2 4
极少量气泡产生并且溶液呈浅绿色时停止加热。
用少量热水预热过滤器,然后将反应溶液趁热过滤,并立即将滤液转
社
入试管中,静置冷却。 学
采
道
文
渠
:
新
号
看到浅绿色晶体析出,取出晶体更,众用少量蒸馏水洗涤2~3次,再用滤
一
公
唯
信
微
纸将晶体吸干。
将制得的硫酸亚铁放在广口瓶中,密闭保存。微信公众号:文采学社
3.注意事项
P51
(1)工业铁屑常附有油污,应先除去油污。
(2)铁屑中常有铁锈,与硫酸反应生成硫酸铁,可向反应溶液
中加入洁净的铁丝或铁片,使硫酸铁与铁反应,生成硫酸亚铁。
社
(3)必须趁热过滤,防止硫酸亚铁析出。学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
P51
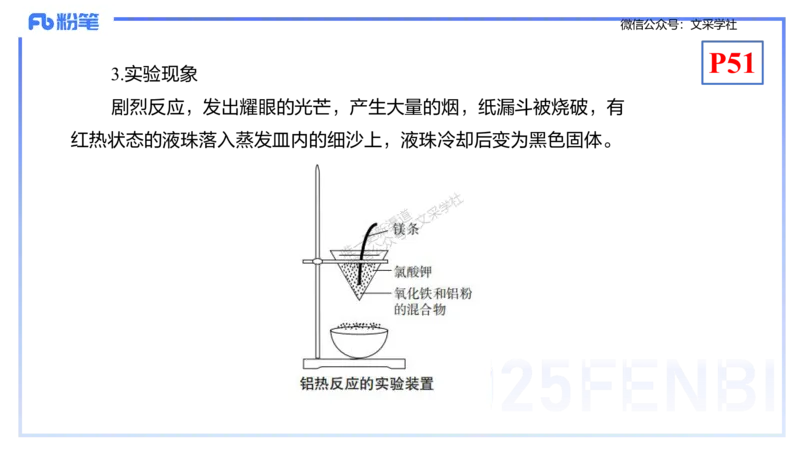
(三)铝热反应
1.实验原理
Fe O +2Al 2Fe+Al O
2 3 2 3
2.实验步骤
社
学
把少量干燥的氧化铁和适量的铝粉均匀混合后放在纸漏
采
道
文
渠
:
新
号
更
斗中,在混合物上面加少量氯酸钾固一体众,中间插一根用砂纸
公
唯
信
微
打磨过的镁条,点燃。微信公众号:文采学社
P51
3.实验现象
剧烈反应,发出耀眼的光芒,产生大量的烟,纸漏斗被烧破,有
红热状态的液珠落入蒸发皿内的细沙上,液珠冷却后变为黑色固体。
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
P51
4.注意事项
(1)要打磨干净镁条表面的氧化膜,否则难以点燃。
(2)纸漏斗要厚一些,并用水润湿。
(3)蒸发皿要垫适量的细沙:一是防止蒸发皿炸裂,二是防止熔融
社
的液体溅出伤人。 学
采
道
文
渠
:
新
号
(4)实验装置不要距人太近,防更止众使人受伤。
一
公
唯
信
微微信公众号:文采学社
P52
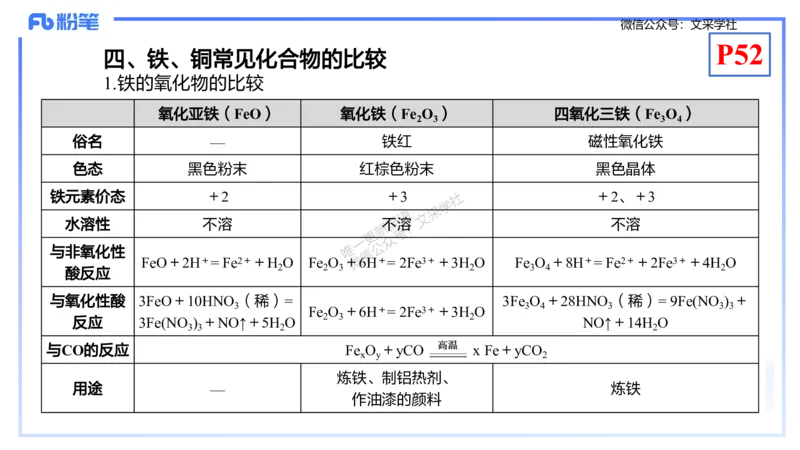
四、铁、铜常见化合物的比较
1.铁的氧化物的比较
氧化亚铁(FeO) 氧化铁(Fe O ) 四氧化三铁(Fe O )
2 3 3 4
俗名 — 铁红 磁性氧化铁
色态 黑色粉末 红棕色粉末 黑色晶体
铁元素价态 +2 +3 社 +2、+3
学
采
道
文
渠
水溶性 不溶 不溶: 不溶
新
号
更
众
一
公
与非氧化性 唯 信
FeO+2H+= Fe2++H O Fe O +微6H+= 2Fe3++3H O Fe O +8H+= Fe2++2Fe3++4H O
2 2 3 2 3 4 2
酸反应
与氧化性酸 3FeO+10HNO (稀)= 3Fe O +28HNO (稀)= 9Fe(NO ) +
3 3 4 3 3 3
Fe O +6H+= 2Fe3++3H O
2 3 2
反应 3Fe(NO ) +NO↑+5H O NO↑+14H O
3 3 2 2
与CO的反应 Fe O +yCO x Fe+yCO
x y 2
炼铁、制铝热剂、
用途 — 炼铁
作油漆的颜料微信公众号:文采学社
P52
2.铁的氢氧化物比较
化学式 Fe(OH) Fe(OH)
2 3
色态 白色固体 红褐色固体
与盐酸反应 Fe(OH) +2H+= Fe2++2H O Fe(OH) +3H+= Fe3++3H O
2 2 3 2
社
学
采
受热分解 — 道 文 2Fe(OH) Fe O +3H O
渠 : 3 2 3 2
新
号
更
众
一
公
唯
可溶性亚铁盐与碱反应信: 可溶性铁盐与碱反应:
微
制备 Fe2++2OH-= Fe(OH) ↓ Fe3++3OH-=Fe(OH) ↓
2 3
(白色絮状沉淀) (红褐色沉淀)
4Fe(OH) +O +2H O=4Fe(OH)
2 2 2 3
二者的关系
白色絮状沉淀→灰绿色沉淀→红褐色沉淀微信公众号:文采学社
P53
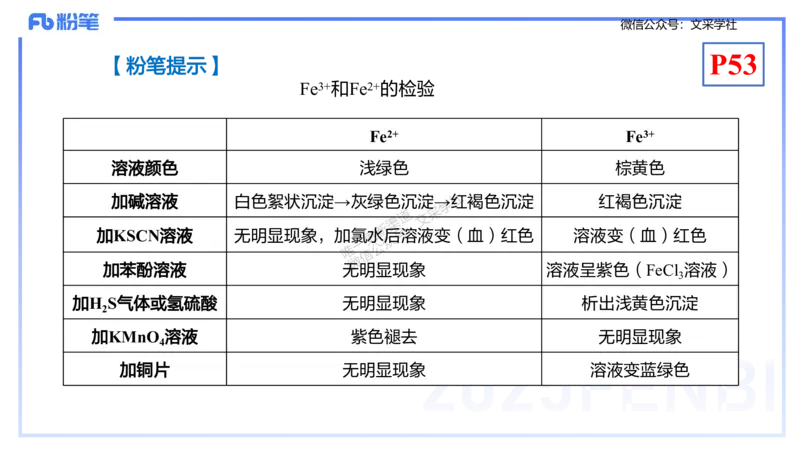
【粉笔提示】
Fe3+和Fe2+的检验
Fe2+ Fe3+
溶液颜色 浅绿色 棕黄色
社
加碱溶液 白色絮状沉淀→灰绿色沉淀→红褐色沉淀 红褐色沉淀
学
采
道
文
渠
:
新
加KSCN溶液 无明显现象,加氯更水后号溶液变(血)红色 溶液变(血)红色
众
一
公
唯
信
微
加苯酚溶液 无明显现象 溶液呈紫色(FeCl 溶液)
3
加H S气体或氢硫酸 无明显现象 析出浅黄色沉淀
2
加KMnO 溶液 紫色褪去 无明显现象
4
加铜片 无明显现象 溶液变蓝绿色微信公众号:文采学社
P53
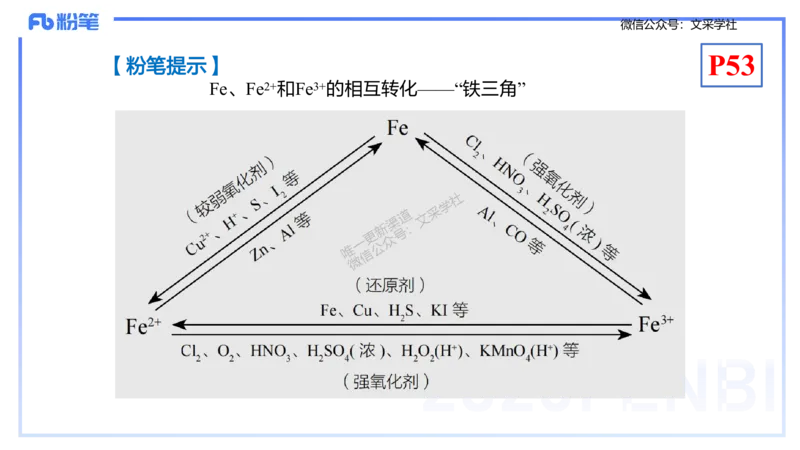
【粉笔提示】
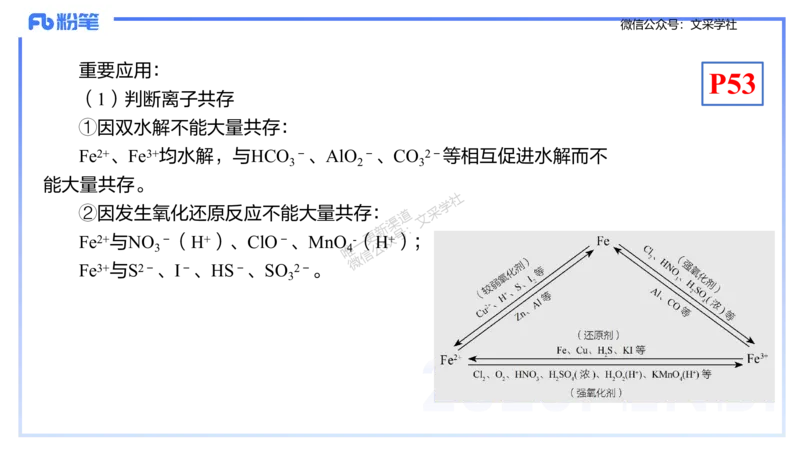
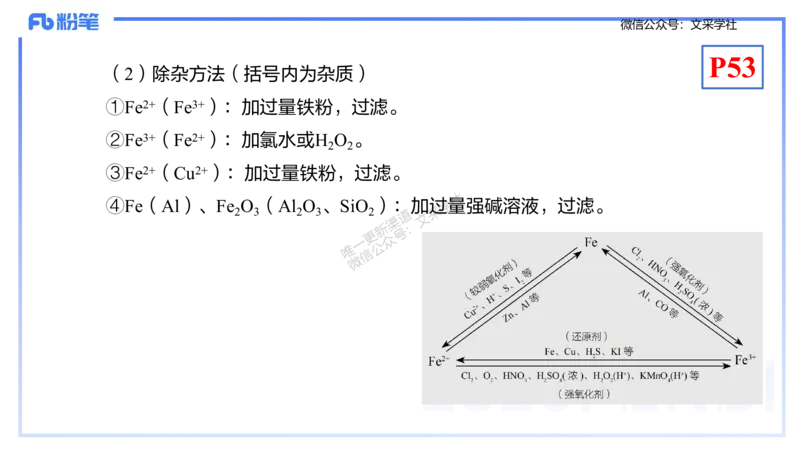
Fe、Fe2+和Fe3+的相互转化——“铁三角”
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
重要应用:
P53
(1)判断离子共存
①因双水解不能大量共存:
Fe2+、Fe3+均水解,与HCO -、AlO -、CO 2-等相互促进水解而不
3 2 3
能大量共存。
社
学
②因发生氧化还原反应不能大量共存: 道 采
文
渠
:
新
号
更
Fe2+与NO -(H+)、ClO-、MnO 一-(H众+);
公
3 唯4
信
微
Fe3+与S2-、I-、HS-、SO 2-。
3微信公众号:文采学社
P53
(2)除杂方法(括号内为杂质)
①Fe2+(Fe3+):加过量铁粉,过滤。
②Fe3+(Fe2+):加氯水或H O 。
2 2
③Fe2+(Cu2+):加过量铁粉,过滤。
社
④Fe(Al)、Fe O (Al O 、SiO ):加过学量强碱溶液,过滤。
2 3 2 3 2 道 采
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
P54
3.氧化铜和氢氧化铜比较
物质 氧化铜 氢氧化铜
化学式 CuO Cu(OH)
2
社
状态 不溶于水的黑色固体(粉末) 学 不溶于水的蓝色晶体
采
道
文
渠
:
新
号
更
众
一
CuO+2H+= Cu2+
唯
+H公O
信2
微 Cu(OH) +2H+= Cu2++2H O
2 2
化学性质 CuO+H Cu+H O
2 2
Cu(OH) CuO+H O
2 2
CuO+CO Cu+CO
2
制备 Cu(OH) CuO+H O Cu2++2OH-= Cu(OH) ↓
2 2 2微信公众号:文采学社
【粉笔提示】
P54
1. 溶液中的 Cu2+ 常为蓝色,可作为 Cu2+ 的判定依据。
2. Cu2+ 与碱反应生成蓝色沉淀 Cu(OH) ,Cu(OH) 溶于氨水形成
2 2
深蓝色溶液,这是鉴定 Cu2+ 的原理之一。
3. 无水 CuSO 遇水变蓝色(生成 CuSO ·5H社O),可作为水的检
4 4 学2
采
道
文
渠
验依据。 新 :
号
更
众
一
公
唯
信
4. CuSO 和石灰乳的混合液就是微无机农药波尔多液,它是一种良
4
好的杀菌剂,可以用来防治多种作物的病害。微信公众号:文采学社
5. Cu O 是一种红色粉末,在非氧化性酸溶液中发生歧化反应:
2 P54
Cu O+2H+ Cu+Cu2++H O。
2 2
6. Cu S、CuS 均为黑色粉末,难溶于水和非氧化性酸,能被硝酸
2
等氧化性酸溶解。
社
CuS 可由反应 H S+CuSO CuS↓+H S学O 制得,该反应不符
2 4 道 2采 4
文
渠
:
新
号
合强酸制弱酸规律。 更 众
一
公
唯
信
微
7. FeS 能与非氧化性酸反应,生成硫化氢,除去 CuS 中混有的
FeS 可以用盐酸。微信公众号:文采学社
P55
1. 下列说法不正确的是( )。
A. 铁是具有银白色光泽的金属
B. 铁制品在潮湿空气中易生锈
社
C. 铁矿石冶炼生铁、生铁冶炼成钢都是化学变化
学
采
道
文
渠
:
新
号
更
D. 生铁是纯铁,钢是含碳量在 0.03%一 ~众 2% 的铁合金
公
唯
信
微微信公众号:文采学社
P56
2. 在给定条件下,下列选项所表示的物质间转化均能实现的是( )。
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微
粉笔教师教育 粉笔教师