文档内容
化学A答案解析
✍ 变试题原题答案
【原卷 1 题】 【正确答案】D
【试题解析】
【原卷 2 题】 【正确答案】D
【试题解析】
【原卷 3 题】 【正确答案】C
【试题解析】
【原卷 4 题】 【正确答案】C
【试题解析】
【原卷 5 题】 【正确答案】A
【试题解析】
33/59【原卷 6 题】 【正确答案】C
【试题解析】
【原卷 7 题】 【正确答案】C
【试题解析】
【原卷 8 题】 【正确答案】A
【试题解析】
【原卷 9 题】 【正确答案】A
【试题解析】
34/59【原卷 10 题】 【正确答案】B
【试题解析】
【原卷 11 题】 【正确答案】C
【试题解析】
【原卷 12 题】 【正确答案】D
【试题解析】
【原卷 13 题】 【正确答案】D
【试题解析】
【原卷 14 题】 【正确答案】B
35/59【试题解析】
【原卷 15 题】 【正确答案】D
【试题解析】
【原卷 16 题】 【正确答案】
【试题解析】
【原卷 17 题】 【正确答案】
36/59【试题解析】
【原卷 18 题】 【正确答案】
【试题解析】
37/59【原卷 19 题】 【正确答案】
【试题解析】
38/59精准训练答案
B.O 的电子式为 ,B错误;
2
✍ 变试题答案
C.基态 Ge位于元素周期表第四周期第ⅣA族,其
1-1【基础】 【正确答案】D 32
【试题解析】【详解】A.氮化硼陶瓷属于无机非金属 价层电子排布式为4s24p2,C错误;
材料,A正确; D.NH 的中心N原子为sp3杂化,其VSEPR模
3
B.硅为半导体材料,B正确;
C.氧化铝硬度大、熔点高,木地板表面的氧化铝有
型: ,D正确;
耐磨和阻燃作用,C正确;
D.明矾常用作净水剂是因为明矾溶液中生成的氢氧
故答案选D。
化铝胶体能吸附水中悬浮的杂质,但不能够杀菌消
2-2【巩固】 【正确答案】B
毒,D错误;
【试题解析】【详解】A.质量数为16和18的O原子
答案选D。
应该表示为16O和18O,18O可作为有机反应示踪原
1-2【巩固】 【正确答案】C 8 8 8
【试题解析】【详解】A. 粒子直径为 1nm~100nm的 子,A错误;
Fe粉为纯净物不属于胶体,若把它分散在水中可形 B.二氯甲烷中含有两根碳氢键和两根碳氯键,键长
成胶体,A错误;
不一样,球棍模型为 ,B正确;
B. 维生素 C常用作水果罐头的抗氧化剂,具有较
强还原性、容易被氧化,B错误;
C.CsCl为离子化合物,用电子式表示的形成过程
C.二氧化氯是利用强氧化性杀菌,酒精是利用使蛋
为: ,C错误;
白质变性杀菌,二者消毒原理不相同,C正确;
D.氮化硅耐高温结构材料属于新型无机非金属材 D.基态 Cu原子核外含有29个电子,价层电子排
29
料,D错误;
布式:3d104s1,D错误;
答案选C。
故选B。
1-3【提升】 【正确答案】A
2-3【提升】 【正确答案】A
【试题解析】【详解】A.由题意可知,氧化铝陶瓷属
【试题解析】【详解】A.基态 Br原子的电子数为
于新型无机非金属材料,不属于金属材料,故A错
35,位于第VIIA族,其价电子排布式为4s24p5,A
误;
B.维生素C具有强大的抗氧化作用,所以常用作还 正确;
原剂,故B正确;
B.SiO 属于共价晶体,Si原子周围连有4个O原
2
C.性能优良的水泥属于传统无机非金属材料,故C
子,呈正四面体形,B错误;
正确;
D.布、麻布的成分是天然有机高分子化合物纤维 C.NiCO 中Ni提供空轨道,CO中C的电负性小
4
素,属于天然有机高分子材料,故D正确;
于O,更易提供孤电子对,故配位键表示错误,正确
故选A。
2-1【基础】 【正确答案】D
【试题解析】【详解】A.H O 中O原子为sp3杂化, 的为 ,C错误;
2 2
球棍模型不是直线形,A错误;
39/59C.N原子的2p能级为半满结构,更稳定,故第一
D.MgCl 中的离子键是通过Mg失电子,Cl得电子
2
电离能大于O,C错误;
形成的,图示得失电子错误,正确的应表示为
D.H O分子间存在氢键,故沸点高于H S,D错
2 2
误;
故选A。
,D错误;
故选A。
4-1【基础】 【正确答案】A
3-1【基础】 【正确答案】A
【试题解析】【详解】A.钠燃烧剧烈,即使佩戴护目
镜,近距离俯视仍可能被高温或飞溅物伤害,A错
【试题解析】【详解】A.二者同主族且O位于S的上
误;
方,O原子半径更小,O原子核对核外电子的束缚更
B.焰色试验可能产生烟雾或有害气体,开启排风设
强,O更难失去电子,因此第一电离能:I (O)>
1
备符合安全规范,B正确;
I (S),A正确;
1
C.导电实验涉及电流,湿手操作易触电,禁止湿手
B.Al3+和O2-电子层结构相同(核外均有10个电
操作正确,C正确;
子),核电荷数越大,离子半径越小,故r(O2-)>
D.加热实验需避免衣物或长发接触热源,束发系紧
r(Al3+),B错误;
衣物符合安全要求,D正确;
C.H O分子间存在氢键,而H S分子间仅存在范德
2 2
故选A。
华力,氢键的强度大于范德华力,故沸点:H O>
2
H S,C错误;
4-2【巩固】 【正确答案】B
2
D.电负性是元素的原子在化合物中吸引电子的能力
【试题解析】【详解】A.金属钠性质活泼,随意丢弃
可能引发危险,正确做法是放回原瓶,故A正确;
的标度,H的电负性(约2.20)大于Al(约1.61),
故χ(Al)<χ(H),D错误; B.钡的化合物并不是都有毒,如硫酸钡(BaSO )
4
答案选A。
难溶于水且无毒,故B错误;
3-2【巩固】 【正确答案】D
C.碱液灼伤处理步骤正确,先大量水冲洗再用2%
【试题解析】【详解】A.同主族元素,从上到下金属
的硼酸溶液冲洗,故C正确;
性增强,其最高价氧化物对应水化物碱性增强,K金
D.硝酸具有腐蚀性和挥发性,使用时需要防护和通
属性强于Na,所以碱性KOH > NaOH,A错误;
风,故D正确;
B.同周期主族元素,从左到右电负性增大,Cl和
答案选B。
Na同周期,且Cl在Na右边,所以电负性
4-3【提升】 【正确答案】C
χ(Cl)>χ(Na),B错误;
【试题解析】【详解】A.钠和白磷性质活泼,需放回
C.碱金属元素从上到下,金属键减弱,沸点降低,
原试剂瓶避免危险,A正确;
K在Na下方,所以沸点TKχC,A正确;
CaO+H O=Ca(OH) ,A正确;
2 2
B.K+、S2-的电子层结构相同,S的核电荷数小,
B.碳酸氢钠的弱碱性使其能中和胃酸,发生反应:
半径大,故r
K+
Z>W ,D错误;
3 3
D.海带中的碘以I⁻形式存在,直接加淀粉不会显蓝 故答案选B。
色,需氧化为I
2
后才能显色,D错误; 9-2【巩固】 【正确答案】C
故选C。 【试题解析】【分析】X最外层电子数为内层2倍,内
8-3【提升】 【正确答案】B 层为K层(2e⁻),故X为C(最外层4e⁻);Z是地壳
【试题解析】【详解】A.向NaHCO
3
溶液中滴加 中含量最高的元素,为O; W与Z同主族
(ⅥA),原子序数更大,故W为S;Y原子序数介
Na[Al(OH) ]溶液,[Al(OH) ]-结合HCO-电离出的氢
4 4 3
于C和O之间,为N元素。
离子生成Al(OH)
3
沉淀和CO
3
2-,HCO
3
- 和[Al(OH)
4
]- 【详解】A.XW
2
为CS
2
(C的价电子对数为
4-2´2
未发生相互促进水解,A错误; 2+ =2,直线形,键角180°),WZ 为SO
2 2
2
B.铁离子会和二氧化硫反应生成亚铁离子和硫酸根
6-2´2
(S的价电子对数为2+ =3,V形,键角小
离子,溶液先变为红棕色,过一段时间又变成浅绿 2
色,Fe3+与SO 络合生成红棕色,则Fe3+与SO 络合 于120°),故A错误;
2 2
反应的反应速率比氧化还原反应生成亚铁离子的速率 4-2´2
B.XZ 为CO ,C的价电子对数为2+ =2,
2 2
2
快,最终显浅绿色说明氧化还原反应的平衡常数更
无孤独电子,CO 为非极性分子,WZ 为SO ,V形
大, B正确; 2 2 2
结构,SO 为极性分子,极性:CO <SO ,故C错
C.新制氯水中含有HCl,加入AgNO 溶液,生成 2 2 2
3
误;
AgCl白色沉淀,HClO和氯气均能与KI发生氧化还
C.C价电子数4,N价电子数5,4<5,故C正
原反应生成碘单质,使溶液变蓝,不能说明氯气与水
确;
的反应存在限度,C错误;
D.Z的气态氢化物为H O,W的气态氢化物为
D.pH=2的HA和H B溶液中,HA放出更多H , 2
2 2
H S,二者均为分子晶体,H O分子间存在氢键,沸
pH相同时,弱酸HA的浓度更高,与Zn反应产生更 2 2
点更高,故D错误;
多H ,说明HA的酸性弱于H B,D错误;
2 2
故选C。
故选B。
9-3【提升】 【正确答案】B
9-1【基础】 【正确答案】B
【试题解析】【分析】由X最外层电子数是内层2倍可
【试题解析】【分析】(YW
2
)
2
XZ为有机物,基态X、
Z原子均有2个单电子,X、Z分别为IVA族和VIA
知X为C(最外层4,内层2); 由Y与X相邻且
族元素,X、Y、Z同周期、原子序数依次增大,若
同周期可知Y为N;由X、Y与Z原子核外电子层
X、Y、Z为第三周期元素,则X、Y、Z分别为Si、
数相同且Z是同周期原子半径最小可知Z为F(第二
P、S;若X、Y、Z为第二周期元素,则X、Y、Z
周期ⅦA族);W原子序数大于Z且最高能级单电
分别为C、N、O;又YW ZXY为无机物,
4
子可推出W可能为Na(3s1)或Al(3p1),据此分
(YW ) XZ为有机物,所以X、Y、Z分别为C、N、
2 2
析解答。 O,W、X、Y、Z原子序数依次增大,能形成
【详解】A.若W为Na,A正确;若为Al,A错 YW ZXY,则W为H,综上所述,W、X、Y、Z分
4
误,题目未明确W,无法确定,A错误; 别为H、C、N、O。
【详解】A.W与Z形成的化合物可能含有非极性键
B.C与F形成CF ,结构为正四面体,B正确;
4
(如H O 中的O-O键),因此并非只含极性共价
2 2
C.第一电离能F>N>C,即Z>Y>X ,C错误;
键,A错误;
D.当电子层数相同时,原子序数越小,半径越大,
B.甲为NH OCN,其中的C原子与N原子形成三
4
43/59键、与O原子形成单键,价层电子对数为2,无孤对 D.1个1,1-环丁二羧酸分子中,σ键包括:6个C-
电子,C原子采取sp杂化,B正确; C键、6个C-H键、4个C-O键、2个O-H键,总计
C.由分析可知,X、Y、Z分别为C、N、O,同一 6+6+4+2=18个,故1 mol的1,1-环丁二羧酸含18
周期从左往右元素第一电离能呈增大趋势,ⅡA与 N 个σ键,D正确;
A
ⅢA、ⅤA与ⅥA反常,即第一电离能顺序应为N 故答案选D。
(Y)>O(Z)>C(X),而非Z>Y>X,C错 10-3【提升】 【正确答案】B
误; 【试题解析】【详解】A.连接4个不同原子或基团的
D.X、Y、Z的氢化物中,水在常温常压下为液体, 碳原子为手性碳原子,则该分子中不含手性碳原子,
氨气和甲烷为气体,H O(Z的氢化物)沸点最高, 故A正确;
2
而非NH (Y的氢化物),D错误; B.该分子中有饱和碳原子(乙基上的碳),采用sp3杂
3
故答案选B。 化,故B错误;
10-1【基础】 【正确答案】C
C.含有羧基,与NaOH、Na CO 、NaHCO 溶液
2 3 3
【试题解析】【详解】A.谷氨酸含有羧基(-COOH)
都能发生反应,故C正确;
和氨基(-NH ),均为亲水基团,氨基酸一般易溶于
2 D.分子中含有8种等效氢:
水,A正确;
B.手性碳需连接四个不同基团,谷氨酸中与氨基 ,故一氯代物
(-NH )相连的碳原子(α碳)连接-COOH、
2
一共有8种,故D正确;
-NH 、-CH CH COOH和-H,为手性碳,且分子中
2 2 2 答案选B。
仅有1个手性碳,B正确; 11-1【基础】 【正确答案】D
C.谷氨酸中羧基(-COOH)的碳原子形成C=O双 【试题解析】【详解】A.Cu与混酸反应,
3Cu+8HNO (稀)=3Cu(NO ) +2NO↑+4H O,离子反应
键,价层电子对数为3,杂化方式为sp2,并非所有 3 3 2 2
为:3Cu+8H++2NO -=3Cu2++2NO↑+4H O,从方程式
3 2
C原子均为sp3杂化,C错误; 知,硝酸根离子由硝酸提供,氢离子由硝酸和硫酸提
供,所以硝酸为2mol时,硫酸为3mol,用混酸中
D.谷氨酸分子内氨基(-NH )与γ-羧基(-
2
H SO 与HNO 物质的量之比最好为3:2,A错误;
2 4 3
COOH)可脱水形成肽键(-CONH-),构成含N、 16g
B.16g硫酸铜的物质的量为 =0.1mol,在途
C、C、C、C的五元环状结构(焦谷氨酸),D正 160g/mol
Δ
确; 径③中,发生的反应为2H SO (浓)+Cu
2 4
故选C。
CuSO +2H O+SO ↑,消耗硫酸0.2mol,B错误;
4 2 2
10-2【巩固】 【正确答案】D
C.若均生成1mol硫酸铜,途径①消耗硫酸1mol硫
【试题解析】【详解】A.碳铂分子中没有连接四个不
酸;途径②消耗1mol硫酸,途径③消耗2mol硫
同基团的碳原子,因此不含手性碳,A错误;
酸,C错误;
B.碳铂中Pt2+与2个NH 的N原子及2个羧酸根的
3 D.相对于途径①、③均有污染空气的气体产生,
O原子配位,配位数为4,B错误;
途径②的优点:铜与氧气反应生成氧化铜,氧化铜
C.1,1-环丁二羧酸中,环丁烷的4个碳均为sp3杂
再被硫酸溶解生成硫酸铜,制取等质量胆矾需要的硫
化,2个羧基碳为sp2杂化,因此sp3杂化的碳原子与 酸少、途径2无污染性气体产生,D正确;
故选D。
sp2杂化的碳原子数之比为2:1,C错误;
【点睛】本题考查制备方案的评价,注意根据反应途
44/59径,写出相关反应的离子方程式或化学方程式,利用 【试题解析】【详解】A.KI中I元素的化合价由-1价
方程式进行判断较为简单。本题的易错点为C,途径
升高到0价,则KI作还原剂,VO 中V元素的化
2 5
8 2
①中制备1mol硫酸铜,需要 molH+和 molNO-,
3 3 3 合价由+5价降低到+4价,则VO 作氧化剂,故氧化
2 5
2
可以由1mol硫酸和 mol硝酸提供。
3 剂与还原剂的物质的量之比为1∶2,A错误;
11-2【巩固】 【正确答案】C
B.生成2mol VOCl ,转移2mol电子,则生成
2
【试题解析】【详解】A.途径①反应的化学方程式为
Δ 1mol VOCl 时转移1mol 电子,B正确;
S+6HNO (浓) H SO +6NO ↑+2H O,浓硝酸体现了 2
3 2 4 2 2
强氧化性,故A正确; C.VO 中V显+5价,处于最高价,O显-2价,处
2 5
B.氧气来源于空气,价格较低,增大氧气的浓度可
于最低价,即VO 既具有氧化性又具有还原性,C
2 5
提高二氧化硫的转化率,从而降低成本,故B正
正确;
确;
C.途径①和途径②中的硫元素的价态都是从0价 D.在酸性过强时,S O2-与H+反应生成S、SO 和
2 3 2
升高到+6价,转移6 mol电子,故C错误;
H O,D正确;
D.途径①中会产生NO 有毒气体,途径②比途径 2
2
①的污染相对较小且原子利用率较高,更能体现“绿 故选A。
色化学”的理念,故D正确; 12-2【巩固】 【正确答案】C
故选C。 【试题解析】【详解】A.配制精确浓度的溶液需用分
11-3【提升】 【正确答案】B 析天平,托盘天平精度不足,A错误;
【试题解析】【详解】A.催化剂在反应前后质量和化 B.酸性条件下不可能生成OH-,正确反应式应包含
学性质不变,参与反应并循环生成,由机理图可知,
H+和H O,B错误;
2
Cu+参与反应①②③并最终再生,Cu+是催化剂;而
Cu+(SO )是中间产物,故A错误; C.煮沸驱赶I ,确保后续滴定仅测定剩余KIO 生成
3 2 3
B.过程②中Cu+(O )氧化SO 生成Cu+(SO ),氧化
2 2 3
的I ,C正确;
2
性O >SO ;过程③中Cu+(SO )氧化丙烯生成
2 3 3
D.I 与淀粉形成的蓝色络合物不易解离,会影响I
CO ,氧化性SO >CO ,所以氧化性: 2 2
2 3 2
与硫代硫酸钠的反应,使滴定终点判断不准确,应在
O >SO >CO ,故B正确;
2 3 2
剩余I 量较少(滴定至溶液呈淡黄色)时再加入淀粉指
2
C.过程③中,丙烯(C H ,C平均-2价)被氧化为
3 6 示剂,D错误;
CO (C+4价),每个C失6e-;Cu+(SO )中S元素化合
2 3 故答案选C。
价由+6降低为0价,每个S得6e-,根据得失电子守
12-3【提升】 【正确答案】D
恒,氧化产物CO 与还原产物S的物质的量之比为
2 【试题解析】【详解】A.应用分析天平称取样品5.000
1:1,故C错误;
g,A错误;
D.总反应需结合所有过程,过程①消耗O ,故总
2 B.FeCl 水解显酸性应用酸式滴定管量取待测液,B
3
Cu+ 错误;
反应应为2C H +6SO +3O 6S+6CO +6H O,
3 6 2 2 2 2
C.滴定指示剂可选择淀粉溶液,为了使结果更可
靠,应该重复进行三次滴定,最终取三次滴定结果的
故D错误;
平均值,C错误;
选B。
D.氯化铁溶液和碘化钾溶液的反应存在一定的限
12-1【基础】 【正确答案】A
45/59度,氯化铁不能完全反应,反应生成碘的量偏小,导
O ~4e-,根据转移电子相等可得消耗的氧气的物质
2
致消耗硫代硫酸钠溶液的体积偏小,使测定结果偏
0.8
低,D正确; 的量为 mol =0.2mol,D正确;
4
故选D。
故选D。
13-1【基础】 【正确答案】C
13-3【提升】 【正确答案】A
【试题解析】【分析】该装置为化学电源,根据原电池
【试题解析】【详解】A.固体氧化物燃料电池中,N
工作原理,通燃料一极为负极,即通N H 一极为负
2 4 极通入O 为正极,M极通入燃料为负极,电解质传
2
极,则另一极为正极,据此分析;
导O2-,阴离子向负极移动,即O2-向M极移动,箭
【详解】A.Pt 电极通入O ,O 作为氧化剂在燃料
2 2 2 头方向表示O2-的移动方向,A正确;
电池中得电子,发生还原反应,作正极,故A说法
B.N极为正极,固体氧化物电解质传导O2-,无
正确;
H O参与,正极反应式应为O +4e-=2O2-,B错误;
2 2
B.原电池中阳离子向正极移动,Pt 为正极,K+由
2
C.燃料可能为H 、CO、CH 等,若燃料为CO,产
负极区(Pt )向正极区(Pt )移动,故B说法正确; 2 4
1 2
物X为CO ,不含H O,C错误;
C.燃料电池的主要能量转化形式是化学能→电能, 2 2
D.燃料电池直接将化学能转化为电能,无需经过热
虽反应本身放热,但能量主要转化为电能而非大量放
能环节,D错误;
热,故C说法错误;
故答案选A。
D.Pt 为正极,O 在碱性条件下得电子生成OH-,
2 2
电极反应式为O +4e-+2H O=4OH-,故D说法正确;
14-1【基础】 【正确答案】B
2 2
答案为C。
【试题解析】【详解】A.由图可知,反应开始一段时
间内Y的浓度变化快,Z的浓度变化慢,故反应①
13-2【巩固】 【正确答案】D
【试题解析】【分析】一种熔融碳酸盐燃料电池的工作 活化能低,反应②活化能高,即E Ⅰ<E Ⅱ,A
a a
原理如图所示,电极B通入O 为正极,电极A通入 错误;
2
B.由题干图像信息可知,4s末时Y为0.8mol/L、Z
的CO和H 作负极。
2
为0.2mol/L,即0~4s内X减少了
【详解】A.根据分析电极A为负极,A错误;
0.8+0.2=1.0mol/L,故0~4s内反应Ⅰ的平均速率
B.B电极通入的氧气在该极上得电子,该电解质溶
1.0mol/L
uX= =0.25mol×L-1×s-1,B正确;
液中无氢氧根,正确的极反应为 4s
C.升高温度,反应Ⅰ、Ⅱ的速率均增大,由题干信息
O +2CO +4e- =2CO2-,B错误;
2 2 3
可知,两个反应均为放热反应,则升高温度平衡逆向
C.电池工作时阳离子在电解质溶液中移向正极,该
移动,故平衡转化率均减小,C错误;
电池中K+从A电极迁移向B电极,C错误;
D.由题干信息可知,两个反应前后气体的系数均保
D.标况下,2.24L甲烷的物质的量为
持不变,即反应体系中气体的总物质的量一直不变,
2.24L
=0.1mol,根据反应 混合气体的质量不变,即体系内气体的平均摩尔质量
22.4L·mol-1
一直保持不变,故体系内气体的平均摩尔质量不再变
CH +H O=CO+3H 可知生成的0.1 molCO和0.3
4 2 2 化,不能说明反应达到新平衡,D错误;
故答案为:B。
molH 进入负极发生氧化反应分别生成CO 和
2 2
14-2【巩固】 【正确答案】C
H
2
O,则共转移电子的物质的量为0.2+0.6=0.8 【试题解析】【详解】A.(Ⅰ)和(Ⅱ)反应前后气体总质量
不变,在恒温恒压条件下,混合气体的密度不变时,
mol,另一极即正极消耗的氧气与转移电子间关系为
容器容积不变,容器内混合气的总物质的量不变,正
46/59逆反应速率相等,反应(Ⅰ)和(Ⅱ)均达到平衡状态,A
反应Ⅱ4NH (g)+3O (g) 2N (g)+6H O(g)
3 2 ƒ 2 2 则平衡
正确;
转化量/mol 0.1 0.075 0.05 0.15
B.催化剂具有选择性,在反应体系未达平衡前使用
nNH =2mol-1.8mol-0.1mol=0.1mol,nO =3mol-2.25mol-0.075mol=0.675mol
3 2
催化剂,有利于反应Ⅱ发生,使甲醇产率提高,B正
,nH O=2.7mol+0.15mol=2.85mol,则反应Ⅰ的平
确; 2
1
C.由图可知, 增大即T减小时,lgK 增大,则降 c4(NO)´c6H O 1.84´2.856
T 2 衡常数K= 2 = >10,D
c4NH ´c5O 0.14´0.6755
3 2
温反应Ⅱ平衡正向移动,则反应Ⅱ为放热反应,△H<
正确;
0,反应正向气体分子数减小,△S<0,故该反应在
故选B。
低温时△H-T△S<0,有利于反应自发进行,C错
误;
15-1【基础】 【正确答案】B
1 【试题解析】【详解】A.生成X是在不饱和碳原子上
D. 增大即T减小时,lgK 增大,则降温反应Ⅱ平
2
T 加上其他原子团,故X是加成产物,生成Y时是苯
衡正向移动,则反应Ⅱ为放热反应lgK 减小,则降温
1 环上的H被硝基代替,故Y是取代产物,A正确;
反应Ⅰ平衡逆向移动,则反应Ⅰ为吸热反应,故升高温
B.M的六元环中与— NO 相连的C为sp3杂化,其
2
度时,反应Ⅰ平衡正向移动,反应Ⅱ平衡逆向移动,如
余碳原子为sp2杂化,B错误;
温度升高对平衡的Ⅱ的影响程度更大,则CO 的转化
2
C.第一步反应的活化能大于第二步反应的活化能,
率可能下降,D正确;
故该反应的决速步为反应①,C正确;
故答案为:C。
D.生成产物Ⅱ的反应的活化能更低,因此反应速率
14-3【提升】 【正确答案】B
更快,且产物Ⅱ的能量更低即产物Ⅱ更稳定,以上2
【试题解析】【详解】A.硝酸工业中物质的转化关系
个角度均有利于产物Ⅱ,D正确;
是NH ®NO®NO ®HNO ,840℃时,反应Ⅰ对应
3 2 3
故选B。
的NH 的转化率达到最高,即生成的NO最多,且温
3 15-2【巩固】 【正确答案】A
度升高化学反应速率增大,A正确;
【试题解析】【详解】A.苯环中的C都是sp2杂化,
B.由题给信息可知,图像中对应的是相同反应时间
生成的中间体中连接-NO 的碳原子为饱和碳原子,
2
的转化率,C点之后,也可能随着温度升高,导致催
这个碳原子杂化方式为sp3,碳的杂化方式发生了变
化剂失活,使反应Ⅰ的反应速率降低,则相同反应时
化,A错误;
间内,NH 的转化率也降低,B错误;
3 B.从图中可知,生成中间体的反应活化能最大,活
C.NH 和N 分别是反应物和生成物,充入NH 和
3 2 3 化能越大反应速率越慢,因此生成中间体的反应为决
O 发生反应,NH 的量逐渐减少,N 的量逐渐增
2 3 2 速步骤,B正确;
cNH
大,因此混合体系中 3 保持不变说明反应Ⅱ达 C.根据图示可知,苯环与NO+ 2 、-OSO 3 H反应生成
cN
2
产物I,苯环上的化学键断裂,与磺酸基和硝基加
到平衡状态(提醒:若给定条件下推出“变量”达到
成,该反应为加成反应,C正确;
“不变”,则可说明反应达到平衡状态),C正确;
D.生成产物2为放热反应,生成产物1为吸热反
D.C点时,反应Ⅰ、反应Ⅱ对应的NH 的转化率分别
3 应,此外中间体生成产物2的活化能更低,反应速率
为90%、5%,则生成NO的物质的量为1.8mol,生
也更快,因此动力学和热力学优势产物均为产物2,
成N 的物质的量为0.05mol,则有:
2 D正确;
反应Ⅰ4NH (g)+5O (g) 4NO(g)+6H O(g) 故选A。
3 2 ƒ 2
转化量/mol 1.8 2.25 1.8 2.7
15-3【提升】 【正确答案】B
47/59【试题解析】【详解】A.“路径I”中CO
2
的碳原子的
H O+H SeO +2SO =Se+2H SO ;
2 2 3 2 2 4
杂化方式为sp,CH OH的碳原子的杂化方式为sp3,
3
1 1
A错误; (4)①据“均摊法”,晶胞中含8´ +6´ =4个
8 2
B.读图可知,“路径I”反应
1
Se、4´ =2个Ga,则该晶体的化学式为InSe 。
H COOH*→CH O*+OH*的Ea=-45.4- 2 2
2 2
②结合①分析,该晶体的密度为
(132.1)=86.7kJ/mol,B正确;
2M
C.根据图示,图中初始为CO *和OH*,只有部分
2
N 2´(115+79´2) ;
A g×cm-3= g×cm-3
反应历程,并没有给出CO
2
和H
2
的相对能量,无法
a2c´10-30 N ´a2c´10-30
A
判断反应是放热反应还是吸热反应,C错误;
(5)A.α-Ti Au立方晶胞结构如图,Au位于顶
3
D.催化剂只改变反应历程,不改变反应始态和终
态,即不改变反应的焓变,D错误;
点、Ti位于面心,则Au周围最近且等距的Ti的个数
为12,正确;
故选B。
16-1【基础】 【正确答案】(1) p B.SeO 的中心原子Se原子的价层电子对数为
3
6-2´3
3+ =3,为sp2杂化,为平面三角形;SeO2-的
2 3
中心原子Se原子的价层电子对数为
(2)Se与Te同主族,非金属性Se>Te,Se更易与H
2
6+2-2´3
生成气态氢化物,从而与Te分离 3+ =4,为sp3杂化,有一对孤对电子,为
2
(3) sp3 四面体 三角锥形,则键角大小关系SeO >SeO2-,错误;
3 3
H O+H SeO +2SO =Se+2H SO C.同周期越靠右,第一电离能越大,其中第ⅡA、
2 2 3 2 2 4
ⅤA的元素由于其电子排布为稳定结构,第一电离能
2´(115+79´2)
(4) InSe
2 N ´a2c´10-30 较大,故As、Se、Br三种元素第一电离能由大到小
A
(5)AC 排序Br>As>Se,正确;
【试题解析】【详解】(1) D.CN-做配体时,氮的电负性大于碳,则碳更容易
主族元素In原子序数为49,价电子排布式: 提供孤电子对而做配原子,错误;
故选AC。
5s25p1,价层电子排布图 ,其
16-2【巩固】 【正确答案】(1)BD
位于元素周期表的p区; (2) KCaF 12
3
(2)非金属性越强,其简单氢化物稳定性越强,Se
(3) LiAsF 和LiPF 均为离子化合物,结构相
6 6
与Te同主族,非金属性Se>Te,Se更易与H 生成气
2
态氢化物,从而与Te分离; 似,阴阳离子带电量均相同,AsF-离子半径大
6
(3)①已知H SeO 分子中含两个羟基,H SeO 中
2 3 2 3 PF-,阴阳离子间吸引力更弱,所以Li+更易迁移
6
6+2-2´3
心原子Se原子的价层电子对数为3+ =4, 高温
2 6LiCO +CH O +12FePO 12LiFePO +6CO+6H O+6CO
2 3 6 12 6 4 4 2 2
为sp3杂化,VSEPR模型的名称四面体。
(4)AC
②由题意,向H SeO 溶液中通入SO 可获得高纯 (5) 在HCl气流中蒸发浓缩、冷却结晶,过滤、
2 3 2
洗涤、干燥
硒,Se化合价降低,结合电子守恒,则硫化合价升
高得到硫酸,发生反应的化学方程式为 2Fe3+ +Fe=3Fe2+ 2H+ +Fe=Fe2+ +H 取少
2
48/59量固体溶于足量盐酸中,再加入BaCl 溶液,若出现 阴阳离子带电量均相同,AsF-离子半径大PF-,阴
2 6 6
白色沉淀则说明含有S元素 阳离子间吸引力更弱,所以Li+更易迁移;
【试题解析】【分析】(5)以废铁屑(含有少量碳和
②根据信息分析,C H O 中的C元素化合价升高到
6 12 6
SiO 杂质)为原料制备无水FeCl 的流程为:在废铁
2 3
CO中的+2价,FePO 转变成LiFePO ,Fe元素从
4 4
屑中加入过量稀盐酸,通过操作1过滤得到含FeCl
2 +3价降到+2价,根据电子守恒和元素守恒可得出发
生反应:
溶液的滤液,往滤液中通入Cl 将FeCl 氧化为
2 2
高温
6LiCO +CH O +12FePO 12LiFePO +6CO+6H O+6CO
2 3 6 12 6 4 4 2 2
FeCl ,将其结晶过滤后的余液加入纯铁粉继续消耗
3
。
过量盐酸,再继续通入Cl 氧化得到浓FeCl 溶液, (4)A.根据成键特点和孤电子对数量分析化合物
2 3
最后结晶得到FeCl ·6H O,最后加入SOCl 加热得
I中C、O、S原子都采取sp3杂化,A正确;
3 2 2
B.化合物Ⅰ中,羟基(-OH)的键能比巯基(-SH)大,巯
到无水FeCl ,据此分析解答。
3
基(-SH)中H更易断裂,酸性更强,更易与Na反
【详解】(1)A.硒(Se)位于第四周期VIA族,其基
应,B错误;
态原子电子排布式为Ar3d104s24p4,A错误; C.化合物Ⅱ为离子化合物,熔化时破坏离子键,熔
沸点更高,为可溶性钠盐,在水中的溶解性也更大,
B.基态N原子的电子排布式为1s22s22p3,根据洪特
C正确;
规则2p上的三个电子分别排在三个兼并轨道上,故
D.O-H的吸电子效应大于甲基,H SO 分子中
2 4
电子共占据5个轨道,电子空间运动状态为5,B正
O-H的极性更大,更易电离出H+,酸性更强,D
确;
错误;
C.氯离子和氯原子电子层数都为3,核电荷数相
故答案为:AC。
同,氯离子核外多一个电子,故半径更大些,C错
误; (5)①根据分析,FeCl ×6H O高温时易分解,且
3 2
D.S的第二电离失去的为3p3上电子,排布为半满 Fe3+易水解,因在HCl气流中蒸发浓缩、冷却结晶,
后续固液分离操作为过滤、洗涤、干燥;
结构,更稳定故,D正确;
故答案为:BD。 ②稀氯化铁溶液中含有的溶质有FeCl 和HCl,故加
3
(2)根据晶胞分析,一个晶胞中含K+的个数为
入纯Fe粉时可能发生:2Fe3+ +Fe=3Fe2+,
1 1
8´ =1,Ca2+的个数为1,F-的个数为6´ =3, 2H+ +Fe=Fe2+ +H ;
8 2 2
故化学式为KCaF
3
;晶胞中距离F-最近的K+数为
③制得的无水FeCl 时发生反应:
3
4,根据化学式KCaF
3
可推导距离K+最近的F-的数量
FeCl ×6H O+6SOCl =FeCl +6SO +12HCl;过
3 2 2 3 2
为12。
程中FeCl 可能将SO 氧化成SO2-,产品中含有S元
3 2 4
(3)①LiAsF 和LiPF 均为离子化合物,影响Li+迁
6 6
素的为SO2-形式,故操作为检验SO2-的方法:取少
4 4
移速率的因素为离子键的强弱,离子键的强弱又和离
子半径和离子带电荷数有关,两者化合物结构相似, 量固体溶于足量盐酸中,再加入BaCl 溶液,若出现
2
49/59白色沉淀则说明含有S元素。 1 1
上属于二分之一,体心属于1,晶胞中含8× +6×
8 2
16-3【提升】 【正确答案】(1) =4个AlF3-,则晶胞中钾离子、钠离子共有12个,
6
结合图2可知,钠离子处于棱心和体心、钾离子处于
(2)B
1
(3) K
2
NaAlF
6
4 晶胞平分8个小立方体的体心,则晶胞中含12´
4
(4) AD 滤液浓度较大时通入过量CO 生成
2 +1=4个Na+、8个K+,其化学式为K NaAlF ;K+处
2 6
氢氧化铝和碳酸氢钠,会有碳酸氢钠固体从溶液中析
于顶点和面心AlF3-构成的正四面体中,则每个K+
出 6
(5) > 电负性B强于Al,故B对OH-的吸 的配位数为4;
引力更强,形成的配位键更稳定,更不容易释放出 (4)①A.Al O 具有两性,能与强碱溶液反应,不
2 3
OH- 能溶于弱碱,“碱溶”时Al O 与NaOH溶液反应生成
2 3
Na[Al(OH) ],所用NaOH溶液不能更换为氨水,故
4
(6) A正确;
B.由于滤渣a中含有难溶的铝硅酸盐,故滤液a中
的溶质主要成分为NaOH、Na[Al(OH) ],没有硅酸
【试题解析】【分析】(3)铝土矿加氢氧化钠溶液, 4
钠,故B错误;
Al O 和氢氧化钠溶液的反应生成四羟基合铝酸钠、
2 3
C.由分析可知,操作X应是灼烧氢氧化铝使之分解
SiO 转化为铝硅酸钠沉淀、Fe O 不溶,过滤,滤液
2 2 3
生成氧化铝,加冰晶石电解氧化铝就可以得到铝,
含四羟基合铝酸钠溶液、通入足量的二氧化碳后反应
故C错误;
生成氢氧化铝沉淀,过滤,洗涤干燥后,将沉淀分三
D.[Al (OH) Cl ] 中a、b可通过控制Al(OH) 和
份,第一份加盐酸得到氯化铝溶液,与第二份氢氧化 2 a b m 3
AlCl 的投料比来控制产品盐基度,故D正确;
铝反应得到聚合氯化铝,第三份灼烧氢氧化铝使之分 3
答案为AD;
解生成氧化铝,加冰晶石使氧化铝熔融、电解之,就
②滤液浓度较大时通入过量CO 生成氢氧化铝和碳
可以得到铝。 2
酸氢钠,碳酸氢钠溶解度较小,因此会有碳酸氢钠固
【详解】(1)
体从溶液中析出,因此并不有利于减少氢氧化铝固体
Al位于周期表中第3周期第ⅢA族,其基态原子的
中的杂质;
价电子排布式为3s23p1,所以基态Al原子价层电子
(5)碱性:[Al(OH) ]->[B(OH) ]-,因为电负性B强
4 4
于Al,故B对OH-的吸引力更强,形成的配位键更
的电子排布图为: ;
稳定,更不容易释放出OH-;
(6)
(2)在第三周期元素中,钠失去1个电子后,就已
经达到稳定结构,所以钠的第二电离能最大,镁最外
已知Al Cl 的结构式为 ,Al Cl-
层为2个电子,失去2个电子后为稳定结构,所以镁 2 6 2 7
的第二电离能较小,第三电离能最大;铝最外层有3
个电子,失去2个电子后还未达稳定结构,其第三电
的结是每个铝连接三个氯原子,还有一个Cl-连接两
离能较小,则图a表示第三周期的第二电离能变化规
律、图b表示第三周期的第三电离能变化规律,选 个铝,其结构式: 。
B;
(3)按均摊法计算,顶点属于晶胞的八分之一,面 17-1【基础】 【正确答案】(1)<
(2)c-a-b或-(a+b-c)
50/59(3) C < 0.4
P =110kPa´ ,
C2H2 0.4+0.2+1.4+0.2
(4) 小于 温度小于220℃,反应未达平衡,
0.2
随温度升高反应速率加快,乙炔转化率升高;当温度 P =110kPa´ ,
H2 0.4+0.2+1.4+0.2
大于220℃,反应已达到平衡,随温度升高平衡逆向 1.4
P =110kPa´ ,故
移动,乙炔转化率降低 0.35 C2H4 0.4+0.2+1.4+0.2
【试题解析】【详解】(1)已知该反应的平衡常数随温
Q =
P
C2H4
=
P P ×P
度升高而降低,故该反应为放热反应,即ΔH <0; C2H2 H2
1
æ 1.4 ö
(2)已知三种物质的燃烧热化学方程式为 ç110kPa´ ÷
è 0.4+0.2+1.4+0.2ø
5 æ 0.4 ö æ 0.2 ö
C 2 H 2g + 2 O 2g =2CO 2g +H 2 O l DH=-akJ×mol-1, ç è 110kPa´ 0.4+0.2+1.4+0.2 ÷ ø ×ç è 110kPa´ 0.4+0.2+1.4+0.2 ÷ ø
1
H + O =H O DH=-bkJ×mol-1, =0.35 kPa-1。
2g 2 2g 2 l
17-2【巩固】 【正确答案】(1)-4kJ·mol-1
C H +3O =2CO +2H O DH=-ckJ×mol-1,
2 4g 2g 2g 2 l (2)低温
(3)bef
依据盖斯定律可知ΔH =c-a-bkJ×mol-1;
1
(4)8:5
(3)A. 恒温恒容条件下,气体总质量不变,密度
(5) 1 1.2 0.975
始终不变,不能作为平衡判据,A错误;
(6)69
B.恒容条件下,惰性气体不改变各组分浓度,反应
【试题解析】【详解】(1)反应的DH=反应物的键能之
速率不变,平衡时间不变,B错误;
和-生成物的键能之和,则反应物的总键能为
C.升温使正、逆反应速率均增大,且正反应放热,
2×745kJ·mol-1+4×413kJ·mol-1=3142kJ·mol-1,生成物
平衡逆向移动,C正确;
的总键能为3×413kJ·mol-1+348kJ·mol-1+351kJ·mol-
故选C;已知速率方程:
1+463kJ·mol-1+745kJ·mol-1=3146kJ·mol-1,则该反应的
v=0.585é ë pC 2 H 2 ù û -0.36 ×é ë pH 2 ù û 0.85 ,当pH 2 一定 DH=-4kJ·mol-1;
(2)该反应是放热熵减反应,DH<0,DS<0,
时,且p C H > p C H 可知,v 220 ℃时,反应已达平
温度在变化,故温度为变量,所以温度不变,说明反
衡,升温使平衡逆向移动(放热反应),转化率降
应达到新的平衡状态,b正确;
低;依据题干所给信息可列相关反应的三段式: n(CO )
c.投料比等于反应的系数比, 2 =1且该比值
C 2 H 2g + H 2g ƒ C 2 H 4g n(CH 4 )
初始物质的量 2 2 反应始终保持不变,c错误;
转化物质的量 1.6´0.875 1.6´0.875 1.6´0.875
d.容器体积和气体质量始终不变,则混合气体的密
平衡物质的量 0.4 0.2 1.6´0.875
度始终不变,混合气体的密度始终为恒量,d错误;
C 2 H 2g + 2H 2g ƒ C 2 H 6g
初始物质的量 2 2 0 e.v 正 (CO 2 )=v 逆 (CH 3 COOH)满足反应达到平衡的条
转化物质的量 1.6´0.125 1.6´0.25 1.6´0.125 件,e正确;
平衡物质的量 0.4 0.2 1.6´0.125
f.容器中反应分子数发生改变,且温度改变,故总
依据三段式可知各个物质的分压为:
压不变,说明反应达到新的平衡状态,f正确。
故选bef;
51/59(4)对于反应ⅰ为气体分子数增加2倍的反应,向体 (2)a.催化剂通过降低反应的活化能,使更多普通
积为1L的恒容密闭容器中,假设起始时CH 、H O 分子转化为活化分子,活化分子百分数增大,从而加
4 2
的物质的量均为1mol,已知CH 的转化率为60%, 快反应速率,a正确;
4
则反应0.6mol甲烷,反应达到平衡时,气体的总物
b.反应i的DH <0,为放热反应,反应物总能量大
1
质的量为2mol+0.6mol×2=3.2mol,初始气体的总物
于生成物总能量,b错误;
质的量为2mol,根据同温、同容条件下,气体的压
c.反应i中所有物质均是气体,正反应气体分子数减
强之比等于气体的物质的量之比,所以,平衡总压与
小,建立平衡的过程中,混合气体总质量始终不变,
初始总压的最简整数比为3.2mol:2mol=8:5;
气体物质的量是变量,气体的相对分子质量是变量,
(5)①根据表中数据:
容器内气体的相对分子质量不再改变说明反应达到了
k×(1.0mol/L)m×(1.0mol/L)0.5=1.2mol·L-1·s-1,
平衡,c正确;
k×(2.0mol/L)m×(1.0mol/L)0.5=2.4mol·L-1·s-1,联立两式
d.压缩反应容器,平衡正向移动,但是平衡常数是
解得m=1,k=1.2;
与温度有关的常数,温度不变,反应的化学平衡常数
②对于实验2,初始浓度CH 为2mol/L,H O为1
4 2
不变,d错误;
mol/L,当进行到c(H O)=0.25mol/L时,参与反应的
2
故选ac。
H O为0.75mol/L,参与反应的CH 为0.375mol/L,
2 4
(3)①0~20min时间内氢气的浓度降低
此时,c(CH )=1.625mol/L,则
4
v=1.2×(1.625mol/L)×(0.25mol/L)0.5=0.975mol·L-1·s-1;
9-5.75mol/L=3.25mol/L,反应生成CO的浓度为
(6)由于密闭容器的容积为1L,则各物质的物质的
0.25mol/L,则反应ii消耗氢气的浓度为0.25mol/L,
量与物质的量浓度在数值上相等,
反应i消耗氢气的浓度为3mol/L,0~20min时间内
初始时,c(CH )为1 mol/L,c(H O)为1 mol/L,由已
4 2 1
´3mol/L
知平衡时CH 4 的转化率为60%,及平衡时c(CO 2 )为 vCH OH= 3 =0.05mol×L-1×min-1 。从图中
3 20min
0.3 mol/L,则平衡时,c(CH )为0.4 mol/L,c(CO )
4 2
为0.3 mol/L,c(H )为0.3mol/L×3+0.3 mol/L×4=2.1
可知,平衡时,cCO=1.2mol/L,则反应ii生成了
2
mol/L,由氧元素守恒,则平衡时,c(H O)为1 mol/L
2 cH O=1.2mol/L,消耗的
2
-0.6 mol/L -0.3 mol/L =0.1 mol/L,反应
i.CH
4
(g)+H
2
O(g)ƒCO(g)+3H
2
(g)的平衡常数K= cCO
2
=cH
2
=1.2mol/L,平衡时
c(CO)×c3(H ) 0.3mol/L´(2.1mol/L)3
2 = »69。 cH =3.6mol/L,则参与反应i的
c(CH )×c(H O) 0.4mol/L´0.1mol/L 2
4 2
17-3【提升】 【正确答案】(1)+41.19
cH
2
=9-1.2-3.6mol/L=4.2mol/L,
(2)ac
cCO =1.4mol/L,生成的cH O=1.4mol/L,所以
2 2
(3) 0.05 2.17 反应i放热,升高温度,
平衡逆向移动 平衡时:cH =3.6mol/L,
2
(4) 增大 T>T 时v逐渐减小的原因是K
m p cCO =3-1.2-1.4mol/L=0.4mol/L,
2
减小对v的降低程度大于k增大对v的提高程度
cH O=1.4+1.2=2.6mol/L,cCO=1.2mol/L,则
【试题解析】【详解】(1)根据生成焓的定义,反应的 2
焓变DH等于生成物的生成焓总和减去反应物的生成 反应ii平衡常数
焓总和,
cH O×cCO 2.6´1.2
K = 2 = »2.17。
ΔH =-110.5-241.82kJ/mol--393.51+0kJ/mol=+41.19kJ/mol cCO ×cH 0.4´3.6
2 2 2
。
52/59②反应i是放热反应,升高温度反应i的平衡逆向移
象是:滴入最后半滴Na S O 标准液,溶液蓝色褪
2 2 3
动,不利于反应正向移动,所以导致甲醇的选择性降
去,且30s内不恢复原色;
低。
(4)由于反应i是放热反应,温度降低时平衡正向 ②Na
2
S
2
O
3
在酸性条件下不稳定,会分解为S和
移动,导致平衡常数K p 增大。当T>T m 时,尽管提 SO ,导致消耗的标准液偏多,实验结果偏大;I 在
2 2
高温度会增大速率常数k,但放热反应平衡常数随温
碱性条件下会发生歧化反应生成I-和IO-,造成消耗
3
度升高而减小,K 减小对v的降低程度大于k增大对
p
的标准液偏少,实验结果偏小;
v的提高程度,导致u逐渐减小。
③结合空白对照,实际消耗的Na S O 标准液体积为
2 2 3
18-1【基础】 【正确答案】(1) 恒压分液漏斗或恒
(V -V )mL,Cu O溶于稀硫酸时发生反应为
压滴液漏斗 安全瓶,防倒吸 1 2 2
Cu O+2H+ =Cu+Cu2+ +H O,可得到关系式
(2) 2 2
6éCuNH ù 2+ +12OH- D 3Cu O¯+22NH +N +9H O 2Cu 2 O : 2Cu2+ : I 2 : 2S 2 O 3 2-,则反应的Cu 2 O的物质的
ë 3 4 û 2 3 2 2 量为
溶液由深蓝色变为无色
n(Cu O)=n(SO2-)=cmol×L-1´(V -V )´10-3L=c(V -V )´10-3mol
2 2 3 1 2 1 2
(3) 滴入最后半滴Na S O 标准液,溶液蓝色褪 ,因此样品的纯度为
2 2 3
c(V -V )´10-3mol´144g×mol-1 14.4c(V -V )
去,且30s内不恢复原色 pH过低,H+与 1 2 ´100%= 1 2 %;
mg m
Na
2
S
2
O
3
反应;pH过高,I
2
与OH-反应,影响测定
配制标准溶液过程中,有少量Na S O 溶液溅出,则
2 2 3
14.4cV -V
结果 1 2 % 偏大 Na S O 标准溶液实际浓度偏小,滴定所消耗的体积
m 2 2 3
【试题解析】【分析】装置A中利用恒压滴液漏斗向盛
偏大,造成测定结果偏大。
有Cu(NH ) Cl 的三颈烧瓶中滴加NaOH溶液,水浴
3 4 2 18-2【巩固】 【正确答案】(1) 恒压滴液漏斗
加热反应生成Cu O,并伴有NH 、N 产生,装置B
2 3 2 Na SO +H SO 浓=Na SO +SO +H O 吸收
2 3 2 4 2 4 2 2
作安全瓶,防止尾气吸收时发生倒吸,装置C用稀
过剩的SO ,防止污染空气 防止CuCl被氧化
硫酸来吸收生成的氨气; 2
防止CuCl溶解造成损失,且可以使固体快速干燥
【详解】(1)从图中可知,仪器a的名称是恒压滴液
漏斗;氨气极易溶于水,因此需要使用装置B来作 (2) 2S O2-+3O +4OH-=4SO2-+2H O 向下
2 4 2 4 2
安全瓶,防止倒吸;
移动量气管,使左右两侧液面相平 25
(2)装置A中Cu(NH ) Cl 与NaOH在水浴加热条
3 4 2 【试题解析】【分析】装置A制备SO
2
,进入装置B中
件下生成Cu O、NH 、N 和H O,离子方程式为
2 3 2 2 发生反应生成CuCl,装置C是为了吸收剩余的
D
6Cu(NH 3 ) 4 2+ +12OH- 3Cu 2 O¯+N 2 +22NH 3 +9H 2 O SO 2 ,防止其排入空气中,污染空气;装置D是为了
吸收CO ,装置E是为了吸收O ,装置F是为了吸
;反应进行完全后,不再有NH 和N 生成,且深蓝 2 2
3 2
收CO,最后装置G是测量剩余N 的体积。
2
色的Cu(NH ) 2+完全转化为Cu O砖红色沉淀,即现
3 4 2 【详解】(1)①由实验装置图可知,盛装70%浓硫
象为装置A、C中无气泡产生且装置A中溶液由深
酸的仪器名称为恒压滴液漏斗;故答案为恒压分液漏
蓝色变为无色;
斗。
(3)①滴定终点时,待测液中的I 与Na S O 标准 ②装置A是制备二氧化硫的装置,浓硫酸与亚硫酸
2 2 2 3
钠反应生成二氧化硫,其反应的化学方程式为
溶液完全反应,不再使淀粉变蓝,因此滴定终点的现
53/59Na SO +H SO 浓=Na SO +SO +H O (浓);故 与反应,E装置是发生装置,C装置作用是收集气
2 3 2 4 2 4 2 2
体,B装置作用是防止水蒸气进入反应装置,D装置
答案为Na SO +H SO 浓=Na SO +SO +H O 是处理COCl 尾气;整个反应流程先用干燥的N 排
2 3 2 4 2 4 2 2 2 2
除装置内空气,然后再通入N 将CCl 气体带入装
③装置C的作用是吸收未反应完的二氧化硫,防止 2 4
置,与E中的Cr O 反应,生成的COCl 有毒气体用
污染空气;故答案为吸收过剩的SO ,防止污染空 2 3 2
2
D装置收集,与D装置中NaOH溶液反应从而进行
气。
吸收处理,为防止D装置中水蒸气进入反应装置,
④由于CuCl在潮湿空气中易被氧化,可知SO 的作
2
还有在C和D装置中间加一个干燥装置B。
用是防止CuCl被氧化;CuCl难溶于乙醇,则洗涤剂
【详解】(1)根据分析,仪器连接顺序为AECBD,
选用乙醇的优点是防止溶解造成损失,且可快速干
故接口顺序为ahi(或ih)debcf;实验装置内不能存在
燥,故答案为防止CuCl被氧化;防止CuCl溶解造
水蒸气,故通入的N 需干燥,试剂X为干燥剂浓硫
成损失,且可以使固体快速干燥。 2
酸,故答案为:hi(或ih)debcf;A;
(2)①根据已知Ⅱ可知装置E的作用是吸收氧气,
(2)三从安全的角度考虑,整套装置的不足之处是
根据得失电子守恒、原子守恒和电荷守恒,反应的离
氯化铬容易受热升华,温度降低后容易在导管内凝
子方程式2S O2-+3O +4OH-=4SO2-+2H O;故答案
2 4 2 4 2
华,从而堵塞导管,故答案为:氯化铬容易受热升
为2S O2-+3O +4OH-=4SO2-+2H O。 华,温度降低后容易在导管内凝华,从而堵塞导管;
2 4 2 4 2
(3)根据COCl 水解生成的两种酸性气体是HCl和
②装置G为量气装置,通入混合气体前,应先使左 2
CO ,COCl 和NaOH溶液反应的离子方程式应该为
右两边液面在同一水平面上,通入混合气体前,装置 2 2
G中量气管的液面较高,需进行的操作为向下移动量 COCl
2
+4OH-=CO
3
2-+2H
2
O+2Cl-,故答案为:
气管,使左右两侧液面相平;故答案为向下移动量气
COCl +4OH-=CO2-+2H O+2Cl-;
2 3 2
管,使左右两侧液面相平。
(4)反应结束后还需要持续通入N ,将生成的
③由分析知,装置F用于吸收CO,由装置F中增加 2
0.14 g CrCl 3 排入C装置被收集,并将COCl 2 完全排入装置
的质量可知,CO的物质的量为 =0.005
28 g/mol D被充分吸收,故答案为:将生成的CrCl 排入C装
3
mol,故混合气体中CO的体积分数为
置被收集,并将COCl 完全排入装置D被充分吸
2
0.005 mol´22.4 L/mol
´100%=25%,故答案为25。 收;
0.448L
(5)由原子个数和得失电子数目守恒可得关系式:
18-3【提升】 【正确答案】(1) hi(或ih)debcf
A 2CrCl 3 ~2CrO 4 2-~3I 2 ~6Na 2 S 2 O 3 ,滴定消耗V mL
(2)氯化铬容易受热升华,温度降低后容易在导管内
cmol/L硫代硫酸钠溶液,则无水三氯化铬质量分数
凝华,从而堵塞导管
1 250mL
cV´10-3mol´ ´ ´Mg/mol
为 3 25.00mL ×100%=
(3)COCl +4OH-=CO2-+2H O+2Cl-
2 3 2 m g
(4)将生成的CrCl 排入C装置被收集,并将COCl cVM cVM
3 2 %,故答案为: ;
3m 3m
完全排入装置D被充分吸收
(6)加热使过量H O 完全分解,以免在酸性条件
cVM 2 2
(5)
3m 下,H O 把Cr O2-还原为Cr3+;步骤Ⅰ中未继续加热
2 2 2 7
(6) 使过量H O 完全分解 偏低 偏低
2 2
一段时间,由于过量的H O 的存在,在后面的步骤
【试题解析】【分析】三氯化铬易潮解,易升华,高温 2 2
下易被氧气氧化,所以实验过程中要确保装置内不能 中子酸性条件下会将Cr O2-还原为Cr +,则滴定时消
2 7 3
存在氧气和水蒸气,A装置用N 将CCl 导入装置参
2 4 耗标准溶液Na S O 体积减小,测定的CrCl 质量分
2 2 3 3
54/59数偏低;普通锥形瓶没有密封效果,将碘量瓶换成普
通锥形瓶将导致I 升华,从而使得消耗Na S O 的量
2 2 2 3
偏小,则样品中无水三氯化铬质量分数的测量结果偏
H: ,最后将H在
低,故答案为:使过量H O 完全分解;偏低;偏
2 2
低。
19-1【基础】 【正确答案】(1)醚键、酰胺基
Pd/C、H 作用得到目标产物I。
(2) 丁二酸二乙酯 还原反应 2
【详解】(1)由I的结构简式可知,I中含氧官能团
(3)
的名称为醚键、酰胺基;
(4) (2)
B的结构简式为: ,是由丁二酸与乙
醇酯化后得到的产物,其名称为:丁二酸二乙酯;
氧化反应
【试题解析】【分析】
工业上合成I的工艺为:将A与B进行取代生成 H→I为 在Pd/C作用下
C,再将C与(CH CO) O进行反应可得到D;将D
3 2
在NaOH溶液中、80℃温度下进行水解,水解产物
再进行酸化生成E(C H N O ),结合E的碳原子和
16 14 2 3 与H 通过还原反应生成I;
2
O原子数以及I的结构可反推出E的结构为:
(3)
,将E在i)SOCl 作
2 B的结构简式为: ,其同分异构体中
满足以下条件:与B含有相同官能团,即仍含有酯基;
用下先转化为 ,再与 水解生成丙二酸:即HOOC-CH -COOH,则醇结构可
2
能 是 以 下 组 合 : CH OH和 CH CH CH CH OH、
3 3 2 2 2
ii) 反应生成F:
CH OH和 CH CH CH(OH)CH 、 CH OH和
3 3 2 3 3
CH CHCH OH、 CH OH和 CH COH、
3 2 2 3 3 3
,将F与G反应生成
CH CH OH和 CH CH CH OH、 CH CH OH和
3 2 3 2 2 3 2
CH CHOH;含有三种不同化学环境的氢原子:由
3 2
于丙二酸两边结合的醇结构不对称,则要求两种醇的
烃基各含一种氢;最后得到符合条件的B的同分异构
55/59体的结构简式为: ;
(4)
根据已知: 的
(6)
快速异构化
信息可知C®X ® Y的转化中,X结构中含有
① ②
的结构单元来满足快速异构化,则反应①
的化学方程式为:
【试题解析】【分析】
;
根据J→G的合成路线图: 根据已知信息RCOOH¾C¾OC¾l2®RCOCl,A(C
8
H
7
ClO
2
,
含羧基结构)与COCl 反应,A中羧基转化为酰氯,
2
生成B,可知A为 。由D(C H O )与乙
7 6 2
,结合苯环与咪唑环性质类似,同时参 醇的反应的条件为浓硫酸和加热,可知该反应为发生
酯化反应,D中有羧基,故D为 ,与乙醇生
考C→X的转化原理,由于N是通过还原反应生成
成E( )。E与CH COOC H 、C H ONa反
,则N结构中存在羰基结构单元,可 3 2 5 2 5
得到J→G的合成路线为: 应,依据已知信息ii,生成F( )。
B 与 F 反应生成 L( ), 异构化为
,则得到J→M的反应类型为:氧化反应;N的结构
简式为: 。
,再脱去HCl生成G,G反应生成
19-2【巩固】 【正确答案】(1)羧基、碳氯键
(2)取代反应
I( ),I与J( )反应脱
(3)
(4)ab
(5) 4 或
56/59c错误;
水生成K( )。 故选ab。
(5)
【详解】(1)
含苯环且能发生银镜反应的D( )的同分异构
根据分析,A为 ,含有的官能团名称
体,苯环的一取代有 ;二取代苯环
上连有醛基、羟基两个取代基,共3种位置;综上符
是羧基、碳氯键。
合要求的同分异构体有4种。
(2)
其中一种核磁共振氢谱上显示四个峰的同分异构体的
E( )与CH COOC H 反应生成
3 2 5 结构简式有 、 。
(6)
F( )的反应类型是取代反应。
F的结构简式为 ,酯基和羰基均为
(3)
吸电子基团,可以使α位C-H极性增强,易断裂,
D为 ,与乙醇生成E( )属于酯 B与F反应生成L,反应方程式为:
化反应,方程式为
。
,根据已知: 可
(4)
得, 异构化为 ,
a.I是 ,含有羧基,能与NaHCO
3
再脱去HCl生成G。
溶液反应,a正确;
19-3【提升】 【正确答案】(1) 苯乙酸 酯化
(取代)反应
b.由题意可知,I( )脱去1分子水
(2) 硝基、酯基
生成K,推出J为其分子式为C H N,结构简式
4 11
(3)C
(4)
为: ,核磁共振氢谱显示峰面积
比为1:4:6,b正确;
c.K中含有2个苯环、1个碳碳双键、1个羰基,
(5)7
则1molK最多能与6+1+1=8 mol H 发生加成反应,
2
57/59(6)
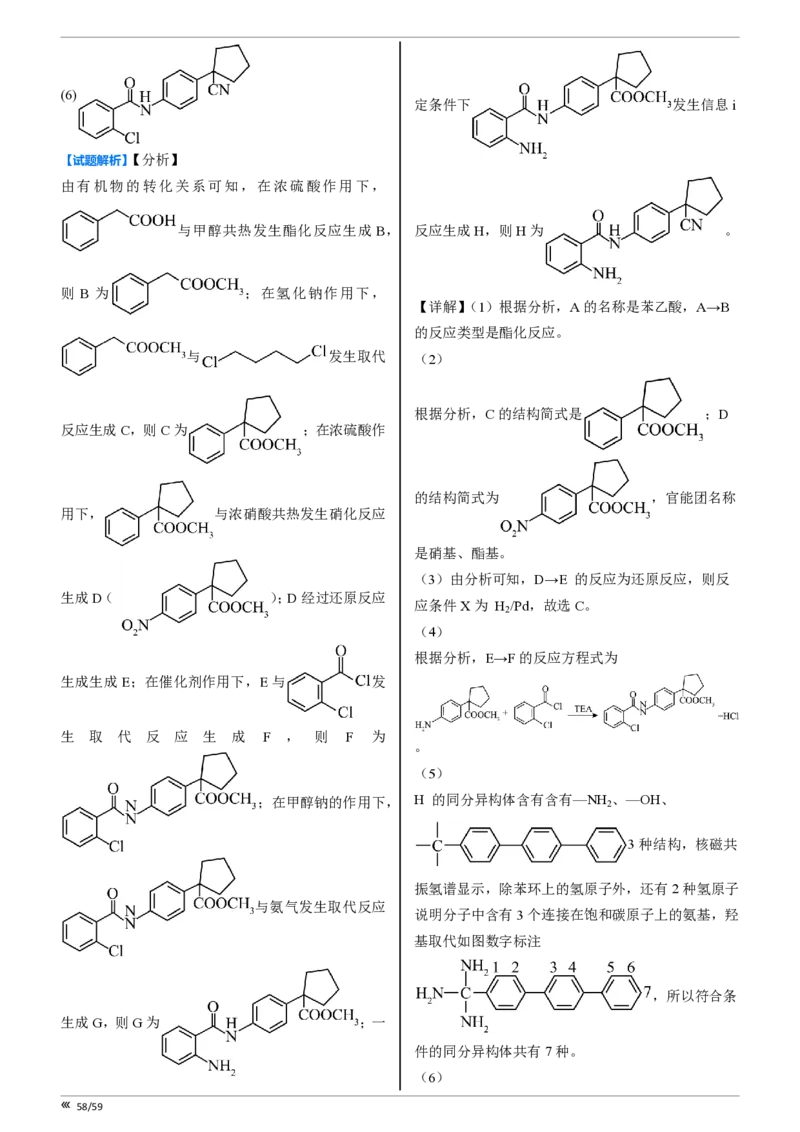
定条件下 发生信息i
【试题解析】【分析】
由有机物的转化关系可知,在浓硫酸作用下,
与甲醇共热发生酯化反应生成 B, 反应生成H,则H为 。
则 B 为 ;在氢化钠作用下,
【详解】(1)根据分析,A的名称是苯乙酸,A→B
的反应类型是酯化反应。
与 发生取代 (2)
根据分析,C的结构简式是 ;D
反应生成C,则C为 ;在浓硫酸作
的结构简式为 ,官能团名称
用下, 与浓硝酸共热发生硝化反应
是硝基、酯基。
(3)由分析可知,D→E 的反应为还原反应,则反
生成D( );D经过还原反应
应条件X为 H /Pd,故选C。
2
(4)
根据分析,E→F的反应方程式为
生成生成E;在催化剂作用下,E与 发
生 取 代 反 应 生 成 F , 则 F 为
。
(5)
;在甲醇钠的作用下, H 的同分异构体含有含有—NH 、—OH、
2
3种结构,核磁共
振氢谱显示,除苯环上的氢原子外,还有2种氢原子
与氨气发生取代反应
说明分子中含有3个连接在饱和碳原子上的氨基,羟
基取代如图数字标注
,所以符合条
生成G,则G为 ;一
件的同分异构体共有7种。
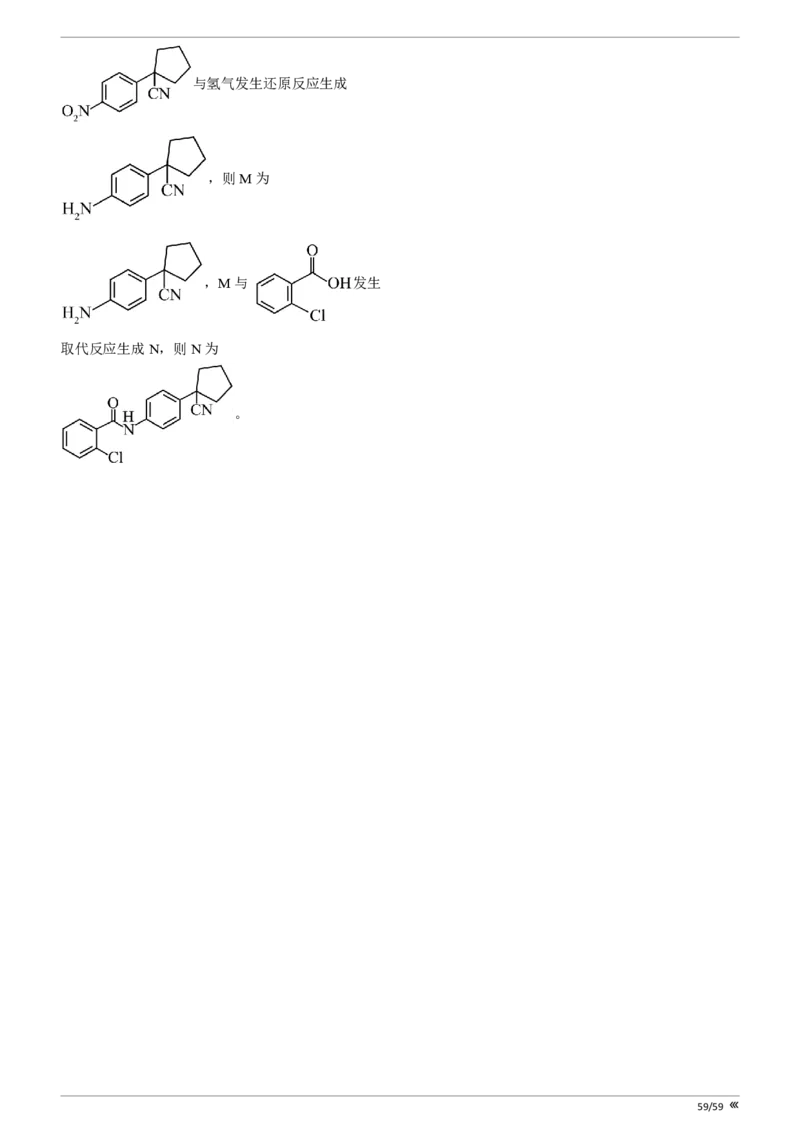
(6)
58/59与氢气发生还原反应生成
,则M为
,M与 发生
取代反应生成N,则N为
。
59/59