文档内容
澄宜六校联盟高三年级 12 月学情调研试卷
化 学
本试卷分选择题和非选择题两部分,全卷满分100分,考试时间75分钟。
注意事项:
1.答题前,考生务必在答题纸姓名栏内写上自己的姓名、考试科目、准考证号等,并
用2B铅笔涂写在答题纸上。
2.每小题选出正确答案后,用2B铅笔把答题纸上对应题号的答案标号涂黑。如需改
动,用橡皮擦干净后,再选涂其他答案。不能答在试题卷上。
3.考试结束,将答题纸交回。
可能用到的相对原子质量:H1C12O16Na23S32Cl 35.5
一、单项选择题:共13题,每题3分,共39分。每题只有一个选项最符合题意。
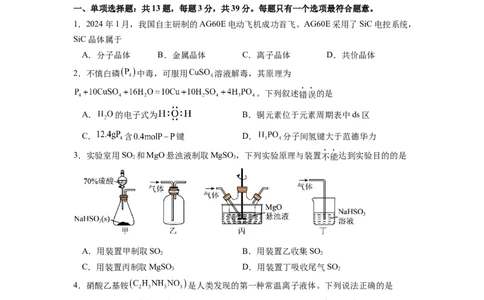
1.2024年1月,我国自主研制的AG60E电动飞机成功首飞。AG60E采用了SiC电控系统,
SiC晶体属于
A.分子晶体 B.金属晶体 C.离子晶体 D.共价晶体
2.不慎白磷 中毒,可服用 溶液解毒,其原理为
。下列叙述错误的是
A. 的电子式为 B.铜元素位于元素周期表中ds区
C. 含 键 D. 分子间氢键大于范德华力
3.实验室用SO 和MgO悬浊液制取MgSO ,下列实验原理与装置不能达到实验目的的是
2 3
A.用装置甲制取SO B.用装置乙收集SO
2 2
C.用装置丙制取MgSO D.用装置丁吸收尾气SO
3 2
4.硝酸乙基铵 是人类发现的第一种常温离子液体。下列说法正确的是
A.电负性: B.第一电离能:
C.稳定性: D.熔点:
阅读下列材料,完成5~7小题:
硫(S)元素在自然界中通常以硫化物、硫酸盐或单质的形式存在。硫有多种单质存在形式。
低价硫有氧气敏感性,在细菌作用下可发生氧化反应;SO 具有强还原性。人类根据需要
2
可将硫元素转化为指定物质,以减少环境污染。常用方法有①空气氧化法②氯氧化法③酸
回收法④混凝沉淀法等。
已知:常温下, , ; ,。
5.下列说法正确的是
A.SO 分子中键角小于SO 分子中键角
2 3
B.二硫化氢(H S)分子的构型为直线形
2 2
C.CaSO·2H O中既有离子键又有非极性共价键
4 2
D.HS的沸点高于水
2
6.下列有关离子方程式书写错误的是
A.空气氧化法中,向含 废水中通入空气,回收硫:
B.氯氧化法中,向含 废水中通入氯气:
C.酸回收法中,向含 废水中通入少量的 酸化,再用足量烧碱溶液吸收 :
,
D.混凝沉淀法中,向含 废水中加入 溶液:
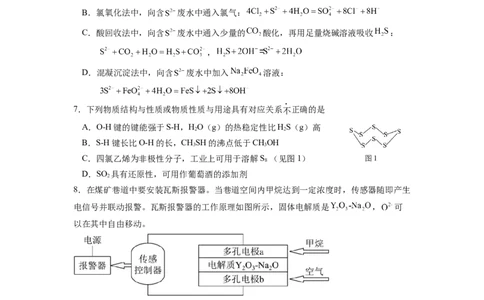
7.下列物质结构与性质或物质性质与用途具有对应关系不正确的是
A.O-H键的键能强于S-H,HO(g)的热稳定性比HS(g)高
2 2
B.S-H键长比O-H的长,CHSH的沸点低于CHOH
3 3
C.四氯乙烯为非极性分子,工业上可用于溶解S (见图1) 图1
8
D.SO 具有还原性,可用作葡萄酒的添加剂
2
8.在煤矿巷道中要安装瓦斯报警器。当巷道空间内甲烷达到一定浓度时,传感器随即产生
电信号并联动报警。瓦斯报警器的工作原理如图所示,固体电解质是 , 可
以在其中自由移动。
当报警器被触发时,下列说法正确的是
A.多孔电极a的电势比多孔电极b高
B.O2-在电解质中向多孔电极a移动,电流方向为由多孔电极a经导线流向多孔电极b
C.多孔电极a的电极反应为CH+4O2--8e-=CO +2H O
4 2 2
D.标准状况下56mL空气(O 体积占比约为1/4)在多孔电极b上完全反应时,流入传
2
感控制器电路的电子的物质的量为0.04mol
9.化合物Z是合成维生素E的一种中间体,其合成路线如下图:下列说法正确的是
A.X分子中所有碳原子不可能共平面 B.Y分子中含有2个手性碳原子
C.Z不能发生消去反应 D.Y和Z能与等物质的量的NaOH反应
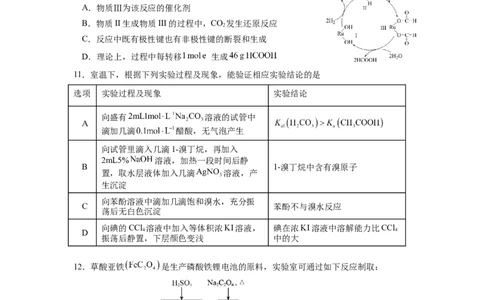
10.含Ru(钌)化合物可催化CO 转化为HCOOH,其反应机理如图所示。下列说法正确的
2
是
A.物质Ⅲ为该反应的催化剂
B.物质II生成物质III的过程中,CO 发生还原反应
2
C.反应中既有极性键也有非极性键的断裂和生成
D.理论上,过程中每转移 生成
11.室温下,根据下列实验过程及现象,能验证相应实验结论的是
选项 实验过程及现象 实验结论
向盛有 溶液的试管中
A
滴加几滴 醋酸,无气泡产生
向试管里滴入几滴1-溴丁烷,再加入
2mL5% 溶液,加热一段时间后静
B 1-溴丁烷中含有溴原子
置,取水层液体加入几滴 溶液,产
生沉淀
向苯酚溶液中滴加几滴饱和溴水,充分振
C 苯酚不与溴水反应
荡后无白色沉淀
向碘的CCl 溶液中加入等体积浓KI溶液, 碘在浓KI溶液中溶解能力比CCl
D 4 4
振荡后静置,下层颜色变浅 中的大
12.草酸亚铁 是生产磷酸铁锂电池的原料,实验室可通过如下反应制取:
已知室温时: 。
下列说法正确的是
A.室温下,向 溶液中加酸调节 时溶液中存在:
B.“酸化溶解”后的溶液中存在:
C.室温时, 能与 反应生成 沉淀
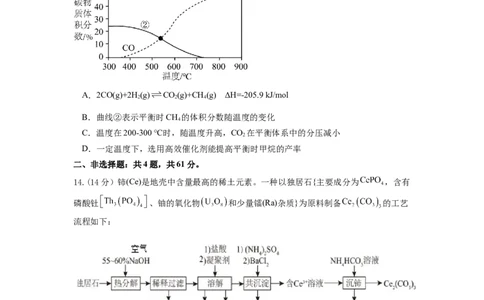
D.室温时,“沉铁”后的上层清液中:13.二氧化碳加氢制甲烷过程中的主要反应如下:
反应Ⅰ:CO(g)+4H(g) CH(g)+2HO(g) ΔH=-164.7 kJ/mol
2 2 4 2 1
反应Ⅱ:CO(g)+H(g) CO(g)+HO(g) ΔH=+41.2 kJ/mol
2 2 2 2
在1.01×105Pa恒压条件下,按n (CO)∶n (H )=1∶1投料比进行反应,平衡时含碳物质体
起始 2 起始 2
积分数随温度的变化如图所示。下列说法正确的是
A.2CO(g)+2H(g) CO(g)+CH (g) ΔH=-205.9 kJ/mol
2 2 4
B.曲线②表示平衡时CH 的体积分数随温度的变化
4
C.温度在200-300 ℃时,随温度升高,CO 在平衡体系中的分压减小
2
D.一定温度下,选用高效催化剂能提高平衡时甲烷的产率
二、非选择题:共4题,共61分。
14.(14分)铈(Ce)是地壳中含量最高的稀土元素。一种以独居石{主要成分为 ,含有
磷酸钍 、铀的氧化物 和少量镭(Ra)杂质}为原料制备 的工艺
流程如下:
图14-1
已知:i.常温下, , ,
, ,
ii.镭是一种放射性元素,位于第七周期第ⅡA族。
回答下列问题:(1)“热分解”步骤中, 转化为难溶于水的 。该反应的化学方程式为
。
(2)溶解时,加絮凝剂调节pH除杂。此过程中,Th完全转化为Th(OH) 沉淀,则应控制
4
pH≥ 。
(3)“共沉渣”的主要成分为 。为防止放射性污染,应将其封存。
(4)“沉铈”过程中发生反应的离子方程式为 。
若“沉铈”中, 恰好沉淀完全 ,此时溶液的pH为5,则溶
液中 mol/L(保留2位有效数字)。
(5)灼烧Ce (CO) 可以获得CeO。CeO 可作载氧体氧化CH 制得合成气(H 和CO),
2 3 3 2 2 4 2
其一般模型如图14-2所示:
图14-2
图14-3
在一定温度下,该模型涉及的主要反应如下:
主反应:
甲烷裂解反应: = +90
2
当 、 时,控制不同 ,平衡时 与温
度的关系如图14-3所示,请说明当反应体系温度低于 时, 越大,温度越
高,越有利于合成气的生成: 。
(5)铈的某种氧化物具有面心立方晶体结构,其结构如图14-4,高温下,该氧化物失去氧
形成氧空位,每失去 ,理论上有 mol 生成。
图14-4
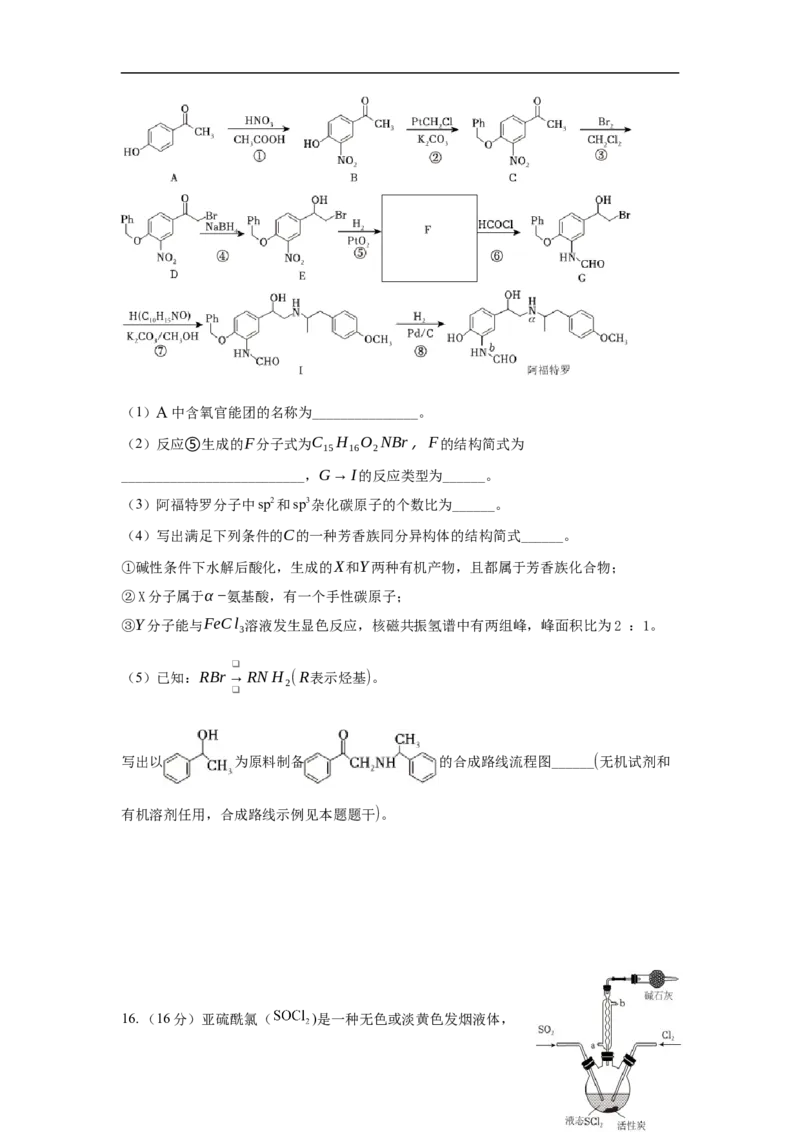
15.(15分)阿福特罗是一种可用于治疗慢性阻塞性肺炎的药品,其合成路线如图(“Pℎ
”表示苯基):(1)A中含氧官能团的名称为_______________。
(2)反应⑤生成的F分子式为C H O NBr,F的结构简式为
15 16 2
__________________________,G→I的反应类型为______。
(3)阿福特罗分子中sp2和sp3杂化碳原子的个数比为______。
(4)写出满足下列条件的C的一种芳香族同分异构体的结构简式______。
①碱性条件下水解后酸化,生成的X和Y两种有机产物,且都属于芳香族化合物;
②X分子属于α−氨基酸,有一个手性碳原子;
③Y分子能与FeCl 溶液发生显色反应,核磁共振氢谱中有两组峰,峰面积比为2 :1。
3
❑
(5)已知:RBr→RN H (R表示烃基)。
2
❑
写出以 为原料制备 的合成路线流程图______(无机试剂和
有机溶剂任用,合成路线示例见本题题干)。
16.(16分)亚硫酰氯( )是一种无色或淡黄色发烟液体,其熔点-105℃,沸点79℃,有强烈刺激性气味,遇水剧烈反应生成两种酸性气体,常用作
脱水剂。
(1)实验室用SCl 、SO 与Cl 在活性炭催化加热条件下制取SOCl ,部分装置(夹持、
2 2 2 2
加热装置略去)如图16-1所示。
① 中S的杂化轨道类型为_____________。
②写出装置中发生反应的化学方程式_______________________。
③碱石灰的作用为___________________________________。 图16-1
(2)测定样品中SOCl 的纯度。准确称量5.9500gSOCl 样品,将其完全溶解于
2 2
500mLNaOH溶液中,发生反应SOCl +4NaOH=Na SO +2NaCl+2H O,取反应
2 2 3 2
液50mL于碘量瓶中,滴加盐酸至NaOH恰好完全反应;再加入
50.00mL 0.1000mol⋅L−1I 溶液,充分反应后,用0.1000mol⋅L−1Na S O 溶液
2 2 2 3
滴定过量的I (I +2Na S O =2NaI+Na S O )。平行滴定三次,反应消耗Na S O
2 2 2 2 3 2 4 6 2 2 3
溶液的平均体积为20.00mL。则样品中SOCl 的质量分数为______(写出计算过程)。
2
(3)实验室常利用SOCl 和FeCl ⋅4H O混合加热制取无水FeCl ,但不使用SOCl
2 2 2 2 2
与FeCl ⋅6H O制取无水FeCl ,其原因是可能发生副反应导致产品不纯。
3 2 3
①SOCl 与FeCl ⋅6H O发生副反应的可能原因是
2 3 2
___________________________________。
②为验证副反应的可能性。请补充完整实验方案:取少量FeCl ⋅6H O于试管中,
3 2
______________________________________________________________________________,
则证明发生了副反应。(实验中必须使用的试剂:SOCl 、NaOH溶液、K [Fe(CN) ]溶
2 3 6
液)
17.(16分)空气中 含量的控制和 资源利用具有重要意义。
(1) (缩写为 )溶液可用于捕集燃煤烟气中 ,转化过程如下。
图17-1
①室温下, 的 , ,吸收后溶液的 ,此时主要
含碳阴离子为_______(写离子符号)。
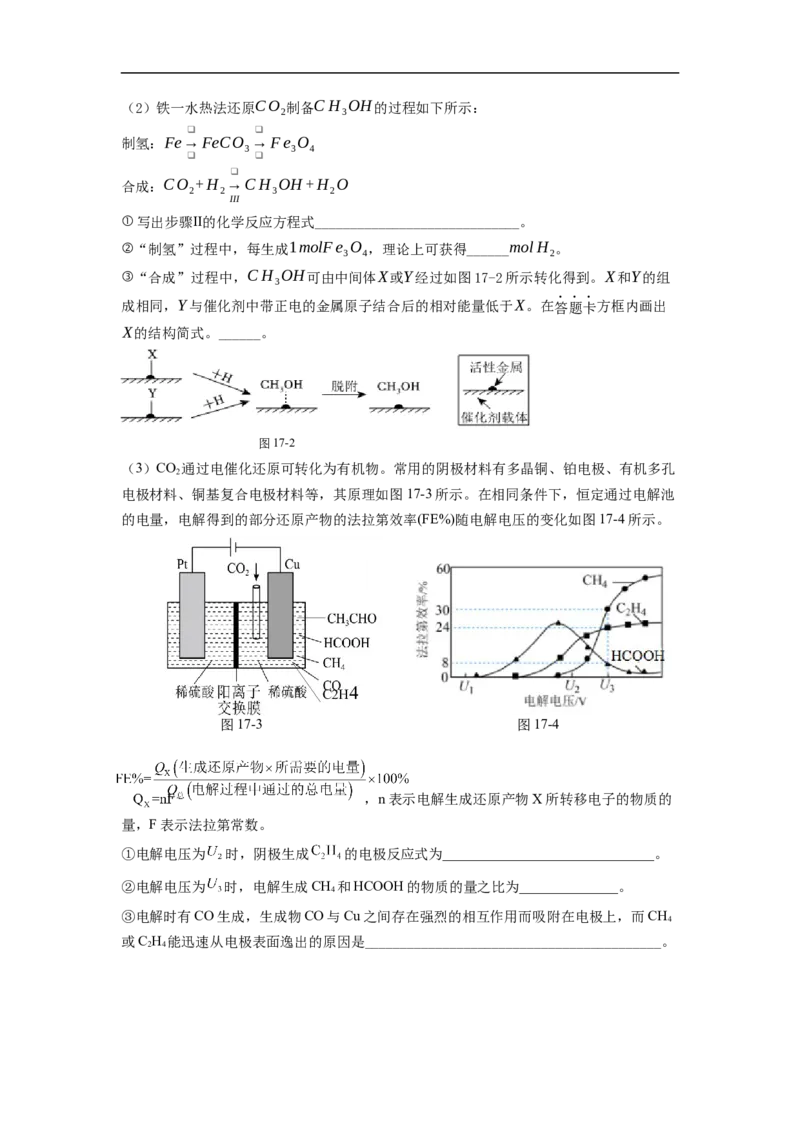
②从结构的角度解释 水溶液能吸收 的理由是______________________________。(2)铁一水热法还原CO 制备CH OH的过程如下所示:
2 3
❑ ❑
制氢:Fe→FeCO →Fe O
3 3 4
❑ ❑
❑
合成:CO +H →CH OH+H O
2 2 3 2
III
①写出步骤Ⅱ的化学反应方程式_____________________________。
②“制氢”过程中,每生成1molFe O ,理论上可获得______molH 。
3 4 2
③“合成”过程中,CH OH可由中间体X或Y经过如图17-2所示转化得到。X和Y的组
3
成相同,Y与催化剂中带正电的金属原子结合后的相对能量低于X。在答题卡方框内画出
X的结构简式。______。
图17-2
(3)CO 通过电催化还原可转化为有机物。常用的阴极材料有多晶铜、铂电极、有机多孔
2
电极材料、铜基复合电极材料等,其原理如图17-3所示。在相同条件下,恒定通过电解池
的电量,电解得到的部分还原产物的法拉第效率(FE%)随电解电压的变化如图17-4所示。
图
C2H4
图17-3 图17-4
,n表示电解生成还原产物X所转移电子的物质的
量,F表示法拉第常数。
①电解电压为 时,阴极生成 的电极反应式为______________________________。
②电解电压为 时,电解生成CH 和HCOOH的物质的量之比为______________。
4
③电解时有CO生成,生成物CO与Cu之间存在强烈的相互作用而吸附在电极上,而CH
4
或C H 能迅速从电极表面逸出的原因是__________________________________________。
2 4