文档内容
专题 05 物质的量
内容概览
考点01 物质的量与摩尔质量
考点02 气体摩尔体积与阿伏加德罗定律
考点03 物质的量浓度
考点04 一定物质的量浓度溶液的配制
考点05 有关阿伏加德罗常数的判断
考点01 物质的量与摩尔质量
1.(23-24高一上·福建莆田·期末)下列叙述错误的个数是
①摩尔是国际单位制中七个基本物理量之一
② 任何物质都含有约 个分子
③ 就是阿伏加德罗常数
④在标准状况下, 任何物质的体积均为
⑤ 的摩尔质量等于 分子的质量
⑥ 中含有 氢分子和 氧原子
A.①②④ B.①②③④ C.③⑤⑥ D.①②③④⑤⑥
2.(23-24高一上·江苏宿迁·期末)下列叙述错误的是
A.物质的量是国际单位制中七个基本物理量之一
B.0.016kg 含有约6.02×1023个氧原子
C.单位物质的量的任何物质都含有约6.02×1023个原子
D.对两种相同物质的量的气体,处于相同温度下,压强越大体积越小
考点02 气体摩尔体积与阿伏加德罗定律
3.(23-24高一上·安徽省芜湖市·期末)下列选项中与17gNH 所含原子数相等的是
3
A.64gO B.2molCO C.22.4LCO D.2gH
2 2 2
4.(23-24高一上·安徽省芜湖市·期末)下列有关物质相关量的说法正确的是
A.同温同压下, 和 的密度相同
B. 氩气含有的质子数为
C.同温同压下,等质量的 和 的电子数相同
学科网(北京)股份有限公司D.质量相同的 和 (重水)所含的质子数相同
5.(23-24高一上·湖北·期末)下列有关气体的说法正确的是
A.在非标准状况下,气体的摩尔体积不可能是22.4L/mol
B.1molHCl气体溶于1LHO中,所得溶液物质的量浓度为1mol/L
2
C.在同温同容条件下,等质量的O 和SO 的压强比为2:1
2 2
D.在同温同压条件下,CO和CO 的密度比为11:7
2
考点03 物质的量浓度
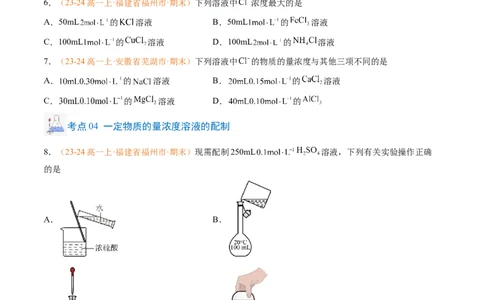
6.(23-24高一上·福建省福州市·期末)下列溶液中 浓度最大的是
A.50mL 的 溶液 B.50mL 的 溶液
C.100mL 的 溶液 D.100mL 的 溶液
7.(23-24高一上·安徽省芜湖市·期末)下列溶液中 的物质的量浓度与其他三项不同的是
A. 的 溶液 B. 的 溶液
C. 的 溶液 D. 的
考点04 一定物质的量浓度溶液的配制
8.(23-24高一上·福建省福州市·期末)现需配制250mL 溶液,下列有关实验操作正确
的是
A. B.
C. D.
9.(23-24高一上·安徽省皖北六校·期末)实验室中做化学实验或进行科学研究时,需要配制各种不同浓
度的溶液。下列关于配制480mL1mol/LNaOH溶液的说法错误的是
A.应选用500mL的容量瓶
B.容量瓶使用之前需要检查是否漏水
学科网(北京)股份有限公司C.称量好的NaOH固体直接转入容量瓶,再加水稀释
D.没有洗涤烧杯和玻璃棒会导致所配溶液浓度偏小
10.(23-24高一上·福建龙岩·期末)实验室需配制80mL NaCl溶液,下列说法正确的是
A.用托盘天平称取NaCl晶体2.34g
B.必须用的玻璃仪器是烧杯、玻璃棒、胶头滴管、量筒、漏斗、100mL容量瓶
C.采用加热的方法来加快NaCl晶体的溶解,趁热迅速将溶液转移至容量瓶中
D.定容时仰视会造成所配制溶液的物质的量浓度偏小
11.(23-24高一上·北京市朝阳区·期末)配制 溶液,下列说法不正确的是
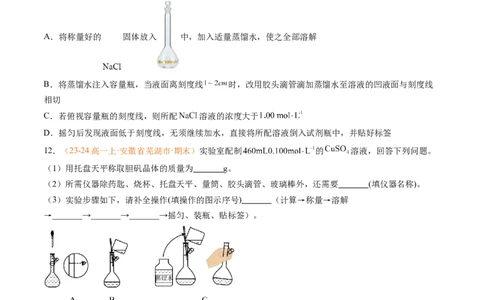
A.将称量好的 固体放入 中,加入适量蒸馏水,使之全部溶解
B.将蒸馏水注入容量瓶,当液面离刻度线 时,改用胶头滴管滴加蒸馏水至溶液的凹液面与刻度线
相切
C.若俯视容量瓶的刻度线,则所配 溶液的浓度大于
D.摇匀后发现液面低于刻度线,无须继续加水,直接将所配溶液倒入试剂瓶中,并贴好标签
12.(23-24高一上·安徽省芜湖市·期末)实验室配制 的 溶液,回答下列问题。
(1)用托盘天平称取胆矾晶体的质量为 g。
(2)所需仪器除药匙、烧杯、托盘天平、量筒、胶头滴管、玻璃棒外,还需要 (填仪器名称)。
(3)实验步骤如下,请补全操作(填操作的图示序号) (计算→称量→溶解
→_______→_______→_______→摇匀、装瓶、贴标签)。
(4)在配制过程中,如果其他操作都正确,而没有洗涤烧杯和玻璃棒,会使配制结果 (填“偏大”
“偏小”或“不变”)。
(5)定容时,若不慎加水超过了刻度线,处理方式是 。
13.(23-24高一上·广东省广州市·期末)学习小组探究硫酸在双氧水与铜的反应中的作用。
(1)配制 的稀硫酸
(a)配制 的稀硫酸,需要 硫酸的体积为 mL。
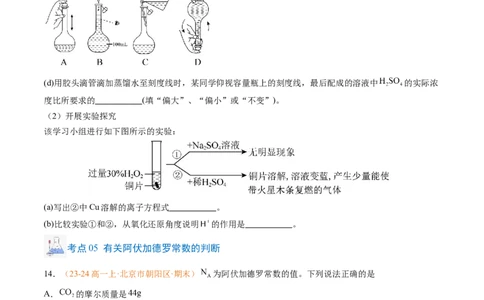
(b)配制溶液时,需要的仪器有100mL容量瓶、玻璃棒、胶头滴管、 (从下图中选择,写出名
称)。
学科网(北京)股份有限公司(c)下列关于100mL容量瓶的操作,正确的是 。
(d)用胶头滴管滴加蒸馏水至刻度线时,某同学仰视容量瓶上的刻度线,最后配成的溶液中 的实际浓
度比所要求的 (填“偏大”、“偏小”或“不变”)。
(2)开展实验探究
该学习小组进行如下图所示的实验:
(a)写出②中Cu溶解的离子方程式 。
(b)比较实验①和②,从氧化还原角度说明 的作用是 。
考点05 有关阿伏加德罗常数的判断
14.(23-24高一上·北京市朝阳区·期末) 为阿伏加德罗常数的值。下列说法正确的是
A. 的摩尔质量是
B. 中含有氢原子的数目为
C.常温常压下, 中含有氯分子的数目为
D. 溶液中,含有 的数目为
15.(23-24高一上·广东省茂名市·期末)下列说法不正确的是
A. 的 的质量为
B.物质的量是国际单位中七个基本物理量之一
C. 中含有 个原子
学科网(北京)股份有限公司D.在标准状况下, 的气体摩尔体积为
16.(23-24高一上·福建省福州市·期末)设 为阿伏加德罗常数的值,下列说法错误的是
A.1.8g 的质子数为
B.14g 的分子数为
C. 溶液中, 的数目为
D.标准状况下,22.4L 的电子数为
17.(23-24高一上·安徽省皖北六校·期末)用 表示阿伏加德罗常数的值,下列叙述正确的是
A. 由 与 组成的混合气体中含有的原子数为
B.1mol 发生反应,转移电子数一定为
C.标准状况下,11.2L 含有分子数为
D. 的 溶液中含 数为
18.(23-24高一上·安徽省部分学校·期末)设N 代表阿伏加德罗常数的值。下列说法正确的是
A
A.常温常压下,18g H O中含有的电子数为9N
2 A
B.100mL 1mol·L-1KClO 溶液中含有的Cl-数为0.1N
3 A
C.7.1gCl 与足量铁在加热条件下完全反应时转移的电子数为0.3N
2 A
D.标准状况下,5.6LCO和O 的混合气体中含有的原子数为0.5N
2 A
1.(23-24高一上·安徽省合肥市六校联盟·期末)用 表示阿伏加德罗常数的值,下列说法正确的是
A.13gZn与足量稀 完全反应,生成的 所含原子数目为
B.0.5mol/L 溶液中含有 和 总物质的量为1mol
C. 气体溶于水,所得溶液中含有的氯化氢分子为
D. 的铁与足量 反应失去电子数为
2.(23-24高一上·福建龙岩·期末)监测 含量是否达到排放标准的反应原理是
. 表示阿伏加德罗常数的值,下列说法正确的是
A.0.1mol 固体中所含离子总数为
B.25℃时, 的HCl溶液中含有 的数目为
C.17g 中含有的原子数目为
D.2.24L 中含有的分子数目为
学科网(北京)股份有限公司3.(23-24高一上·河南省开封市联考·期末)下列说法中,正确的是
A. 的摩尔质量是
B.标准状况下, 的体积是
C. 中含有的氧原子数约为
D. 溶液中 是
4.(23-24高一上·湖北省A9高中联盟·期末)N 表示阿伏加德罗常数的值,下列说法正确的是
A
A.11.2LNH 含有的分子数目为0.5N
3 A
B.0.1mol/LNaCl溶液中含有Na+数目为0.1N
A
C.1molCl 和铁在一定条件下完全反应,转移电子数目为3N
2 A
D.1 mol H O+中含有电子数为10 N
3 A
5.(23-24高一上·北京市东城区·期末) 为阿伏加德罗常数的值。下列说法不正确的是
A. 中氢原子数目为
B.常温常压下, 中氮分子数目为
C. 溶液中 数目为
D. 铝与足量盐酸完全反应,转移的电子数目为
6.(23-24高一上·广东省广州市·期末)设 为阿伏加德罗常数的值。下列说法正确的是
A. 中一定含有
B. 中含有 的数目为
C. 中含有共价键的数目为
D. 溶解在1L水中,所得溶液中溶质的物质的量浓度为
7.(23-24高一上·湖南省名校联考联合体·期末)设 为阿伏加德罗常数的值,下列说法正确的是
A. 溶于适量水中,所得溶液中 和 微粒总数为
B. 的盐酸中含有的氯化氢分子数为
C.常温常压下, 氘气 含有的中子数为
D.已知 ,如果有 参加反应,则由水还原的 分子数目为
8.(23-24高一上·湖北省A9高中联盟·期末)下列有关气体的说法正确的是
A.在非标准状况下,气体的摩尔体积不可能是22.4L/mol
B.1molHCl气体溶于1LHO中,所得溶液物质的量浓度为1mol/L
2
C.在同温同容条件下,等质量的O 和SO 的压强比为2:1
2 2
学科网(北京)股份有限公司D.在同温同压条件下,CO和CO 的密度比为11:7
2
9.(23-24高一上·北京市东城区·期末)配制 溶液,某同学的实验记录如下。
Ⅰ.将称量好的 固体放入烧杯中,用适量蒸馏水溶解。
Ⅱ.将烧杯中的溶液注入 容量瓶,再用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,将洗涤液也都注入
容量瓶。
Ⅲ.将蒸馏水注入容量瓶,当液面离容量瓶颈部的刻度线 时,改用胶头滴管滴加蒸馏水,至溶液的
凹液面与刻度线相切。
Ⅳ.盖好瓶塞,反复上下颠倒,摇匀。
下列是该同学的实验分析,其中不正确的是
A.步骤Ⅰ中称量的 固体为
B.步骤Ⅰ和Ⅱ用到同一支玻璃棒,其作用分别是搅拌和引流
C.步骤Ⅱ中洗涤液不慎酒到容量瓶外,则配成的溶液中 的实际浓度比所要求的小
D.步骤Ⅳ摇匀后,发现容量瓶中液面比刻度线低,应该再滴加少量蒸馏水
10.(23-24高一上·湖北省A9高中联盟·期末)回答下列问题
(1)标准状况下,11.2LCO和CO 的混合气体,质量为18 g,则混合气体的平均摩尔质量是
2
g/mol。
(2)下图是某学校实验室从市场买回的试剂标签上的部分内容。
化学试剂
体积:500 mL
品名:浓硫酸
化学式:HSO
2 4
相对分子质量:98
密度:1.84 g·cm-3
质量分数:98%
则浓硫酸的物质的量浓度为 mol/L。
(3)向浓度相等、体积均为100 mL的A、B两份NaOH溶液中,分别通入一定量的CO 后,逐滴加入0.1
2
mol·L-1盐酸,产生CO 的体积(标准状况)与所加盐酸的体积关系如图所示。
2
①B曲线中,原溶液通入CO 后,所得溶液中溶质成分的化学式为 。
2
②A曲线中,消耗盐酸体积从30mL到90mL反应的离子方程式为 。
③A曲线中,原溶液通入CO 的体积为 mL(标准状况)。
2
学科网(北京)股份有限公司(4)复杂氧化物可改写成常见氧化物的形式,如Fe O 可改写为FeO·Fe O,Fe O 可改写为2FeO·Fe O。
3 4 2 3 4 5 2 3
①Fe O 改写成常见氧化物的形式为 。
5 7
②Pb O 改写成常见氧化物的形式为 。
3 4
11.(23-24高一上·安徽省部分学校·期末)物质的量在实验与科研中应用广泛。请回答下列问题:
(1)实验室欲用 的浓硫酸配制 稀硫酸 。
①下列操作正确的是 (填序号)。
操
作
选
项
②用量筒量取浓硫酸的体积为 。
③配制溶液的过程中,其他操作都正确,下列不当操作对所配溶液浓度的影响:
用量筒量取浓硫酸时俯视读数: (填“偏大”“偏小”或“无影响”,下同)。
稀释浓硫酸时,未冷却到室温即转移到容量瓶中: 。
将量取浓硫酸后的量筒进行洗涤,并将洗涤液转移到容量瓶中: 。
(2)室温下测得 的密度为 ,则室温下 的气体摩尔体积为 (用含 的代
数式表示)。
(3)为测定 溶液的浓度,某同学设计了如下实验方案。
实验原理: 。
实验步骤:
ⅰ.按图安装装置(夹持仪器略去),并检查装置气密性;
ⅱ.在各仪器中加入图示试剂;
ⅲ.调整 中两液面使其相平,使 中液面保持在0或略低于0刻度位置,读数并记录;
学科网(北京)股份有限公司ⅳ.将 液全部滴入A中并搅拌,反应完成后,再滴加稀硫酸至体系不再有气体产生;
ⅴ.待体系恢复到室温,移动 管,保持 中两液面相平,读数并记录、处理数据。
①步骤ⅲ需“调整 中两液面使其相平”的原因是 。
②将实验过程中测得的数据转化为 的质量时,其质量为 ,则 为
(列出计算式)。
③有同学认为用同样的装置和方法不能测定 溶液的浓度,其原因为 。
学科网(北京)股份有限公司