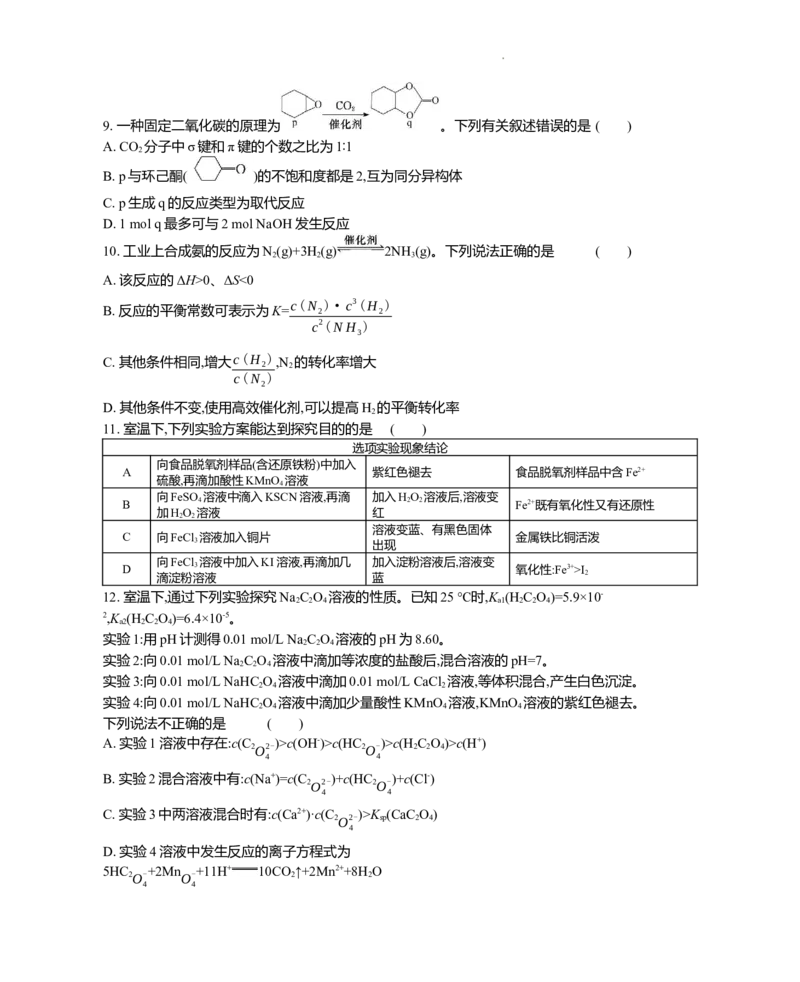
文档内容
绝密★启用前
江苏省 20232024 学年高三上学期期末迎考卷
化 学
注意事项:
1. 本试卷100分,考试用时75分钟。
2. 答题前,考生务必将班级、姓名、学号写在密封线内。
可能用到的相对原子质量:H—1 C—12 N—14 O—16 S—32 K—39 Fe—56 Cu—64 I—
127
一、 单项选择题:本题包括13小题,每小题3分,共计39分。每小题只有一个选项最符合题意。
1. 中国空间站建造成功、神舟系列飞船顺利往返,均展示了我国科技发展的巨大成就。下列相关叙述
正确的是 ( )
A. 空间站太阳翼伸展关键部件采用碳化硅材料,SiC属于无机非金属材料
B. 核心舱太阳能电池采用砷化镓(GaAs)材料,GaAs属于金属材料
C. 飞船火箭使用偏二甲肼[(CH ) N—NH ]作燃料,(CH ) N—NH 属于烃类
3 2 2 3 2 2
D. 飞船返回舱使用氮化硅耐高温结构材料,Si N 属于分子晶体
3 4
2. 反应2NH Cl+Ca(OH) CaCl +2NH ↑+2H O可用于实验室制备氨气。下列说法正确的是 (
4 2 2 3 2
)
·· ··
A. CaCl 的电子式为·Cl·Ca·Cl B. H O的空间结构为V形
2 · · · 2
·· ··
C. NH 是非极性分子 D. NH Cl仅含极性共价键
3 4
3. 实验室为制备二氧化氯(ClO )设计如下实验。已知:ClO 易溶于水,且与水不反应,沸点为11 ℃。反
2 2
应原理:SO +2NaClO +H SO 2ClO +2NaHSO 。下列说法不正确的是 ( )
2 3 2 4 2 4
甲 乙 丙 丁
A. 装置甲用于制备SO ,橡皮管a的作用是便于浓硫酸顺利流下
2
B. 装置乙中集气瓶的作用是防止倒吸
C. 装置丙中冰水浴的目的是液化并回收ClO
2
D. 装置丁中饱和NaHSO 溶液的作用是吸收SO 尾气
3 2
4. 下列物质性质与用途具有对应关系的是 ( )
A. 氨极易溶于水,液氨可用作制冷剂
B. H 具有还原性,可作为氢氧燃料电池的燃料
2
C. H O分子间形成氢键,H O(g)的热稳定性比H S(g)的高
2 2 2
学科网(北京)股份有限公司D. 氨气具有碱性,用浓氨水检验氯气管道是否泄漏
5. 硫酸亚铁铵\[(NH ) Fe(SO ) \]俗称莫尔盐,在生产生活中有多种应用。下列说法不正确的是( )
4 2 4 2
A. 可用K [Fe(CN) ]试剂检验莫尔盐是否已氧化变质
3 6
B. S 有4个 σ 键电子对
O2-
4
C. 基态O2-的价层电子轨道表示式为
D. N 中的键角大于NH
H+ 3
4
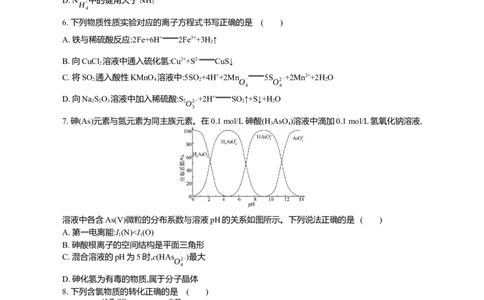
6. 下列物质性质实验对应的离子方程式书写正确的是 ( )
A. 铁与稀硫酸反应:2Fe+6H+ 2Fe3++3H ↑
2
B. 向CuCl 溶液中通入硫化氢:Cu2++S2- CuS↓
2
C. 将SO 通入酸性KMnO 溶液中:5SO +4H++2Mn 5S +2Mn2++2H O
2 4 2 O- O2- 2
4 4
D. 向Na S O 溶液中加入稀硫酸:S +2H+ SO ↑+S↓+H O
2 2 3 2O2- 2 2
3
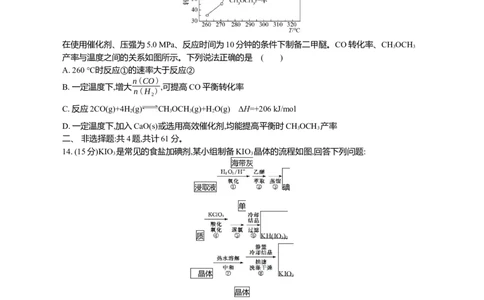
7. 砷(As)元素与氮元素为同主族元素。在0.1 mol/L砷酸(H AsO )溶液中滴加0.1 mol/L氢氧化钠溶液,
3 4
溶液中各含As(Ⅴ)微粒的分布系数与溶液pH的关系如图所示。下列说法正确的是 ( )
A. 第一电离能:I (N)0、ΔS<0
c(N )·c3(H )
B. 反应的平衡常数可表示为K= 2 2
c2(N H )
3
C. 其他条件相同,增大
c(H )
,N 的转化率增大
2 2
c(N )
2
D. 其他条件不变,使用高效催化剂,可以提高H 的平衡转化率
2
11. 室温下,下列实验方案能达到探究目的的是 ( )
选项实验现象结论
向食品脱氧剂样品(含还原铁粉)中加入
A 紫红色褪去 食品脱氧剂样品中含Fe2+
硫酸,再滴加酸性KMnO 溶液
4
向FeSO 溶液中滴入KSCN溶液,再滴 加入HO 溶液后,溶液变
B 4 2 2 Fe2+既有氧化性又有还原性
加HO 溶液 红
2 2
溶液变蓝、有黑色固体
C 向FeCl 溶液加入铜片 金属铁比铜活泼
3 出现
向FeCl 溶液中加入KI溶液,再滴加几 加入淀粉溶液后,溶液变
D 3 氧化性:Fe3+>I
滴淀粉溶液 蓝 2
12. 室温下,通过下列实验探究Na C O 溶液的性质。已知25 ℃时,K (H C O )=5.9×10-
2 2 4 a1 2 2 4
2,K (H C O )=6.4×10-5。
a2 2 2 4
实验1:用pH计测得0.01 mol/L Na C O 溶液的pH为8.60。
2 2 4
实验2:向0.01 mol/L Na C O 溶液中滴加等浓度的盐酸后,混合溶液的pH=7。
2 2 4
实验3:向0.01 mol/L NaHC O 溶液中滴加0.01 mol/L CaCl 溶液,等体积混合,产生白色沉淀。
2 4 2
实验4:向0.01 mol/L NaHC O 溶液中滴加少量酸性KMnO 溶液,KMnO 溶液的紫红色褪去。
2 4 4 4
下列说法不正确的是 ( )
A. 实验1溶液中存在:c(C )>c(OH-)>c(HC )>c(H C O )>c(H+)
2O2- 2O- 2 2 4
4 4
B. 实验2混合溶液中有:c(Na+)=c(C )+c(HC )+c(Cl-)
2O2- 2O-
4 4
C. 实验3中两溶液混合时有:c(Ca2+)·c(C )>K (CaC O )
2O2- sp 2 4
4
D. 实验4溶液中发生反应的离子方程式为
5HC +2Mn +11H+ 10CO ↑+2Mn2++8H O
2O- O- 2 2
4 4
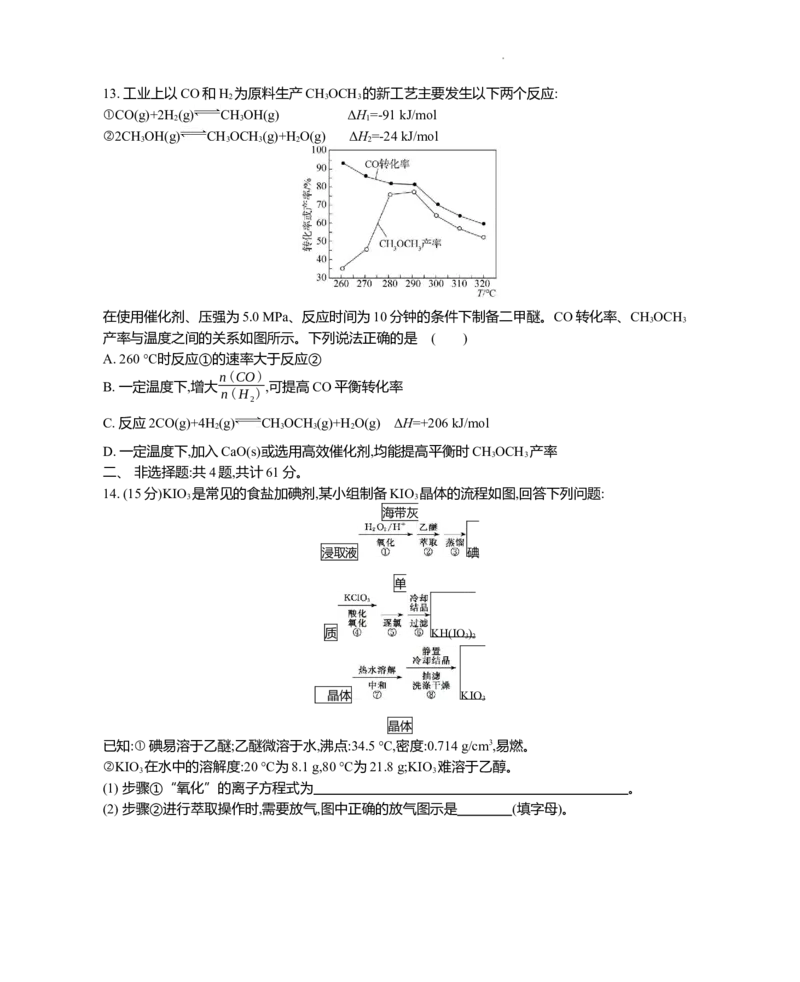
学科网(北京)股份有限公司13. 工业上以CO和H 为原料生产CH OCH 的新工艺主要发生以下两个反应:
2 3 3
①CO(g)+2H (g) CH OH(g) ΔH =-91 kJ/mol
2 3 1
②2CH OH(g) CH OCH (g)+H O(g) ΔH =-24 kJ/mol
3 3 3 2 2
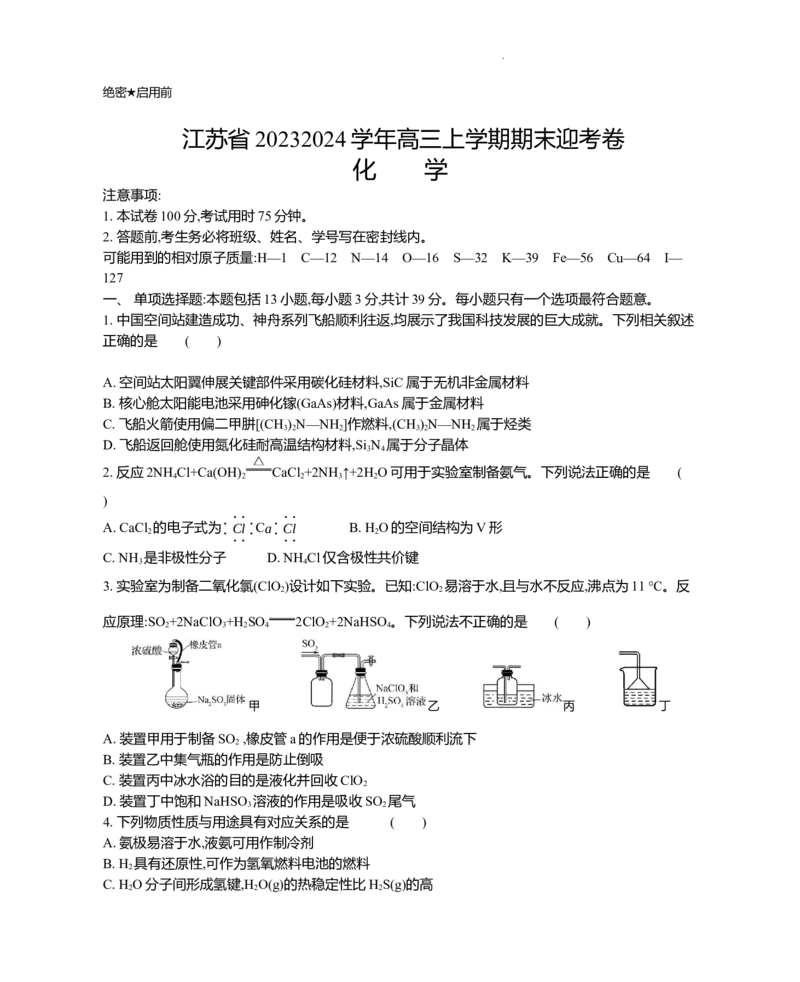
在使用催化剂、压强为5.0 MPa、反应时间为10分钟的条件下制备二甲醚。CO转化率、CH OCH
3 3
产率与温度之间的关系如图所示。下列说法正确的是 ( )
A. 260 ℃时反应①的速率大于反应②
n(CO)
B. 一定温度下,增大 ,可提高CO平衡转化率
n(H )
2
C. 反应2CO(g)+4H (g) CH OCH (g)+H O(g) ΔH=+206 kJ/mol
2 3 3 2
D. 一定温度下,加入CaO(s)或选用高效催化剂,均能提高平衡时CH OCH 产率
3 3
二、 非选择题:共4题,共计61分。
14. (15分)KIO 是常见的食盐加碘剂,某小组制备KIO 晶体的流程如图,回答下列问题:
3 3
海带灰
浸取液 碘
单
质 KH(IO)
3 2
晶体 KIO
3
晶体
已知:①碘易溶于乙醚;乙醚微溶于水,沸点:34.5 ℃,密度:0.714 g/cm3,易燃。
②KIO 在水中的溶解度:20 ℃为8.1 g,80 ℃为21.8 g;KIO 难溶于乙醇。
3 3
(1) 步骤①“氧化”的离子方程式为 。
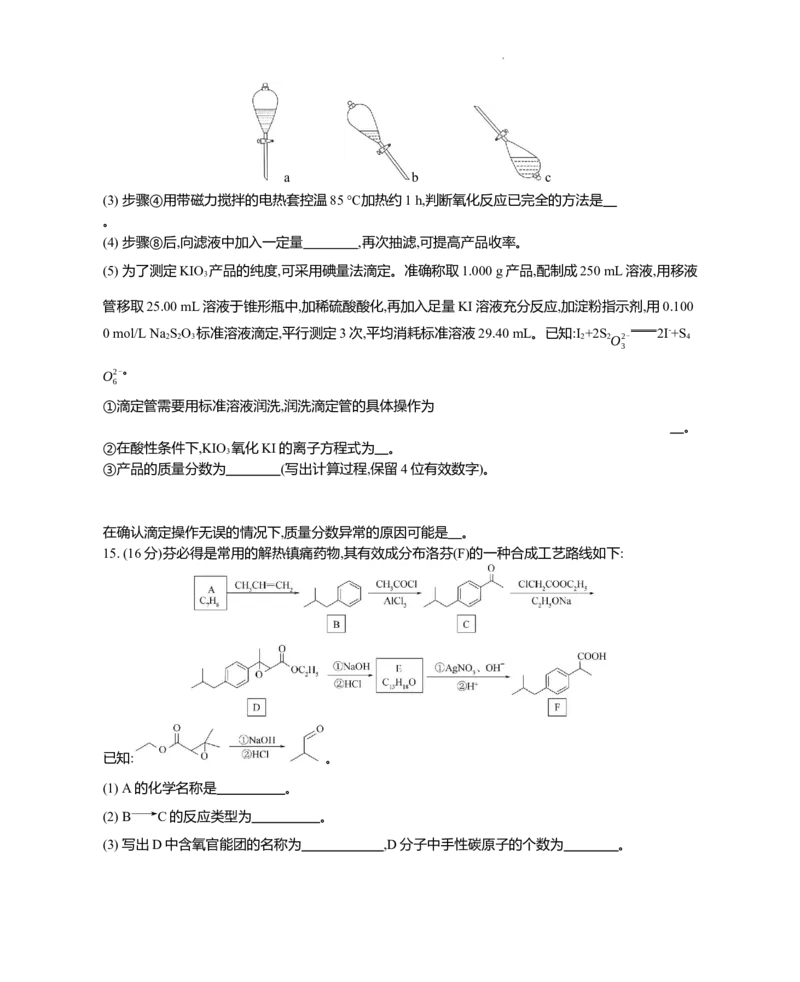
(2) 步骤②进行萃取操作时,需要放气,图中正确的放气图示是 (填字母)。
学科网(北京)股份有限公司a b c
(3) 步骤④用带磁力搅拌的电热套控温85 ℃加热约1 h,判断氧化反应已完全的方法是
。
(4) 步骤⑧后,向滤液中加入一定量 ,再次抽滤,可提高产品收率。
(5) 为了测定KIO 产品的纯度,可采用碘量法滴定。准确称取1.000 g产品,配制成250 mL溶液,用移液
3
管移取25.00 mL溶液于锥形瓶中,加稀硫酸酸化,再加入足量KI溶液充分反应,加淀粉指示剂,用0.100
0 mol/L Na S O 标准溶液滴定,平行测定3次,平均消耗标准溶液29.40 mL。已知:I +2S 2I-+S
2 2 3 2 2O2- 4
3
。
O2-
6
①滴定管需要用标准溶液润洗,润洗滴定管的具体操作为
。
②在酸性条件下,KIO 氧化KI的离子方程式为 。
3
③产品的质量分数为 (写出计算过程,保留4位有效数字)。
在确认滴定操作无误的情况下,质量分数异常的原因可能是 。
15. (16分)芬必得是常用的解热镇痛药物,其有效成分布洛芬(F)的一种合成工艺路线如下:
已知: 。
(1) A的化学名称是 。
(2) B C的反应类型为 。
(3) 写出D中含氧官能团的名称为 ,D分子中手性碳原子的个数为 。
学科网(北京)股份有限公司(4) 分子结构修饰可提高药物的治疗效果,降低毒副作用,布洛芬可用 进行成酯修
饰,请写出该化学方程式: 。
(5) 写出同时满足下列条件的E的一种同分异构体的结构简式: 。
①能发生银镜反应;②除苯环外不含其他环状结构且苯环上有4个取代基;③核磁共振氢谱显示有6
组峰。
(6) 布洛芬有多种合成方法,试根据所学知识写出以化合物C为原料,经另一路线制备布洛芬的合成路
线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
已知:R—Br R—COOH。
16. (15分)柠檬酸亚铁(FeC H O )是一种易被人体吸收的高效铁制剂,医疗上可以用来治疗缺铁性贫血。
6 6 7
某课题组以硫铁矿烧渣(含Fe O 、SiO 、少量Al O 等)为原料,先制备碳酸亚铁,再与柠檬酸反应可以
2 3 2 2 3
制得柠檬酸亚铁。其工艺流程如下:
已知:相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol/L计算):
金属离子 Al3+ Fe2+ Fe3+
沉淀开始pH 3.1 5.9 1.2
沉淀完全 pH 5.1 6.9 3.2
(1) 基态Fe原子价层电子排布式为 。
(2) “浸泡”时加入过量硫酸的目的: 。
(3) “除杂”时有同学提出下列两种途径,请选择较合理的途径并说明理由:
。
途径一:浸泡滤液 FeSO
4
途径二:浸泡滤液 Fe(OH) FeSO
3 4
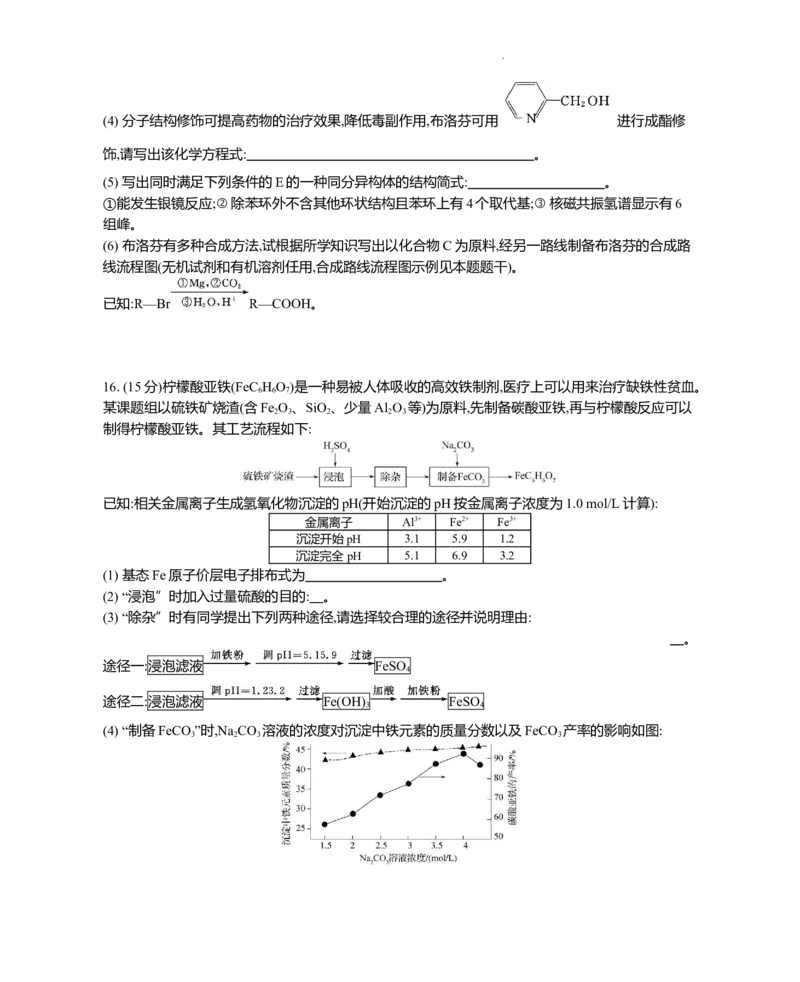
(4) “制备FeCO ”时,Na CO 溶液的浓度对沉淀中铁元素的质量分数以及FeCO 产率的影响如图:
3 2 3 3
学科网(北京)股份有限公司Na CO 溶液的浓度大于4 mol/L时,FeCO 的产率有所下降,而沉淀中铁元素质量分数仍在上升的原因
2 3 3
是 。
(5) 已知柠檬酸亚铁易被氧化,能溶于水,不溶于乙醇。设计实验方案,用“除杂”后的FeSO 溶液制备
4
柠檬酸亚铁晶体:
,静置、过滤、洗涤、干燥, 获得柠檬酸亚铁晶体(必须用到的试剂有:Fe粉、4 mol/L Na CO 溶液、柠
2 3
檬酸溶液、无水乙醇)。
17. (15分)氮的化合物在工农业生产中有着重要的作用,氮的化合物也会对大气及水体等产生污染,在
利用这些物质的同时,治理和减少污染是重要的课题。
(1) NH 和N H 是氮元素的两种重要的氢化物。
3 2 4
①工业上常用NH 的水溶液和次氯酸钠反应生成水合肼(N H ·H O),写出该反应的化学方程式:
3 2 4 2
。
②N H 能使锅炉内壁的铁锈(Fe O ·xH O)变成磁性氧化层,减缓锅炉锈蚀,且不产生污染物。写出N H
2 4 2 3 2 2 4
与铁锈反应的化学方程式: 。
(2) NO和NO 是氮元素的两种常见氧化物,它们之间可以相互转化。NO 会造成光化学烟雾。
2 x
①2NO(g)+O (g) 2NO (g)由以下反应复合而成。
2 2
反应Ⅰ. 2NO(g) N O (g) ΔH
2 2 1
反应Ⅱ.N O (g)+O (g) 2NO (g) ΔH
2 2 2 2 2
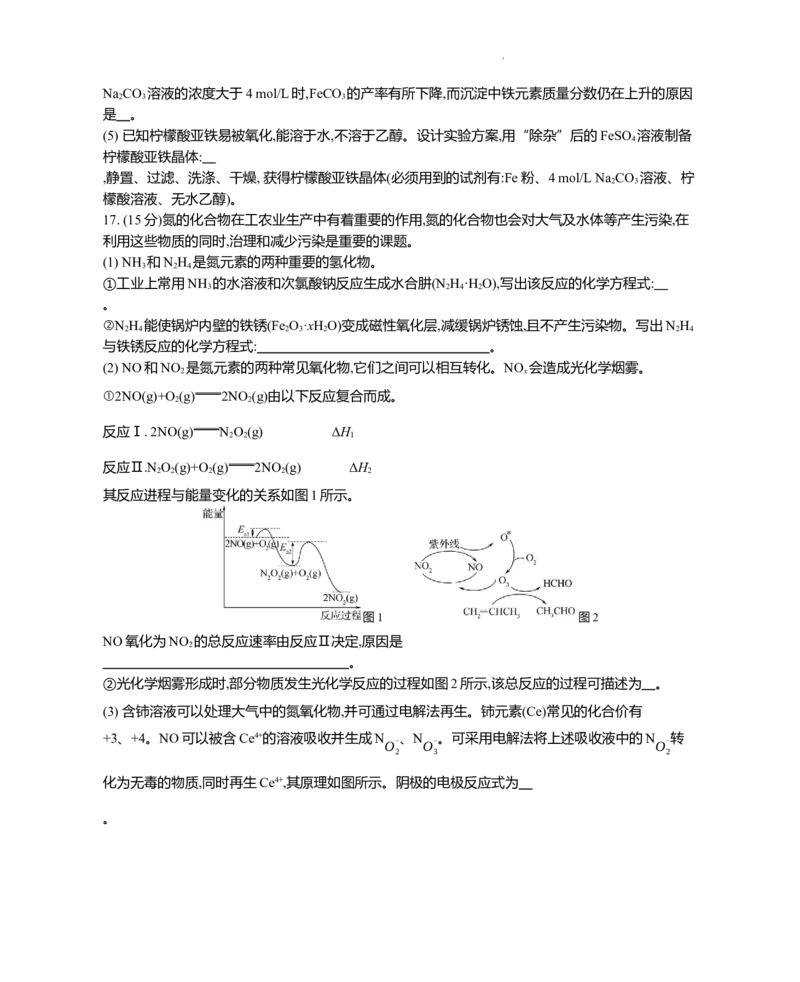
其反应进程与能量变化的关系如图1所示。
图1 图2
NO氧化为NO 的总反应速率由反应Ⅱ决定,原因是
2
。
②光化学烟雾形成时,部分物质发生光化学反应的过程如图2所示,该总反应的过程可描述为 。
(3) 含铈溶液可以处理大气中的氮氧化物,并可通过电解法再生。铈元素(Ce)常见的化合价有
+3、+4。NO可以被含Ce4+的溶液吸收并生成N 、N 。可采用电解法将上述吸收液中的N 转
O- O- O-
2 3 2
化为无毒的物质,同时再生Ce4+,其原理如图所示。阴极的电极反应式为
。
学科网(北京)股份有限公司学科网(北京)股份有限公司学科网(北京)股份有限公司