文档内容
江苏省 20232024 学年高三上学期期末迎考卷
化学参考答案与评分标准
1. A 解析:GaAs属于新型无机非金属材料,B错误;烃只含碳和氢两种元素,(CH)N—NH 不属于烃类,C错误;氮化硅耐高温,属于共
32 2
价晶体,D错误。
·· ··
2. B 解析:CaCl 的电子式为[·Cl·]-Ca2+[·Cl·]-,A错误;HO的空间结构为V形,B正确;NH 是极性分子,C错误;NHCl是离子
2 · · · · 2 3 4
·· ··
化合物,其中含有离子键和极性共价键,D错误。
3. D 解析:装置甲用于制备SO ,橡皮管a的作用是平衡气压,便于浓硫酸顺利流下,A正确;装置乙中集气瓶的作用是防止锥形瓶中
2
的液体倒吸,B正确;ClO 的沸点较低,装置丙的水槽盛放冰水可以液化ClO,起到冷凝回收作用,C正确;装置丁烧杯里应该盛放NaOH
2 2
溶液,可吸收未反应完的二氧化硫,防止污染空气,饱和NaHSO 溶液与二氧化硫不反应,D错误。
3
4. B 解析:氨易液化,液氨汽化时吸收大量的热,因此可作制冷剂,A错误;O的非金属性强于S,则HO(g) 的热稳定性比HS(g)的高,与
2 2
水分子间形成氢键无关,C错误;用浓氨水检验氯气管道是否泄漏,发生反应:3Cl+8NH 6NHCl+N,利用的是氨气的还原性,能与氯
2 3 4 2
气反应生成氯化铵,与其碱性无关,D错误。
5. A 解析:莫尔盐中的铁元素为+2价,易被空气中的氧气氧化为+3价,检验莫尔盐中是否存在铁离子应用亚铁氰化钾{K\[Fe(CN)}
4 6
溶液或KSCN溶液,A错误;S O2-中,中心S原子的价层电子对数为4,采用sp3杂化,有4个σ键电子对,B正确;由基态O2-的价层电子排
4
布式为2s22p6知,C正确;NH
3
分子中孤电子对对成键电子的排斥使得其键角小于N H+,D正确。
4
6. D 解析:铁与稀硫酸反应生成硫酸亚铁和氢气,其离子方程式为Fe+2H+ Fe2++H↑,A错误;向CuCl 溶液中通入硫化氢生成CuS
2 2
沉淀,硫化氢为弱酸,在离子方程式中不能拆开,其离子方程式为Cu2++HS CuS↓+2H+,B错误;将SO 通入酸性KMnO 溶液中,离子
2 2 4
方程式为5SO 2 +2H 2 O+2Mn O- 5S O2-+2Mn2++4H+,C错误;向Na 2 S 2 O 3 溶液中加入稀硫酸,离子方程式为S 2O2-+
4 4 3
↑+S↓+HO,D正确。
2
7. D 解析:氮原子核外2p能级是半充满较稳定的结构,故第一电离能:I
1
(N)>I
1
(O),A错误;砷酸根离子(As O3-)中,中心As原子的价层
4
电子对数为4,为sp3杂化,空间结构为正四面体形,B错误;由图可知,混合溶液的pH为5时,c(H
2
As O-)最大,C错误。
4
8. C 解析:漂白粉的有效成分是Ca(ClO),与CO、HO反应生成HClO,HClO见光分解生成HCl和O,不能生成Cl,A错误;加热
2 2 2 2 2
MgCl 溶液时,MgCl 水解生成Mg(OH),应该在HCl气流中加热MgCl 溶液,B错误;电解NaCl溶液生成NaOH、H 和Cl,Cl 具有强
2 2 2 2 2 2 2
氧化性,与铁单质在点燃条件下反应生成FeCl,C正确;NaCl溶液和CO 不能反应生成NaHCO,D错误。
3 2 3
9. C 解析:CO 分子的结构式为O C O,双键中含有1个σ键和1个π键,所以该分子中σ键和π键的个数之比为1∶1,A正确;p和
2
环己酮的分子式都是CH O,结构不同,二者互为同分异构体,B正确;由原理可知,p和CO 发生加成反应生成q,C错误;1 mol q中含有
6 10 2
1 mol碳酸酯基,则最多可与2 mol NaOH发生反应,D正确。
c2(NH )
10. C 解析:该反应是气体分子数目减小的反应,ΔS<0,由ΔH-TΔS<0知,ΔH<0,A错误;该反应的平衡常数K= 3 ,B
c(N )·c3(H )
2 2
c(H )
错误;其他条件相同,增大 2 ,相当于增大H 2 的浓度,平衡正向移动,N 2 的转化率增加,C正确;使用高效催化剂,不能改变H 2 的平
c(N )
2
衡转化率,D错误。
11. D 解析:向食品脱氧剂样品(含还原铁粉)中加入硫酸后,铁粉会与硫酸反应生成硫酸亚铁,酸性KMnO 溶液为强氧化剂,会氧化亚
4
铁离子,则滴加酸性KMnO 溶液,紫红色褪去,不能说明原食品脱氧剂样品中含Fe2+,A错误;向FeSO 溶液中滴入KSCN溶液,无明显现
4 4
象,再滴加HO 溶液,HO 会将亚铁离子氧化为铁离子,则加入HO 溶液后,溶液变红,只能说明Fe2+有还原性,B错误;向FeCl 溶液加
2 2 2 2 2 2 3
入铜片会发生反应:2FeCl+Cu 2FeCl+CuCl,可看到溶液颜色改变,无黑色固体出现,说明氧化性:Fe3+>Cu2+,C错误;向FeCl 溶液中
3 2 2 3
加入KI溶液,再滴加几滴淀粉溶液,FeCl 溶液会与KI溶液反应生成FeCl 和I,则溶液变蓝,说明氧化性:Fe3+>I,D正确。
3 2 2 2
学科网(北京)股份有限公司12. B 解析:Na 2 C 2 O 4 溶液pH为8.60,溶液显碱性,C 2O2-分步水解,且以第一步水解为主,则溶液中存在:c(C 2O2-)>c(OH-)>c(HC 2O-
4 4 4
)>c(H
2
C
2
O
4
)>c(H+),A正确;实验2的混合溶液中电荷守恒:c(H+)+c(Na+)=2c(C 2O2-)+c(HC 2O-)+c(Cl-)+c(OH-),当混合溶液的pH=7,即
4 4
c(H+)=c(OH-),所以c(Na+)=2c(C 2O2-)+c(HC 2O-)+c(Cl-),B错误;实验3中两溶液混合时有沉淀产生,则c(Ca2+)·c(C 2O2-)>K
sp
(CaC
2
O
4
),C
4 4 4
正确;酸性高锰酸钾溶液具有强氧化性,能氧化HC 2O-生成CO
2
,Mn O-被还原为Mn2+,离子方程式为5HC 2O-+2Mn O-+11H+
4 4 4 4
10CO↑+2Mn2++8HO,D正确。
2 2
13. A 解析:260 ℃时,CO转化率高但CHOCH 产率很低,说明此时反应①CO转化成CHOH的速率快,反应②CHOH转化成
3 3 3 3
n(CO)
CHOCH 的速率慢,即此时反应①的速率大于反应②,A正确;一定温度下,增大 ,可提高H 的平衡转化率,CO平衡转化率降
3 3 n(H ) 2
2
低,B错误;根据盖斯定律,反应①×2+反应②得到2CO(g)+4H(g) CHOCH(g)+HO(g) ΔH=2ΔH+ΔH=-(2×91+24)kJ/mol=-206
2 3 3 2 1 2
kJ/mol,C错误;一定温度下,选用高效催化剂不能提高平衡转化率,D错误。
14. (1) 2I-+2H++H
2
O
2
I
2
+2H
2
O(2分) (2) c(1分) (3) 反应液褪色(1分) (4) 乙醇(1分) (5) ①从滴定管上口加入少量标准液,倾
斜着转动滴定管,使液体润湿内壁,然后从下部放出,重复23次(3分) ②I O-+5I-+6H+ 3I
2
+3H
2
O(2分) ③104.9%(3分,计算过程
3
见解析) ④滴定摇动锥形瓶时,过量的I-被空气氧化成I(或含有KClO 杂质)(2分)
2 3
解析:海带灰浸取液中含碘离子,在酸性条件下,I-被过氧化氢氧化为碘单质,从水溶液中分离碘可采用乙醚萃取、经分液后得到有机层,
蒸馏碘的乙醚溶液得到碘单质,碘单质在酸性条件下被KClO 氧化为碘酸根离子,反应过程中存在生成氯气的副反应,经过逐氯,冷却
3
结晶、过滤得到 KH(IO) 晶体,经热水溶解、中和后得到KIO,利用碘酸钾的溶解度随温度升高增幅较大,采用冷却结晶法,过滤得到
32 3
碘酸钾,KIO 难溶于乙醇,则向滤液中加乙醇,可促进碘酸钾析出,能提高产量。(3)碘水呈棕黄色,氯气在加热条件下难溶于酸性溶液,
3
则用带磁力搅拌的电热套控温85 ℃加热,反应过程中,溶液颜色逐渐变浅,当反应液完全褪色,说明氧化反应已完成。(4)已知KIO 难
3
溶于乙醇,步骤⑧后,向滤液中加入一定量乙醇,能析出碘酸钾晶体,再次抽滤,可提高产品收率。(5)③用碘量法测定KIO
3
产品的纯度,
1 1
反应原理为IO- +5I-+6H+ 3I+3HO、I+2SO2- 2I-+SO2- ,则可得到关系式:KIO3I6SO2- ,n(KIO)= n(SO2- )= ×0.100 0
3 2 2 2 2 3 4 6 3 2 2 3 3 6 2 3 6
mol/L×29.4×10-3 L=4.9×10-4 mol
250mL
m(KIO ) 4.9×10-4mol×214g/mol×
产品中KIO 的质量分数= 3 ×100%= 25.00mL×100%≈104.9%。若滴定操作无
3
m(样品)
1.000g
误,则实验过程中有其他途径生成了碘单质或有其他能消耗硫代硫酸钠的杂质存在,原因可能是滴定摇动锥形瓶时,过量的I-被空气氧
化成I(或含有KClO 杂质)。
2 3
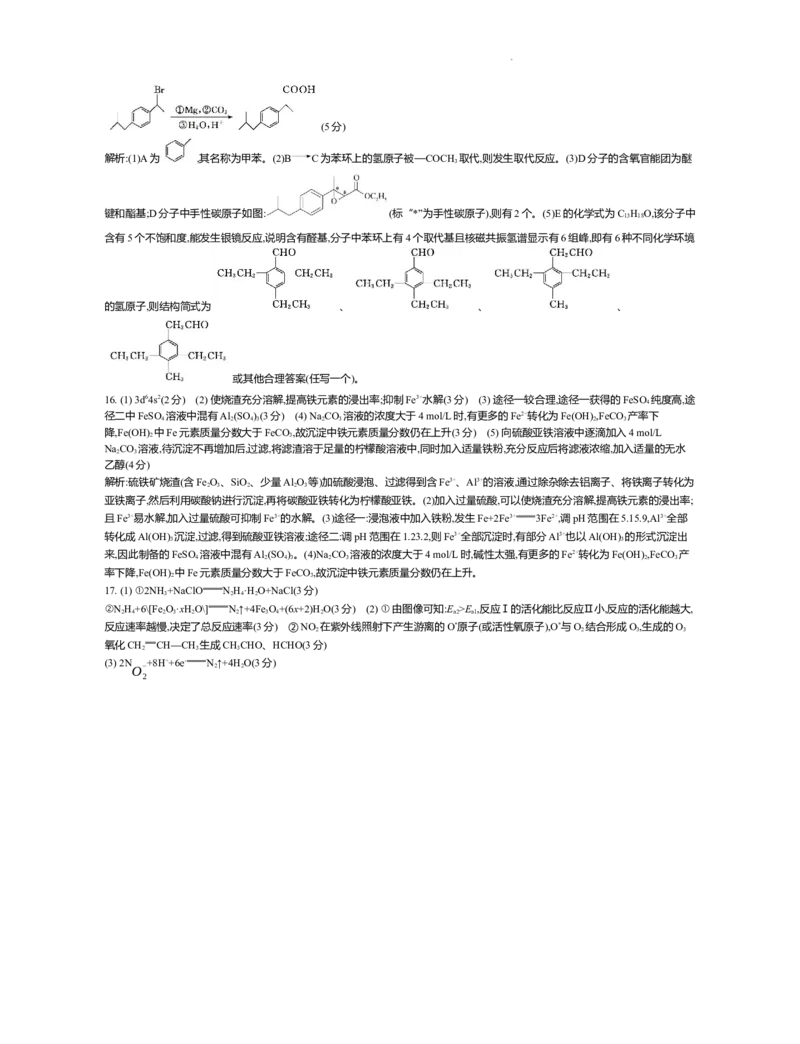
15. (1) 甲苯(1分) (2) 取代反应(2分)
(3) 酯基和醚键(2分) 2(2分)
(4) +
+HO(2分)
2
(5) (2分,其他合理答案均给分)
(6)
学科网(北京)股份有限公司(5分)
解析:(1)A为 ,其名称为甲苯。(2)B C为苯环上的氢原子被—COCH 取代,则发生取代反应。(3)D分子的含氧官能团为醚
3
键和酯基;D分子中手性碳原子如图: (标“*”为手性碳原子),则有2个。(5)E的化学式为C H O,该分子中
13 18
含有5个不饱和度,能发生银镜反应,说明含有醛基,分子中苯环上有4个取代基且核磁共振氢谱显示有6组峰,即有6种不同化学环境
的氢原子,则结构简式为 、 、 、
或其他合理答案(任写一个)。
16. (1) 3d64s2(2分) (2) 使烧渣充分溶解,提高铁元素的浸出率;抑制Fe3+水解(3分) (3) 途径一较合理,途径一获得的FeSO 纯度高,途
4
径二中FeSO 溶液中混有Al(SO)(3分) (4) NaCO 溶液的浓度大于4 mol/L时,有更多的Fe2+转化为Fe(OH),FeCO 产率下
4 2 43 2 3 2 3
降,Fe(OH) 中Fe元素质量分数大于FeCO,故沉淀中铁元素质量分数仍在上升(3分) (5) 向硫酸亚铁溶液中逐滴加入4 mol/L
2 3
NaCO 溶液,待沉淀不再增加后,过滤,将滤渣溶于足量的柠檬酸溶液中,同时加入适量铁粉,充分反应后将滤液浓缩,加入适量的无水
2 3
乙醇(4分)
解析:硫铁矿烧渣(含FeO、SiO、少量AlO 等)加硫酸浸泡、过滤得到含Fe3+、Al3+的溶液,通过除杂除去铝离子、将铁离子转化为
2 3 2 2 3
亚铁离子,然后利用碳酸钠进行沉淀,再将碳酸亚铁转化为柠檬酸亚铁。(2)加入过量硫酸,可以使烧渣充分溶解,提高铁元素的浸出率;
且Fe3+易水解,加入过量硫酸可抑制Fe3+的水解。(3)途径一:浸泡液中加入铁粉,发生Fe+2Fe3+ 3Fe2+,调pH范围在5.15.9,Al3+全部
转化成Al(OH) 沉淀,过滤,得到硫酸亚铁溶液;途径二:调pH范围在1.23.2,则Fe3+全部沉淀时,有部分Al3+也以Al(OH) 的形式沉淀出
3 3
来,因此制备的FeSO 溶液中混有Al(SO)。(4)NaCO 溶液的浓度大于4 mol/L时,碱性太强,有更多的Fe2+转化为Fe(OH),FeCO 产
4 2 43 2 3 2 3
率下降,Fe(OH) 中Fe元素质量分数大于FeCO,故沉淀中铁元素质量分数仍在上升。
2 3
17. (1) ①2NH
3
+NaClO N
2
H
4
·H
2
O+NaCl(3分)
②N
2
H
4
+6\[Fe
2
O
3
·xH
2
O\] N
2
↑+4Fe
3
O
4
+(6x+2)H
2
O(3分) (2) ①由图像可知:E
a2
>E
a1
,反应Ⅰ的活化能比反应Ⅱ小,反应的活化能越大,
反应速率越慢,决定了总反应速率(3分) ②NO 在紫外线照射下产生游离的O*原子(或活性氧原子),O*与O 结合形成O,生成的O
2 2 3 3
氧化CH CH—CH 生成CHCHO、HCHO(3分)
2 3 3
(3) 2N O-+8H++6e- N
2
↑+4H
2
O(3分)
2
学科网(北京)股份有限公司学科网(北京)股份有限公司