文档内容
2024-2025 学年高一化学上学期期中模拟卷
(考试时间:60分钟 试卷满分:100分)
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准
考证号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,
用橡皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.测试范围:第1章~第2章(人教版2019必修第一册)。
5.难度系数:0.67
6.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23
第Ⅰ卷(选择题 共 48 分)
一、选择题:本题共16个小题,每小题3分,共48分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
1.中华文明源远流长,现代科技造就美好生活。下列科技产品和技艺中,不涉及化学变化的是
A.青铜器皿除锈 B.节日燃放烟花 C.用侯氏制碱法制取纯碱 D.雕刻玉器
2.对下列物质分类全部正确的是
①纯碱 ②食盐水 ③石灰水 ④NaOH ⑤液氯 ⑥KMnO
4
A.碱:①④ B.电解质:①②
C.常见氧化剂:⑤⑥ D.混合物:②⑤
3.氧化还原反应是一类重要的化学反应,广泛存在于生产和生活中,下列变化中不涉及氧化还原反应的是
A.钢铁的锈蚀 B.钟乳石的形成
C.绿色植物的光合作用 D.食物的腐败
4.类比推理是化学学科中常用的一种思维方法,下列推理的结论正确的是
A.根据CO 是酸性氧化物,推测NO 也是酸性氧化物
2 2
B.根据HCl是由分子构成的,推测HF也是由分子构成的
C.根据硫酸是强酸,推测碳酸也是强酸
D.根据NaO与水反应生成NaOH,推测Fe O 与水反应生成Fe(OH)
2 2 3 3
5.下列生活中的物质与其有效成分的化学式、用途的对应关系中,不正确的是
A.小苏打的有效成分是NaCO,可做发酵粉
2 3
B.食盐的有效成分是NaCl,可做调味剂
1
学学科科网网((北北京京))股股份份有有限限公公司司C.复方氢氧化铝片的有效成分是Al(OH) ,可做抗酸剂
3
D.漂白粉的有效成分是Ca(ClO) ,可做消毒剂
2
6.下列电离方程式中书写正确的是
A. B.
C. D.
7.化学实验中颜色变化可将化学抽象之美具体为形象之美。下列叙述正确的是
A.将氯气持续通入稀的酚酞溶液中,溶液先变红后褪色
B.在氯化亚铁溶液中滴入新制的氯水,溶液变成棕黄色
C.用玻璃棒将碳酸钠溶液点在pH试纸上,试纸变成红色
D.用洁净的玻璃棒蘸取硝酸钾在煤气灯外焰上灼烧,火焰呈紫色
8.实验室制备氧气的化学方程式:KMnO KMnO +MnO+O ↑,对于该反应有关说法错误的是
4 2 4 2 2
A.KMnO 只作氧化剂 B.部分氧元素被氧化
4
C.锰元素被还原 D.该反应既属于分解反应,也属于氧化还原反应
9.在给定的条件下,下列选项所示的物质间转化均能实现的是
A.Fe O Fe FeCl
2 3 3
B.NaClO溶液 HClO O
2
C.Al Al O Al(OH)
2 3 3
D.NaOH溶液 NaHCO 溶液 CO
3 2
10.某化学小组需要配制 的 溶液,下列实验操作会使所得溶液浓度偏低的是
A.用托盘天平称取 固体
B.向小烧杯中加水使氢氧化钠溶解并冷却至室温
C.定容过程观察容量瓶内液面时俯视刻度线
D.把溶液转移到洗净但未干燥的容量瓶中
11.下列各组离子中,能在溶液中大量共存的是
A.Na+、OH-、HCO 、Cl- B.K+、H+、ClO-、Cl-
C.K+、H+、MnO 、Cl– D.Na+、OH-、ClO-、Cl-
12.下列离子检验的方法和结论正确的是
A.某溶液中滴加硝酸银溶液生成白色沉淀,说明原溶液中有Cl-
B.某溶液中滴加氯化钡溶液生成白色沉淀,说明原溶液中有SO
C.某溶液中滴加氢氧化钠溶液生成蓝色沉淀,说明原溶液中有Cu2+
D.某溶液中滴加稀硫酸溶液生成无色气体,说明原溶液中有CO
13.下列说法中错误的是
A.0.1molNa CO 和NaHCO 的混合物含有的氧原子数为0.3N
2 3 3 A
B.常温常压下,22.4LO 的物质的量为1mol
2
2
学学科科网网((北北京京))股股份份有有限限公公司司C.1molCO 中含有的原子总数为3N
2 A
D.1L0.1mol/LNa SO 溶液中含有0.2molNa+
2 4
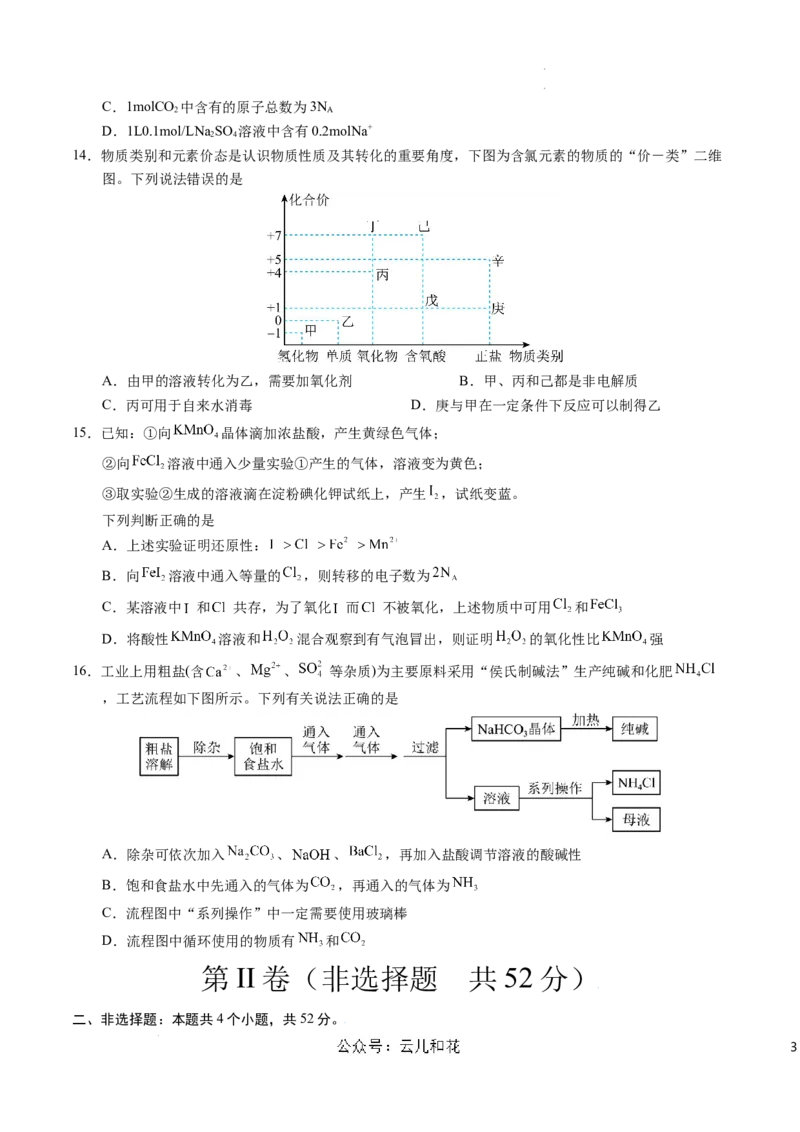
14.物质类别和元素价态是认识物质性质及其转化的重要角度,下图为含氯元素的物质的“价-类”二维
图。下列说法错误的是
A.由甲的溶液转化为乙,需要加氧化剂 B.甲、丙和己都是非电解质
C.丙可用于自来水消毒 D.庚与甲在一定条件下反应可以制得乙
15.已知:①向 晶体滴加浓盐酸,产生黄绿色气体;
②向 溶液中通入少量实验①产生的气体,溶液变为黄色;
③取实验②生成的溶液滴在淀粉碘化钾试纸上,产生 ,试纸变蓝。
下列判断正确的是
A.上述实验证明还原性:
B.向 溶液中通入等量的 ,则转移的电子数为
C.某溶液中 和 共存,为了氧化 而 不被氧化,上述物质中可用 和
D.将酸性 溶液和 混合观察到有气泡冒出,则证明 的氧化性比 强
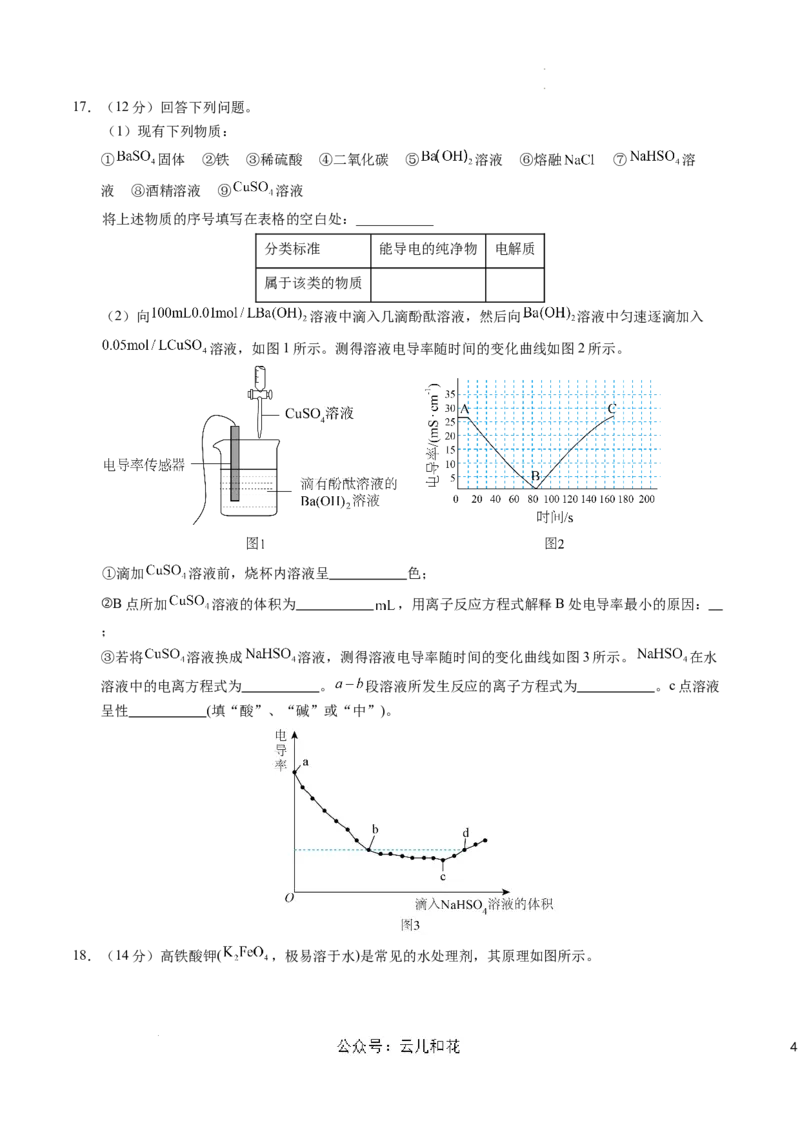
16.工业上用粗盐(含 、 、 等杂质)为主要原料采用“侯氏制碱法”生产纯碱和化肥
,工艺流程如下图所示。下列有关说法正确的是
A.除杂可依次加入 、 、 ,再加入盐酸调节溶液的酸碱性
B.饱和食盐水中先通入的气体为 ,再通入的气体为
C.流程图中“系列操作”中一定需要使用玻璃棒
D.流程图中循环使用的物质有 和
第 II 卷(非选择题 共 52 分)
二、非选择题:本题共4个小题,共52分。
3
学学科科网网((北北京京))股股份份有有限限公公司司17.(12分)回答下列问题。
(1)现有下列物质:
① 固体 ②铁 ③稀硫酸 ④二氧化碳 ⑤ 溶液 ⑥熔融 ⑦ 溶
液 ⑧酒精溶液 ⑨ 溶液
将上述物质的序号填写在表格的空白处:___________
分类标准 能导电的纯净物 电解质
属于该类的物质
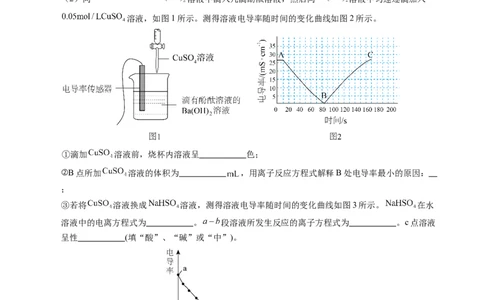
(2)向 溶液中滴入几滴酚酞溶液,然后向 溶液中匀速逐滴加入
溶液,如图1所示。测得溶液电导率随时间的变化曲线如图2所示。
①滴加 溶液前,烧杯内溶液呈 色;
②B点所加 溶液的体积为 ,用离子反应方程式解释B处电导率最小的原因:
;
③若将 溶液换成 溶液,测得溶液电导率随时间的变化曲线如图3所示。 在水
溶液中的电离方程式为 。 段溶液所发生反应的离子方程式为 。c点溶液
呈性 (填“酸”、“碱”或“中”)。
18.(14分)高铁酸钾( ,极易溶于水)是常见的水处理剂,其原理如图所示。
4
学学科科网网((北北京京))股股份份有有限限公公司司【查阅资料】向胶体中加入电解质后,胶体因失去稳定性而发生离子的聚集以至沉淀,称为电解质对
胶体的聚沉作用,简称胶体的聚沉。
请回答下列问题:
(1) 中铁元素的化合价为 价。
(2)过程①中活性菌表现了 (填“氧化”或“还原”)性,该过程的还原产物是
(填离子符号);过程③属于 (填“物理”或“化学”)变化。
(3)根据上述原理分析,作水处理剂时, 的作用有 (填两个)。
(4)制备高铁酸钾常用的反应原理为 (反应未配平)。
①该反应中,Cl元素的化合价由 价变为 价;通过该反应说明:在碱性条件下,氧化性
(填“>”、“=”或“<”) 。
②配平该反应的化学方程式,并用双线桥法表示电子转移的方向和数目: ,将该反应改写为
离子方程式: 。
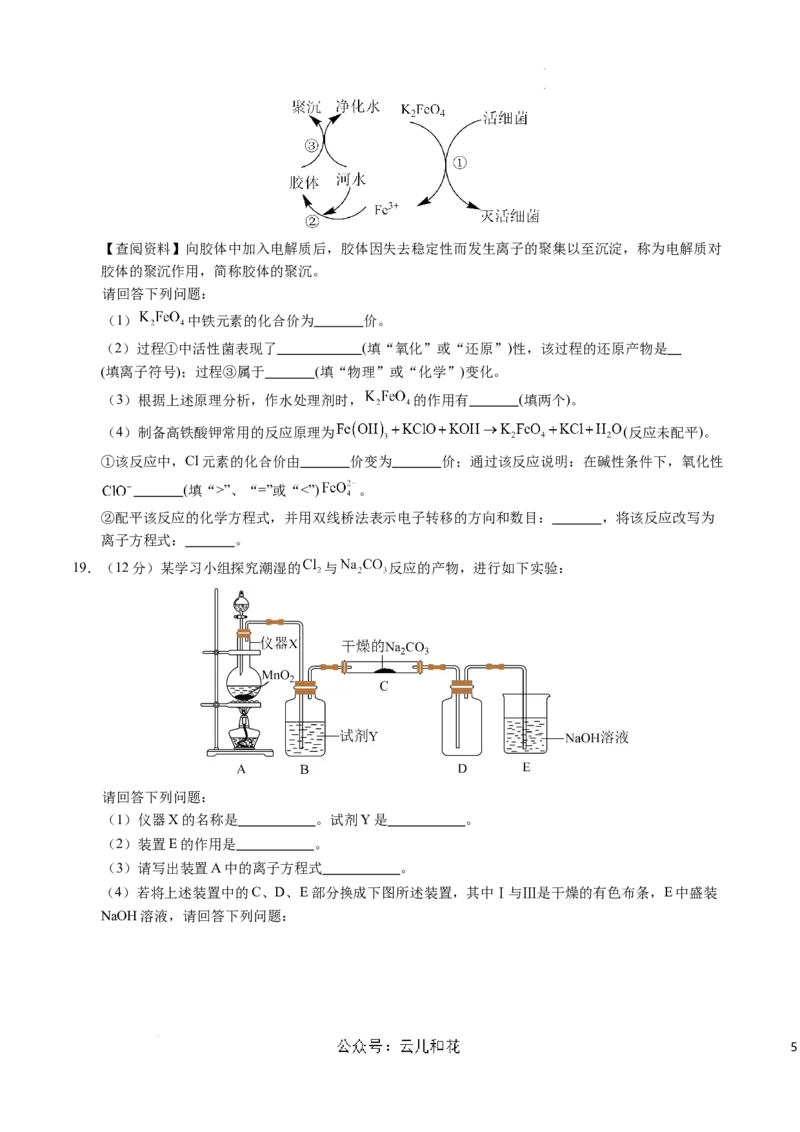
19.(12分)某学习小组探究潮湿的 与 反应的产物,进行如下实验:
请回答下列问题:
(1)仪器X的名称是 。试剂Y是 。
(2)装置E的作用是 。
(3)请写出装置A中的离子方程式 。
(4)若将上述装置中的C、D、E部分换成下图所述装置,其中Ⅰ与Ⅲ是干燥的有色布条,E中盛装
NaOH溶液,请回答下列问题:
5
学学科科网网((北北京京))股股份份有有限限公公司司①装置C的作用是验证氯气是否具有漂白性,则装置C中应装入的物质是 。
a、浓硫酸 b、生石灰 c、 固体 d、NaOH固体
②描述Ⅰ、Ⅲ处的现象 ,从物质性质角度说明Ⅰ、Ⅲ处现象不同的原因 。
20.(14分)常见的八种物质间存在如图转化关系,其中仅A、B、C为单质,其他物质均为化合物且由
X、Y、Z、W四种元素中的两种或三种组成。A的焰色试验火焰呈黄色,B具有助燃性,固态乙可用
于人工降雨,戊和丁的水溶液均呈碱性,甲的相对分子质量为78。常温下,各物质的状态如表所示:
物
A B C 甲 乙 丙 丁 戊
质
状 固态 气态 气态 固态 气态 液态 固态 固态
态
请回答下列问题:
(1)图中属于酸性氧化物的是 (填化学式,下同),属于盐的是 。
(2)反应①~⑤中,不属于氧化还原反应的是 (填标号,下同);属于置换反应的是 ,
反应⑤的离子方程式为 。
(3)向丁的饱和溶液中通入足量气体乙,可观察到的现象为 ,发生反应的化学方程
式为 。
(4)当固体甲(足量)将由44g乙和18g丙蒸气组成的混合气体完全吸收时,反应后固体质量增加了
g。
6
学学科科网网((北北京京))股股份份有有限限公公司司