文档内容
海淀区 2024—2025 学年第二学期期末练习
高三化学
2025. 05
本试卷共8页,100分。考试时长90分钟。考生务必将答案答在答题卡上,在试卷上作答无
效。考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 O 16 S 32 Ca 40 Se 79 In 115
第一部分
本部分共 14题,每题3分,共42分。在下列各题的四个选项中,选出最符合题目要求的一项。
1. SiO 气凝胶材料疏松多孔,具有三维网状结构,可用于航天器、新能源汽车电池的隔热和阻
2
燃。SiO 气凝胶的结构示意图如下。
2
下列说法不正确的是
4 4 4 O
A.SiO 晶体属于共价晶体 O O Si
2 Si O O
O O
化 B.SiO 晶体具有较高的硬度和熔点 O Si 表示链延长
2 Si O O
C.SiO 气凝胶材料的密度大于SiO 晶体的 O O Si
2 2 Si O
O O
D.两种物质中均有Si、O原子间的σ键
2.下列化学用语或图示表达正确的是
A.1s电子云图:
B.HCl的电子式:H+[ Cl ]-
C.丙烯的结构简式:CH
3 6
3d 4s
D.基态Fe原子的价层电子轨道表示式:
3.铅蓄电池的结构示意图如右图。下列关于铅蓄电池的说法正确的是
A.放电时,PbO 作负极
2
B.放电时,H+向负极方向移动
C.充电时,铅蓄电池负极连接电源正极
Pb HSO 溶液
D.充电时,阳极的电极反应为PbSO - 2e- + 2HO = PbO + 4H+ + SO2- PbO 2 2 4
4 2 2 4
4.下列依据相关数据作出的推断中,正确的是
A.依据离子半径:Br-<I-,可推断结构相似的晶体的熔点:NaBr>NaI
B.依据元素的电负性:C<N<F,可推断分子极性:CF >NF
4 3
C.依据分子中羟基的数目,可推断HO(CH)CHO在水中的溶解度大于葡萄糖的
25
D.依据元素的第一电离能:Mg>Al,可推断单质的还原性:Mg>Al
高三年级(化学) 第1页(共8页)5.为研究浓硝酸与Cu的反应,进行右图所示实验。下列说法不正确的是
4 4 4
A.滴入浓硝酸后,无需加热即可反应
B.反应开始后,试管中产生红棕色气体,说明浓硝酸具有氧化性
C.反应消耗0.05 mol Cu时,转移电子数约为6.02×1022
D.若将铜片换成铝片,无明显现象,说明还原性:Al<Cu
6.下列方程式与所给事实不相符的是
4 4 4
A.室温下测得0.1 mol·L-1氨水的pH约为11:NH·HO NH+ + OH-
3 2 4
B.潜艇中用NaO 吸收CO 并供氧:2NaO + 2CO = 2NaCO + O
2 2 2 2 2 2 2 3 2
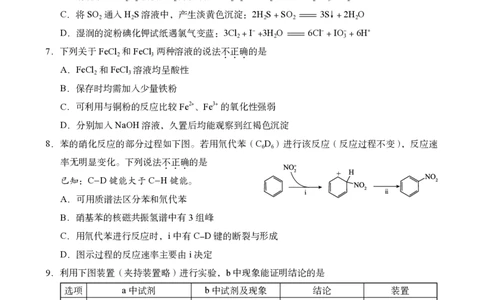
C.将SO 通入HS溶液中,产生淡黄色沉淀:2HS + SO = 3S↓+ 2HO
2 2 2 2 2
D.湿润的淀粉碘化钾试纸遇氯气变蓝:3Cl + I- +3HO = 6Cl- + IO- + 6H+
2 2 3
7.下列关于FeCl 和FeCl 两种溶液的说法不正确的是
2 3
4 4 4
A.FeCl 和FeCl 溶液均呈酸性
2 3
B.保存时均需加入少量铁粉
C.可利用与铜粉的反应比较Fe2+、Fe3+的氧化性强弱
D.分别加入NaOH溶液,久置后均能观察到红褐色沉淀
8.苯的硝化反应的部分过程如下图。若用氘代苯(CD)进行该反应(反应过程不变),反应速
6 6
率无明显变化。下列说法不正确的是
4 4 4
已知:C-D键能大于C-H键能。
A.可用质谱法区分苯和氘代苯
B.硝基苯的核磁共振氢谱中有3组峰
C.用氘代苯进行反应时,ⅰ中有C-D键的断裂与形成
D.图示过程的反应速率主要由ⅰ决定
9.利用下图装置(夹持装置略)进行实验,b中现象能证明结论的是
选项 a中试剂 b中试剂及现象 结论 装置
电石(含CaS杂质,易 酸性 KMnO 溶液
A 4 a中反应生成CH
水解)与饱和食盐水 褪色 2 2
苯、液溴和铁粉的混 AgNO 溶液中出现
B 3 a中反应生成HBr
合物 淡黄色沉淀
苯酚钠溶液中出现 HCO 的酸性强于
C NaCO 固体与稀硫酸 2 3
2 3 浑浊 苯酚的
滴有酚酞的NaOH溶
D NaClO固体与浓盐酸 氯气具有漂白性
液褪色
高三年级(化学) 第2页(共8页)10.为研究水垢中CaSO 的去除,称量0.5 g CaSO·2HO于烧
4 4 2
杯中,加入100 mL蒸馏水,持续搅拌并用传感器监测溶液中
c(Ca2+)的变化。18 s时滴入3滴饱和NaCO 溶液,55 s时继续
2 3
滴加饱和NaCO 溶液(忽略对溶液体积的影响),数据如右图。
2 3
下列说法正确的是
A.BC段c(Ca2+)下降,是因为平衡CaSO(s) Ca2+(aq) +SO2-(aq)
4 4
逆向移动
B.由CD段推测,加入的CaSO·2HO未完全溶解
4 2
C.不同时刻溶液中c(SO2-)大小排序:D>B>C
4
D.A到F的过程中,消耗n(CO2-)约为8.5×10-4 mol
3
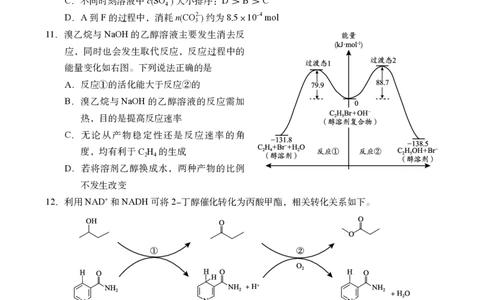
11.溴乙烷与NaOH的乙醇溶液主要发生消去反
应,同时也会发生取代反应,反应过程中的
能量变化如右图。下列说法正确的是
A.反应①的活化能大于反应②的
B.溴乙烷与NaOH的乙醇溶液的反应需加
热,目的是提高反应速率
C.无论从产物稳定性还是反应速率的角
度,均有利于CH 的生成
2 4
D.若将溶剂乙醇换成水,两种产物的比例
不发生改变
12.利用NAD+和NADH可将2-丁醇催化转化为丙酸甲酯,相关转化关系如下。
下列说法不正确的是
4 4 4
A.①中,1 mol 2-丁醇转化为2-丁酮,转移2 mol电子
B.①中,NAD+转化为NADH,部分碳原子的杂化方式改变
C.②中,2-丁酮和NADH均发生氧化反应
D.每合成1 mol丙酸甲酯,理论上须投入1 mol NAD+
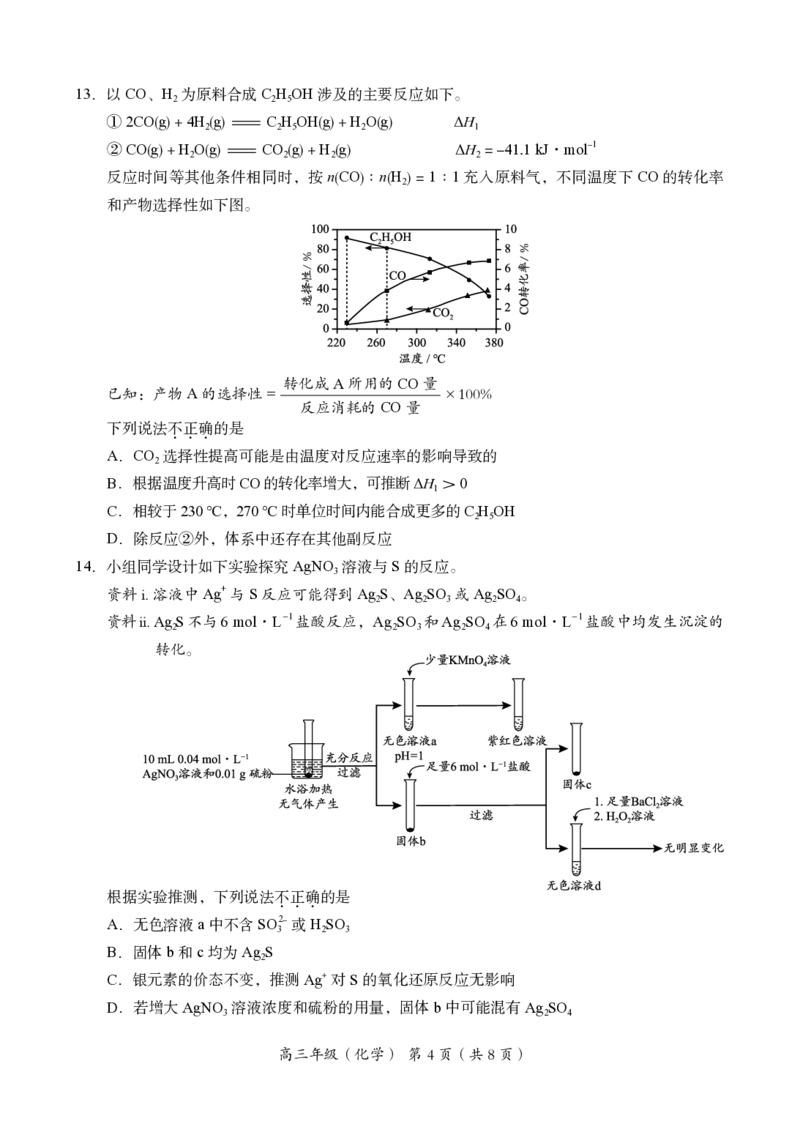
高三年级(化学) 第3页(共8页)13.以CO、H 为原料合成CHOH涉及的主要反应如下。
2 2 5
① 2CO(g) + 4H(g) = CHOH(g) + HO(g) ΔH
2 2 5 2 1
② CO(g) + HO(g) = CO(g) + H(g) ΔH = -41.1 kJ·mol-1
2 2 2 2
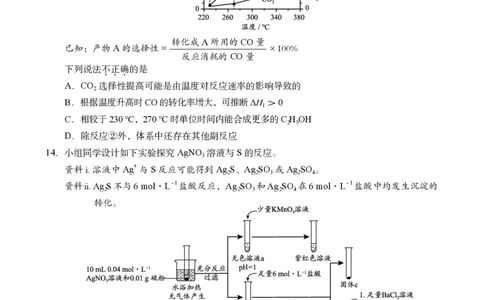
反应时间等其他条件相同时,按n(CO)∶n(H) = 1∶1充入原料气,不同温度下CO的转化率
2
和产物选择性如下图。
转化成A所用的CO量
已知:产物A的选择性= ×100%
反应消耗的CO量
下列说法不正确的是
4 4 4
A.CO 选择性提高可能是由温度对反应速率的影响导致的
2
B.根据温度升高时CO的转化率增大,可推断ΔH >0
1
C.相较于230 ℃,270 ℃时单位时间内能合成更多的CHOH
2 5
D.除反应②外,体系中还存在其他副反应
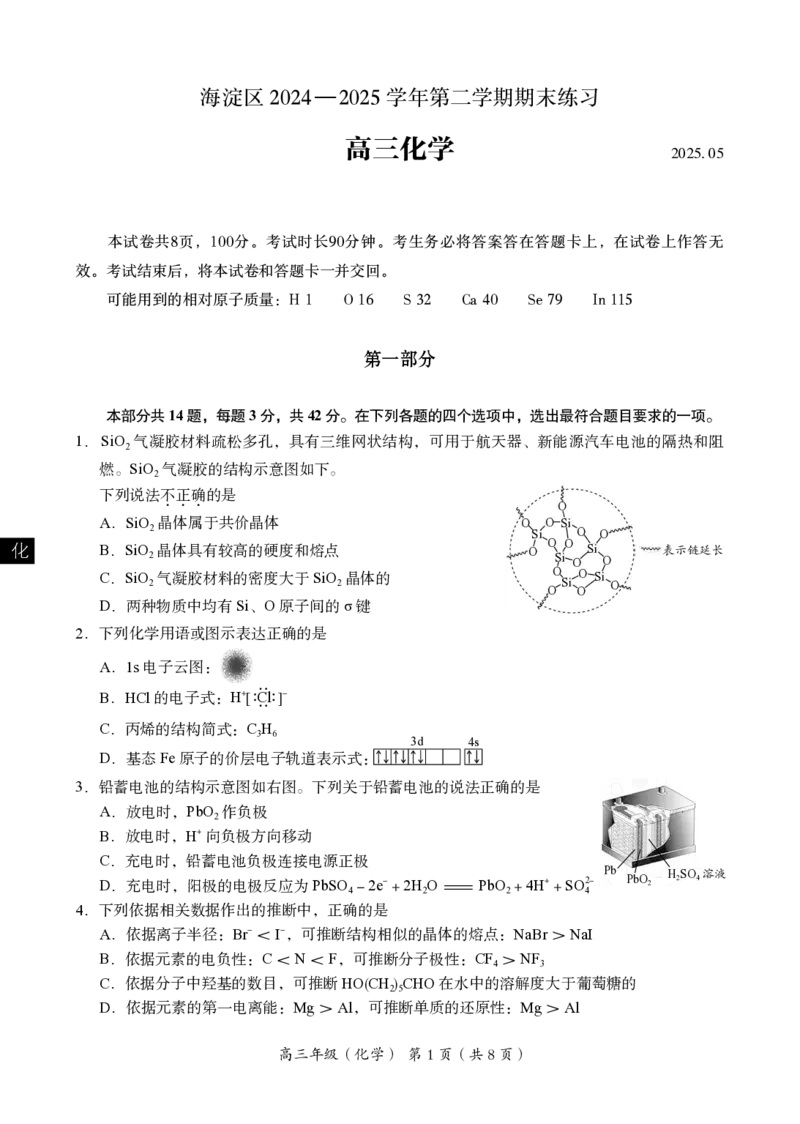
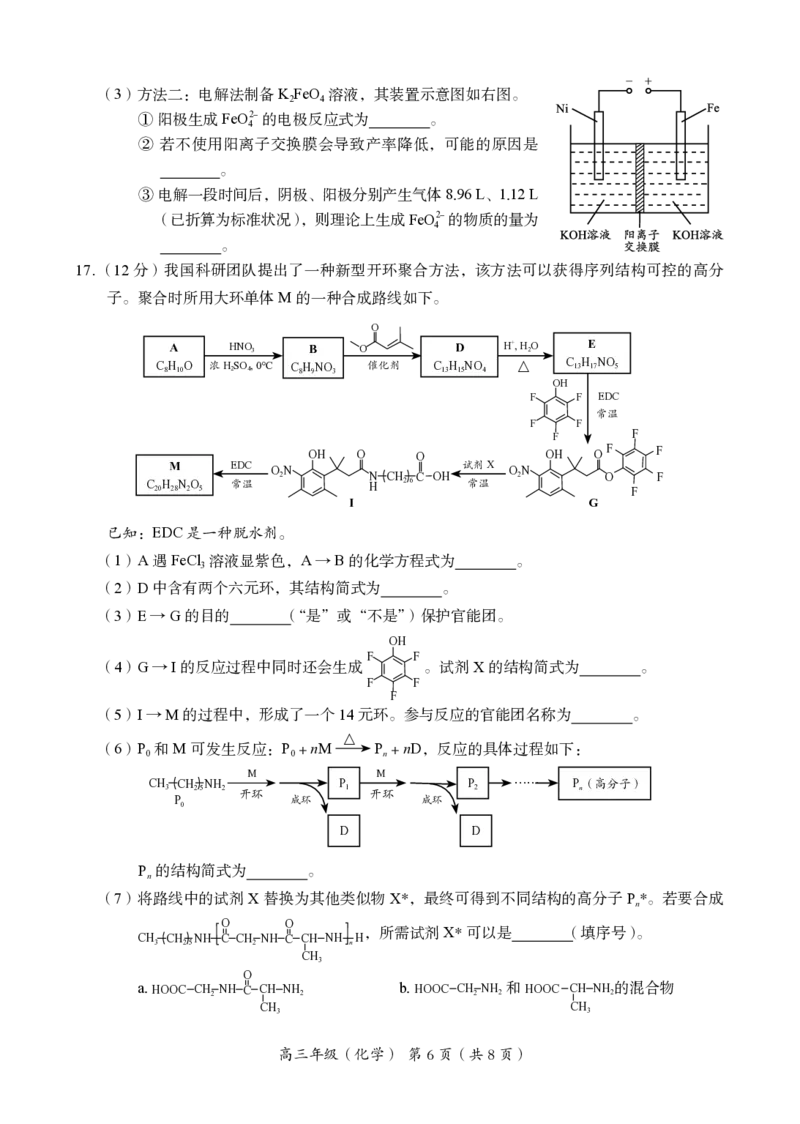
14.小组同学设计如下实验探究AgNO 溶液与S的反应。
3
资料i. 溶液中Ag+与S反应可能得到AgS、AgSO 或AgSO。
2 2 3 2 4
资料ii. AgS不与6 mol·L-1盐酸反应,Ag SO 和Ag SO 在6 mol·L-1盐酸中均发生沉淀的
2 2 3 2 4
转化。
根据实验推测,下列说法不正确的是
4 4 4
A.无色溶液a中不含SO2-或HSO
3 2 3
B.固体b和c均为AgS
2
C.银元素的价态不变,推测Ag+对S的氧化还原反应无影响
D.若增大AgNO 溶液浓度和硫粉的用量,固体b中可能混有AgSO
3 2 4
高三年级(化学) 第4页(共8页)第二部分
本部分共5题,共58分。
15.(10分)我国科学家在中国空间站首次实现了铟硒半导体的微重力培养,铟(In)和硒(Se)
的单质是制备铟硒半导体的重要原料。
(1)主族元素In原子序数为49,其位于元素周期表的 区。
(2)粗硒中主要含碲(Te)单质等杂质。硒与碲同主族,可用气态氢化物热解法制备少量的
高纯硒,流程如下图。
H
粗硒 2 硒化氢气体 高纯硒
加热 高温
结合元素周期律解释该法能分离硒和碲的原因: 。
(3)氧化挥发法是制备高纯硒的另一种方法。粗硒经高温氧化后产生SeO 蒸气,SeO 冷凝
2 2
后溶于水形成HSeO 溶液,除杂后向溶液中通入SO 可获得高纯硒。
2 3 2
① 已知HSeO 分子中含两个羟基,HSeO 中Se的杂化方式为 。
2 3 2 3
② 向HSeO 溶液中通入SO 时,发生反应的化学方程式为
2 3 2
。
(4)一种铟硒半导体晶体的晶胞如右图,晶胞底面边长为a pm,
高为 c pm。
① 该晶体的化学式为 。
② 阿伏加德罗常数为N ,该晶体的密度为 g·cm-3。
A
( 已知:1 pm = 10-10 cm)
16.(12分)高铁酸钾(KFeO)是一种高效净水剂,可采用不同的方法制备。
2 4
(1)KFeO 可以去除水中HS、NH 等物质,同时生成红褐色胶体。净水过程中利用的KFeO
2 4 2 3 2 4
的性质是_______。
(2)方法一:化学氧化法制备KFeO 固体。
2 4
已知:FeO2-仅在强碱性溶液中稳定存在。
4
① 制粗品:向饱和 KOH 和 KClO 混合溶液中滴加 Fe(NO ) 溶液并不断搅拌,析出
3 3
沉淀,过滤所得固体为 KFeO 粗品。生成KFeO 反应的离子方程式为 。
2 4 2 4
② 重结晶:将KFeO 粗品溶于稀KOH溶液,过滤,随后向滤液中加入饱和KOH溶液,
2 4
冰水浴冷却,过滤、洗涤、干燥后得到KFeO。
2 4
ⅰ.重结晶时,第一次过滤后滤渣的主要成分是 。
ⅱ.向滤液中加入饱和KOH溶液的目的是 。
高三年级(化学) 第5页(共8页)(3)方法二:电解法制备KFeO 溶液,其装置示意图如右图。
2 4
① 阳极生成FeO2-的电极反应式为 。
4
② 若不使用阳离子交换膜会导致产率降低,可能的原因是
。
③ 电解一段时间后,阴极、阳极分别产生气体8.96 L、1.12 L
( 已折算为标准状况),则理论上生成FeO2-的物质的量为
4
。
17.(12分)我国科研团队提出了一种新型开环聚合方法,该方法可以获得序列结构可控的高分
子。聚合时所用大环单体M的一种合成路线如下。
O
A HNO 3 B O D H+, H 2 O E
C 8 H 10 O 浓H 2 SO 4 , 0℃ C 8 H 9 NO 3 催化剂 C 13 H 15 NO 4 △ C 13 H 17 NO 5
OH
F F EDC
常温
F F
F F
OH O O OH O F F
M EDC ON 试剂X ON
2 N CH C OH 2 O F
C 20 H 28 N 2 O 5 常温 H 2 6 常温 F
I G
已知:EDC是一种脱水剂。
(1)A遇FeCl 溶液显紫色,A→B的化学方程式为 。
3
(2)D中含有两个六元环,其结构简式为 。
(3)E→G的目的 (“是”或“不是”)保护官能团。
OH
F F
(4)G→I的反应过程中同时还会生成 。试剂X的结构简式为 。
F F
F
(5)I→M的过程中,形成了一个14元环。参与反应的官能团名称为 。
△
(6)P 和M可发生反应:P + nM P + nD,反应的具体过程如下:
0 0 n
M M
CH CH NH P P …… P(高分子)
3 25 2 开环 1 开环 2 n
P 成环 成环
0
D D
P 的结构简式为 。
n
(7)将路线中的试剂X替换为其他类似物X*,最终可得到不同结构的高分子P*。若要合成
n
O O
,所需试剂X*可以是 (填序号)。
CH CH NH C CH NH C CH NH H
3 25 2 n
CH
3
O
a.HOOC CH 2 NH C CH NH 2 b.HOOC CH 2 NH 2 和 HOOC CH NH 2 的混合物
CH CH
3 3
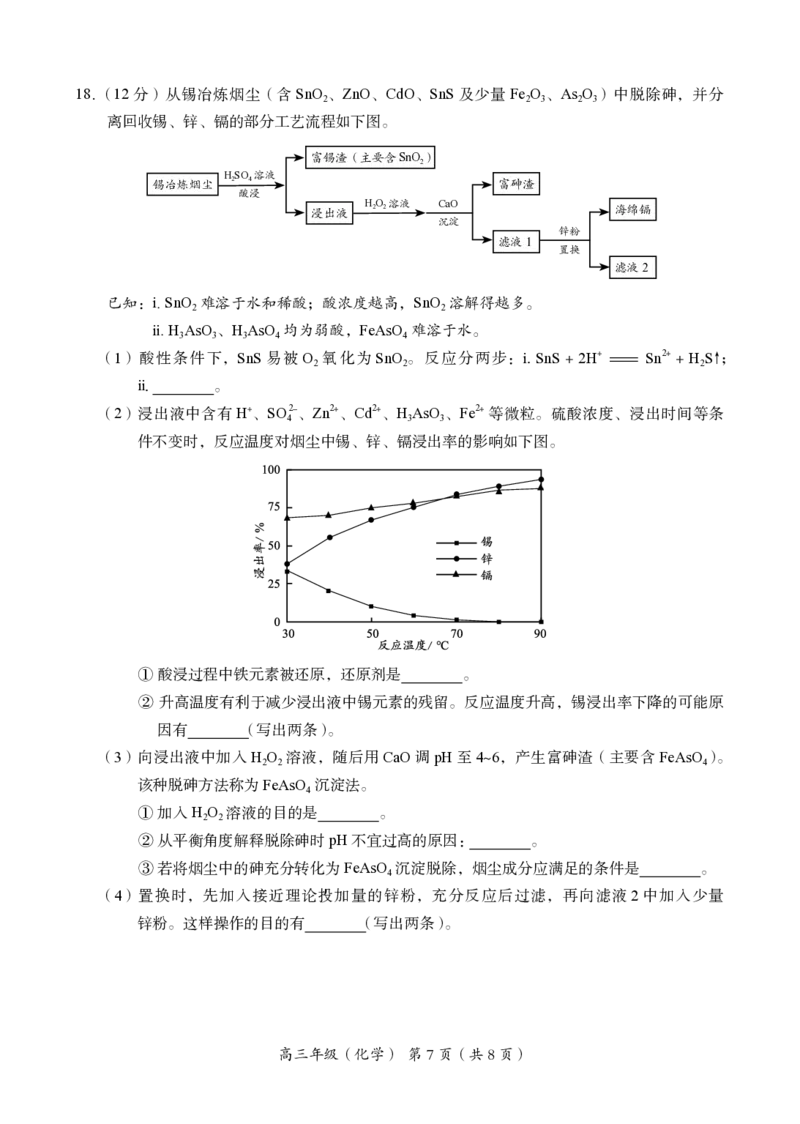
高三年级(化学) 第6页(共8页)18.(12分)从锡冶炼烟尘(含SnO、ZnO、CdO、SnS及少量FeO、AsO)中脱除砷,并分
2 2 3 2 3
离回收锡、锌、镉的部分工艺流程如下图。
富锡渣(主要含SnO)
2
HSO 溶液
锡冶炼烟尘 2 4 富砷渣
酸浸
HO 溶液 CaO
浸出液 2 2 海绵镉
沉淀
锌粉
滤液1
置换
滤液2
已知:ⅰ. SnO 难溶于水和稀酸;酸浓度越高,SnO 溶解得越多。
2 2
ⅱ. HAsO、HAsO 均为弱酸,FeAsO 难溶于水。
3 3 3 4 4
(1)酸性条件下,SnS易被O 氧化为SnO。反应分两步:ⅰ. SnS + 2H+ = Sn2+ + HS↑;
2 2 2
ⅱ. 。
(2)浸出液中含有H+、SO2-、Zn2+、Cd2+、HAsO、Fe2+等微粒。硫酸浓度、浸出时间等条
4 3 3
件不变时,反应温度对烟尘中锡、锌、镉浸出率的影响如下图。
① 酸浸过程中铁元素被还原,还原剂是 。
② 升高温度有利于减少浸出液中锡元素的残留。反应温度升高,锡浸出率下降的可能原
因有 (写出两条)。
(3)向浸出液中加入HO 溶液,随后用CaO调pH至4~6,产生富砷渣(主要含FeAsO)。
2 2 4
该种脱砷方法称为FeAsO 沉淀法。
4
① 加入HO 溶液的目的是 。
2 2
② 从平衡角度解释脱除砷时pH不宜过高的原因: 。
③ 若将烟尘中的砷充分转化为FeAsO 沉淀脱除,烟尘成分应满足的条件是 。
4
(4)置换时,先加入接近理论投加量的锌粉,充分反应后过滤,再向滤液2中加入少量
锌粉。这样操作的目的有 (写出两条)。
高三年级(化学) 第7页(共8页)19.(12分)小组同学用实验1所示方法制备铜配合物,并探究其组成。
【实验1】
(1)ⅰ中生成了Cu(OH) 沉淀,发生反应的离子方程式为 。
2
(2)小组同学推测ⅱ中发生反应:Cu(OH) + 4NH·HO [Cu(NH)]2+ + 4HO + 2OH-,
2 3 2 34 2
蓝色针状晶体可能含[Cu(NH)]SO 或[Cu(NH)](OH)。
34 4 34 2
① 实验证明蓝色针状晶体中含SO2-,补全实验操作及现象:将洗净后的蓝色针状晶体置
4
于试管中,用蒸馏水溶解, 。
② 将洗净后的蓝色针状晶体溶于蒸馏水,测得溶液呈碱性。该现象不能说明蓝色针状
晶体中含OH-,原因是 。
③ 甲同学查阅资料发现,加热时配合物中作配体的NH 会逸出。他据此设计实验2检验
3
蓝色针状晶体的组成。
【 实验2】
实验装置 现象
烧杯中的溶液变红,试管底部产生大
量红色固体
a.甲同学推测,若蓝色针状晶体中含[Cu(NH)](OH),充分加热后预期在试管底部观
34 2
察到黑色固体。这样推测的理由是 。
b. 实验后试管底部未产生预期的黑色固体,甲同学推断蓝色针状晶体中不含
[Cu(NH)](OH)。小组同学认为甲的推断不严谨,从物质性质角度说明理由: 。
34 2
(3)乙同学通过实验发现,按实验1的方案制备铜配合物时,若仅将ⅰ中的氨水换成适量
NaOH溶液,只有少量蓝色沉淀溶解。实验1中蓝色沉淀能全部溶解的原因是 。
(4)结合乙的实验,小组同学推测蓝色针状晶体中几乎不含[Cu(NH)](OH),结合离子方程式
34 2
说明理由: 。
高三年级(化学) 第8页(共8页)海淀区高三年级第二学期期末练习
化学试卷参考答案
第一部分共14题,每小题3分,共42分。
题号 1 2 3 4 5 6 7
答案 C A D A D D B
题号 8 9 10 11 12 13 14
答案 C C B B D B C
第二部分共5题,共58分。
15. (1)p(1分)
(2)Se与Te同主族,非金属性Se>Te,Se更易与H 生成气态氢化物,从而与Te
2
分离(2分)
(3)① sp3(1分)
② H O + H SeO +2SO === Se + 2H SO (2分)
2 2 3 2 2 4
(4)① InSe
2
(2分) ② 2×
𝑁
(
A×
1
a
1
2
5
𝑐
+
×
7
1
9
0
×
−3
2
0
) (2分)
16. (1)氧化性(1分)
(2)① 4K+ + 2Fe3+ + 10OH- + 3ClO- === 2K FeO ↓ + 3Cl- + 5H O(2分)
2 4 2
② ⅰ.Fe(OH) (1分)
3
ⅱ.增大K+浓度,促进K FeO 析出;维持K FeO 的稳定(2分)
2 4 2 4
(3)① Fe - 6e- + 8OH-=== FeO 2- + 4H O(2分)
4 2
② 阳极产生的FeO 2-可能扩散至阴极被还原,造成损失(或OH-迁移至阳极放电,
4
发生副反应)(2分)
③ 0.1 mol(2分)
17. (1) 浓硫酸 (2分)
0℃
(2) (2分)
(3)不是 (1分)
(4) (2分)
(5)羧基、羟基(2分)
(6) (2分)
(7)a(1分)18. (1)2Sn2+ + O + 2H O == 2SnO ↓ + 4H+ (2分)
2 2 2
(2)① H S(SnS或其他合理答案)(1分)
2
② 温度升高,Sn2+被氧化为SnO 的速率加快;ZnO、CdO与酸反应的速率加快,
2
使相同时间内剩余酸浓度减小,使SnO 的溶解度降低(2分)
2
(3)① 将Fe2+氧化为Fe3+,将H AsO 氧化为H AsO ,并在调pH后与Fe3+形成FeAsO
3 3 3 4 4
沉淀(2分)
② pH过高会产生Fe(OH) 沉淀,c(Fe3+)降低,FeAsO (s) Fe3+(aq) + AsO 3-(aq)
3 4 4
正向移动,As去除率下降(2分)
③ n(Fe O )>n(As O ) (1分)
2 3 2 3
(4)避免锌粉过量,影响海绵镉的纯度;除去滤液中的Cd2+,避免污染或减少ZnSO
4
滤液中的杂质。(2分)
19. (1)Cu2+ + 2NH ·H O === Cu(OH) ↓ + 2NH +(2分)
3 2 2 4
(2)①加入(盐酸酸化的)BaCl 溶液,有白色沉淀生成(1分)
2
②[Cu(NH ) ]2+中的 NH 进入溶液并形成 NH ·H O,电离出 OH-使溶液呈碱性
3 4 3 3 2
(1分)
③a. 加热[Cu(NH ) ](OH) 使 NH 逸出后产生 Cu(OH) ,Cu(OH) 受热继续分解为
3 4 2 3 2 2
CuO(2分)
b. NH 具有还原性,即使[Cu(NH ) ](OH) 分解生成CuO也可能被还原为Cu或
3 3 4 2
Cu O(2分)
2
(3)用氨水制备Cu(OH) 时,溶液c(NH +)较高,可与OH-反应并产生NH ·H O,均
2 4 3 2
可促进反应Cu(OH) + 4NH ·H O [Cu(NH ) ]2+ + 4HO + 2OH-的发生。(2分)
2 3 2 3 4 2
(4)ⅰ中反应Cu2+ + 2NH ·H O === Cu(OH) ↓+ 2NH +产生的NH +正好能与ⅱ中
3 2 2 4 4
Cu(OH) + 4NH ·H O [Cu(NH ) ]2+ + 4HO + 2OH-产生的OH-完全反应,溶液
2 3 2 3 4 2
中c(OH-)很低。(结合总反应作答,也可给分)(2分)