文档内容
湘 豫 名 校 联 考
— 学年高三春季学期第三次模拟考试
2024 2025
化学参考答案
题号
1 2 3 4 5 6 7 8 9 10 11 12 13 14
答案
D A C C B C D C D B A D C A
一、选择题:本题共 小题,每小题 分,共 分。在每小题给出的四个选项中,只
14 3 42
有一项是符合题目要求的。
【解析】蛋白质是由 、 、、 等元素组成的烃的衍生物,而不属于烃类, 项错误;蛋白质遇重金属盐
1.D CH O N A
(如 )会发生变性,不是盐析, 项错误;蛋白质转化为氨基酸是水解反应,不是分解, 项错误;实验室一
2+
Cu B C
般通过测定有机样品中氮元素的质量分数计算其中蛋白质的含量, 项正确。故选 。
D D
【解析】乙烯分子中的 键电子云: , 项正确;乙烯的结构简式为 , 项错误;水分
2.A π A CH2 CH2 B
子的 模型名称为四面体形,而非正四面体形, 项错误;乙醇分子中的官能团为羟基,其电子式为
VSEPR C
, 项错误。故选 。
D A
【解析】高锰酸钾溶液不能用盐酸酸化, 项错误;加入稀盐酸后产生无色气体,该气体能使澄清石灰水变
3.C A
浑浊,该气体可能是 ,也可能是 ,故原无色晶体可能是碳酸盐、碳酸氢盐,也可能是亚硫酸盐或亚硫
CO2 SO2
酸氢盐, 项错误;无色溶液中加入银氨溶液后水浴加热,试管内壁有光亮的银镜产生,这说明无色溶液 中
B C
含有还原性物质, 项正确;用湿润的淀粉 试纸靠近红棕色气体,试纸变蓝,说明该气体具有强氧化性,
C KI
可能是 ,也可能是溴蒸气, 项错误。故选 。
NO2 D C
【解析】油渍属于油脂,可在热的纯碱溶液中水解生成易溶于水的甘油和高级脂肪酸钠盐, 项正确;胃酸的
4.C A
主要成分是盐酸,导致胃酸患者出现症状的主要原因是胃酸过多,常用含 或 ( )的药物治疗,
NaHCO3 AlOH3 B
项正确; 具有漂白性,能使品红溶液褪色,但不能使紫色石蕊溶液褪色, 项错误;苯酚与甲醛在不同条件下
SO2 C
既可能生成线型高分子,也可能生成网状高分子,故既可能有热塑性,也可能有热固性, 项正确。故选 。
D C
【解析】 分子中含有 个手性碳原子,但由于碳碳双键有一端连的是两个氢原子,故不具有顺反异构,
5.B X 3 A
项错误; 既有醛基,也有碳碳双键,故能发生取代反应、加成反应、氧化反应和加聚反应, 项正确; 的分
X B H
子式为
C10 nH16 n +2O2 n +1
,
C
项错误;
1molH
完全水解最多消耗(n
-1
)
molH2O
,
D
项错误。故选
B
。
高温
【解析】粗硅冶炼时主要反应的化学方程式为 , 项错误;表示物质的燃烧热时,
6.C SiO2+2CSi+2CO↑ A
生成的是 (), 项错误; 项是锂电池负极反应式的一种书写形式, 项正确;浓氨水过量时,硫酸铜与
H2Ol B C C
其反应生成[ ( )] , 项错误。故选 。
2+
CuNH3 4 D C
【解析】本题实验装置为溶液的蒸发装置,常用于溶液的蒸发、浓缩、结晶等。分离 和碘的混合物,
7.D NaCl
用到的方法是升华,而该装置不能收集碘蒸气, 项错误;由于 ( ) ,将
A FeCl3+3H2OFeOH 3+3HCl FeCl3
溶液蒸干过程中,促进平衡向右移动,且 易挥发,最终无法得到 晶体, 项错误;加热固体的装置应
HCl FeCl3 B
使用坩埚, 项错误;将 溶液蒸发浓缩、冷却结晶、过滤即得到胆矾, 项正确。故选 。
C CuSO4 D D
化学参考答案 第 页 共 页
1 ( 6 )
{#{QQABJQis4ggYgESACJ4KQw3UCQkQsJAiJUoERRCRKAwKAZFABKA=}#}【解析】基态 原子中的电子只有一种自旋取向,则可知 为 元素, 的最高正化合价与最低负化合
8.C X X H Y
价之和为 , 位于第 族,为 或 , 的不同类型能级上的电子数相同,根据构造原理,其电子排布式
0Y ⅣA C SiM
为 或 ,可能是 或 ,结合离子液体的化学式 , 只可能为 ,又根据
2 2 4 2 2 6 2
1s2s2p 1s2s2p3s O Mg Y2X5ZX3ZM3 M O
、、、 为原子序数依次增大的短周期主族元素,则 为 , 为 。形成离子液体的物质化学式为
XYZ M Y CZ N
。四种元素的原子半径: , 项错误;四种元素的基态原子第一电离能:
C2H5NH3NO3 C>N>O>H A N>O>
, 项错误; 与 、 、 均能形成多种化合物, 项正确;离子液体: ,属于离子化合物,
C>HB H CNO C C2H5NH3NO3
但其熔点低,常温下呈液态, 项错误。故选 。
D C
放电
【解析】由银锌蓄电池工作原理 ( )可知,放电时 和 化合价
9.D Ag2O2+2Zn+2H2O充电2Ag+2ZnOH 2 Ag O
均降低,均被还原, 项错误;反应过程中消耗了水,故电解质溶液的碱性会增强, 项错误;由题可知,该蓄电
A B
池电解质溶液为碱性,故充电时阳极的电极反应为 , 项错误;银锌蓄电
- -
2Ag-4e +4OH Ag2O2+2H2OC
池的电解质溶液可能是 的水溶液, 项正确。故选 。
KOH D D
【解析】由工艺流程可知,焙烧时,除了 被氧化生成 外, 也被氧化成 ,故生成
10.B S SO2 Mo MoO3 1molSO2
时,转移的电子数大于 N , 项错误;“碱浸”时,发生反应的离子方程式为 2- 2- ,
6 A A MoO3+CO3 MoO4 +CO2↑
项正确;“重结晶”的目的是得到更纯的 · ,在重结晶过程中会有晶体的损失,产量会更低
B Na2MoO4 2H2O
些, 项错误;该工艺中排放出来的 会形成酸雨,但 不会产生酸雨, 项错误。故选 。
C SO2 CO2 D B
【解析】 中 的化合价为 ,图示中 只有一个氧空位,则晶胞的化学式为 , 的平
11.A CeO2 Ce +4 CeO2- x Ce4O7 Ce
均价态为 ,则通入 后 被还原, 项错误;由题图可知, 中 的配位数为 , 项正确;由
+3.5 CH4 CeO2 A CeO2 O 4B
A
项分析可知,
CeO2- x
中
Ce
的平均价态为
+3.5
,则n(
Ce 4+
)
∶
n(
Ce 3+
)
=1∶1
,
C
项正确;若
CeO2
中
Ce
、
O
最
短距离为a ,则 晶胞的边长为43a ,则其密度为1293 ·
-3
, 项正确。故选 。
cm CeO2 cm a3N g cm D A
3 4 A
【解析】 的基态电子排布式为[ ] , 项错误;根据元素周期律,同主族元素从上至下,非
10 2 3
12.D As Ar3d4s4p A
金属性依次减弱,其最高价含氧酸的酸性依次减弱,故K ( ) K ( ), 项错误;
a1 H3PO4 > a1 H3AsO4 B NaH2AsO4
为强碱弱酸盐,但由题图可知, 的电离程度大于水解程度,溶液显酸性, 项错误;当溶液
-
H2AsO4 C pH=7
时,根据水溶液的电荷守恒有c(
+
)c(
+
) c(
3-
) c(
2-
)c(
-
)c(
-
),此
Na + H =3 AsO4 +2 HAsO4 + H2AsO4 + OH
时c(
+
)c(
-
),c(
-
)c(
2-
),所以c(
+
) [c(
3-
) c(
2-
)], 项正确。
H = OH H2AsO4 = HAsO4 Na =3 AsO4 + HAsO4 D
故选 。
D
【解析】由 H 、H 可知,题图中曲线 表示 的选择性,表示 的选择性,则曲线
13.C Δ 1<0Δ 2>0 a CO c CH3OH b
表示 的转化率, 项错误;催化剂不影响平衡, 项错误; 时, 的转化率为 , 的选择性
CO2 A B 300℃ CO2 30% CO
为 , 的选择性为 ,由此可知,此时n( ) ,n( ) ,n( )
70% CH3OH 30% H2 =0.52mol CO2 =0.7mol CO =
,n( ) ,则反应 的平衡常数K , 项正确;随着温度的升高,以反应 为主,
0.21mol H2O =0.3mol Ⅱ ≈0.173C Ⅱ
容器内
n平
H2 逐渐增大, 项错误。故选 。
n平 D C
CO2
【解析】结合题意可知,本题是通过甲装置提供 ,乙装置提供 ,在丙装置中制得碳酸镧。由于
14.A CO2 NH3
极易溶于水,故进入丙装置时要防倒吸,故装置的连接顺序应为 , , 项正确;甲装置是启普发
NH3 a→cb→dA
生器,所用固体试剂须为不溶于水的块状固体,故在制 时不能用 代替 , 项错误;由于
CO2 NaHCO3 CaCO3 B
在较高的 条件下会生成碱式碳酸镧[ ( ) ],故应先通 ,再通 ,所以操作时应先打开
pH LaOH CO3 CO2 NH3
,一段时间后再打开 , 项错误;甲装置可用于实验室制备 ,但不能用于实验室制备 和 , 项
K1 K2 C H2 O2 Cl2 D
错误。故选 。
A
化学参考答案 第 页 共 页
2 ( 6 )
{#{QQABJQis4ggYgESACJ4KQw3UCQkQsJAiJUoERRCRKAwKAZFABKA=}#}二、非选择题:本题共 小题,共 分。
4 58
分 【答案】 分 分
15.(14 ) (1)ds(1 ) 74%(2 )
增大固体反应物接触面积 加快反应速率 提高转化率 分 关键词 加快反应速率
(2) , , (1 , “ ”)
高温
分 未写条件扣 分 写 加热 灼烧 均给分
(3)2CuFeS2+O2Cu2S+2FeS+SO2(2 , 1 , “ ”“ ” )
制硫酸等 分
(4) (1 )
(5)3 N A(2 分 , 写成 3×6.02×10 23、1.806×10 24 均给分 )
分 粗铜 分
(6)①N2O5(2 ) (1 )
分
②NO2-e - +NO3 - N2O5(2 )
【解析】() 位于元素周期表的 区。铜的晶胞为面心立方最密堆积,设其晶胞边长为a,铜原子的半径
1Cu ds
为R,则 R a,a R,晶胞立方体的体积为a3 ( R) 3 , 个 原子的体积为 4 R3 ,空间利
4 = 2 =22 = 22 4 Cu 4× π
3
4 R3
用率为4× 3 π 。
( R)
3
×100%≈74%
22
()矿石熔炼时要将其粉碎,其目的是增大固体反应物接触面积,加快反应速率,提高转化率。
2
高温
()由题意可知,黄铜矿熔炼时生成 和 ,故其化学方程式为 。
3 Cu2S FeS 2CuFeS2+O2Cu2S+2FeS+SO2
()烟气中的主要成分是 ,可用于制备硫酸等。
4 SO2
()根据反应的化学方程式可知,每生成 ,有 被氧化,根据化合价的变化可知转移的
5 1molCu 0.5molCu2S
电子数目为 N 。
3 A
()由装置图及题干信息可知,石墨 为负极,石墨 为正极,电解池中 为阳极, 为阴极,故 为 ,乙池
6 Ⅰ Ⅱ A B Y N2O5
中电极 的材料为粗铜。石墨电极 发生的电极反应式为 。
- -
A Ⅰ NO2-e +NO3N2O5
分 【答案】 分
16.(15 ) (1) (1 )
分
(2)2S2Cl2+2H2O4HCl+SO2↑+3S↓(2 )
圆底烧瓶 分
(3)① (1 )
分
②2MnO4 - +10Cl - +16H + 2Mn 2+ +5Cl2↑+8H2O(2 )
分
③c→d→a→b(2 )
除去过量的氯气 防止环境污染 防止空气中的水蒸气进入装置 与 反应 答出 点得 分 共 分
④ , ; A S2Cl2 ( 1 1 , 2 )
防止 过低 会转化为 防止 过高 会与滴入的 反应生成 均会干扰滴
(4)① pH ,CrO 2 4 - Cr2O 2 7 -; pH , Ag + AgOH,
定 答 把溶液中 完全转化为 沉淀 给 分 答出 点得 分 共 分
( “ SO2 BaSO3 ” 1 , 1 1 , 2 )
当滴入最后半滴 溶液时 白色沉淀中出现砖红色 且半分钟内砖红色未消失 分
② AgNO3 , , (1 )
分
③93.6%(2 )
【解析】() 所有原子符合最外层 电子稳定结构,根据 和 原子结构可知, 要形成 个共价键,
1S2Cl2 8 S Cl S 2 Cl
只需形成 个共价键,故其电子式为 。
1
()根据题干中信息, 溶于水生成 、 、,则其发生反应的化学方程式为
2 S2Cl2 HClSO2 S 2S2Cl2+2H2O
。
4HCl+SO2↑+3S↓
() 、、 装置中均用到的玻璃容器是圆底烧瓶。
3①ABC
装置是 与浓盐酸反应制 的装置,发生反应的离子方程式为
- - +
②C KMnO4 Cl2 2MnO4 +10Cl +16H
。
2+
2Mn +5Cl2↑+8H2O
化学参考答案 第 页 共 页
3 ( 6 )
{#{QQABJQis4ggYgESACJ4KQw3UCQkQsJAiJUoERRCRKAwKAZFABKA=}#}根据题意, 制备实验的顺序是:制备 除 干燥 制 收集 防水 尾气处理,
③ S2Cl2 Cl2→ HCl→ → S2Cl2→ S2Cl2→ →
故装置连接顺序是 ( )(按气流流出方向)。
e→j→k→h→i→c→d→a→b→f→g
该实验中碱石灰既要除去氯气,防止环境污染,也要防止空气中的水蒸气进入收集装置,使之与 反
④ S2Cl2
应。故其作用是除去过量的氯气,防止环境污染;防止空气中的水蒸气进入装置 与 反应。
A S2Cl2
() (所含杂质为 )纯度的测定。该题是应用沉淀滴定法进行测定,使用该方法时,首先将 和
4S2Cl2 SCl2 S2Cl2
中的 元素转化为 ,以 为指示剂,用标准的 溶液进行滴定的过程。在实验过程中,
- 2-
SCl2 Cl Cl CrO4 AgNO3
同时要保证溶液的 ,当溶液酸性较强时, 会转化为 ,使指示剂失效,当溶液碱性较强时,会
2- 2-
pH CrO4 Cr2O7
产生 干扰滴定结果。
AgOH
加入 ( )溶液调节 至 左右的作用是若 过低, 会转化为 , 过高,会与滴
2- 2-
① BaOH2 pH 9.0 pH CrO4 Cr2O7 pH
入的 反应生成 ,均会干扰滴定。
+
Ag AgOH
实验中,当 达到滴定终点后,再滴入 溶液,即生成砖红色的 沉淀,故滴定终点的判断
-
② Cl AgNO3 Ag2CrO4
依据是当滴入最后半滴 溶液时,产生砖红色沉淀,且半分钟内砖红色未消失。
AgNO3
及 均会与水反应产生 ,故该题计算时可利用 原子守恒进行计算。设原 产品中
-
③S2Cl2 SCl2 Cl Cl 1.35g
为x , 为y ,结合题意可得: x y ,x y -3 。最终得
S2Cl2 molSCl2 mol 135 +103 =1.352 +2 =0.1×20.40×10 ×10
到其纯度约为 。
93.6%
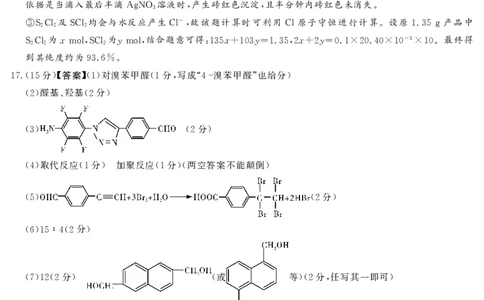
分 【答案】 对溴苯甲醛 分 写成 溴苯甲醛 也给分
17.(15 ) (1) (1 , “4 ” )
醛基 羟基 分
(2) 、 (2 )
分
(3) (2 )
取代反应 分 加聚反应 分 两空答案不能颠倒
(4) (1 ) (1 )( )
分
(5) (2 )
分
(6)15∶4(2 )
分 或 等 分 任写其一即可
(7)12(2 ) ( )(2 , )
【解析】由 题 干 信 息 及 已 知 信 息 可 推 出 该 流 程 中, 为 , 为 , 为
B C F
,为 ,为 。
G I
() 的结构简式为 ,其名称为对溴苯甲醛或 溴苯甲醛。
1C 4-
化学参考答案 第 页 共 页
4 ( 6 )
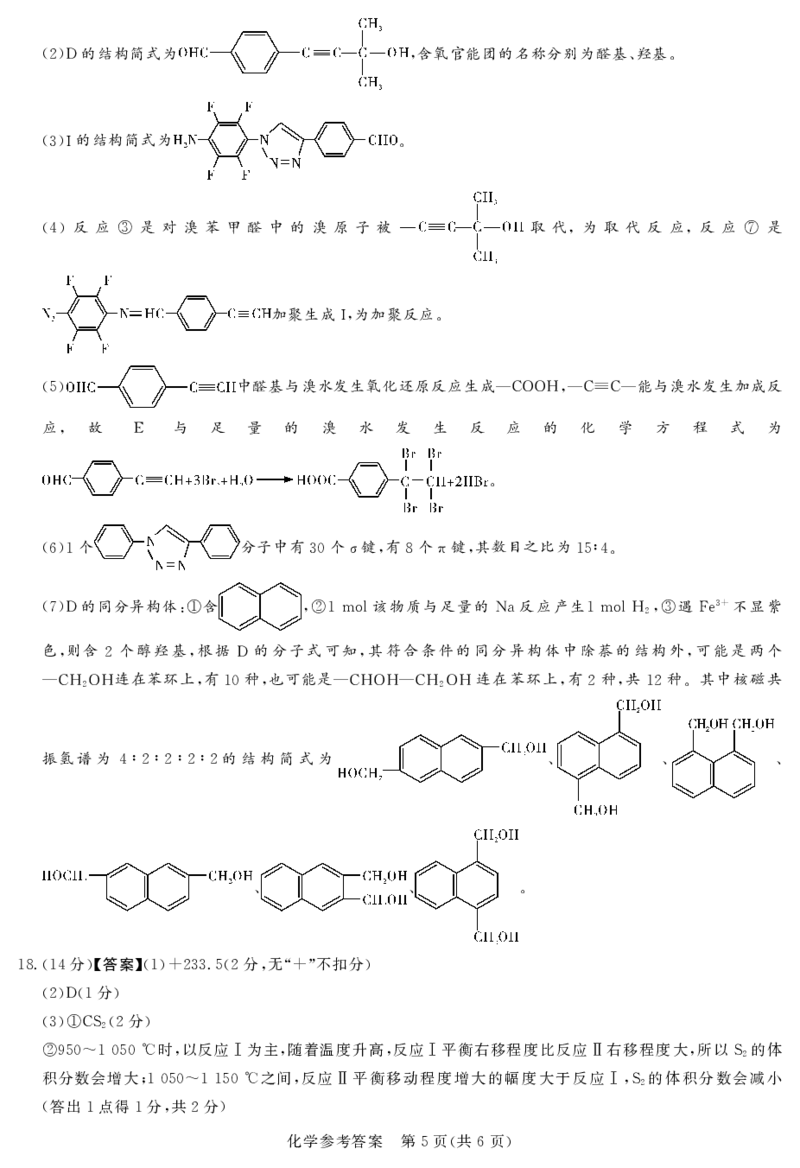
{#{QQABJQis4ggYgESACJ4KQw3UCQkQsJAiJUoERRCRKAwKAZFABKA=}#}() 的结构简式为 ,含氧官能团的名称分别为醛基、羟基。
2D
()的结构简式为 。
3I
()反 应 是 对 溴 苯 甲 醛 中 的 溴 原 子 被 取 代,为 取 代 反 应,反 应 是
4 ③ ⑦
加聚生成 ,为加聚反应。
I
() 中醛基与溴水发生氧化还原反应生成— ,— —能与溴水发生加成反
5 COOH C≡C
应, 故 与 足 量 的 溴 水 发 生 反 应 的 化 学 方 程 式 为
E
。
() 个 分子中有 个 键,有 个 键,其数目之比为 。
61 30 σ 8 π 15∶4
() 的同分异构体: 含 , 该物质与足量的 反应产生 , 遇 不显紫
3+
7D ① ②1mol Na 1molH2 ③ Fe
色,则含 个醇羟基,根据 的分子式可知,其符合条件的同分异构体中除萘的结构外,可能是两个
2 D
— 连在苯环上,有 种,也可能是— — 连在苯环上,有 种,共 种。其中核磁共
CH2OH 10 CHOH CH2OH 2 12
振氢谱为 的结构简式为 、 、 、
4∶2∶2∶2∶2
、 、 。
分 【答案】 分 无 不扣分
18.(14 ) (1)+233.5(2 , “+” )
分
(2)D(1 )
分
(3)①CS2(2 )
时 以反应 为主 随着温度升高 反应 平衡右移程度比反应 右移程度大 所以 的体
②950~1050℃ , Ⅰ , , Ⅰ Ⅱ , S2
积分数会增大 之间 反应 平衡移动程度增大的幅度大于反应 的体积分数会减小
;1050~1150℃ , Ⅱ Ⅰ,S2
答出 点得 分 共 分
( 1 1 , 2 )
化学参考答案 第 页 共 页
5 ( 6 )
{#{QQABJQis4ggYgESACJ4KQw3UCQkQsJAiJUoERRCRKAwKAZFABKA=}#}减小各组分的浓度 使平衡正向移动 提高 的去除率 分
③ , , H2S (1 )
分 全对得 分 少选得 分 有错不给分
④ABD(2 , 2 , 1 , )
分 写 也给分 分 未写单位扣 分
⑤92.3%(2 , 0.923 ) 121kPa(2 , 1 )
【解析】()根据反应 和反应 ,利用盖斯定律可得: () () () ()
1 Ⅰ Ⅱ CH4 g+2H2SgCS2 g+4H2 g
H · -1 。
Δ =+233.5kJ mol
()已知反应 的 S · -1 · -1 ,H · -1 ,根据 G H TS 可
2 Ⅰ Δ =+150.28J mol K Δ 1=+169.8kJ mol Δ =Δ 1- Δ <0
求得T ,故选 。
>1130K≈857℃ D
() 将 与 按体积比 投料,并用 稀释,在不同温度下反应达到平衡时,由于 是反应 的生
3① H2S CH4 2∶1 N2 S2 Ⅰ
成物同时又是反应 的反应物,因此 所在曲线是 的体积分数。 时,以反应 为主,随着温度升
Ⅱ Y S2 950~1050℃ Ⅰ
高,反应 速率大于反应 , 的体积分数会增大, 之间,反应 速率增大的幅度大于反应 ,
Ⅰ ⅡS2 1050~1150℃ Ⅱ Ⅰ
的体积分数会减小。根据方程式中的数量关系, 所在曲线为 的体积分数, 所在曲线为 的体积
S2 Z H2 X CS2
分数。
由于 是反应 的生成物同时又是反应 的反应物,因此 所在曲线是 。 时,以反应
② S2 Ⅰ Ⅱ Y S2 950~1050℃ Ⅰ
为主,随着温度升高,反应 速率大于反应 , 的体积分数会增大, 之间,反应 速率增大
Ⅰ Ⅱ S2 1050~1150℃ Ⅱ
的幅度大于反应 , 的体积分数会减小。
Ⅰ S2
往容器中充入 的目的是减小各组分的浓度,使平衡正向移动,提高 的去除率。
③ N2 H2S
随着反应的进行,气体物质的量增大,恒压条件下容器体积增大, 可以;气体密度等于气体总质量除以
④ A
体积,反应前后气体质量不变,体积增大,气体密度减小, 可以;v( )v( )未标明正、逆,无法说明,
B CH4 = CS2
不可以;随着反应的进行,含碳物质的总物质的量不变,而气体的总物质的量在改变,其体积分数改变,
C D
可以。
由题图可知, 达到平衡时,( ) ,( ) ,( ) ,( ) ,
⑤ 1000℃ φH2 =5.5% φCS2 =1.25% φS2 =0.25% φ H2S =0.25%
则 的去除率为 1.25%×2+0.25%×2 。反应 压强平衡常数K
H2S ×100%≈92.3% Ⅰ p=
1.25%×2+0.25%×2+0.25%
( ) ( )
5.5%×100kPa 2 × 0.25%×100kPa 。
( ) 2 =121kPa
0.25%×100kPa
化学参考答案 第 页 共 页
6 ( 6 )
{#{QQABJQis4ggYgESACJ4KQw3UCQkQsJAiJUoERRCRKAwKAZFABKA=}#}