文档内容
化学参考答案
一、选择题:本题共14小题,每小题3分。
题号 1 2 3 4 5 6 7
答案 A D B C D C A
题号 8 9 10 11 12 13 14
答案 A C B B C D D
【解析】
1.活性银离子为重金属离子能使蛋白质变性,A正确。重油在高温、高压和催化剂作用下通
过裂化和裂解反应转化为小分子烃,B 错误。“天目一号”气象星座卫星的光伏发电系统
工作时可将光能转化为电能,C错误。淀粉和纤维素分子式均为(C H O ) ,但n不相同,
6 10 5 n
分子式不相同,不互为同分异构体,但它们水解的最终产物均是葡萄糖,D错误。
2.CS 的分子空间构型为直线形,A错误。NaCl为离子化合物,其电子式错误,B错误。SiO
2 2
为共价晶体,电子式书写错误,C 错误。激发态碳原子可能的电子排布轨道表示式:
,D正确。
3.FeCl 具有强氧化性,用于刻蚀铜板的反应,A错误。臭氧具有强氧化性,可用于自来水杀
3
菌消毒,B 正确。SiC 硬度大,可用于制作砂轮磨料,C 错误。石墨中每个 C 原子以 sp2
杂化形成平面结构,未杂化的 2p 电子其轨道相互平行且相互重叠,使 p 轨道中电子在整
个C原子平面中运动,因此石墨有类似金属晶体的导电性, D错误。
4.向NaOH溶液中通入少量CO :CO + 2OH-= CO2+ H O,A错误。水解反应为可
2 2 3 2
逆反应,B错误。18O反应后应该在18OH-中,D错误。
5.瓷坩埚中含有二氧化硅,高温下熔融的碳酸钠与二氧化硅反应,应该选用铁坩埚,A错误。
收集氨气的试管口要放适量的棉花,以防止氨气与空气产生对流现象,B 错误。液溴具有
挥发性,挥发的液溴能腐蚀橡胶,不能用橡皮塞,C 错误。碘易升华,加热碘和氯化钠固
体的固体混合物后,升华的碘遇冷重新变为固体,所以用该方法分离碘和氯化钠固体,D
正确。
6.该反应氧化剂与还原剂之比为1∶1,A错误。B选项未说明标况,B错误。每形成0.4mol
O—H,说明生成H
2
O 0.2mol,则转移电子数目为0.2N
A
,C正确。每1mol
1
3
7
7Cl含有的中子
数为20N ,D错误。
A
化学参考答案·第1页(共6页)
{#{QQABCQetwgo4kETACS4LUQEwCwsQkIGgJcoMQRCQKAQDgINIFIA=}#}7.加聚反应又称加成聚合反应,聚苯胺不是由苯胺通过加聚反应得到的,A错误。聚苯胺分
子中的共轭大π键体系,为电荷传递提供了通路,经过掺杂处理后具有导电性,B 正确。
由聚苯胺结构式可知,苯胺脱氢程度越高,y 值越小,1−y 越大,当 y=0 时。两种六元环
数量相等,C正确。苯胺具有碱性,与盐酸反应的离子方程式正确。
8.冠醚中的所有原子不在同一个平面,A错误。乙中五元环存在大π键,参与形成大π键的
电子总数为6个,B正确。超分子内部通过非共价键、氢键、静电作用、疏水作用等弱相
互作用结合形成超分子,C 正确。HClO 分子中氧的电负性大,3 个非羟基氧吸电子效应
4
使O—H键极性增强,D正确。
9.已知X、Y、Z、M、W是五种短周期主族元素,其原子半径与原子序数的关系如图甲,则
X 位于第一周期,为氢元素,Y、Z 位于第二周期,M、W 位于第三周期;X、Y、Z、M
可形成化合物,Z与W同主族,M形成+1价阳离子,其原子半径最大,则M为Na;Z形
成 2 个共价键,则位于 VIA 族,则 Z 为氧元素,W为硫元素;Y 形成 4 个共价键,则 Y
为碳元素,据此分析解答。C 的氢化物有很多种烃,相对分子量过大时可能存在沸点大于
H S,A正确。Z为O元素,M为Na元素,W为S元素,电子层数越多,微粒半径越大,
2
电子层数相同时,核电荷数越大,微粒半径越小,S2−含有3个电子层,Na+和O2−均含有2
个电子层,核电荷数 Na>O,则离子半径:r(S2−)>r(O2−)>r(Na+),B 正确。H O 为共价
2 2
化合物,分子中含有极性键和非极性键,而Na O 为离子化合物,含有离子键和非极性键,
2 2
化学键类型不完全相同,C 错误。非金属性越强,最高价氧化物对应水化物的酸性越强,
非金属性:S>C,则酸性H SO >H CO ,D正确。
2 4 2 3
10.麦芽糖也是还原糖,和水解产物葡萄糖一样,都能发生铜镜反应,故B错误。
11.苯甲酸为一元弱酸,加水稀释时,电离平衡右移,则0.01mol/L苯甲酸溶液稀释100倍时,
溶液 pH 增加小于 2,A 错误。由电离常数可知,苯甲酸根离子的水解常数
K 1014 c(C H COOH)c(OH)
K w 0.16109 6 5 ,则 0.1mol/L 苯甲酸钠溶液中
h K 6.25105 c(C H COO)
a 6 5
溶 液 pH82lg2 , B 正 确 。 苯 甲 酸 钠 溶 液 中 存 在 质 子 守 恒 关 系
c(H+)+c(C H COOH)=c(OH),C 错误。苯甲酸为一元弱酸,则苯甲酸钠在溶液中水解
6 5
使溶液呈碱性,则用氢氧化钠标准溶液滴定苯甲酸溶液时,应用酚酞作指示剂,D错误。
12.氨气的催化氧化根据能量图关系可以看出是放热反应,A正确。NH 中共价键为极性键,
3
参与反应发生断键,Fe3+转化为Fe2+,化合价降低,体现氧化性,B正确。根据转化关系,
Fe3+应为催化剂,Fe2+是反应过程中的中间产物,C错误。过程Ⅲ每消耗0.5 mol O ,转移
2
电子数为2N ,D正确。
A
化学参考答案·第2页(共6页)
{#{QQABCQetwgo4kETACS4LUQEwCwsQkIGgJcoMQRCQKAQDgINIFIA=}#}13.充电时,甲电极连接外加电源的正极,则充电时,甲电极为电解池的阳极,电极反应式
为Bi+3F-−3e-=BiF ,乙电极为阴极,反应式为MgF +2e-=Mg+2F-,又充电时,
3 2
电解池的阳极、阴极与原电池的正极、负极对应,所以放电时,乙电极为负极,Mg失去
电子结合F-生成MgF,电极反应式为Mg+2F-−2e-=MgF,甲为正极,正极上BiF+3e-
2 2 3
=Bi+3F-,据此解答。放电时,甲为正极,乙为负极,甲电极的电极电势更高,A错
误。放电时,乙电极为负极,电极反应式为Mg+2F-−2e-=MgF ,B错误。充电时,
2
装置将电能转化为化学能,C 错误。充电时,乙电极为阴极,反应式为 MgF +2e-
2
=Mg+2F-,所以导线上每通过 0.1mol 电子,生成 0.1mol F-,则乙电极质量减少
0.1mol×19g/mol=1.9g,D正确。
14.溶液碱性越强,溶液中 RN H 浓度越大,随着盐酸的加入先转化为RN H,后转化为
2 4 2 5
RN H2,所以曲线①表示RN H2,曲线②表示RN H,曲线③表示RN H ,A错误。根
2 6 2 6 2 5 2 4
c(RN H2)c(OH)
据曲线可知在常温下,X点时(RN H2)(RN H),K 2 6 109.5;
2 6 2 5 b2 c(RN H)
2 5
c(RN H)c(OH)
Z 点 (RN H)(RN H ), K 2 5 103.5, Y 点 时
2 5 2 4 b1 c(RN H )
2 4
(RN H2)(RN H ), K ·K =c2(OH-)=10−9.5×10−3.5=10−13,所以该点溶液 c(OH-)
2 6 2 4 h1 h2
1014
=10−6.5 mol/L,c(H+)= mol/L107.5mol/L,因此溶液显弱碱性,B错误。由图像可知,
106.5
X、Z 点溶液中(RN H)相同,但体积不同,故浓度不等,C 错误。V(HCl)=10mL 时,
2 5
溶 液 中 溶 质 为 RN H , RN H H ORH H2 OH , K =10−9.5 ,
2 5 2 5 2 2 6 b2
RN HRH H H,K =10−10.5,则c(RN H2)>c(RN H ),D正确。
2 5 2 4 h2 2 6 2 4
二、非选择题:本题共4小题,共58分。
15.(除特殊标注外,每空2分,共14分)
(1)B→E→B(3分)
(2)电解(1分) a(1分)
(3)③②①④⑤⑥
(4)①防倒吸(1分) ②中和生成的氢离子,促进反应正向进行
③过滤、洗涤、干燥
(5)在盐酸酸化的氯化亚铁溶液中滴加硫氰化钾溶液,无明显现象,再向其中加入少量
BaO ,溶液变为红色,证明BaO 的氧化性比FeCl 的强
2 2 3
化学参考答案·第3页(共6页)
{#{QQABCQetwgo4kETACS4LUQEwCwsQkIGgJcoMQRCQKAQDgINIFIA=}#}【解析】(1)根据反应原理,需要制备氧气。由于钡是活泼金属,能与水、CO 发生反应,
2
因此需要除去氧气中的水蒸气,然后通入玻璃管中和钡发生反应,同时应防止空气中的
水和二氧化碳进入E装置,因此装置的连接顺序是A→B→E→B。
(3)由于有气体参加反应,所以首先要检查装置的气密性,然后电解制氧气,排尽装置
内的空气,对玻璃管进行加热,发生反应,反应完全后,停止加热,故实验操作的顺序
是③②①④⑤⑥。
(4)①氨气极易溶于水,因此仪器X的作用是防倒吸。
16.(除特殊标注外,每空2分,共14分)
(1)温度升高,NH 挥发,使生成的[Zn(NH ) ]2+减少
3 3 4
(2)Fe(OH) (1分) SiO (1分)
3 2
(3)Mn2++2NH ·H O+H O = MnO ↓+2NH+2H O
3 2 2 2 2 4 2
(4)2.16×1014 C
(5)12 1
【解析】热镀锌灰锌渣主要成分为ZnO及少量Zn、Fe O 、CuO、MnO、SiO ,加入过量
2 3 2
NH −NH Cl溶液,生成[Zn(NH ) ]2+、[Cu(NH ) ]2+,同时生成Fe(OH) 、Mn(OH) 等,SiO
3 4 3 4 3 4 3 2 2
不溶解,过滤一起除去,再向滤液中加入H O 溶液,进一步除锰,反应的离子方程式为
2 2
Mn2++2NH ·H O+H O =MnO ↓+2NH+2H O,再加入(NH ) S,进行除铜,反
3 2 2 2 2 4 2 4 2
应的离子方程式为[Cu(NH ) ]2++S2−=CuS↓+4NH 。
3 4 3
(4)当(NH)S加入量≥100%时,锌的回收率下降的可能原因是[Zn(NH)]2+与S2−结合生成了硫
42 34
化锌,离子方程式为[Zn(NH)]2+(aq)+S2−(aq)=ZnS(s)+4NH(aq),该反应的平衡常数为
34 3
c4(NH ) 1 1 1 1
K 3 mol2 L2 2.161014
c([Zn(NH ) ]2)c(S2) K K (ZnS) 2.9109 1.61024
3 4 稳 sp
n(Cu2)
mol2 L2。当(NH ) S加入量为120%时,铜锌比约为2.0×10−6, 较小,
4 2 n([Zn(NH ) ]2)
3 4
继续加大(NH ) S加入量会导致锌的回收率下降且不经济。
4 2
(5)根据晶胞结构可知 CuMnCl 晶体中 Cu+的配位数为 12,A、B 位的离子均恰好与 C
3
位的离子相切,设晶胞边长为a,则2r +2r = 2a,2r +2r =a,则t=1。
A C B C
17.(除特殊标注外,每空2分,共15分)
(1)HCOOHH+ + HCOO-
(2)③(1分) <(1分) 反应的S 0且自发,则H 0
(3)①< ②10 ③0.2
化学参考答案·第4页(共6页)
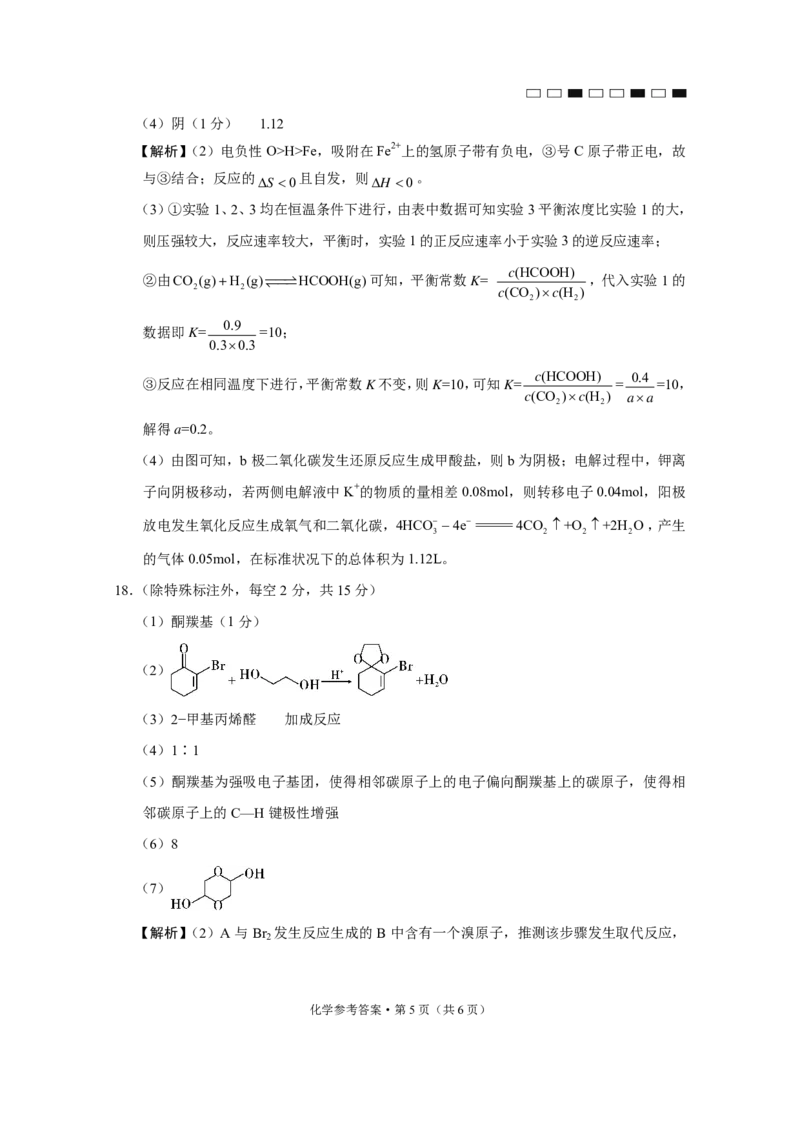
{#{QQABCQetwgo4kETACS4LUQEwCwsQkIGgJcoMQRCQKAQDgINIFIA=}#}(4)阴(1分) 1.12
【解析】(2)电负性O>H>Fe,吸附在Fe2+上的氢原子带有负电,③号C原子带正电,故
与③结合;反应的
S 0
且自发,则
H 0
。
(3)①实验1、2、3均在恒温条件下进行,由表中数据可知实验3平衡浓度比实验1的大,
则压强较大,反应速率较大,平衡时,实验1的正反应速率小于实验3的逆反应速率;
c(HCOOH)
②由CO (g)H (g)HCOOH(g)可知,平衡常数K= ,代入实验1的
2 2 c(CO )c(H )
2 2
0.9
数据即K= =10;
0.30.3
c(HCOOH) 0.4
③反应在相同温度下进行,平衡常数K不变,则K=10,可知K= = =10,
c(CO )c(H ) aa
2 2
解得a=0.2。
(4)由图可知,b极二氧化碳发生还原反应生成甲酸盐,则b为阴极;电解过程中,钾离
子向阴极移动,若两侧电解液中K+的物质的量相差0.08mol,则转移电子0.04mol,阳极
放电发生氧化反应生成氧气和二氧化碳,4HCO 4e=4CO +O +2H O,产生
3 2 2 2
的气体0.05mol,在标准状况下的总体积为1.12L。
18.(除特殊标注外,每空2分,共15分)
(1)酮羰基(1分)
(2)
(3)2−甲基丙烯醛 加成反应
(4)1∶1
(5)酮羰基为强吸电子基团,使得相邻碳原子上的电子偏向酮羰基上的碳原子,使得相
邻碳原子上的C—H键极性增强
(6)8
(7)
【解析】(2)A与Br 发生反应生成的 B中含有一个溴原子,推测该步骤发生取代反应,
2
化学参考答案·第5页(共6页)
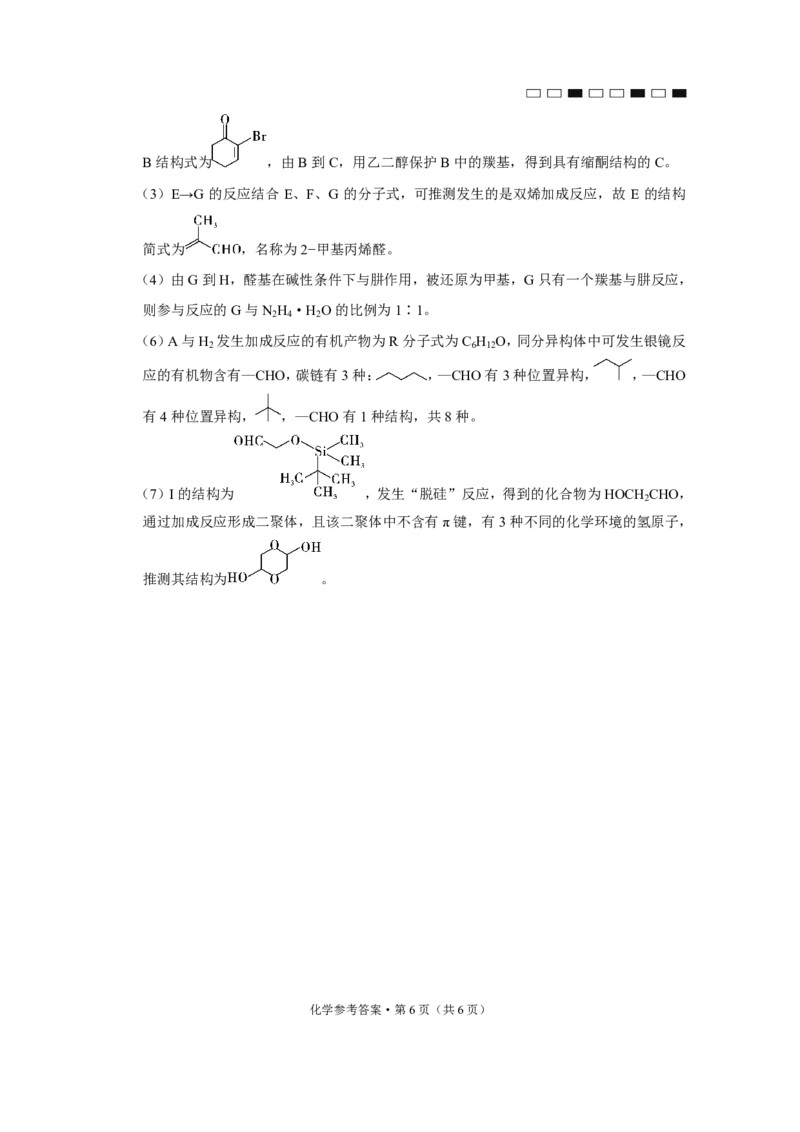
{#{QQABCQetwgo4kETACS4LUQEwCwsQkIGgJcoMQRCQKAQDgINIFIA=}#}B结构式为 ,由B到C,用乙二醇保护B中的羰基,得到具有缩酮结构的C。
(3)E→G 的反应结合 E、F、G 的分子式,可推测发生的是双烯加成反应,故 E 的结构
简式为 ,名称为2−甲基丙烯醛。
(4)由G到H,醛基在碱性条件下与肼作用,被还原为甲基,G只有一个羰基与肼反应,
则参与反应的G与N H ·H O的比例为1∶1。
2 4 2
(6)A与H 发生加成反应的有机产物为R分子式为C H O,同分异构体中可发生银镜反
2 6 12
应的有机物含有—CHO,碳链有3种: ,—CHO有3种位置异构, ,—CHO
有4种位置异构, ,—CHO有1种结构,共8种。
(7)I的结构为 ,发生“脱硅”反应,得到的化合物为HOCH CHO,
2
通过加成反应形成二聚体,且该二聚体中不含有π键,有3种不同的化学环境的氢原子,
推测其结构为 。
化学参考答案·第6页(共6页)
{#{QQABCQetwgo4kETACS4LUQEwCwsQkIGgJcoMQRCQKAQDgINIFIA=}#}