文档内容
2024-2024 学年第二学期高三 2 月月考化学试卷
考试时间:75分钟
注意事项:
1.答题前填写好自己的姓名、班级、考号等信息
2.请将答案正确填写在答题卡上
可能用到的相对原子质量:H: 1 C: 12 N:14 O:16 S:32 Cl:35.5 Na:23 Mg:24 Al:27 K:39 Fe:56 Ba:137
第I卷(选择题)
一、单选题(每题3分 共42分)
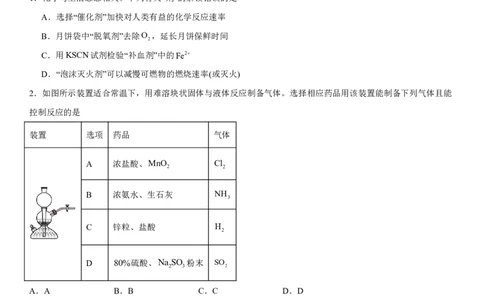
1.化学与生活息息相关。下列有关“剂”的解读错误的是
A.选择“催化剂”加快对人类有益的化学反应速率
B.月饼袋中“脱氧剂”去除O ,延长月饼保鲜时间
2
C.用KSCN试剂检验“补血剂”中的Fe2
D.“泡沫灭火剂”可以减慢可燃物的燃烧速率(或灭火)
2.如图所示装置适合常温下,用难溶块状固体与液体反应制备气体。选择相应药品用该装置能制备下列气体且能
控制反应的是
装置 选项 药品 气体
A 浓盐酸、MnO Cl
2 2
B 浓氨水、生石灰 NH
3
C 锌粒、盐酸 H
2
D 80%硫酸、Na SO 粉末 SO
2 3 2
A.A B.B C.C D.D
3.设N 为阿伏加德罗常数的值。下列叙述正确的是
A
A.4.6g由NO 和N O 组成的混合气体中含原子总数为0.3N
2 2 4 A
B.一定条件下,将1molHI置于密闭容器中充分分解,得到产物的分子总数为N
A
C.在核反应方程 238UAX4He中,0.1molAX含中子数为9N
92 a 2 a A
D.标准状况下,11.2LOF (气体)与水完全反应(生成O 和HF)时转移电子数为2N
2 2 A
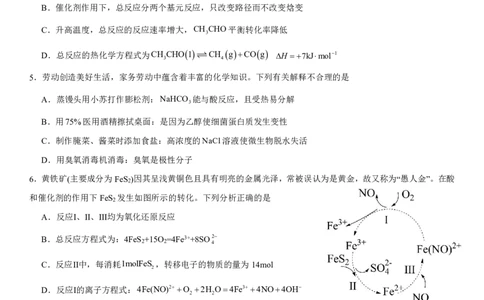
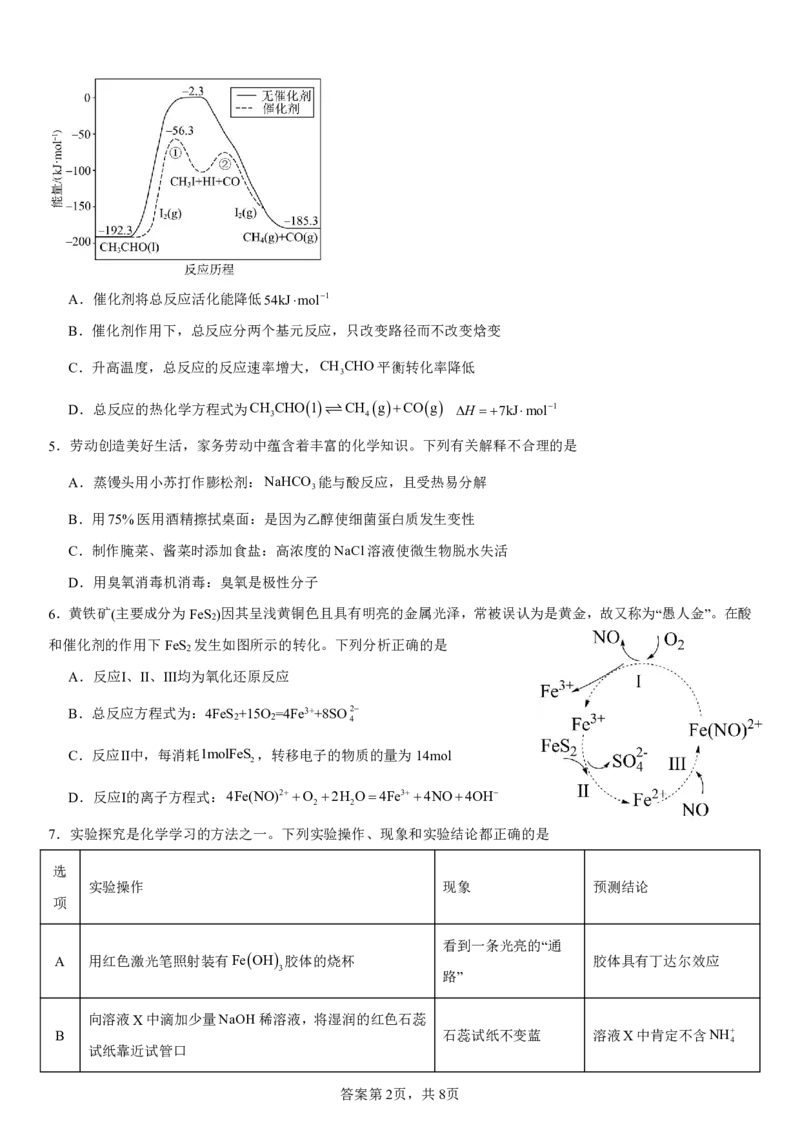
4.已知CH CHO1 CH gCOg H,该反应的反应历程与能量变化如图所示。下列叙述错误的是
3 4
答案第1页,共8页
{#{QQABJQyp4gCwkATACK5qVUXWCUsQsIKhLQoMxRCeOARDgBFIBIA=}#}A.催化剂将总反应活化能降低54kJmol1
B.催化剂作用下,总反应分两个基元反应,只改变路径而不改变焓变
C.升高温度,总反应的反应速率增大,CH CHO平衡转化率降低
3
D.总反应的热化学方程式为CH CHO1 CH gCOg H 7kJmol1
3 4
5.劳动创造美好生活,家务劳动中蕴含着丰富的化学知识。下列有关解释不合理的是
A.蒸馒头用小苏打作膨松剂:NaHCO 能与酸反应,且受热易分解
3
B.用75%医用酒精擦拭桌面:是因为乙醇使细菌蛋白质发生变性
C.制作腌菜、酱菜时添加食盐:高浓度的NaCl溶液使微生物脱水失活
D.用臭氧消毒机消毒:臭氧是极性分子
6.黄铁矿(主要成分为FeS )因其呈浅黄铜色且具有明亮的金属光泽,常被误认为是黄金,故又称为“愚人金”。在酸
2
和催化剂的作用下FeS 发生如图所示的转化。下列分析正确的是
2
A.反应Ⅰ、Ⅱ、Ⅲ均为氧化还原反应
B.总反应方程式为:4FeS +15O =4Fe3++8SO2
2 2 4
C.反应Ⅱ中,每消耗1molFeS ,转移电子的物质的量为14mol
2
D.反应Ⅰ的离子方程式:4Fe(NO)2O 2H O4Fe34NO4OH
2 2
7.实验探究是化学学习的方法之一。下列实验操作、现象和实验结论都正确的是
选
实验操作 现象 预测结论
项
看到一条光亮的“通
A 用红色激光笔照射装有FeOH 胶体的烧杯 胶体具有丁达尔效应
3
路”
向溶液X中滴加少量NaOH稀溶液,将湿润的红色石蕊
B 石蕊试纸不变蓝 溶液X中肯定不含NH
4
试纸靠近试管口
答案第2页,共8页
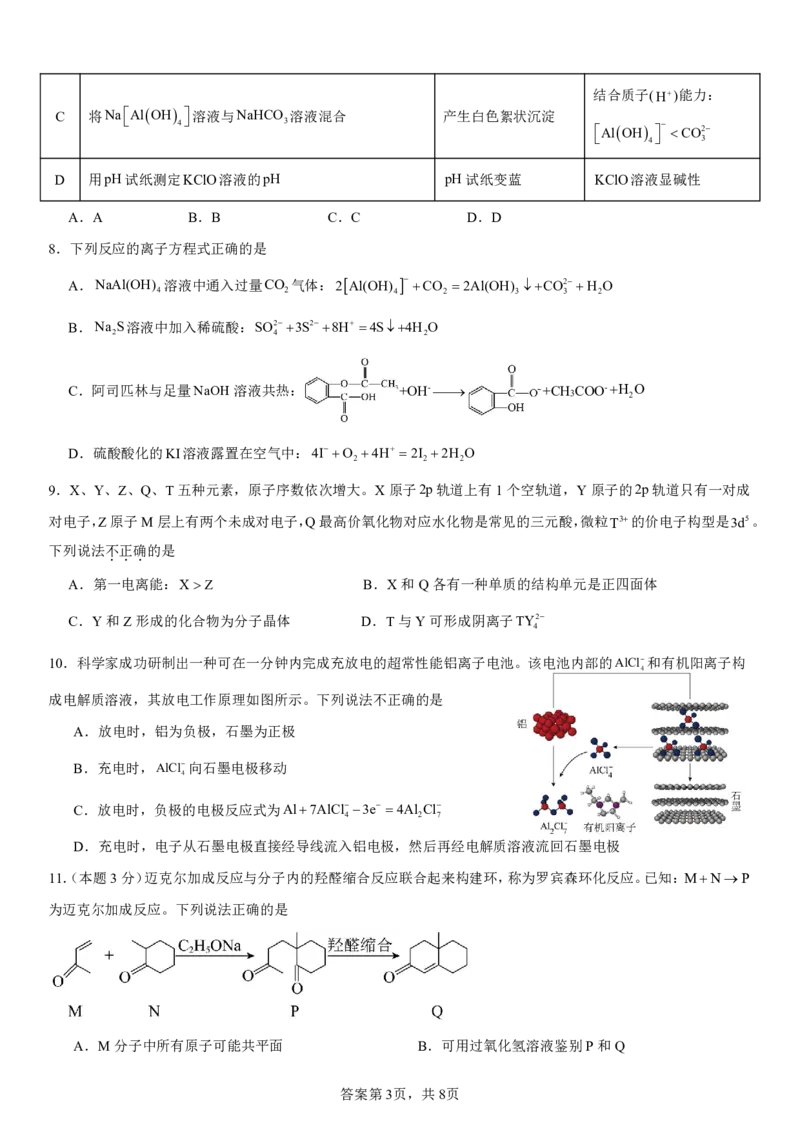
{#{QQABJQyp4gCwkATACK5qVUXWCUsQsIKhLQoMxRCeOARDgBFIBIA=}#}结合质子(H)能力:
C 将Na AlOH 4 溶液与NaHCO 3 溶液混合 产生白色絮状沉淀 AlOH CO2
4 3
D 用pH试纸测定KClO溶液的pH pH试纸变蓝 KClO溶液显碱性
A.A B.B C.C D.D
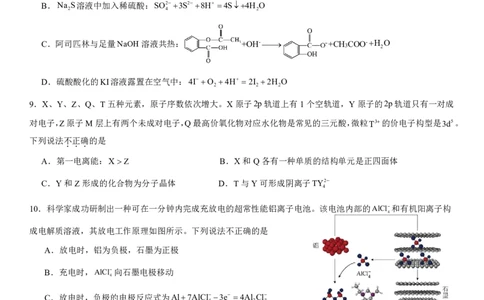
8.下列反应的离子方程式正确的是
A.NaAl(OH) 溶液中通入过量CO 气体:2Al(OH) CO 2Al(OH) CO2H O
4 2 4 2 3 3 2
B.Na S溶液中加入稀硫酸:SO23S28H 4S4H O
2 4 2
C.阿司匹林与足量NaOH溶液共热: +OH- +CH COO-H O
3 2
D.硫酸酸化的KI溶液露置在空气中:4IO 4H 2I 2H O
2 2 2
9.X、Y、Z、Q、T五种元素,原子序数依次增大。X原子2p轨道上有1个空轨道,Y原子的2p轨道只有一对成
对电子,Z原子M层上有两个未成对电子,Q最高价氧化物对应水化物是常见的三元酸,微粒T3的价电子构型是3d5。
下列说法不正确的是
...
A.第一电离能:XZ B.X和Q各有一种单质的结构单元是正四面体
C.Y和Z形成的化合物为分子晶体 D.T与Y可形成阴离子TY2
4
10.科学家成功研制出一种可在一分钟内完成充放电的超常性能铝离子电池。该电池内部的AlCl和有机阳离子构
4
成电解质溶液,其放电工作原理如图所示。下列说法不正确的是
A.放电时,铝为负极,石墨为正极
B.充电时,AlCl向石墨电极移动
4
C.放电时,负极的电极反应式为Al7AlCl3e 4Al Cl
4 2 7
D.充电时,电子从石墨电极直接经导线流入铝电极,然后再经电解质溶液流回石墨电极
11.(本题3分)迈克尔加成反应与分子内的羟醛缩合反应联合起来构建环,称为罗宾森环化反应。已知:MNP
为迈克尔加成反应。下列说法正确的是
A.M分子中所有原子可能共平面 B.可用过氧化氢溶液鉴别P和Q
答案第3页,共8页
{#{QQABJQyp4gCwkATACK5qVUXWCUsQsIKhLQoMxRCeOARDgBFIBIA=}#}C.含醛基、四元环和手性碳原子的N的同分异构体有5种
D. 和 在乙醇钠条件下反应可得到
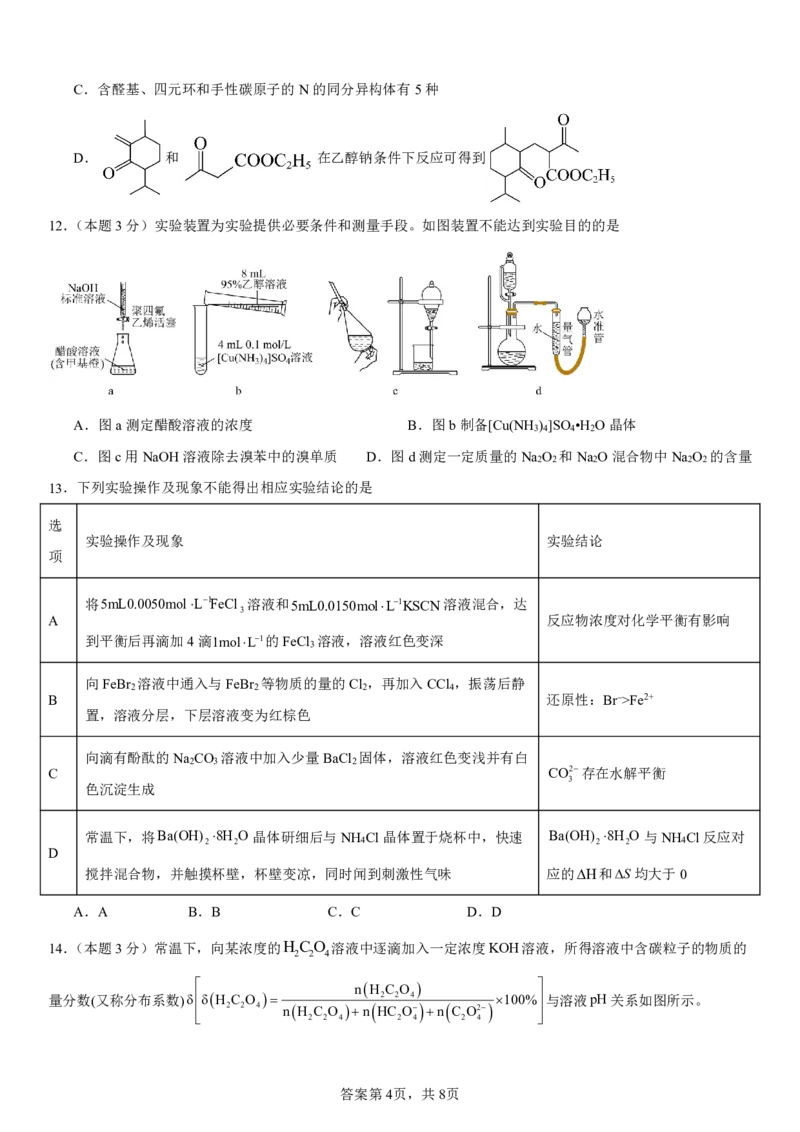
12.(本题3分)实验装置为实验提供必要条件和测量手段。如图装置不能达到实验目的的是
A.图a测定醋酸溶液的浓度 B.图b制备[Cu(NH ) ]SO •H O晶体
3 4 4 2
C.图c用NaOH溶液除去溴苯中的溴单质 D.图d测定一定质量的Na O 和Na O混合物中Na O 的含量
2 2 2 2 2
13.下列实验操作及现象不能得出相应实验结论的是
选
实验操作及现象 实验结论
项
将5mL0.0050molL1FeCl 溶液和5mL0.0150molL1KSCN溶液混合,达
3
A 反应物浓度对化学平衡有影响
到平衡后再滴加4滴1molL1的FeCl
3
溶液,溶液红色变深
向FeBr 溶液中通入与FeBr 等物质的量的Cl ,再加入CCl ,振荡后静
2 2 2 4
B 还原性:Br⁻>Fe2+
置,溶液分层,下层溶液变为红棕色
向滴有酚酞的Na CO 溶液中加入少量BaCl 固体,溶液红色变浅并有白
2 3 2
C CO2存在水解平衡
3
色沉淀生成
常温下,将Ba(OH) 8H O 晶体研细后与NH Cl晶体置于烧杯中,快速 Ba(OH) 8H O 与NH Cl反应对
2 2 4 2 2 4
D
搅拌混合物,并触摸杯壁,杯壁变凉,同时闻到刺激性气味 应的H和S均大于0
A.A B.B C.C D.D
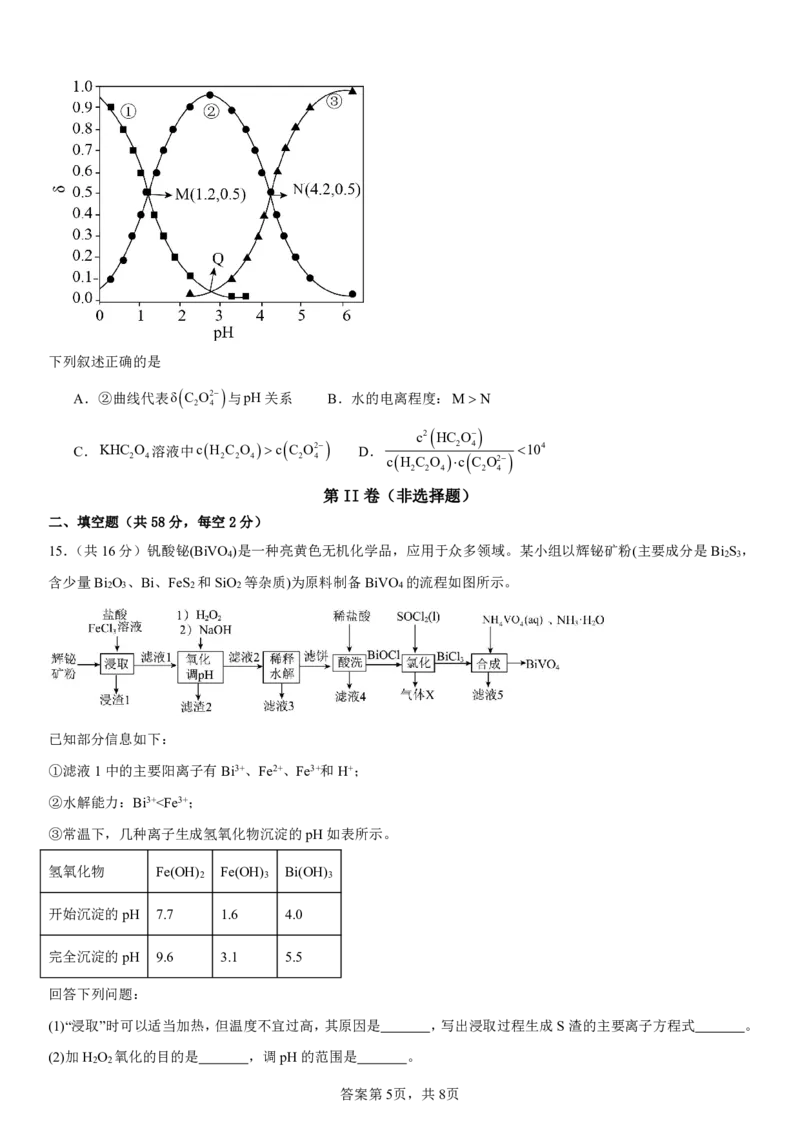
14.(本题3分)常温下,向某浓度的HCO 溶液中逐滴加入一定浓度KOH溶液,所得溶液中含碳粒子的物质的
2 2 4
nH C O
量分数(又称分布系数)δδH C O 2 2 4 100%与溶液pH关系如图所示。
2 2 4 nH C O n HC O n C O2
2 2 4 2 4 2 4
答案第4页,共8页
{#{QQABJQyp4gCwkATACK5qVUXWCUsQsIKhLQoMxRCeOARDgBFIBIA=}#}下列叙述正确的是
A.②曲线代表δ
C
O2
与pH关系 B.水的电离程度:MN
2 4
c2
HC
O
C.KHC O 溶液中cH C O c C O2 D. 2 4 104
2 4 2 2 4 2 4 cH C O c C O2
2 2 4 2 4
第II 卷(非选择题)
二、填空题(共58分,每空2分)
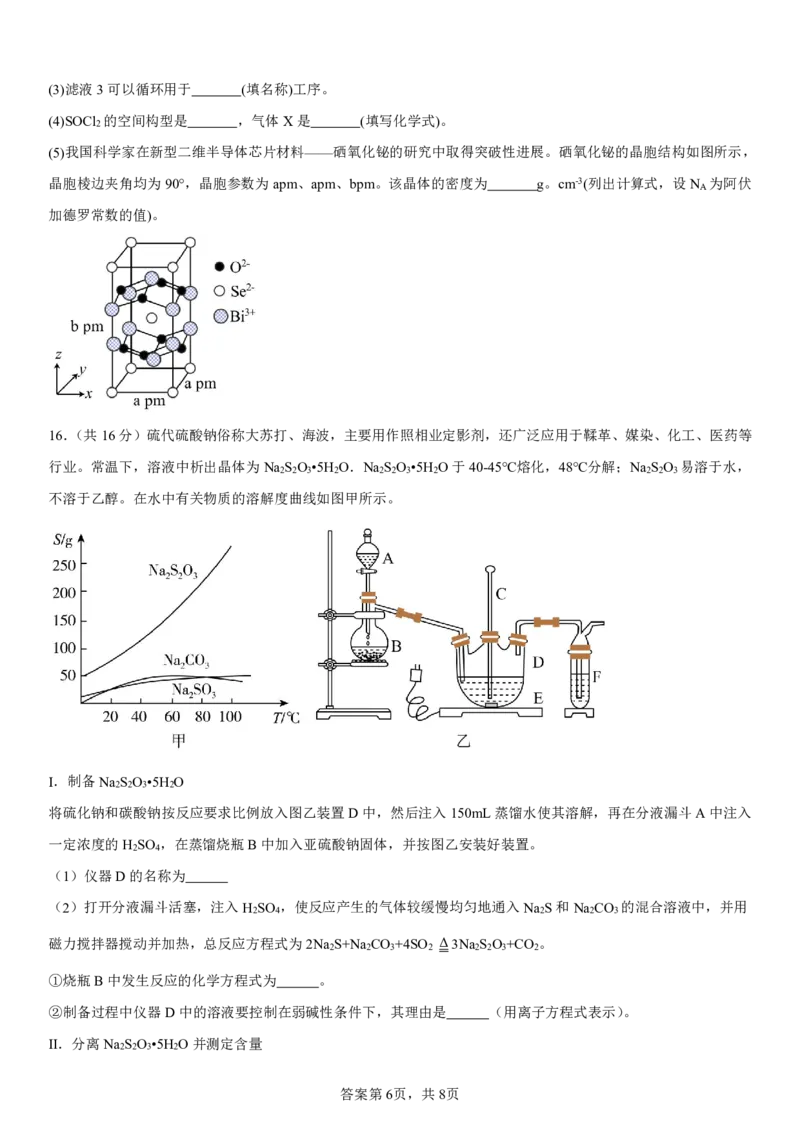
15.(共16分)钒酸铋(BiVO )是一种亮黄色无机化学品,应用于众多领域。某小组以辉铋矿粉(主要成分是Bi S ,
4 2 3
含少量Bi O 、Bi、FeS 和SiO 等杂质)为原料制备BiVO 的流程如图所示。
2 3 2 2 4
已知部分信息如下:
①滤液1中的主要阳离子有Bi3+、Fe2+、Fe3+和H+;
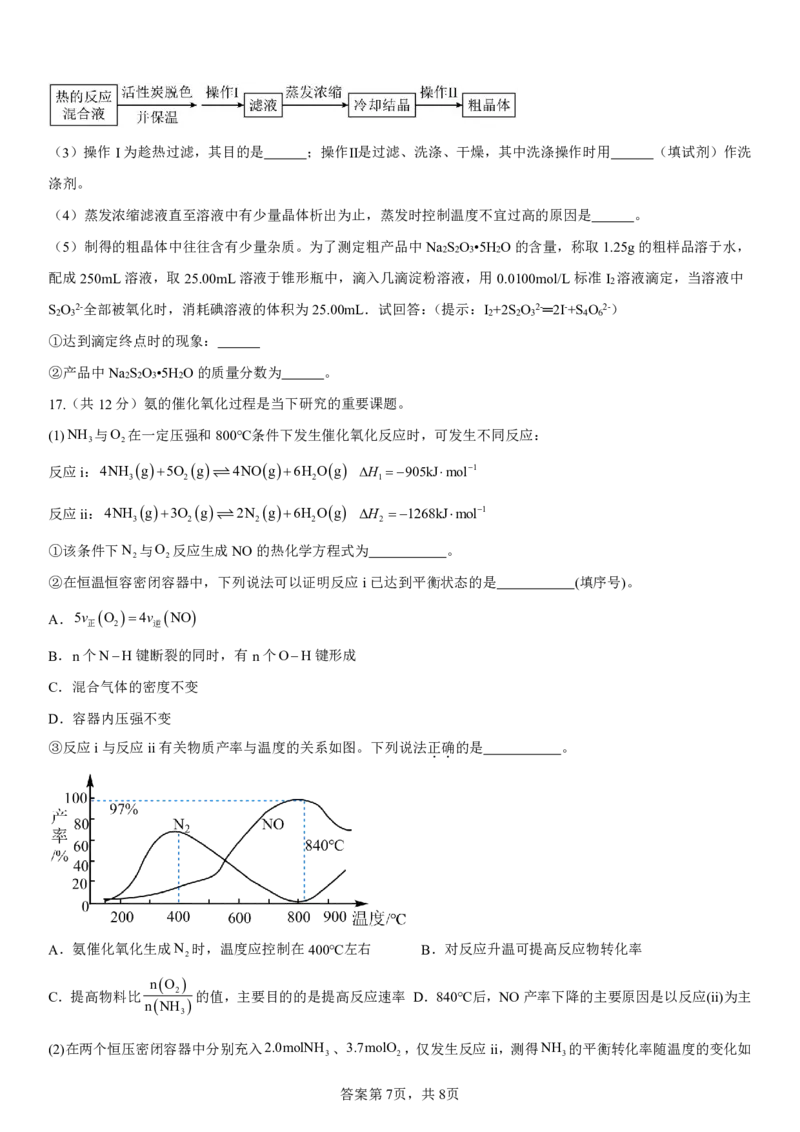
②水解能力:Bi3+”或“<”)
1 2
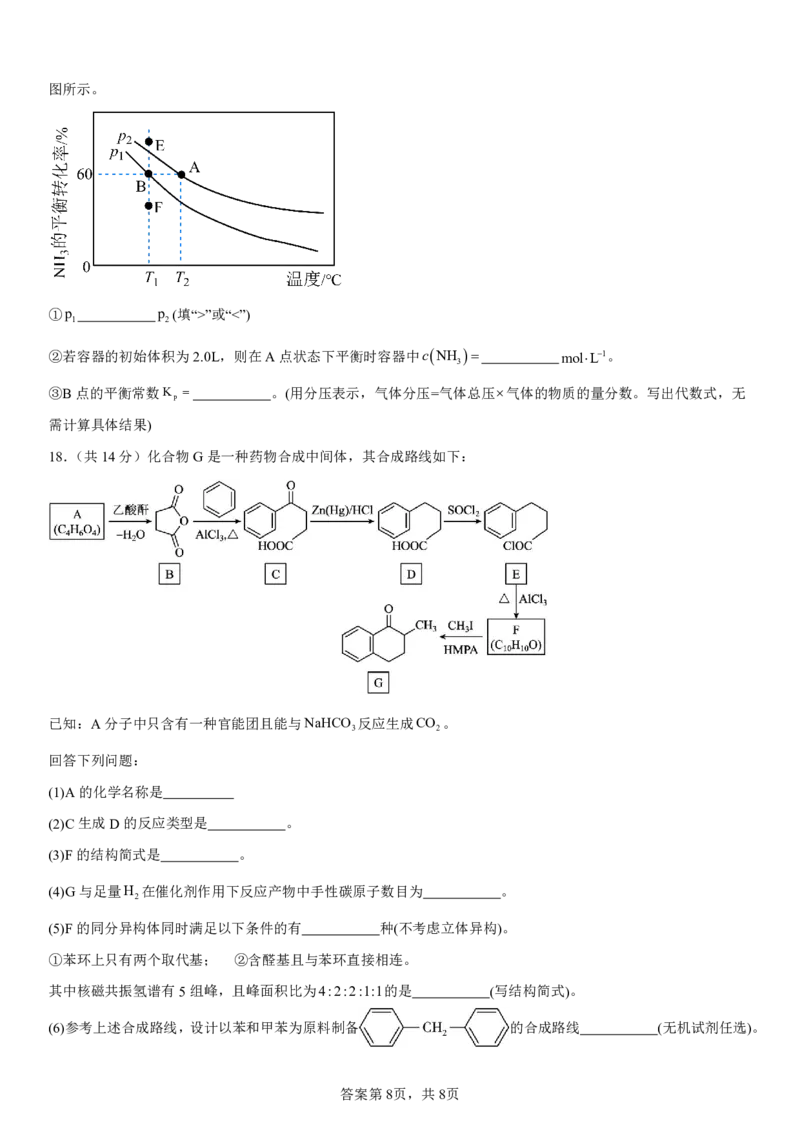
②若容器的初始体积为2.0L,则在A点状态下平衡时容器中cNH molL1。
3
③B点的平衡常数K 。(用分压表示,气体分压=气体总压气体的物质的量分数。写出代数式,无
p
需计算具体结果)
18.(共14分)化合物G是一种药物合成中间体,其合成路线如下:
已知:A分子中只含有一种官能团且能与NaHCO 反应生成CO 。
3 2
回答下列问题:
(1)A的化学名称是
(2)C生成D的反应类型是 。
(3)F的结构简式是 。
(4)G与足量H 在催化剂作用下反应产物中手性碳原子数目为 。
2
(5)F的同分异构体同时满足以下条件的有 种(不考虑立体异构)。
①苯环上只有两个取代基; ②含醛基且与苯环直接相连。
其中核磁共振氢谱有5组峰,且峰面积比为4:2:2:1:1的是 (写结构简式)。
(6)参考上述合成路线,设计以苯和甲苯为原料制备 的合成路线 (无机试剂任选)。
答案第8页,共8页
{#{QQABJQyp4gCwkATACK5qVUXWCUsQsIKhLQoMxRCeOARDgBFIBIA=}#}