文档内容
2021 年辽宁省沈阳市中考化学试卷
一、单选题(本大题共13小题,共15.0分)
1. 逻辑推理是一种重要的化学思维方法。下列推理合理的是( )
A. 因为碱溶液呈碱性,所以显碱性的溶液一定都是碱的溶液
B. 混合物中至少含有两种物质,则混合物中至少含有两种元素
C. 溶液是均一、稳定的,所以均一、稳定的物质一定是溶液
D. 物质在发生化学变化时,原子的种类不变,则元素的种类也不会改变
2. 下列富含糖类的食品是
A. ①③ B. ①④ C. ②④ D. ①②
3. 关于水的净化的知识,说法正确的是( )
A. 采用过滤的方法,可以将硬水转变成软水
B. 可以往自来水中加入胆矾作为絮凝剂
C. 用过滤的方法可以从食盐水中获得食盐
D. 滤纸要紧贴漏斗的内壁,是为了防止过滤时液体流速过慢
4. 下列用途中,主要是由物质的化学性质决定的是( )
A. 用铜丝作导线
B. 用干冰作制冷剂
C. 用氢气作燃料
D. 用金刚石裁玻璃
5. 有关燃烧与灭火说法正确的是
A. 可燃物与氧气接触就会燃烧
B. 隔绝氧气可以灭火
C. 水灭火的原理是降低可燃物着火点
D. 温度达可燃物着火点就能燃烧
6. 胡萝卜中富含的维生素A 具有预防夜盲症、抗衰老和促进骨髓生长等功效,其化学式为 C H O 。下列
1 20 30
说法正确的是
A. 维生素A 的相对分子质量为286 g
1
B. 维生素A 分子是由碳元素,氢元素和氧元素组成
1C. 维生素A 中碳元素的质量分数最大
1
D. 维生素A 中碳元素、氢元素、氧元素的质量比为20:30:1
1
7. 硫酸氢钠是一种酸式盐,其水溶液显酸性。它的固体与过氧化钠粉末加热时发生如下反应:
,则X的化学式为
A. B. C. Na D. NaOH
8. 下列物质的性质与用途的对应关系错误的是
A. 苏打可与盐酸反应,可用于治疗胃酸过多症
B. 活性炭疏松多孔可用于吸附水中杂质
C. 氮气的化学性质不活泼可作焊接金属的保护气
D. 浓硫酸具有强吸水性,可用作干燥剂
9. 下列实验方法不正确的是
A. 用肥皂水区分硬水和软水
B. 实验室用双氧水制氧气,用MnO 作催化剂
2
C. 用燃着的木条鉴别O 、CO 和空气三瓶无色气体
2 2
D. 将5克NaCl倒入50mL水中溶解,配得50克10%的NaCl溶液
10. 下列各组离子中,能在 的溶液中大量共存的是
A. 、 、 、 B. 、 、 、
C. 、 、 、 D. 、 、 、
11. 有一固体物质(不含结晶水)的溶液甲,在一定温度下,经历如下变化:
溶液甲 溶液乙 溶液丙
据此判断下列结论中正确的是( )
A. 该温度下,固体物质的溶解度是 30g/100g 水
B. 溶液丙再蒸发 10g 水,析出晶体的质量一定大于 3g
C. 溶液乙一定是不饱和溶液
D. 溶液乙和溶液丙的溶质质量分数可能相等
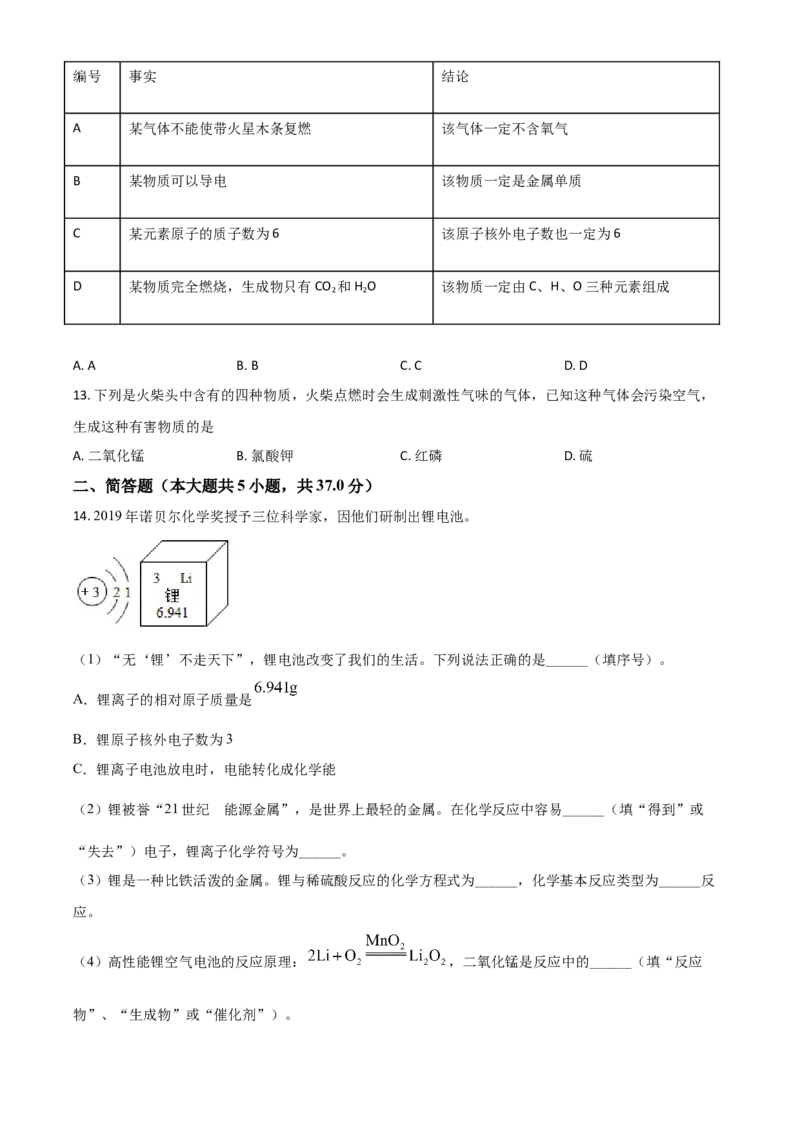
12. 下列由事实得出的结论正确的是( )编号 事实 结论
A 某气体不能使带火星木条复燃 该气体一定不含氧气
B 某物质可以导电 该物质一定是金属单质
C 某元素原子的质子数为6 该原子核外电子数也一定为6
D 某物质完全燃烧,生成物只有CO 和H O 该物质一定由C、H、O三种元素组成
2 2
A. A B. B C. C D. D
13. 下列是火柴头中含有的四种物质,火柴点燃时会生成刺激性气味的气体,已知这种气体会污染空气,
生成这种有害物质的是
A. 二氧化锰 B. 氯酸钾 C. 红磷 D. 硫
二、简答题(本大题共5小题,共37.0分)
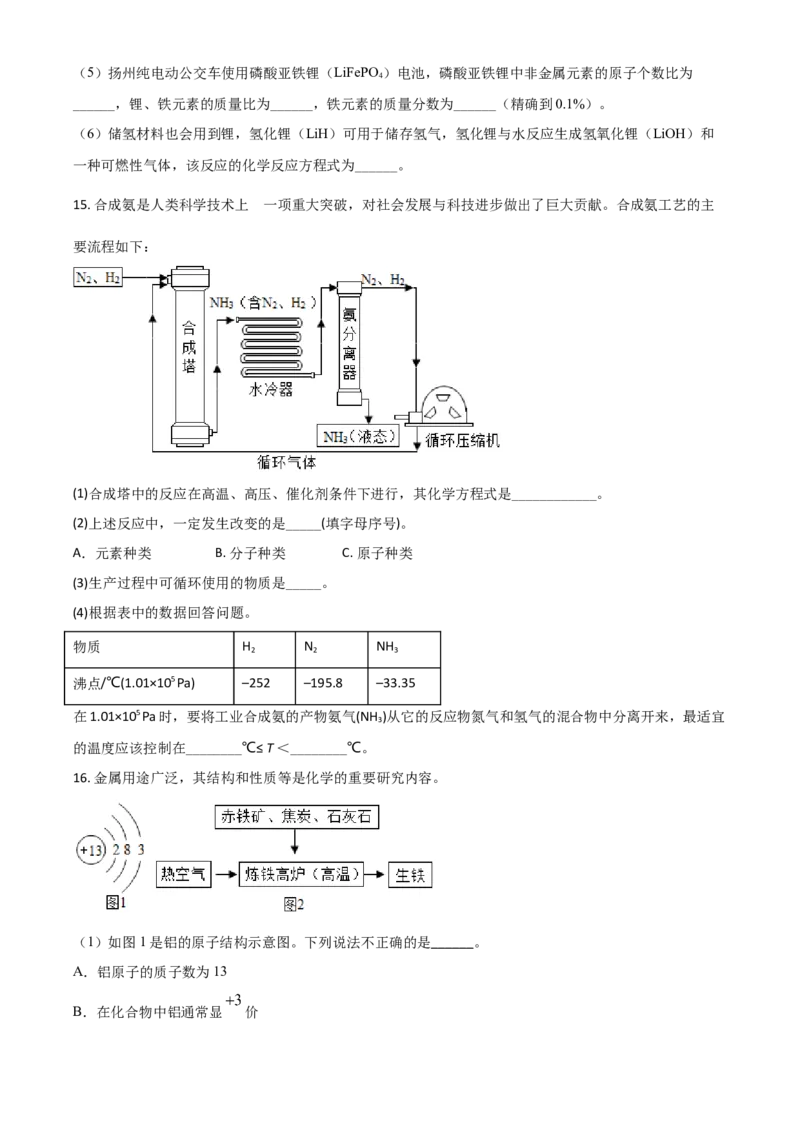
14. 2019年诺贝尔化学奖授予三位科学家,因他们研制出锂电池。
(1)“无‘锂’不走天下”,锂电池改变了我们的生活。下列说法正确的是______(填序号)。
A.锂离子的相对原子质量是
B.锂原子核外电子数为3
C.锂离子电池放电时,电能转化成化学能
的
(2)锂被誉“21世纪 能源金属”,是世界上最轻的金属。在化学反应中容易______(填“得到”或
“失去”)电子,锂离子化学符号为______。
(3)锂是一种比铁活泼的金属。锂与稀硫酸反应的化学方程式为______,化学基本反应类型为______反
应。
(4)高性能锂空气电池的反应原理: ,二氧化锰是反应中的______(填“反应
物”、“生成物”或“催化剂”)。(5)扬州纯电动公交车使用磷酸亚铁锂(LiFePO )电池,磷酸亚铁锂中非金属元素的原子个数比为
4
______,锂、铁元素的质量比为______,铁元素的质量分数为______(精确到0.1%)。
(6)储氢材料也会用到锂,氢化锂(LiH)可用于储存氢气,氢化锂与水反应生成氢氧化锂(LiOH)和
一种可燃性气体,该反应的化学反应方程式为______。
的
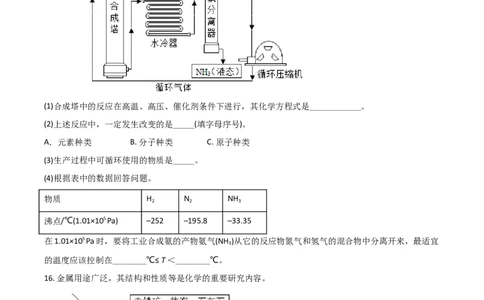
15. 合成氨是人类科学技术上 一项重大突破,对社会发展与科技进步做出了巨大贡献。合成氨工艺的主
要流程如下:
(1)合成塔中的反应在高温、高压、催化剂条件下进行,其化学方程式是____________。
(2)上述反应中,一定发生改变的是_____(填字母序号)。
A.元素种类 B. 分子种类 C. 原子种类
(3)生产过程中可循环使用的物质是_____。
(4)根据表中的数据回答问题。
物质 H N NH
2 2 3
沸点/℃(1.01×105 Pa) –252 –195.8 –33.35
在1.01×105 Pa时,要将工业合成氨的产物氨气(NH )从它的反应物氮气和氢气的混合物中分离开来,最适宜
3
的温度应该控制在________℃≤ T <________℃。
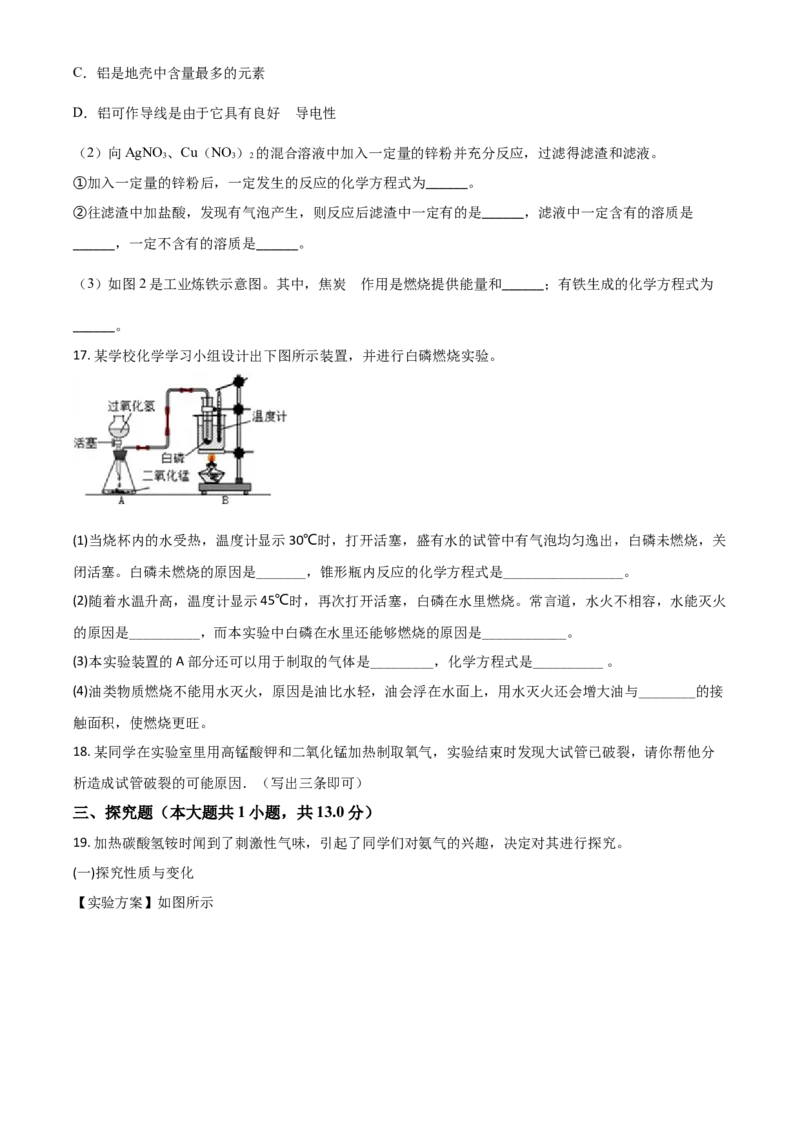
16. 金属用途广泛,其结构和性质等是化学的重要研究内容。
(1)如图1是铝的原子结构示意图。下列说法不正确的是______。
A.铝原子的质子数为13
B.在化合物中铝通常显 价C.铝是地壳中含量最多的元素
的
D.铝可作导线是由于它具有良好 导电性
(2)向AgNO、Cu(NO ) 的混合溶液中加入一定量的锌粉并充分反应,过滤得滤渣和滤液。
3 3 2
①加入一定量的锌粉后,一定发生的反应的化学方程式为______。
②往滤渣中加盐酸,发现有气泡产生,则反应后滤渣中一定有的是______,滤液中一定含有的溶质是
______,一定不含有的溶质是______。
的
(3)如图2是工业炼铁示意图。其中,焦炭 作用是燃烧提供能量和______;有铁生成的化学方程式为
______。
17. 某学校化学学习小组设计出下图所示装置,并进行白磷燃烧实验。
(1)当烧杯内的水受热,温度计显示30℃时,打开活塞,盛有水的试管中有气泡均匀逸出,白磷未燃烧,关
闭活塞。白磷未燃烧的原因是_______,锥形瓶内反应的化学方程式是_________________。
(2)随着水温升高,温度计显示45℃时,再次打开活塞,白磷在水里燃烧。常言道,水火不相容,水能灭火
的原因是__________,而本实验中白磷在水里还能够燃烧的原因是____________。
(3)本实验装置的A部分还可以用于制取的气体是_________,化学方程式是__________ 。
(4)油类物质燃烧不能用水灭火,原因是油比水轻,油会浮在水面上,用水灭火还会增大油与________的接
触面积,使燃烧更旺。
18. 某同学在实验室里用高锰酸钾和二氧化锰加热制取氧气,实验结束时发现大试管已破裂,请你帮他分
析造成试管破裂的可能原因.(写出三条即可)
三、探究题(本大题共1小题,共13.0分)
19. 加热碳酸氢铵时闻到了刺激性气味,引起了同学们对氨气的兴趣,决定对其进行探究。
(一)探究性质与变化
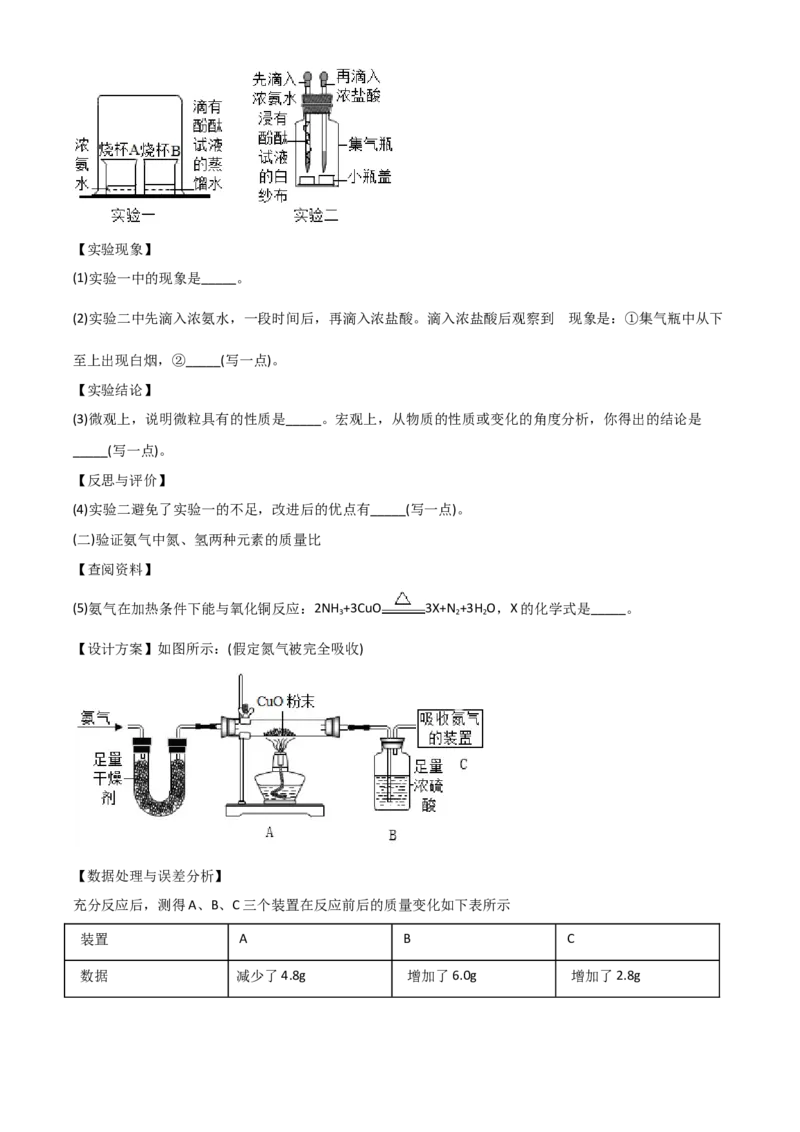
【实验方案】如图所示【实验现象】
(1)实验一中的现象是_____。
的
(2)实验二中先滴入浓氨水,一段时间后,再滴入浓盐酸。滴入浓盐酸后观察到 现象是:①集气瓶中从下
至上出现白烟,②_____(写一点)。
【实验结论】
(3)微观上,说明微粒具有的性质是_____。宏观上,从物质的性质或变化的角度分析,你得出的结论是
_____(写一点)。
【反思与评价】
(4)实验二避免了实验一的不足,改进后的优点有_____(写一点)。
(二)验证氨气中氮、氢两种元素的质量比
【查阅资料】
(5)氨气在加热条件下能与氧化铜反应:2NH +3CuO 3X+N +3H O,X的化学式是_____。
3 2 2
【设计方案】如图所示:(假定氮气被完全吸收)
【数据处理与误差分析】
充分反应后,测得A、B、C三个装置在反应前后的质量变化如下表所示
装置 A B C
数据 减少了4.8g 增加了6.0g 增加了2.8g(6)甲同学利用A、B、C三组装置所提供的数据,乙同学利用B、C两组装置所提供的数据,计算出的氮、
氢元素的质量比都与理论值明显不符,分析产生误差的原因是_____。
(7)若用A、C两组装置所提供的数据计算,与理论值是否相符?写出简单的计算过程证明你的结论_____。
(三)探究用途与制法
(8)在一定条件下,可用氮气和氢气制得氨气。工业上常用氨气生产氮肥(NH ) SO ,施肥时,要避免与之混
4 2 4
用的是_____(填序号)。
A.硝酸钾 B.草木灰(主要成分是K CO )
2 3
C.熟石灰 D.氯化钾
(9)工业上生产的(NH ) SO 中常常混有少量KCl,检验其是否含有KCl的操作方法是_____。
4 2 4