文档内容
2025-2026 学年高二化学上学期第一次月考卷
已知: (g)= (g)+H(g) ΔH= +100.3 kJ·mol-1 ①
2 1
(考试时间:60 分钟 试卷满分:100 分) (g)+I 2 (g)= (g)+2HI(g) ΔH 2 = +89.3 kJ·mol-1 ②
注意事项:
则氢气和碘蒸气反应生成碘化氢气体的热化学方程式为
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考证号
A.H (g)+I (s)=2HI(g) ΔH= -11.0 kJ·mol-1
填写在答题卡上。 2 2
2.回答第Ⅰ卷时,选出每小题答案后,用 2B 铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮 B.H 2 (g)+I 2 (g)=2HI(g) ΔH= -11.0 kJ·mol-1
擦干净后,再选涂其他答案标号。写在本试卷上无效。 C.H +I =2HI ΔH= -11.0 kJ·mol-1
2 2
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
D.H 2 (g)+I 2 (g)=2HI(g) ΔH= +11.0 kJ·mol-1
19
4.测试范围:第一章~第二章第二节(人教版 20 )。
4.下列依据热化学方程式得出的结论正确的是
5.难度系数:0.6
A.若 C(石墨,s)=C(金刚石,s) AH>0,则石墨比金刚石稳定
6.考试结束后,将本试卷和答题卡一并交回。
B.2H (g)+O (g)==2H O(g) ΔH=-483.6kJ·mol-1,则 H 的燃烧热为 241.8kJ•mol-1
2 2 2 2
可能用到的相对原子质量:H 1 C 12 O 16
C.已知 NaOH(aq)+ HCl(aq)=NaCl(aq) +H O(1) ΔH=-57.3kJ·mol-1,则 20.0 gNaOH 固体与稀盐酸完全中和,
2
第Ⅰ卷(选择题 共 60 分)
放出 28.65kJ 的热量
一、选择题:本题共 20 个小题,每小题 3 分,共 60 分。在每小题给出的四个选项中,只有一项是符合题目
D.已知 2C(s)+2O (g)=2CO (g) ΔH 2C(S)+O (g)--2CO(g) ΔH 则ΔH >ΔH
2 2 1 2 2 1 2
要求的。
5.在 36g 碳不完全燃烧所得气体中,CO 占 体积, 占 体积,且
1.天工开物中有“煤饼烧石成灰”的记载。“烧石成灰”指高温条件下碳酸钙转化为生石灰。下列反应中能
量变
; 。与这些碳完全燃烧相比,损失的热量是
化与“烧石成灰”一致的是
A.乙醇燃烧 B.酸碱中和 A.221kJ B.283kJ C.566kJ D.345kJ
C.铝热反应 D.氢氧化钡与氯化铵的反应 6.碳酸钠晶体( )失水可得到 或 ,两个反应过程中的能量变化如
2.已知电解液态水制备 和 的能量变化如图所示: 图所示,下列说法错误的是
则下列表示 在足量氧气中完全燃烧的热化学方程式正确的是
A.
B.
C. A.
B.向 Na CO (s)中滴加几滴水,温度升高
D. 2 3
C.反应
3.环戊二烯( )是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。
D.向 2mL 1mol/L 醋酸溶液中滴加 1mol/L Na CO 溶液,有气泡产生,由此推测:醋酸酸性更强
2 3
试题 第 1 页(共 8 页) 试题 第 2 页(共 8 页)7.某小组用如下图所示简易量热计进行中和反应反应热的测定。近似处理实验所用酸、碱溶液的密度为 1.0g· 表所示:
cm⁻ 、比热容为 4.2J/(g·℃),忽略量热计的比热容。三次实验数据如下表所示:
3
实验 速率
① 0.10 0.10 v
② 0.20 0.10 2v
③ 0.20 0.40 4v
④ 0.40 a 12v
反应前体系的温度/℃
实验 反应后体系温 温度差平均
下列说法错误的是
次数 50mL 0.50mol/L 50mL 0.55mol/L 平均 度/℃ 值/℃
盐酸 NaOH 溶液 值 A. , B.其他条件相同,升高温度,速率常数(k)增大
1 24.9 25.1 28.2 C.体积不变时通入 气,压强增大,反应速率加快 D.表格中,
2 24.8 25.2 27.0 ∆t
10.一定条件下,向某密闭容器中充入 HI,发生反应:2HI(g) H (g)+I (g) ΔH >0,达到平衡状态。该
2 2
3 25.0 25.0 28.2
反应经过以下两步基元反应完成:
设该实验放热为 Q,理论上放热为 Q 理论。下列说法不正确的是
①2HI → 2H + 2I ΔH ②2I→I ΔH
1 2 2
A.从实验装置上看,还缺少的仪器为温度计
下列分析不正确的是
B.∆t=2.8℃
A.ΔH <0、ΔH >0
1 2
C.计算得 Q=1.344kJ
B.反应物的分子必须发生碰撞才能发生基元反应
D.Q 比 Q 理论略微偏小的原因可能是量取溶液体积时俯视量筒读数
C.缩小容器体积,①的反应速率增大
8.如图为两种制备硫酸的途径(反应条件略),下列说法不正确的是
D.加入催化剂,能降低该反应的活化能
11.某实验小组以 H O 分解为例,研究浓度、催化剂对该反应速率的影响。在常温下按如下方案完成实验。
2 2
实验编号 反应物 催化剂
① 10mL2%H O 溶液 无
2 2
② 无
MnO 粉末
A.途径①和途径②的反应热是不相等的 ③ 10mL4%H 2 O 2 溶液 2
下列说法不正确的是
B.含 的浓溶液、含 的稀溶液,分别与足量的 溶液反应,二者放出的热量是相
A.实验①和②对比研究的是 H O 溶液的浓度对该反应速率的影响
2 2
等的
B.实验②和③对比研究的是催化剂对该反应速率的影响
C. 在空气中燃烧放出的热量大于在纯氧中燃烧放出的热量
C.实验②的反应物应为 5mL 2%H O 溶液
2 2
D.若 ,则 为放热反应
D.实验③的反应速率应比实验①的快
9.一定条件下,反应 的速率方程为 ,k 为速率常数(只与温度、 12.NO 和 CO 是环境污染性气体,可在 表面转化为无害气体,有关化学反应的物质变化过程及能量
2
催化剂、接触面积有关,与浓度无关),m、n 是反应级数,可以是整数、分数。实验测得速率与浓度关系如 变化过程分别如图甲、乙所示。下列说法不正确的是
试题 第 7 页(共 8 页) 试题 第 8 页(共 8 页)A.用排饱和食盐水法收集氯气
B.实验室制备乙酸乙酯时,将乙酸乙酯不断蒸出
C.高炉炼铁时,将焦炭和铁矿石预先粉碎
D.夏天打开可乐有大量泡沫溢出
16.治理汽车尾气中 NO 和 CO 污染的一种方法的反应原理为 ,某一
温度下,其化学平衡常数 。下列说法正确的是
A.总反应的
A.反应达到平衡时,CO、NO 的转化率相等
B.为了实现转化,需不断向反应器中补充 和
B.化学平衡常数的表达式为
C.该反应正反应的活化能小于逆反应的活化能
D.CO 为还原剂
C.此温度下,因 K 值较大,故化学反应速率较快
13.在气体反应体系中,能使反应物中活化分子数和活化分子百分数同时增加的方法是
D.加入催化剂,反应物的活化分子百分数增大,有效碰撞次数增多,反应速率增大
①增大反应物浓度 ②增大压强 ③升高温度 ④加入催化剂
17.在一绝热的恒容容器中,发生反应: ,下列描述中能表明反应已达到平衡状
A.①③ B.②③ C.③④ D.②④
态是
14.为研究反应 的反应进程中的能量变化,在 和 的混合溶液
①某时刻 v(B)=2v(C)且不等于零
中加入 ,过程变化如下: ②单位时间内生成 nmolB,同时生成 2nmolC
③B 的浓度不变
④混合气体的平均相对分子质量不变
⑤混合气体的压强不变
⑥混合气体的密度不变
⑦容器内 A、C、D 三种气体的浓度之比为
3∶2∶1
⑧
反应机理如下:
容器内温度不变
A.④⑤⑥⑦⑧ B.②④⑤⑥⑧ C.①②⑥⑦⑧ D.②③⑤⑥⑦
第一步:
18.在催化剂作用下,向 1L 密闭容器中加入 X 和 Y,发生反应:X(g)+2Y(s) 2Z(s),X 的转化率
第二步: 随温度的变化如图所示。下列说法不正确的是
下列有关该反应的说法正确的是
A. (已知其中有 2 个 O 为-1 价)中 S 元素化合价为+7
B.总反应是吸热反应
C.第一步基元反应是该反应的决速步骤
D. 改变了总反应的反应历程和焓变
A.该反应ΔH>0
15.下列事实不能用勒夏特列原理解释的是
B.使用更高效的催化剂,可能使 b 点移动到 d 点
试题 第 1 页(共 8 页) 试题 第 2 页(共 8 页)二、填空题(除标注外,每空 2 分,共 40 分)
C.400℃,反应的平衡常数 K=0.4
D.bc 段变化的原因可能是 400℃以上催化剂活性降低 21.甲烷是一种在日常生活及有机合成中用途十分广泛的气体。我校某化学研究小组的同学对甲烷在高温下
气相裂解反应的原理及其应用展开了研究。
19.模拟工业合成氨在恒温恒容的密闭容器中发生如下反应: 。 时刻
(1)甲烷的电子式为 。
到达平衡后,在 时刻改变某一条件,其反应过程如图所示,下列说法正确的是
(2)已知 CH (g)+2O (g)=CO (g)+2H O(l) △H =-890.4kJ•mol-1
4 2 2 2 1
C H (g)+ O (g)=2CO (g)+H O(l) △H =-1299.6kJ•mol-1
2 2 2 2 2 2
2H (g)+O (g)=2H O(l) △H =-571.6kJ•mol-1
2 2 2 3
则甲烷气相裂解反应:2CH(g) C H (g)+3H (g)的△H= 。
4 2 2 2
(3)该研究小组在研究过程中发现:当甲烷分解时,lgX(X 表示平衡时的气体分压)与温度(℃)的关系如图所示:
A.Ⅰ、Ⅱ两过程到达平衡时,平衡常数:
B.Ⅰ、Ⅱ两过程到达平衡时, 的体积分数:Ⅰ<Ⅱ
C. 时刻改变的条件可以是向密闭容器中加 和 混合气
D.Ⅰ、Ⅱ两过程到达平衡的标志:混合气体的密度不再变化
20. 与 重整技术是获得合成气 、 、实现碳中和的重要途径之一、在一定条件下,向密闭容 ①T 1 ℃时,向 2L 恒容密闭容器中充入 0.3molC 2 H 4 只发生反应 2C 4 H (g) C 2 H 4 (g)+2H 2 (g),达到平衡时测得 c
(C H )=c(CH ),此时 CH 的转化率为 (结果保留一位小数)。
器中通入物质的量均为 的 和 ,发生反应:CH (g)+CO (g) 2CO(g)+2H(g),测得平衡时 的 2 4 4 4
4 2 2
②对上述平衡状态,若改变温度至 T ℃,经 10s 后再次达到平衡时测得 c(CH )=2c(C H ),则 10s 内 C H
2 4 2 4 2 4
转化率与温度、压强的关系如图所示[已知气体分压(p)=总压 物质的量分数,用平衡分压代替平衡浓度可得 的
平均反应速率 v(C H )= ,上述变化过程中 T T。(填“>”或“<”)
2 4 1 2
到平衡常数 Kp]:下列说法正确的是
(4)若容器中发生反应 2CH(g) C H (g)+3H (g),计算该反应在图中温度为 A 点时的压强平衡常数 K =
4 2 2 2 p
(用平衡分压代替平衡浓度)。
22.回答下列问题:
(1)用括号内的字母代号填空:中和热测定实验时,使用的酸和碱最好是 (A.恰好完全反应;B.酸
稍过量;C.碱稍过量),溶液混合的时候应 (A.一次性快速倒入;B.缓缓滴入),若用环形
A.该反应的ΔH<0
铜丝代替环形玻璃搅拌棒,会导致测定数据 (A.偏高;B.偏低)。
B. 点 的生成速率小于氢气的消耗速率
(2)保护环境已成为当前和未来的一项全球性重大课题。为解决目前燃料使用过程中的环境污染问题,并缓解
C. 点对应温度下该反应的平衡常数 能源危机,有的专家提出利用太阳能促进燃料循环使用的构想,如图所示:
D.随着温度升高,对平衡限度的影响:温度小于压强
第 II 卷(非选择题 共 40
分)
试题 第 7 页(共 8 页) 试题 第 8 页(共 8 页)请写出 将 转化成无毒物质的热化学方程式: 。
(2)利用 还原 的反应 的速率方程为 该反应在
不同条件下的反应速率如下:
温度 反应速率
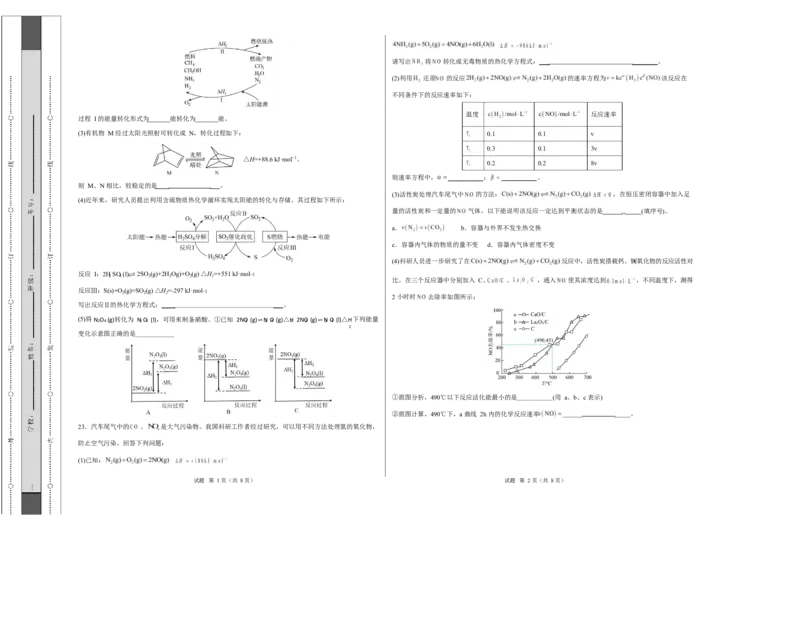
过程 I 的能量转化形式为 能转化为 能。
(3)有机物 M 经过太阳光照射可转化成 N,转化过程如下: 0.1 0.1 v
0.3 0.1 3v
△H=+88.6 kJ·mol−1。
0.2 0.2 8v
则速率方程中, ; 。
则 M、N 相比,较稳定的是 。
(3)活性炭处理汽车尾气中 的方法: ,在恒压密闭容器中加入足
(4)近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。其过程如下所示:
量的活性炭和一定量的 气体,以下能说明该反应一定达到平衡状态的是 (填序号)。
a. b.容器与外界不发生热交换
c.容器内气体的物质的量不变 d.容器内气体密度不变
(4)科研人员进一步研究了在 反应中,活性炭搭载钙、镧氧化物的反应活性对
反应 I:2H
2
SO
4
(l) 2SO
2
(g)+2H
2
Og)+O
2
(g) △H
1
=+551 kJ·mol−1
比。在三个反应器中分别加入 C、 、 ,通入 使其浓度达到 ,不同温度下,测得
反应Ⅲ:S(s)+O
2
(g)=SO
2
(g) △H
2
=-297 kJ·mol−1
2小时时 去除率如图所示:
写出反应Ⅱ的热化学方程式: 。
(5)将N 2O 4(g)转化为 N2 O4 (l),可用来制备硝酸。①已知 2NO2 (g)⇌N2 O4 (g)△H1 2NO2 (g)⇌N2 O4 (l)△H下列能量
2
变化示意图正确的是
①据图分析,490℃以下反应活化能最小的是 (用 a、b、c 表示)
②据图计算,490℃下,a 曲线 2h 内的化学反应速率 。
23.汽车尾气中的 、 是大气污染物。我国科研工作者经过研究,可以用不同方法处理氮的氧化物,
防止空气污染。回答下列问题:
(1)已知:
试题 第 1 页(共 8 页) 试题 第 2 页(共 8 页)