文档内容
2025-2026 学年高二化学上学期第一次月考卷
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考证
号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.测试范围:专题1(苏教版2019选择性必修1)
5.难度系数:0.65
6.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32 Fe 56 Cu 64
第Ⅰ卷(选择题 共 39 分)
一、选择题:本题共 13 个小题,每小题 3 分,共 39 分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
1.下列诗词描述的变化中,放热反应和吸热反应都有发生的是
A.北宋:苏轼《石炭》中“投泥泼水愈光明,烁玉流金见精悍”描写了煤炭的性质
B.北宋王安石(元日》中“爆竹声中一岁除,春风送暖入屠苏”描述了春节的习俗
C.南宋辛弃疾《青玉案》中“东风夜放花千树,更吹落,星如雨”描述元宵夜焰火
D.明于谦《石灰吟》中“粉骨碎身浑不怕,要留清白在人间”用石灰石比拟报国志士
2.下列有关原电池、电解池的说法正确的是
A.原电池的两极一定是由活动性不同的两种金属组成
B.理论上说,任何能自发进行的氧化还原反应都可设计成原电池
C.将镁和铝用导线连接放入氢氧化钠溶液中组成原电池,镁电极作为负极
D.在电解精炼铜装置中,粗铜为阳极材料,精铜为阴极材料,电解质溶液为 溶液,电解一段时
间后, 溶液浓度不变
3.保护钢铁有利于节约资源、保护环境,下列钢铁的保护方法中不正确的是
A.铁栅栏上涂上油漆 B.铁闸与直流电源正极相连
C.轮船底部镶嵌锌块 D.家用铁锅水洗后及时擦干
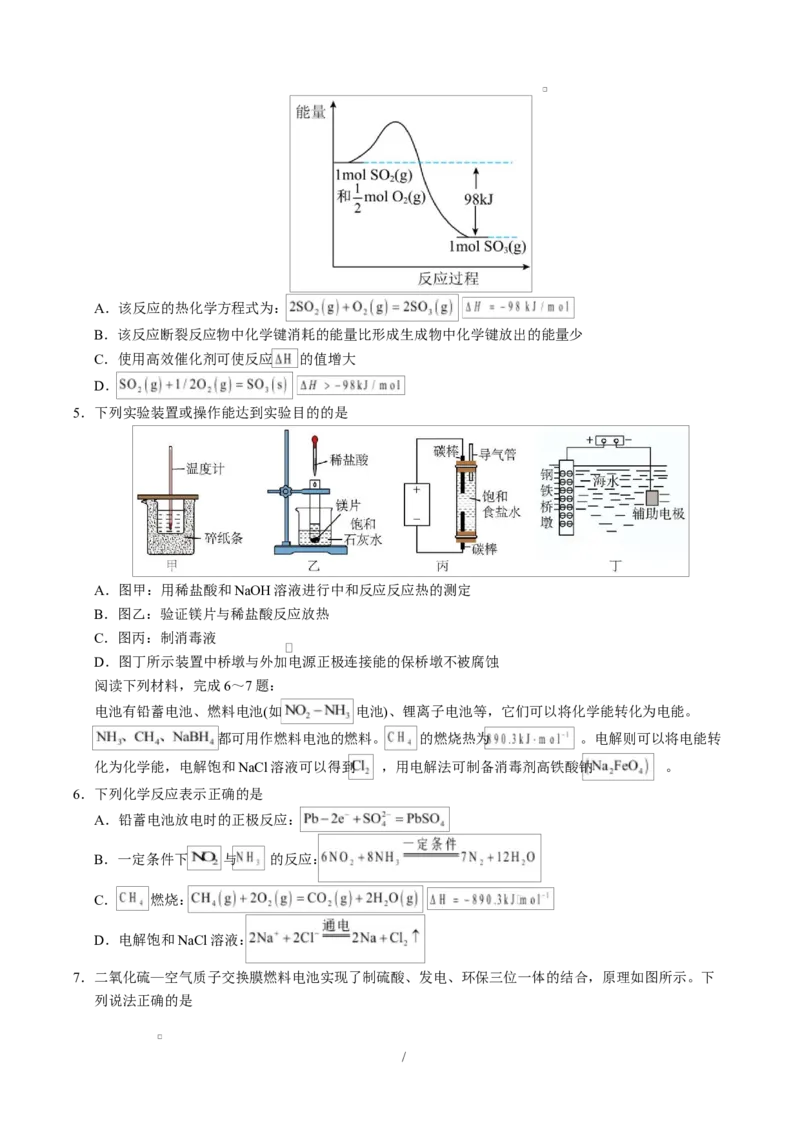
4.接触法制硫酸生产中的关键工序是 的催化氧化,该反应过程中能量变化如图所示,下列说法正确的
是
/A.该反应的热化学方程式为:
B.该反应断裂反应物中化学键消耗的能量比形成生成物中化学键放出的能量少
C.使用高效催化剂可使反应 的值增大
D.
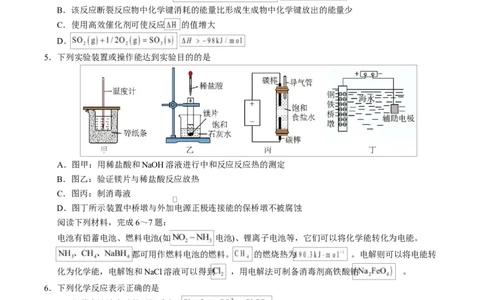
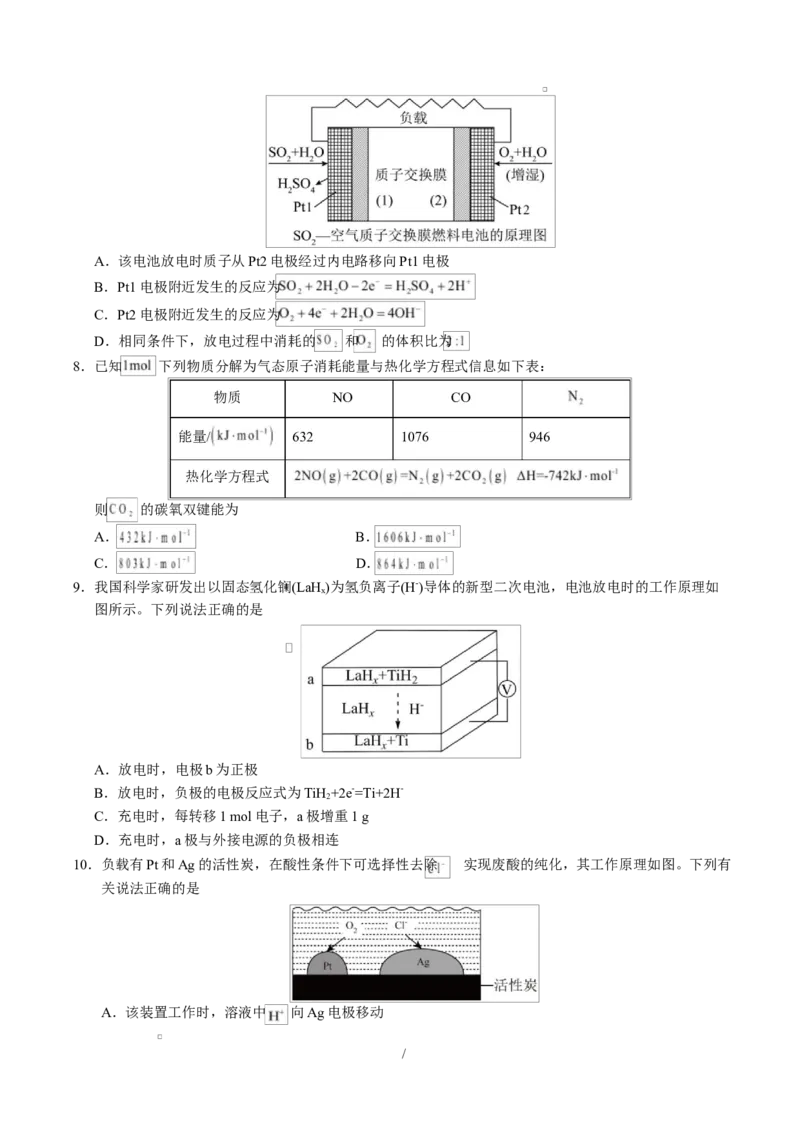
5.下列实验装置或操作能达到实验目的的是
A.图甲:用稀盐酸和NaOH溶液进行中和反应反应热的测定
B.图乙:验证镁片与稀盐酸反应放热
C.图丙:制消毒液
D.图丁所示装置中桥墩与外加电源正极连接能的保桥墩不被腐蚀
阅读下列材料,完成6~7题:
电池有铅蓄电池、燃料电池(如 电池)、锂离子电池等,它们可以将化学能转化为电能。
都可用作燃料电池的燃料。 的燃烧热为 。电解则可以将电能转
化为化学能,电解饱和NaCl溶液可以得到 ,用电解法可制备消毒剂高铁酸钠 。
6.下列化学反应表示正确的是
A.铅蓄电池放电时的正极反应:
B.一定条件下 与 的反应:
C. 燃烧:
D.电解饱和NaCl溶液:
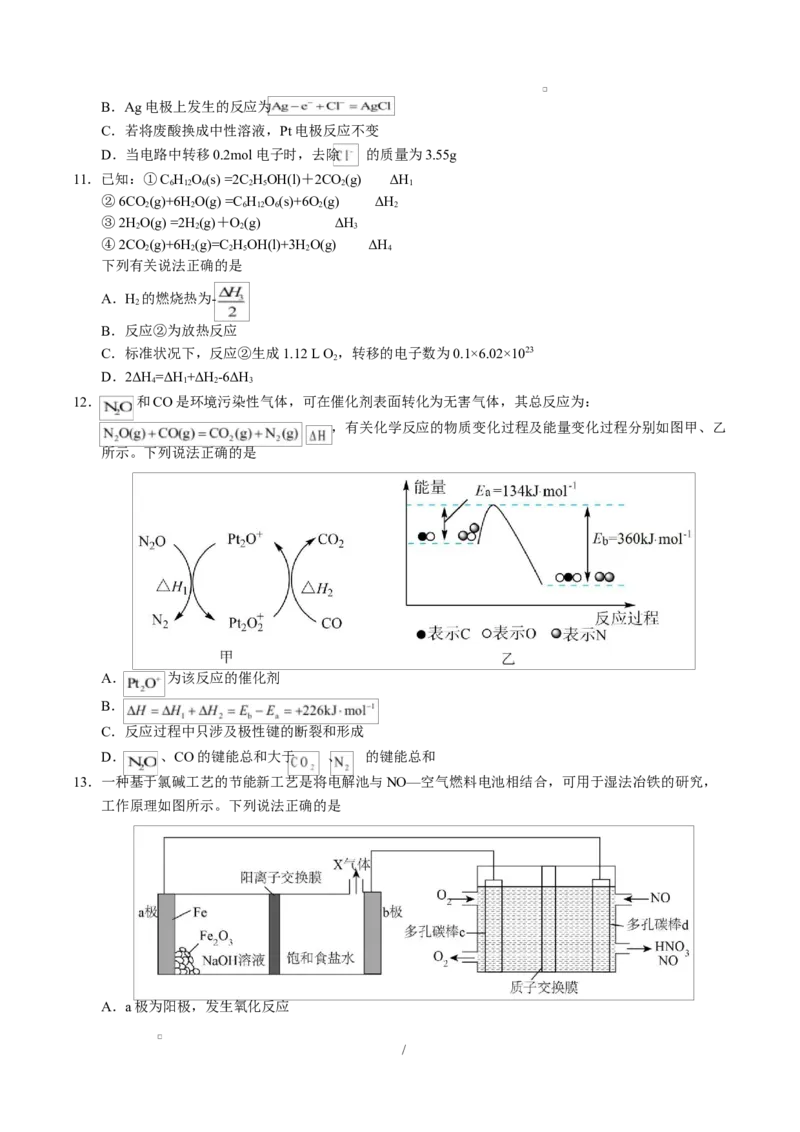
7.二氧化硫—空气质子交换膜燃料电池实现了制硫酸、发电、环保三位一体的结合,原理如图所示。下
列说法正确的是
/A.该电池放电时质子从Pt2电极经过内电路移向Pt1电极
B.Pt1电极附近发生的反应为
C.Pt2电极附近发生的反应为
D.相同条件下,放电过程中消耗的 和 的体积比为
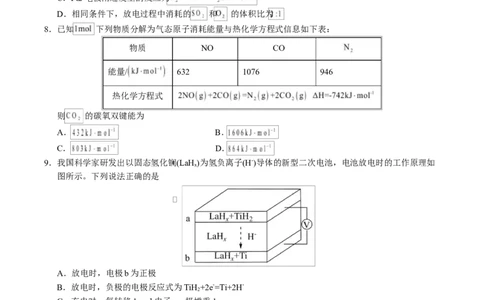
8.已知 下列物质分解为气态原子消耗能量与热化学方程式信息如下表:
物质 NO CO
能量/ 632 1076 946
热化学方程式
则 的碳氧双键能为
A. B.
C. D.
9.我国科学家研发出以固态氢化镧(LaH )为氢负离子(H-)导体的新型二次电池,电池放电时的工作原理如
x
图所示。下列说法正确的是
A.放电时,电极b为正极
B.放电时,负极的电极反应式为TiH +2e-=Ti+2H-
2
C.充电时,每转移1 mol电子,a极增重1 g
D.充电时,a极与外接电源的负极相连
10.负载有Pt和Ag的活性炭,在酸性条件下可选择性去除 实现废酸的纯化,其工作原理如图。下列有
关说法正确的是
A.该装置工作时,溶液中 向Ag电极移动
/B.Ag电极上发生的反应为
C.若将废酸换成中性溶液,Pt电极反应不变
D.当电路中转移0.2mol电子时,去除 的质量为3.55g
11.已知:①C H O(s) =2C HOH(l)+2CO(g) ΔH
6 12 6 2 5 2 1
② 6CO (g)+6HO(g) =C H O(s)+6O(g) ΔH
2 2 6 12 6 2 2
③ 2H O(g) =2H (g)+O(g) ΔH
2 2 2 3
④ 2CO (g)+6H(g)=C HOH(l)+3H O(g) ΔH
2 2 2 5 2 4
下列有关说法正确的是
A.H 的燃烧热为-
2
B.反应②为放热反应
C.标准状况下,反应②生成1.12 L O ,转移的电子数为0.1×6.02×1023
2
D.2ΔH=ΔH +ΔH -6ΔH
4 1 2 3
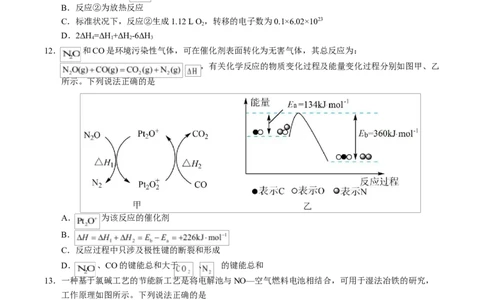
12. 和CO是环境污染性气体,可在催化剂表面转化为无害气体,其总反应为:
,有关化学反应的物质变化过程及能量变化过程分别如图甲、乙
所示。下列说法正确的是
A. 为该反应的催化剂
B.
C.反应过程中只涉及极性键的断裂和形成
D. 、CO的键能总和大于 、 的键能总和
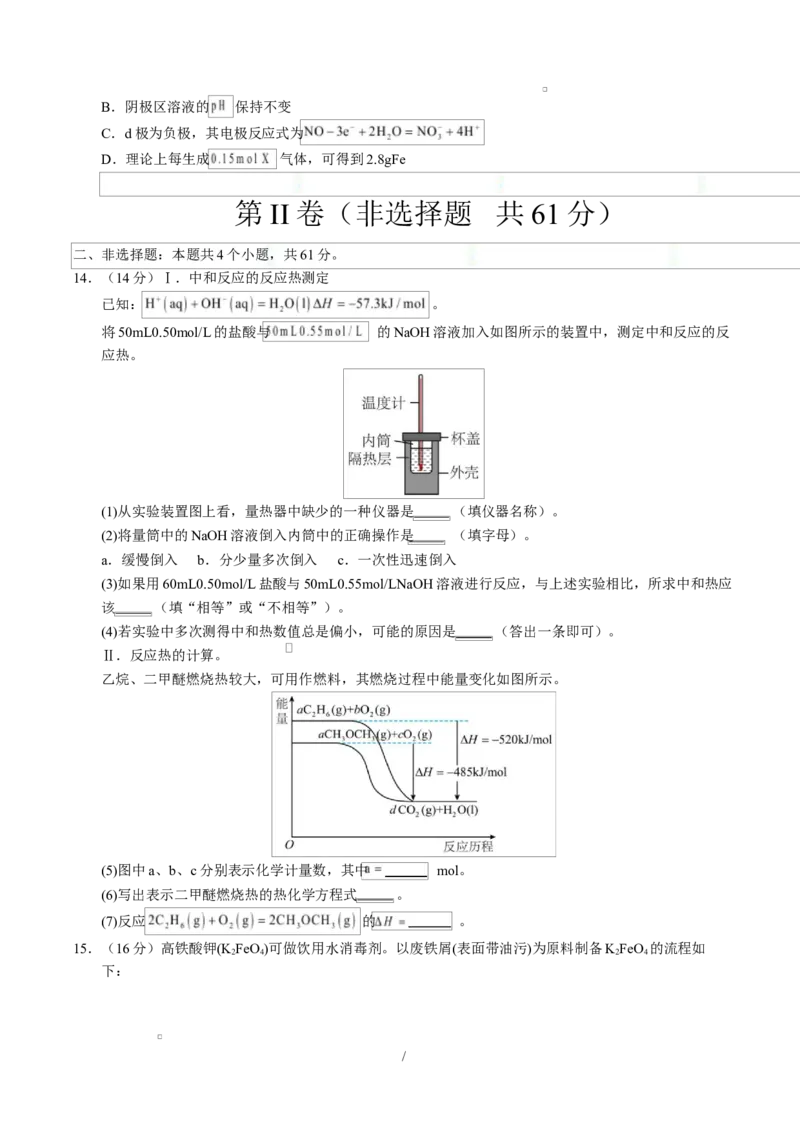
13.一种基于氯碱工艺的节能新工艺是将电解池与NO—空气燃料电池相结合,可用于湿法冶铁的研究,
工作原理如图所示。下列说法正确的是
A.a极为阳极,发生氧化反应
/B.阴极区溶液的 保持不变
C.d极为负极,其电极反应式为
D.理论上每生成 气体,可得到2.8gFe
第 II 卷(非选择题 共 61 分)
二、非选择题:本题共4个小题,共61分。
14.(14分)Ⅰ.中和反应的反应热测定
已知: 。
将50mL0.50mol/L的盐酸与 的NaOH溶液加入如图所示的装置中,测定中和反应的反
应热。
(1)从实验装置图上看,量热器中缺少的一种仪器是 (填仪器名称)。
(2)将量筒中的NaOH溶液倒入内筒中的正确操作是 (填字母)。
a.缓慢倒入 b.分少量多次倒入 c.一次性迅速倒入
(3)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所求中和热应
该 (填“相等”或“不相等”)。
(4)若实验中多次测得中和热数值总是偏小,可能的原因是 (答出一条即可)。
Ⅱ.反应热的计算。
乙烷、二甲醚燃烧热较大,可用作燃料,其燃烧过程中能量变化如图所示。
(5)图中a、b、c分别表示化学计量数,其中 mol。
(6)写出表示二甲醚燃烧热的热化学方程式 。
(7)反应 的 。
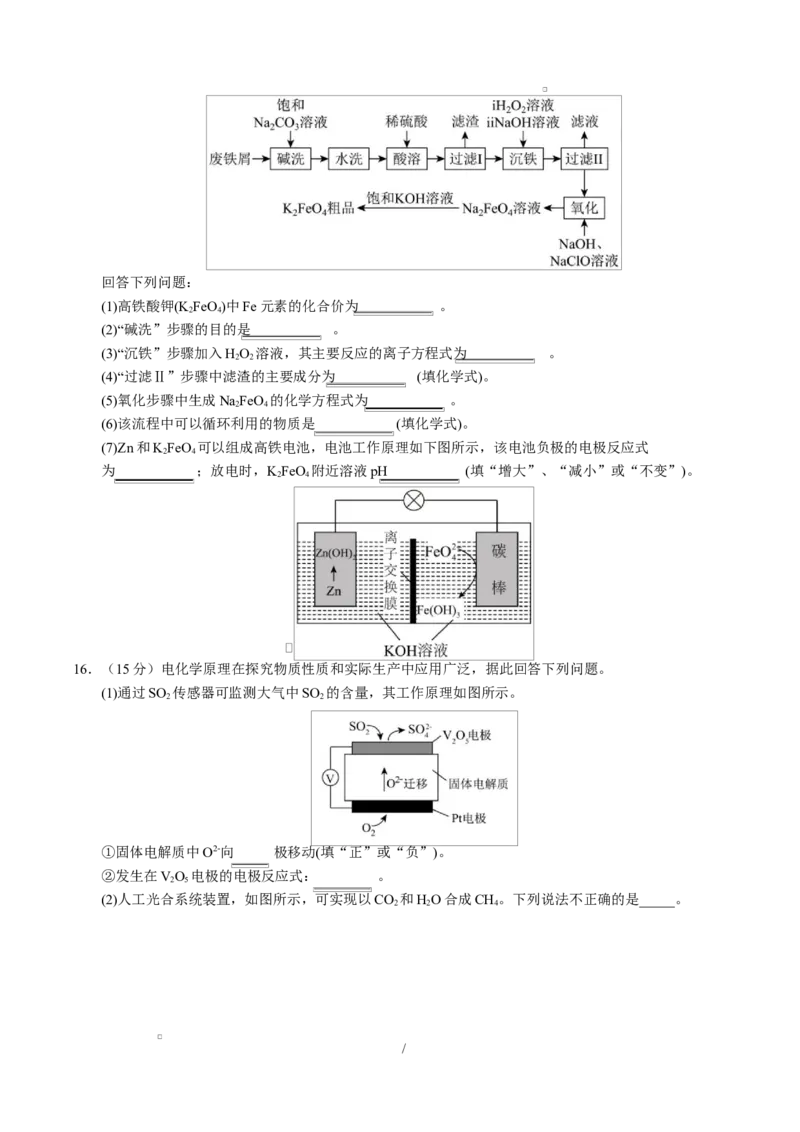
15.(16分)高铁酸钾(K FeO)可做饮用水消毒剂。以废铁屑(表面带油污)为原料制备KFeO 的流程如
2 4 2 4
下:
/回答下列问题:
(1)高铁酸钾(K FeO)中Fe元素的化合价为 。
2 4
(2)“碱洗”步骤的目的是 。
(3)“沉铁”步骤加入HO 溶液,其主要反应的离子方程式为 。
2 2
(4)“过滤Ⅱ”步骤中滤渣的主要成分为 (填化学式)。
(5)氧化步骤中生成NaFeO 的化学方程式为 。
2 4
(6)该流程中可以循环利用的物质是 (填化学式)。
(7)Zn和KFeO 可以组成高铁电池,电池工作原理如下图所示,该电池负极的电极反应式
2 4
为 ;放电时,KFeO 附近溶液pH (填“增大”、“减小”或“不变”)。
2 4
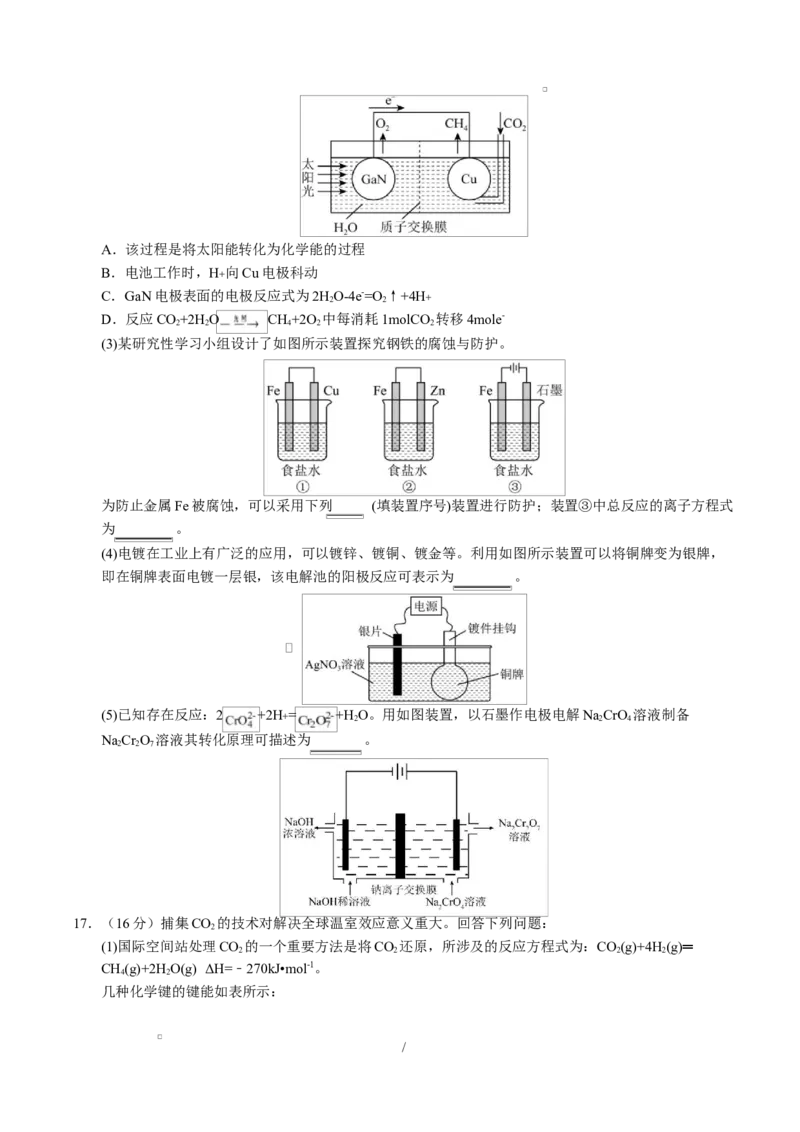
16.(15分)电化学原理在探究物质性质和实际生产中应用广泛,据此回答下列问题。
(1)通过SO 传感器可监测大气中SO 的含量,其工作原理如图所示。
2 2
①固体电解质中O2-向 极移动(填“正”或“负”)。
②发生在VO 电极的电极反应式: 。
2 5
(2)人工光合系统装置,如图所示,可实现以CO 和HO合成CH。下列说法不正确的是_____。
2 2 4
/A.该过程是将太阳能转化为化学能的过程
B.电池工作时,H+ 向Cu电极科动
C.GaN电极表面的电极反应式为2H
2
O-4e-=O
2
↑+4H+
D.反应CO+2H O CH+2O 中每消耗1molCO 转移4mole-
2 2 4 2 2
(3)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。
为防止金属Fe被腐蚀,可以采用下列 (填装置序号)装置进行防护;装置③中总反应的离子方程式
为 。
(4)电镀在工业上有广泛的应用,可以镀锌、镀铜、镀金等。利用如图所示装置可以将铜牌变为银牌,
即在铜牌表面电镀一层银,该电解池的阳极反应可表示为 。
(5)已知存在反应:2 +2H+= +H
2
O。用如图装置,以石墨作电极电解Na
2
CrO
4
溶液制备
NaCr O 溶液其转化原理可描述为 。
2 2 7
17.(16分)捕集CO 的技术对解决全球温室效应意义重大。回答下列问题:
2
(1)国际空间站处理CO 的一个重要方法是将CO 还原,所涉及的反应方程式为:CO(g)+4H(g)═
2 2 2 2
CH(g)+2HO(g) ΔH=﹣270kJ•mol-1。
4 2
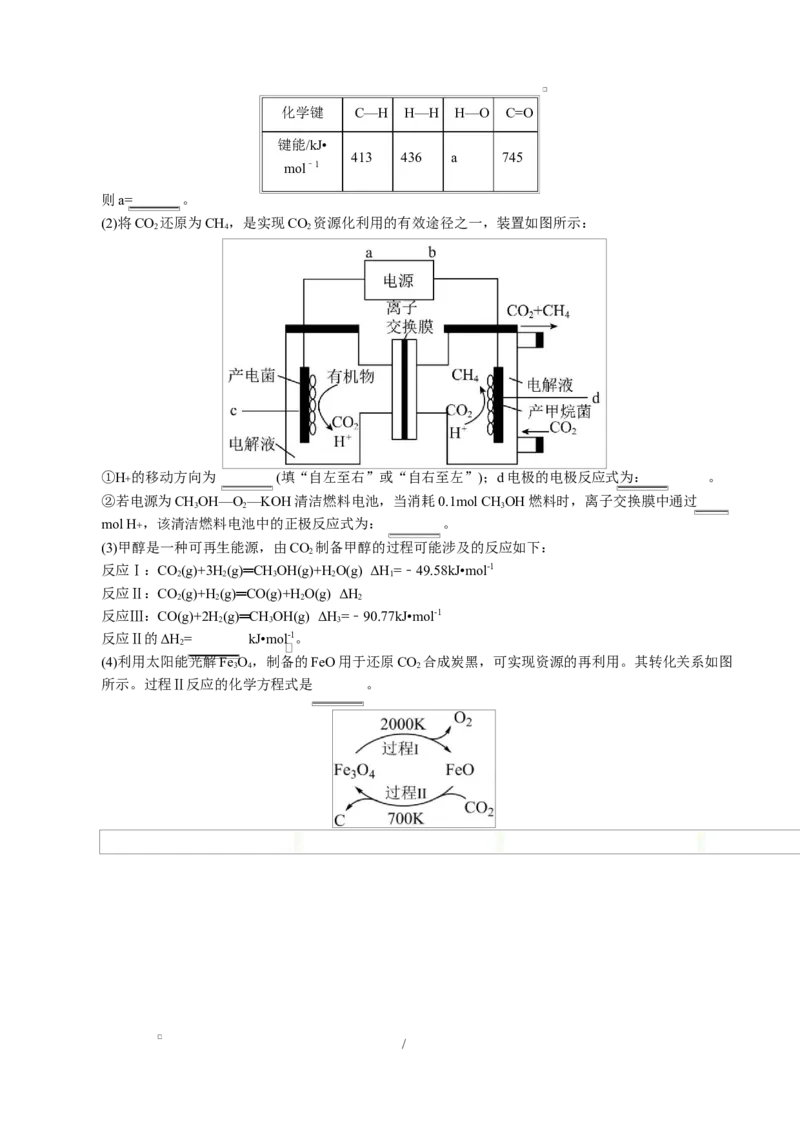
几种化学键的键能如表所示:
/化学键 C—H H—H H—O C=O
键能/kJ•
413 436 a 745
mol﹣1
则a= 。
(2)将CO 还原为CH,是实现CO 资源化利用的有效途径之一,装置如图所示:
2 4 2
①H+ 的移动方向为 (填“自左至右”或“自右至左”);d电极的电极反应式为: 。
②若电源为CHOH—O—KOH清洁燃料电池,当消耗0.1mol CH OH燃料时,离子交换膜中通过
3 2 3
mol H+ ,该清洁燃料电池中的正极反应式为: 。
(3)甲醇是一种可再生能源,由CO 制备甲醇的过程可能涉及的反应如下:
2
反应Ⅰ:CO(g)+3H(g)═CH OH(g)+H O(g) ΔH=﹣49.58kJ•mol-1
2 2 3 2 1
反应Ⅱ:CO(g)+H(g)═CO(g)+H O(g) ΔH
2 2 2 2
反应Ⅲ:CO(g)+2H(g)═CH OH(g) ΔH=﹣90.77kJ•mol-1
2 3 3
反应Ⅱ的ΔH= kJ•mol-1。
2
(4)利用太阳能光解Fe O,制备的FeO用于还原CO 合成炭黑,可实现资源的再利用。其转化关系如图
3 4 2
所示。过程Ⅱ反应的化学方程式是 。
/