文档内容
2024~2025学年度2022级高三下学期开学考试答案
1.D
【详解】A.透闪石属于硅酸盐,A错误。
B.喀斯特地貌主要是石灰岩(碳酸钙)地区的特殊地貌。在水的参与下,水中溶解的二氧化碳与碳酸钙
发生化学反应,生成碳酸氢钙,化学方程式为CaCO +CO +H O=Ca(HCO )。当溶蚀后的碳酸氢钙溶液受
3 2 2 3 2
热或压力改变时,碳酸氢钙又会分解为碳酸钙重新沉淀(Ca(HCO )=CaCO +CO +H O),日积月累便形
3 2 3 2 2
成了石林、溶洞等喀斯特地貌,B错误。
C.焰色试验不属于吸收光谱,而是属于发射光谱 。当金属或其化合物在无色火焰中灼烧时,原子中的
电子吸收能量,从能量较低的轨道跃迁到能量较高的轨道,处于激发态。而激发态是不稳定的,电子会
很快跃迁回能量较低的轨道,将多余的能量以光的形式放出。由于不同元素的原子结构不同,电子跃迁
时能量的变化也不同,发出光的波长也不同,因此会使火焰呈现出不同的颜色,C错误。
D.柳絮主要成分是纤维素、木质素、半纤维素等。纤维素在酸或纤维素酶等催化剂的作用下,能够逐步
水解,最终可以得到葡萄糖,D正确。
2.A
【详解】B.电负性:N>H,NH 中N原子带负电荷、H原子带正电荷,B错误。
3
C.NH NH 的结构式应为 ,C错误。
2 2
D.Fe失电子变成Fe2+,失去的是4s能级上的电子,基态Fe2+的价层电子排布式应为3d6,D错误。
3.C
【详解】A.NaOH会腐蚀托盘天平的托盘,应把NaOH放在小烧杯中称量,A错误。
B.配制标准溶液定容时应平视液体凹液面,B错误。
D.滴定管选择错误,且锥形瓶中未滴加指示剂,D错误。
4.D
【详解】A.对比X、Y的结构简式可知,X中醛基与HN-R中氨基发生加成反应,碳原子杂化方式由
2
sp2变为sp3,A正确。
B.由题可知,反应II形成了C=N双键,属于消去反应,B正确。
C.由Y的结构简式可知,羟基所连碳原子为手性碳原子,C正确。
D.苯环为平面结构,C=N双键也为平面结构,但两个平面由碳碳单键连接,碳碳单键可以旋转,两个平
面不一定任何时候重叠,因此虚框中所有原子可能共面,D错误。
5.C
【详解】C.石墨中C-C的键长比金刚石中C-C的键长短,石墨中C-C的键能大,熔沸点高。
6.D
【详解】A.CHCOOH是弱电解质,离子方程式书写时要保留化学式。用白醋除铁锈的离子方程式应
3
为:Fe O·xHO+6CHCOOH=(3+x)H O+2Fe3+ +6CHCOO-,A错误。
2 3 2 3 2 3
B . 泡 沫 灭 火 器 里 装 的 是 Al (SO ) 溶 液 和 NaHCO 溶 液 , 离 子 方 程 式 应 为 : Al3++3HCO
2 4 3 3
—=Al(OH) ↓+3CO ↑,B错误。
3 3 2
C.向漂白液(NaClO溶液)滴加少量洁厕灵(盐酸)会发生氧化还原反应产生 Cl ,离子方程式应为:
2
ClO-+Cl-+2H+=H O+Cl ↑,C错误。
2 2
7.B
【详解】W、X、Y、Z四种主族元素,原子序数依次增大,分别位于三个不同短周期。W和X可形成原
子个数比为2:1的18e—分子,则W和X分别为H元素和N元素,该18e—分子为NH;由Y的原子序数
2 4
等于W与X的原子序数之和可知,Y为O元素;Z核外未成对电子只有1个且在球形原子轨道上,则Z
为Na元素。
A.第一电离能:N>O>H,A正确。
B.O、O 互为同素异形体,但O 是极性分子,B错误。
2 3 3
C.NH 中N原子有1对孤电子对,HO中O原子有2对孤电子对,孤电子对数越多,孤电子对对成键电
3 2
第 1 页 共 6 页子对排斥力越大,键角越小,C正确。
D.NaN与水反应后生成NH ,NH 会使湿润红色石蕊试纸变蓝,D正确。
3 3 3
8.C
【详解】A.NaClO溶液有漂白性,无法用pH试纸测定其pH值,A错误。
B.Fe3+被Fe还原为Fe2+,B错误。
C.向盛有2 mL 0.1mol/L NaCl溶液的试管中滴加2滴0.1mol/L AgNO 溶液,出现白色沉淀,即得到
3
AgCl的悬浊液。然后再滴加4滴0.1mol/L KI溶液,白色沉淀慢慢转化成黄色沉淀,AgCl沉淀变为AgI
沉淀,说明溶解度:AgCl>AgI,二者为同类型沉淀,也可说明K (AgI)T。该反应△H>0,升温平衡正移,故k 增大的倍数
2 2 1 正
大于k 增大的倍数,B错误。
逆
C.平衡后恒温下再加入SiHCl (g),平衡正向移动,但该反应为气体体积不变的反应,再达平衡时
3
x(SiHCl )不变,C正确。
3
D.由图可知,T K温度下,SiHCl 平衡时物质的量的分数为80%,由方程式系数比可知,SiHCl 和
1 3 2 2
SiCl 平衡时物质的量的分数均为10%。又知平衡时v =v =k ·x2 (SiHCl )=k ·x(SiHCl)·x(SiCl ),可
4 正 逆 正 3 逆 2 2 4
得:
k x(SiH Cl )·x(SiCl ) c(SiH Cl )·c(SiCl ) 0.1×0.1 1
正 2 2 4 2 2 4
= = =K= = ,D正确。
k x2 (SiHCl ) c2 (SiHCl ) 0.82 64
逆 3 3
14.D
【详解】A.曲线M表示NH+ 分布分数随pH变化,右侧虚线曲线表示NH ·HO的分布分数随pH变化,
4 3 2
A正确。
B.HCO 的 ,图中pH=8.3时c(CO2- )=c(HCO),此时K ·K =c2(H+)=(10-8.3)2,得到
2 3 3 2 3 a1 a2
HCO 的K =10-10.3,B正确。
2 3 a2
C.由图可知,K (NH ·HO)=10-4.7,HCO 的K =10-6.3,0.1mol·L-1的NH HCO 溶液HCO-的水解程度比
b 3 2 2 3 a1 4 3 3
NH +的大,所以c(NH+ )>c(HCO- ),C正确。
4 4 3
D.25℃时0.1mol·L-1的NH HCO 溶液呈碱性,pH=7时溶液中已加入少量HCl,则此时电荷守恒式为
4 3
c(NH+ )+c(H+)=2c(CO2- )+c(HCO- )+c(Cl-)+c(OH-),把c(H+)=c(OH-)代入上式,可得
4 3 3
c(NH+ )=2c(CO2- )+c(HCO- )+c(Cl-),D错误。
4 3 3
15.(15分)(除特殊标注外,每空各2分)
(1)
(2)①增大反应物接触面积,加快反应速率 ② ③1.9~2.1(1分,在此
范围内都得分)
(3)Cu、Fe
(4)①阳(1分) ②SnS4- + 4e- = Sn + 4S2-
4
1 3 3
(5)4 (1分) ( , , )
4 4 4
【详解】(1)Sn位于第五周期第ⅣA族,其基态价电子排布图为 。
(2)①“焙烧”前对黝锡矿进行研磨,目的是增大反应物接触面积,加快反应速率。
②“滤液”中主要含有的离子为SnS4- 、S2-、Na+等,结合流程中“焙烧”的反应物可知主要发生的化学反
4
应方程式为 。
③由图可知,NaS的量为黝锡矿的量之比为1.9~2.1范围内,Sn的挥发损失率、残留在渣中的Sn几乎为
2
零,溶进溶液中的Sn量达到较高值。
(3)C将Cu、Fe单质还原出来,“滤渣”中可回收的金属是Cu、Fe。
第 3 页 共 6 页(4)“净化”后溶液主要含SnS4- 、Na+等,作电解池阴极区电解液,SnS4- 在阴极得电子生成Sn,阴极的
4 4
电极方程式为SnS4- + 4e- = Sn + 4S2-,纯锡作阴极、惰性电极阳极。
4
(5)灰锡中每个Sn原子以单键与其他4个Sn原子相连在空间构成正四面体,且该Sn原子在正四面体的
体心,所以灰锡中每个Sn原子周围与它最近且距离相等的Sn原子有4个。由晶胞图可知A原子的分数
1 1 1 3 3
坐标为(0,0,0)、C原子的分数坐标为(1, , ),则B原子的分数坐标为( , , )。
2 2 4 4 4
16.(14分)(每空各2分)
(1)球形冷凝管 碱石灰会吸收尾气中SO 和HCl,导致吸收水蒸气能力减弱
2
(2)
(3)取少量反应后固体溶于稀盐酸中,滴加几滴K[Fe(CN) ](铁氰化钾)溶液,若产生蓝色沉淀,则说
3 6
明反应后固体中含有Fe2+
(4)5
(5)①C →C
1 2
②FeCl 和KI的反应是可逆反应,当电流表指针读数为零,说明反应达到平衡状态,再向左烧杯里加入
3
FeCl 固体,Fe2+浓度增大使反应向逆反应方向进行。
2
【详解】(1)仪器X名称为球形冷凝管。仪器P中宜盛放五氧化二磷或无水氯化钙以防止烧杯中蒸发的
水蒸气进入圆底烧瓶,若P中盛放的是碱石灰,碱石灰会吸收尾气中SO 和HCl,导致吸收水蒸气能力减
2
弱。
(2)FeCl ·6HO和足量SOCl 反应的化学方程式: ;
3 2 2
(3)取少量反应后固体溶于稀盐酸中,滴加几滴K[Fe(CN) ](铁氰化钾)溶液,若产生蓝色沉淀,则说
3 6
明反应后固体中含有Fe2+。
(4)若要配制1 L 0.04 mol·L-1的FeCl 溶液,为使配制过程中不出现浑浊现象,OH-的浓度最大为
3
√4.0×10−38
3 mol/L=1×10-12mol/L,则H+浓度为1×10-2mol/L,盐酸溶质的物质的量至少为1×10-2mol,
0.04
溶液体积至少为5×10-3L=5 mL,所以需要2 mol/L的盐酸5 mL。
(5)①由分析可知,Fe3+的氧化性强于I,原电池中C 电极为正极,C 电极为负极,则外电路中电流方
2 1 2
向为C →C 。
1 2
②FeCl 和KI的反应是可逆反应,当电流表指针读数为零,说明反应达到平衡状态,再向左烧杯里加入
3
FeCl 固体,Fe2+浓度增大使反应向逆反应方向进行。
2
17.(14分)(除特殊标注外,每空各2分)
(1)+244.6
(2)低温(1分) K>K =K
a b c
(3)6 (1分)
催化剂
(4)
(5)① I ②80% 0.25
【详解】(1)CH、CO和H 的燃烧热(ΔH)分别为-893kJ· mol-1、-283kJ· mol-1和-285.8kJ· mol-1,可计
4 2
算出CH(g)+CO(g) 2CO(g)+2H(g) △H=[-893-(2×-283)-(2×-285.8)]kJ· mol-1=+244.6kJ· mol-1。
4 2 2
(2)该反应△H<0、△S<0,代入公式△G=△H-T△S<0可知该反应低温下自发。由图可知,a点温度小
于b点,则a点平衡常数大于b点,平衡常数是温度函数,温度不变,平衡常数不变,由图可知,b点温
第 4 页 共 6 页度与c点相同,则b点平衡常数等于c点,所以a、b、c三点平衡常数的大小关系为K>K =K。
a b c
(3)根据循环图易判断中间体为6种。
(4)根据循环图,CO 催化加氢制甲醇,产物有HO,故总反应的化学方程式为
2 2
。
(5)①甲醇分解反应为可逆反应,可逆反应不可能完全反应,则原料中甲醇的物质的量大于消耗甲醇的
物质的量,由方程式可知,转化为甲醛的甲醇的物质的量与产品中甲醛的物质的量相等,则相同温度
时,甲醛的选择性大于甲醇的收率,所以表示选择性的是曲线I。
②由图可知,T℃平衡时,甲醛的收率为60%、选择性为75%,则平衡体系中甲醛的物质的量
1
2mol×60%=1.2mol,消耗的甲醇的物质的量为1.2mol÷75%=1.6mol,由题意可得:
由上述数据可知,甲醇的转化率为 。
平衡时,CHOH的物质的量为0.4mol,HCHO的物质的量为1.2mol,CO的物质的量为0.4mol,H 的物
3 2
质的量为2mol,混合气体的总物质的量为4 mol,CO的物质的量分数为0.1,H 的物质的量分数为0.5,
2
0.1×0.52
CHOH的物质的量分数为0.1,反应II的平衡常数K = =0.25。
3 x
0.1
18.(15分)(除特殊标注外,每空各2分)
(1)1,3,5-苯三酚或间苯三酚(1分)
(2)(酮)羰基(1分) 醚键(1分)
吡啶
(3)
(4)在吡咯中,氮原子的孤对电子参与了大π键的形成,这使得氮原子上的电子云密度降低,从而减弱
了其碱性,故碱性:吡啶>吡咯。
(5)ac
(6)3(1分)
(7)
或 (3分)
【详解】B和乙醇发生取代反应生成C,C中羟基断裂,D中断裂C-Cl键,发生取代反应生成E和HCl,
第 5 页 共 6 页则D为 。
(1)A系统命名为1,3,5-苯三酚或间苯三酚。
(2)C的含氧官能团名称为羟基、(酮)羰基、醚键。
吡啶
(3)C+D→E的化学方程式为 。
(4)吡咯是一个五元杂环化合物,其中氮原子与两个碳原子相连,形成一个环状结构,在吡咯中,氮原
子的孤对电子参与了大π键的形成,这使得氮原子上的电子云密度降低,从而减弱了其碱性,故碱性:
吡啶>吡咯。
(5)G和H分子中的官能团不相同,可用红外光谱鉴别,a正确。G和H分子中都有碳碳双键,都可以
使酸性高锰酸钾溶液褪色,b错误。H分子中有羟基,可与水形成分子间氢键,而G分子中无羟基,故水
溶性H高于G,c正确。
(6)可以发生银镜反应,说明分子中有-CHO;能与NaHCO 溶液反应,说明分子中有-COOH;分子中
3
有两个-CH,考虑顺反异构,可写出满足上述条件的B的同分异构体有3种,分别为 、
3
、 。其中,核磁共振氢谱有三组峰的同分异构体的结构简式为 。
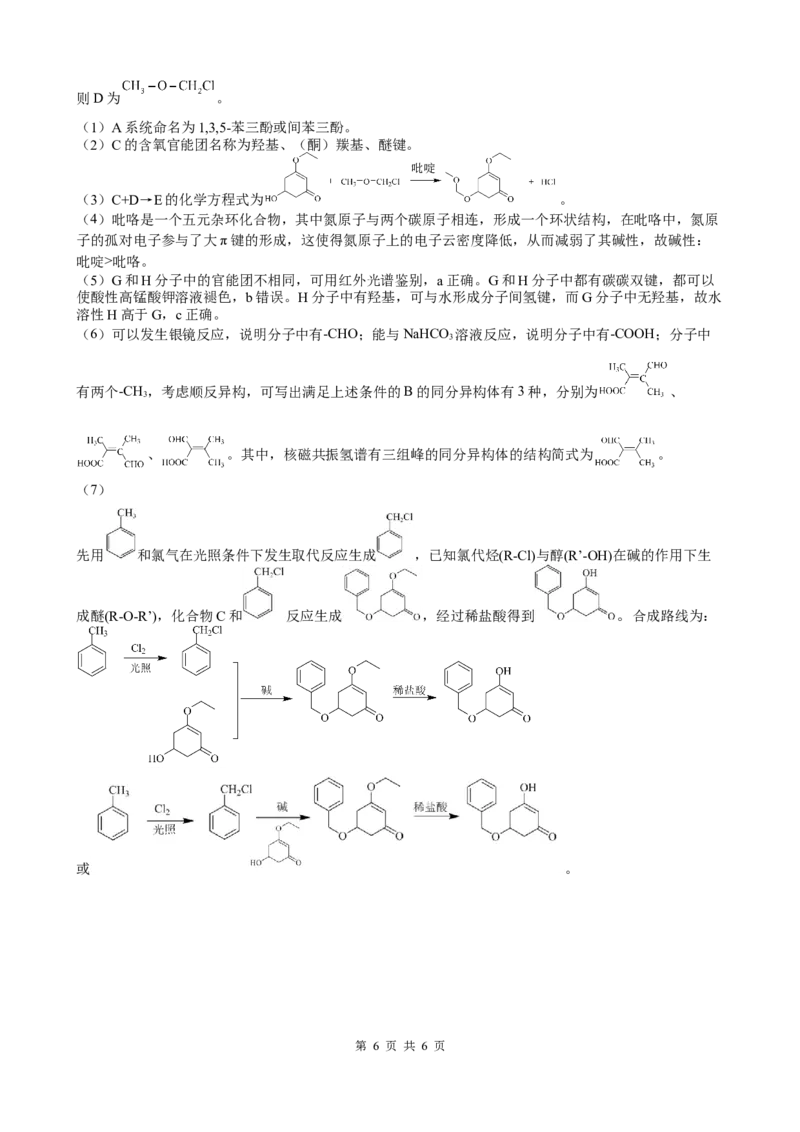
(7)
先用 和氯气在光照条件下发生取代反应生成 ,已知氯代烃(R-Cl)与醇(R’-OH)在碱的作用下生
成醚(R-O-R’),化合物C和 反应生成 ,经过稀盐酸得到 。合成路线为:
或 。
第 6 页 共 6 页