文档内容
山西大学附中
2025~2026 学年第一学期高三年级 10 月模块诊断
化学试题
考试时间:75分钟 考查范围:有机化学和化学反应原理
可能用到的相对原子质量:
一、选择题(每小题只有一个选项符合题意)
1. 近年来,我国科技发展取得了巨大成就。下列说法正确的是
的
A. 高效光解水催化剂能降低化学反应 焓变
B. 运载火箭所采用的“液氢液氧”推进剂可把化学能全部转化为热能
C. 脑机接口融入医疗:植入式电极中的石墨烯属于烯烃
D. 小麦保存时常常采用低温冷冻技术,原因之一是温度低,腐烂速率会减慢
【答案】D
【解析】
【详解】A.催化剂只能降低反应的活化能,不能改变反应的焓变,A错误;
B.化学能无法全部转化为热能,部分会转化为动能等其他形式,B错误;
C.石墨烯是碳的单质,属于无机物,而烯烃是有机物,C错误;
D.低温可降低微生物活性,减缓腐烂速率,D正确;
故选D。
2. 下列化学用语或图示表达正确的是
A. 聚苯乙烯的结构简式:
B. 有机物 的名称:3-醛基戊烷
C. 邻羟基苯甲醛分子内形成的氢键:
D. 用化学方程式表示合成涤纶:
第1页/共28页
学科网(北京)股份有限公司【答案】C
【解析】
【详解】A.聚苯乙烯由苯乙烯(CH=CH-C H)聚合而成,聚苯乙烯的结构简式为: ,
2 6 5
A错误;
B.该有机物含醛基(-CHO),命名时应以含醛基的最长碳链为主链,醛基碳为1号碳,名称应为“2-乙
基丁醛”,B错误;
C.邻羟基苯甲醛中,羟基(-OH)的H与醛基(-CHO)的羰基O距离近,可形成分子内氢键,图示正确
表示了羟基H与醛基O的氢键作用,C正确;
D.涤纶为对苯二甲酸与乙二醇的缩聚产物,n个二元酸(HOOC-C H-COOH)和n个乙二醇
6 4
(HOCH CHOH)反应时,生成一条高分子链,应脱去 分子 ,方程式表示为:
2 2
,D错误;
故选C。
3. 常温下,下列各组粒子在指定溶液中一定能大量共存的是
A. 澄清透明溶液: 、 、 、
B. 由水电离出 为 的溶液: 、 、 、
C. 使甲基橙变红色的溶液: 、 、 、
D. 的溶液中: 、 、 、
【答案】A
【解析】
第2页/共28页
学科网(北京)股份有限公司【详解】A. 、 、 、 相互之间不反应,澄清透明溶液中能共存,故选A;
B.由水电离出 为 的溶液,水电离受到抑制,溶液可能为强酸或强碱性;若酸性,
与 发生氧化还原反应;若碱性, 与OH-反应,故不选B;
C.甲基橙变红说明溶液为酸性, 与H+反应生成Al3+, 与H+生成HSiO 沉淀,故不选
2 3
C;
D.由 得c(H+)=0.1 mol/L,溶液呈酸性, 与H+反应生成CO 和HO,故不
2 2
选D;
选A。
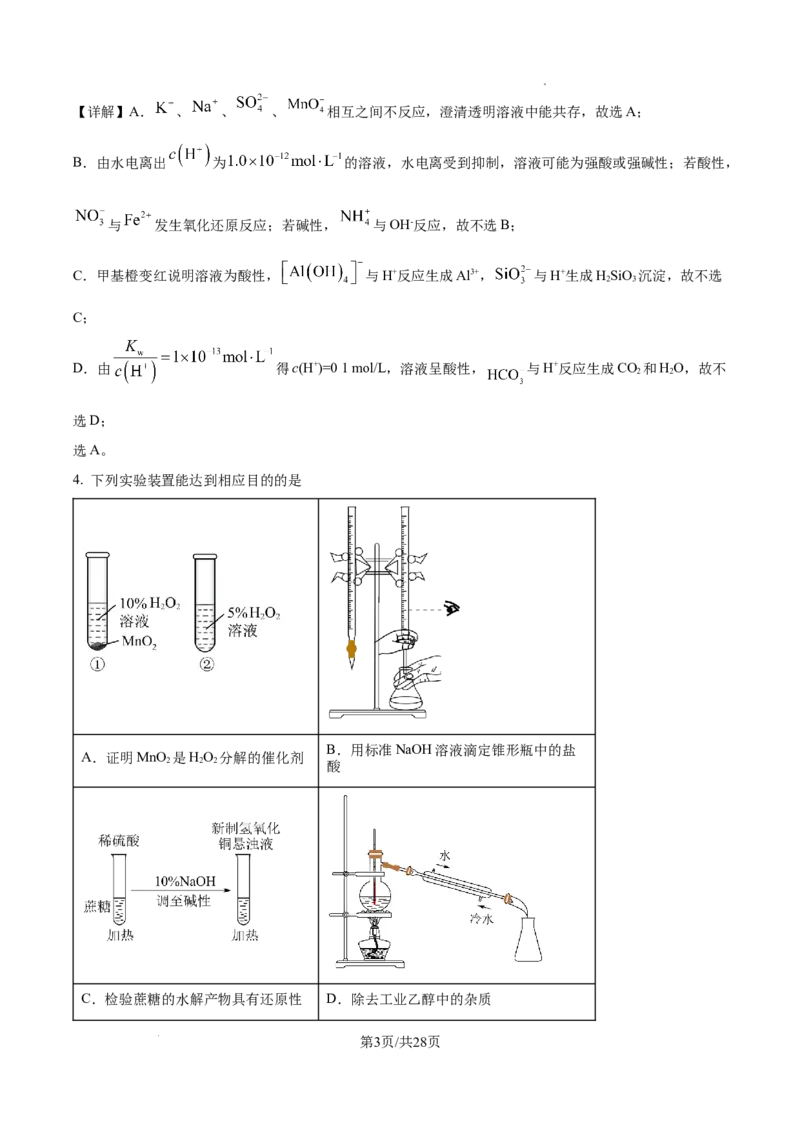
4. 下列实验装置能达到相应目的的是
B.用标准NaOH溶液滴定锥形瓶中的盐
A.证明MnO 是HO 分解的催化剂
2 2 2 酸
C.检验蔗糖的水解产物具有还原性 D.除去工业乙醇中的杂质
第3页/共28页
学科网(北京)股份有限公司A. A B. B C. C D. D
【答案】C
【解析】
【详解】A.要证明MnO 是HO 分解的催化剂,需控制HO 浓度相同,对比有无MnO 时的反应速率,
2 2 2 2 2 2
并验证MnO 质量和化学性质不变,A错误;
2
B.图中左侧是碱式滴定管(橡胶管+玻璃珠),右侧是酸式滴定管(玻璃活塞),应用碱式滴定管盛装标
准NaOH溶液,且滴定过程中,眼睛要盯着锥形瓶中的溶液,观察颜色变化,B错误;
C.蔗糖水解需稀硫酸催化,生成的葡萄糖(还原性糖)与新制氢氧化铜反应需碱性环境,C正确;
D.蒸馏法除去工业乙醇中的杂质,温度计水银球应位于蒸馏烧瓶支管口,以测定馏分温度,D错误;
故选C。
5. 氨磺必利可用于精神分裂症治疗,合成氨磺必利的一种中间体结构简式如图所示。下列关于该中间体的
说法错误的是
A. 能发生加成反应、取代反应、氧化反应、还原反应
B. 与足量氢气加成后的产物中含有5个手性碳原子
C. 一定条件下1 mol该中间体最多与3 mol 发生加成反应
D. 该中间体具有碱性,且①、②、③处的C-N键长相等
【答案】D
【解析】
【详解】A.该中间体含苯环(可加成、取代)、氨基(可氧化、取代)、羰基(可还原)、肽键(可取
代)等,能发生加成、取代、氧化、还原反应,A正确;
B.与足量 加成后,苯环变为环己烷环(含4个手性碳),五元环中与N相连的碳(若连乙基等不同基
团)也为手性碳,共5个手性碳,B正确;
C.苯环需3 mol 加成,酰胺羰基难加成,故1 mol中间体最多与3 mol 加成,C正确;
D.含氨基和脂肪胺N(显碱性),但①(苯环C-N单键)、②(环C-N单键)为普通单键,③(酰胺C-
N键,因共轭具部分双键性)键长更短,三者键长不相等,D错误;
第4页/共28页
学科网(北京)股份有限公司故答案选D。
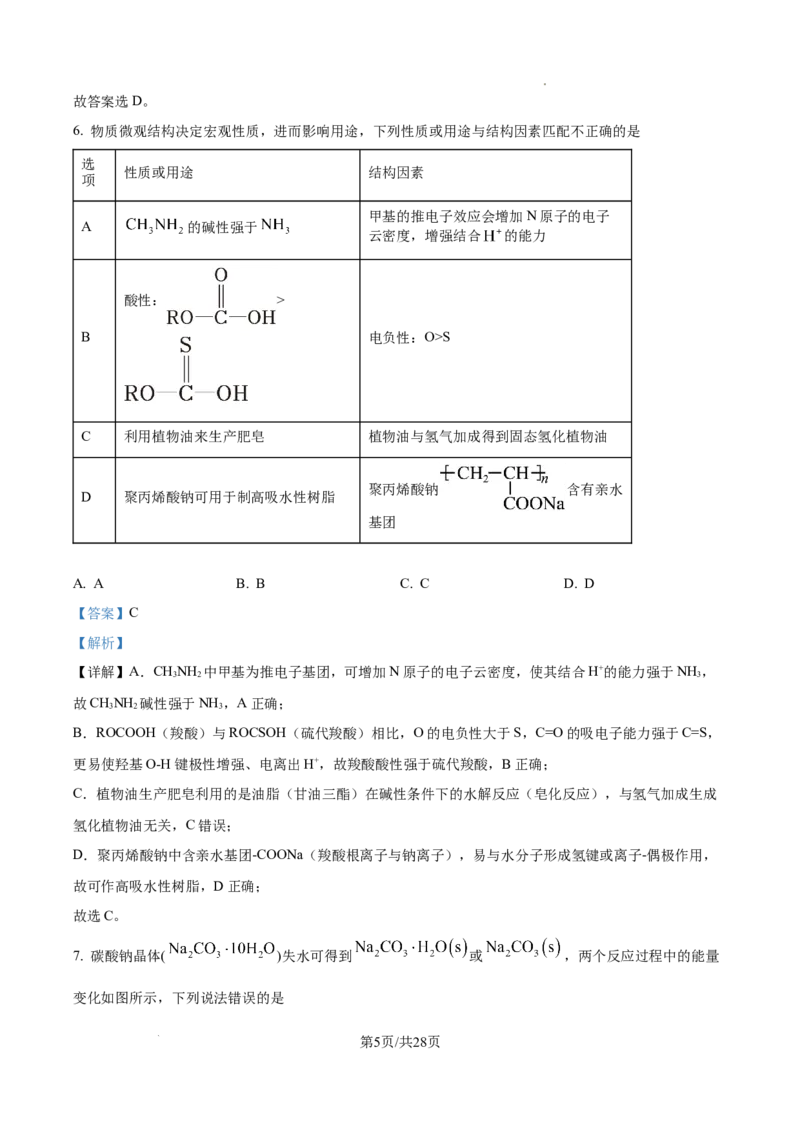
6. 物质微观结构决定宏观性质,进而影响用途,下列性质或用途与结构因素匹配不正确的是
选
性质或用途 结构因素
项
甲基的推电子效应会增加N原子的电子
A 的碱性强于
云密度,增强结合 的能力
酸性: >
B 电负性:O>S
C 利用植物油来生产肥皂 植物油与氢气加成得到固态氢化植物油
聚丙烯酸钠 含有亲水
D 聚丙烯酸钠可用于制高吸水性树脂
基团
A. A B. B C. C D. D
【答案】C
【解析】
【详解】A.CHNH 中甲基为推电子基团,可增加N原子的电子云密度,使其结合H+的能力强于NH ,
3 2 3
故CHNH 碱性强于NH ,A正确;
3 2 3
B.ROCOOH(羧酸)与ROCSOH(硫代羧酸)相比,O的电负性大于S,C=O的吸电子能力强于C=S,
更易使羟基O-H键极性增强、电离出H+,故羧酸酸性强于硫代羧酸,B正确;
C.植物油生产肥皂利用的是油脂(甘油三酯)在碱性条件下的水解反应(皂化反应),与氢气加成生成
氢化植物油无关,C错误;
D.聚丙烯酸钠中含亲水基团-COONa(羧酸根离子与钠离子),易与水分子形成氢键或离子-偶极作用,
故可作高吸水性树脂,D正确;
故选C。
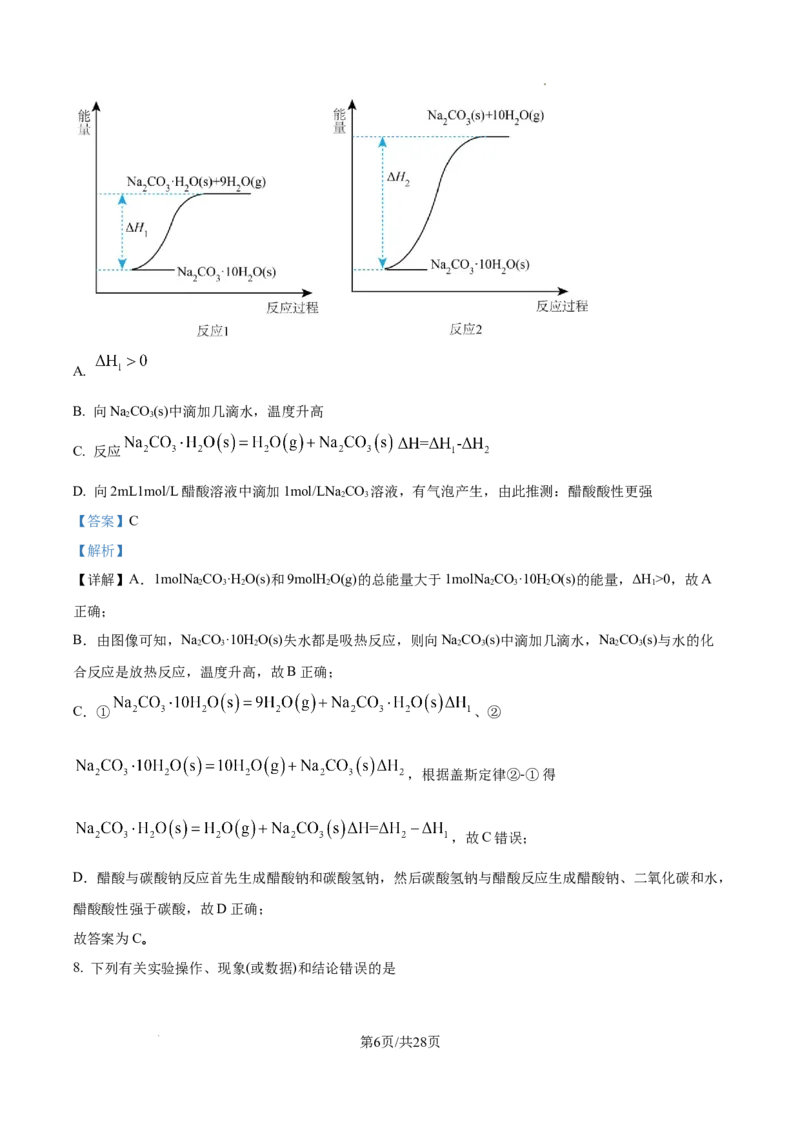
7. 碳酸钠晶体( )失水可得到 或 ,两个反应过程中的能量
变化如图所示,下列说法错误的是
第5页/共28页
学科网(北京)股份有限公司A.
B. 向NaCO(s)中滴加几滴水,温度升高
2 3
C. 反应
D. 向2mL1mol/L醋酸溶液中滴加1mol/LNa CO 溶液,有气泡产生,由此推测:醋酸酸性更强
2 3
【答案】C
【解析】
【详解】A.1molNa CO·H O(s)和9molH O(g)的总能量大于1molNa CO·10H O(s)的能量,ΔH>0,故A
2 3 2 2 2 3 2 1
正确;
B.由图像可知,NaCO·10H O(s)失水都是吸热反应,则向NaCO(s)中滴加几滴水,NaCO(s)与水的化
2 3 2 2 3 2 3
合反应是放热反应,温度升高,故B正确;
C.① 、②
,根据盖斯定律②-①得
,故C错误;
D.醋酸与碳酸钠反应首先生成醋酸钠和碳酸氢钠,然后碳酸氢钠与醋酸反应生成醋酸钠、二氧化碳和水,
醋酸酸性强于碳酸,故D正确;
故答案为C。
8. 下列有关实验操作、现象(或数据)和结论错误的是
第6页/共28页
学科网(北京)股份有限公司选
实验操作 实验现象或数据 结论
项
向某甲酸样品中先加入足量
A NaOH溶液,再做银镜反应 出现银镜 该样品中不一定混有甲醛
实验
反应一段时间停止加
和空气的混合气体通
B 热后, 持续红 该反应
过热的
热
存在平衡:
向硫酸铜稀溶液中加入足量 溶液从蓝色变为黄绿
C
NaCl固体 色
向Zn和稀硫酸正在反应的
单位时间内产生的气 使用催化剂可加快反应速
D 溶液中滴加少量 溶
体增多 率,使平衡正向移动
液
A. A B. B C. C D. D
【答案】D
【解析】
【详解】A.甲酸中含有醛基的结构,在强碱性条件下可发生银镜反应,无需甲醛存在,结论正确,A正
确;
B.反应停止加热后Cr O 持续红热,说明反应放热维持温度,ΔH<0,结论正确,B正确;
2 3
C.加入Cl-使Cu2+的配位结构改变,颜色变化证明存在配位平衡,结论正确,C正确;
D.CuSO 与Zn反应生成Cu,形成原电池加快反应速率,但反应不可逆且无平衡移动,结论错误,D错误;
4
故选D。
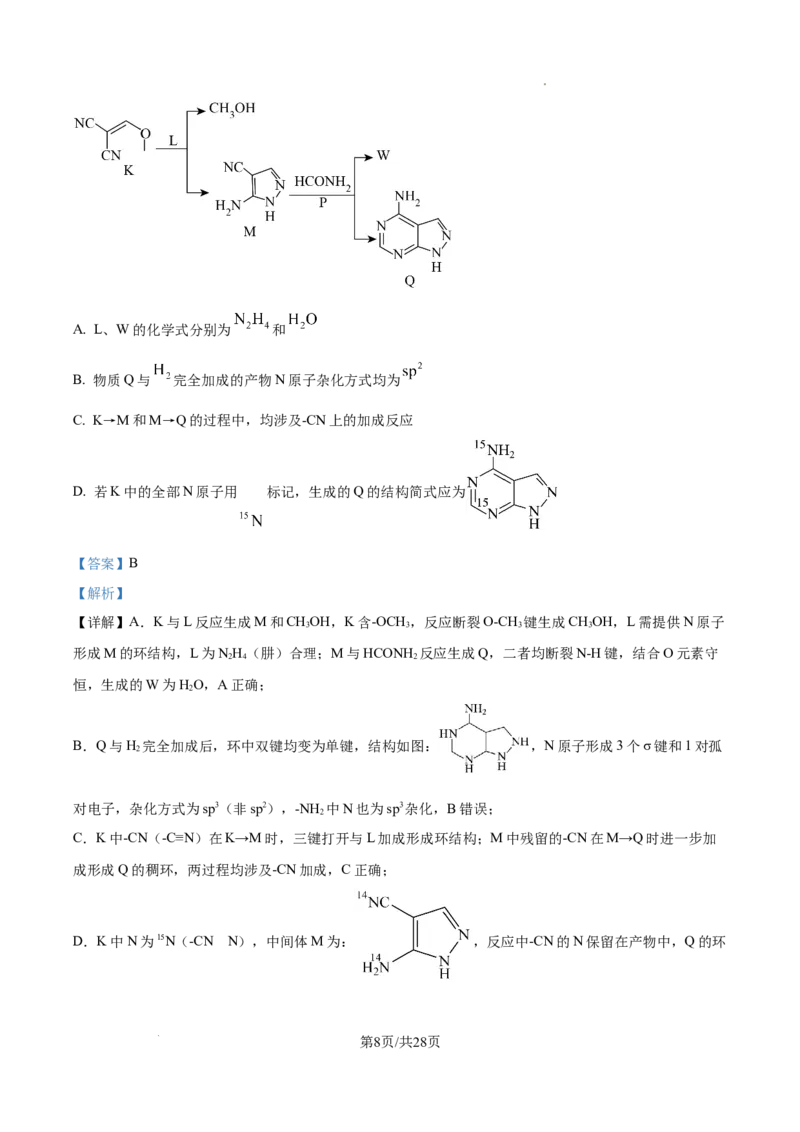
9. 由化合物K、L和P合成药物中间体Q,转化关系如图。已知:生成Q时,M与 中均有N-H
键断裂。下列说法错误的是
第7页/共28页
学科网(北京)股份有限公司A. L、W的化学式分别为 和
B. 物质Q与 完全加成的产物N原子杂化方式均为
C. K→M和M→Q的过程中,均涉及-CN上的加成反应
D. 若K中的全部N原子用 标记,生成的Q的结构简式应为
【答案】B
【解析】
【详解】A.K与L反应生成M和CHOH,K含-OCH ,反应断裂O-CH 键生成CHOH,L需提供N原子
3 3 3 3
形成M的环结构,L为NH(肼)合理;M与HCONH 反应生成Q,二者均断裂N-H键,结合O元素守
2 4 2
恒,生成的W为HO,A正确;
2
B.Q与H 完全加成后,环中双键均变为单键,结构如图: ,N原子形成3个σ键和1对孤
2
对电子,杂化方式为sp3(非sp2),-NH 中N也为sp3杂化,B错误;
2
C.K中-CN(-C≡N)在K→M时,三键打开与L加成形成环结构;M中残留的-CN在M→Q时进一步加
成形成Q的稠环,两过程均涉及-CN加成,C正确;
D.K中N为15N(-CN N),中间体M为: ,反应中-CN的N保留在产物中,Q的环
的
第8页/共28页
学科网(北京)股份有限公司及-NH 中的N均来自K的15N,生成的Q的结构简式为 ,D正确;
2
故选B。
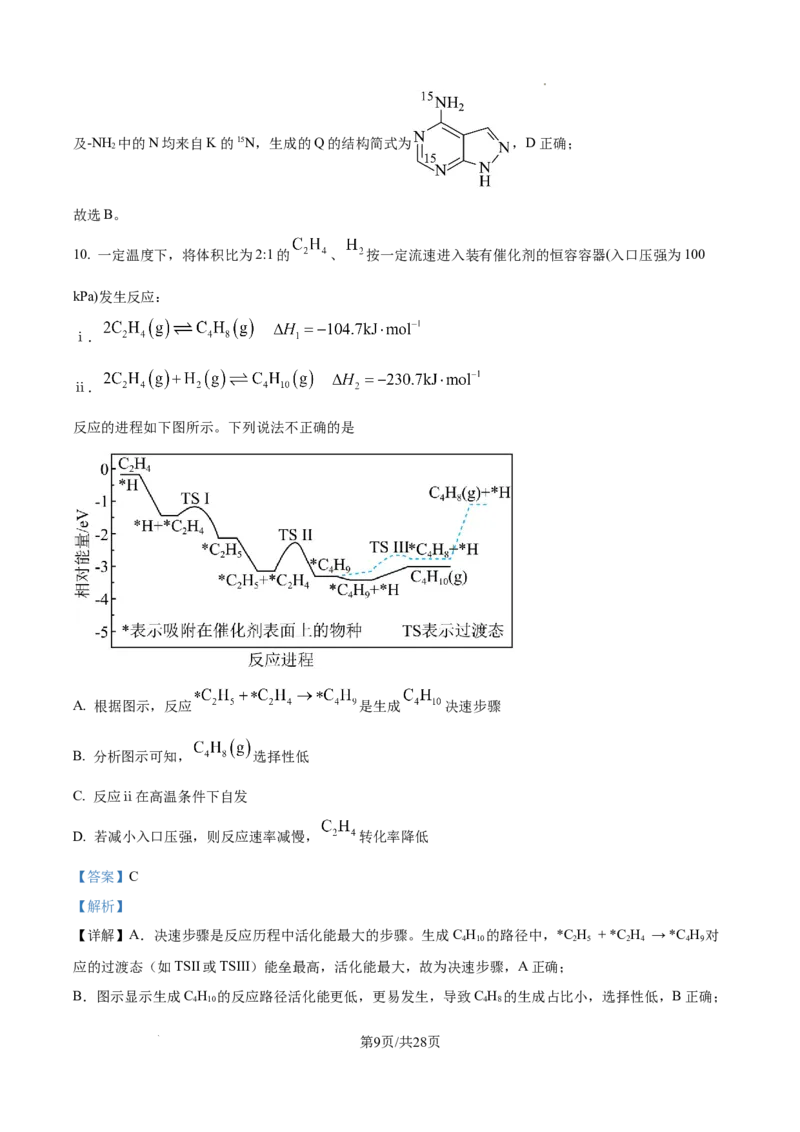
10. 一定温度下,将体积比为2:1的 、 按一定流速进入装有催化剂的恒容容器(入口压强为100
kPa)发生反应:
ⅰ.
ⅱ.
反应的进程如下图所示。下列说法不正确的是
A. 根据图示,反应 是生成 决速步骤
B. 分析图示可知, 选择性低
C. 反应ⅱ在高温条件下自发
D. 若减小入口压强,则反应速率减慢, 转化率降低
【答案】C
【解析】
【详解】A.决速步骤是反应历程中活化能最大的步骤。生成C H 的路径中,*C H + *C H → *C H 对
4 10 2 5 2 4 4 9
应的过渡态(如TSⅡ或TSⅢ)能垒最高,活化能最大,故为决速步骤,A正确;
B.图示显示生成C H 的反应路径活化能更低,更易发生,导致C H 的生成占比小,选择性低,B正确;
4 10 4 8
第9页/共28页
学科网(北京)股份有限公司C.反应ⅱ的ΔH=-230.7 kJ/mol(ΔH<0),气体分子数减少(ΔS<0),根据ΔG=ΔH-TΔS,ΔH<0、ΔS<0
2
时,高温下反应不自发,C错误;
D.减小入口压强,气体浓度降低,反应速率减慢;反应ⅰ、ⅱ均为气体分子数减少的反应,减小压强平
衡逆向移动,C H 转化率降低,D正确;
2 4
故选C。
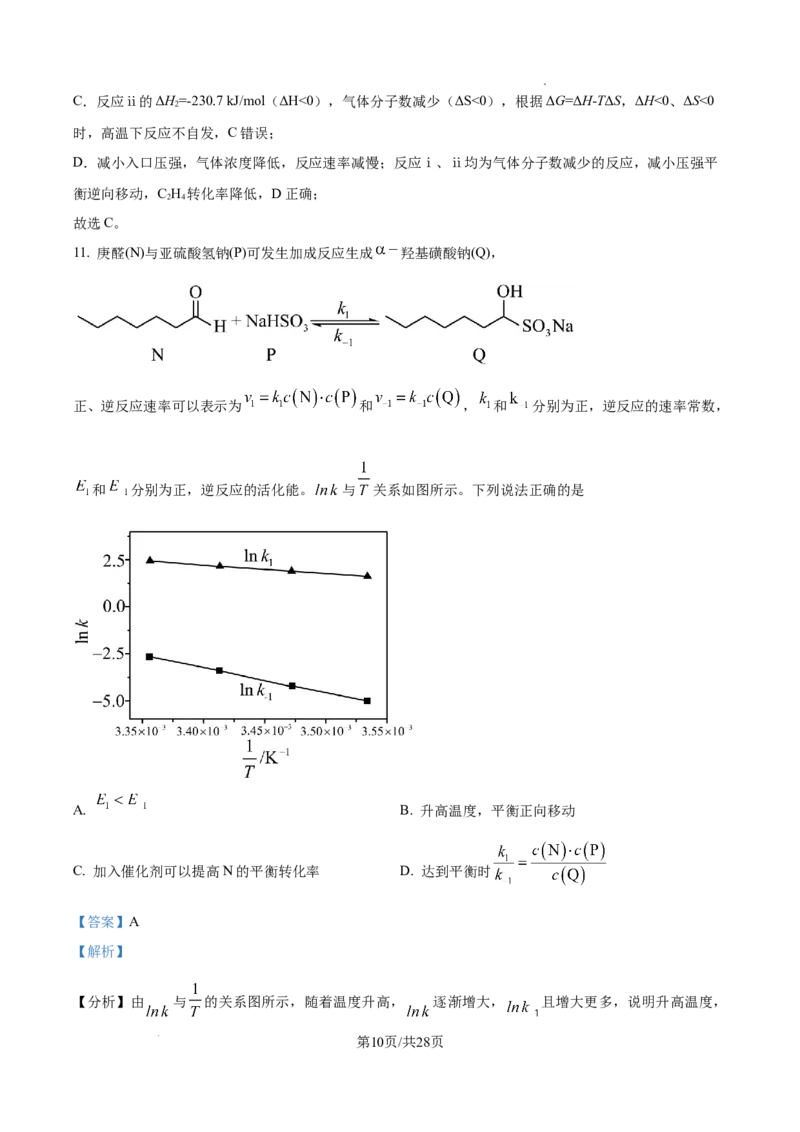
11. 庚醛(N)与亚硫酸氢钠(P)可发生加成反应生成 羟基磺酸钠(Q),
正、逆反应速率可以表示为 和 , 和 分别为正,逆反应的速率常数,
和 分别为正,逆反应的活化能。 与 关系如图所示。下列说法正确的是
A. B. 升高温度,平衡正向移动
C. 加入催化剂可以提高N的平衡转化率 D. 达到平衡时
【答案】A
【解析】
【分析】由 与 的关系图所示,随着温度升高, 逐渐增大, 且增大更多,说明升高温度,
第10页/共28页
学科网(北京)股份有限公司逆反应速率增加更多,平衡应逆向移动,则该反应正向应为放热反应。
【详解】A.根据分析可知该反应为放热反应,所以正反应活化能更小,即 ,A正确;
B.该反应正向为放热反应,升高温度,平衡逆向移动,B错误;
C.催化剂同等程度改变正逆反应速率,不影响平衡,N的平衡转化率不变,C错误;
D.达到平衡时,正逆反应速率相等,则有 = ,则 ,D
错误;
故选A。
12. 甲醇有“木醇”与“木精”之名,现代甲醇是直接在一氧化碳、二氧化碳和氢的一个催化作用的工业过程中
制 造 的 。 向 2L 恒 容 密 闭 容 器 中 充 入 和 , 在 一 定 条 件 下 , 发 生 反 应
。在甲、乙两种不同催化剂的
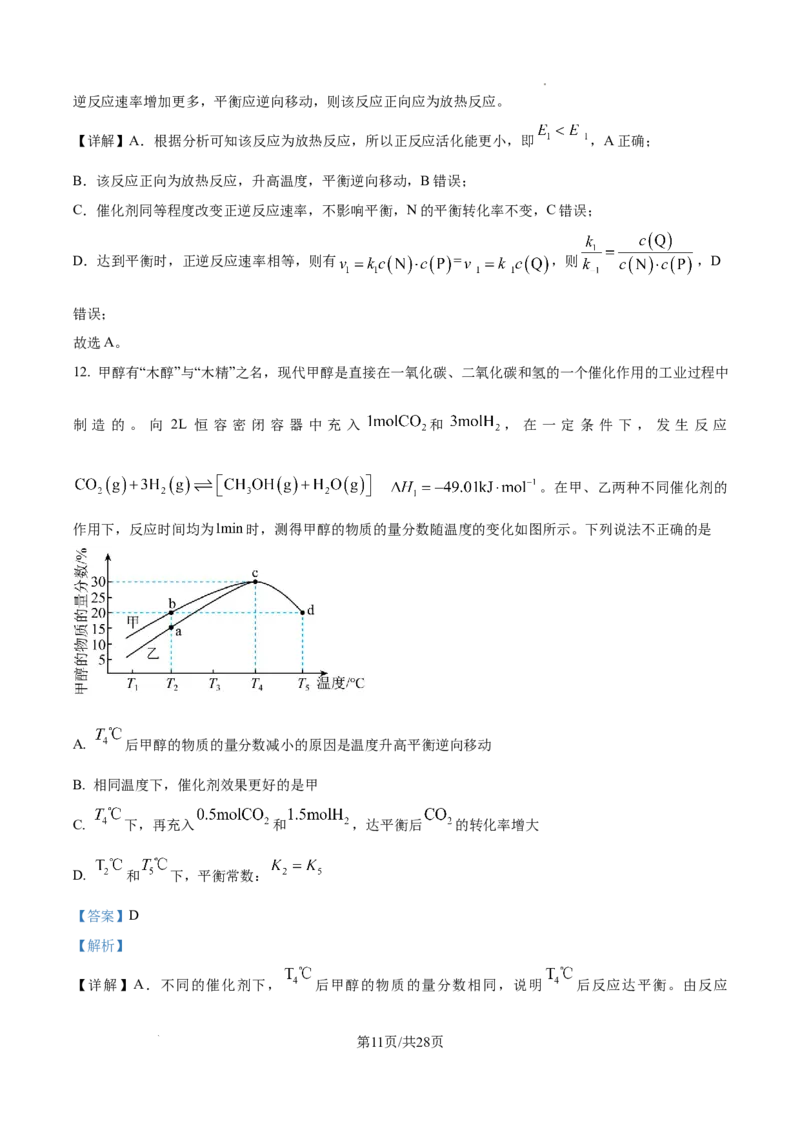
作用下,反应时间均为 时,测得甲醇的物质的量分数随温度的变化如图所示。下列说法不正确的是
A. 后甲醇的物质的量分数减小的原因是温度升高平衡逆向移动
B. 相同温度下,催化剂效果更好的是甲
C. 下,再充入 和 ,达平衡后 的转化率增大
D. 和 下,平衡常数:
【答案】D
【解析】
【详解】A.不同的催化剂下, 后甲醇的物质的量分数相同,说明 后反应达平衡。由反应
第11页/共28页
学科网(北京)股份有限公司知,升温,平衡逆向移动。故甲醇的物质的量分数减小的原因是温度升高,平衡逆向移动,所以物
质的量分数减小,A正确;
B.相同条件下甲催化下甲醇的物质的量分数更大,催化剂效果更好,B正确;
C. 下,再充入 和 ,相当于加压,平衡正向移动, 的转化率增大,C正确;
D. ,正反应放热,温度升高,平衡逆向移动,平衡常数减小, ,D错误;
故选D。
13. 工业上可用“氨催化氧化法”生产NO,以氨气、氧气为原料,在Pt-Rh合金催化剂存在下生成NO和
副产物 的两个竞争反应化学方程式如下:
Ⅰ.
Ⅱ.
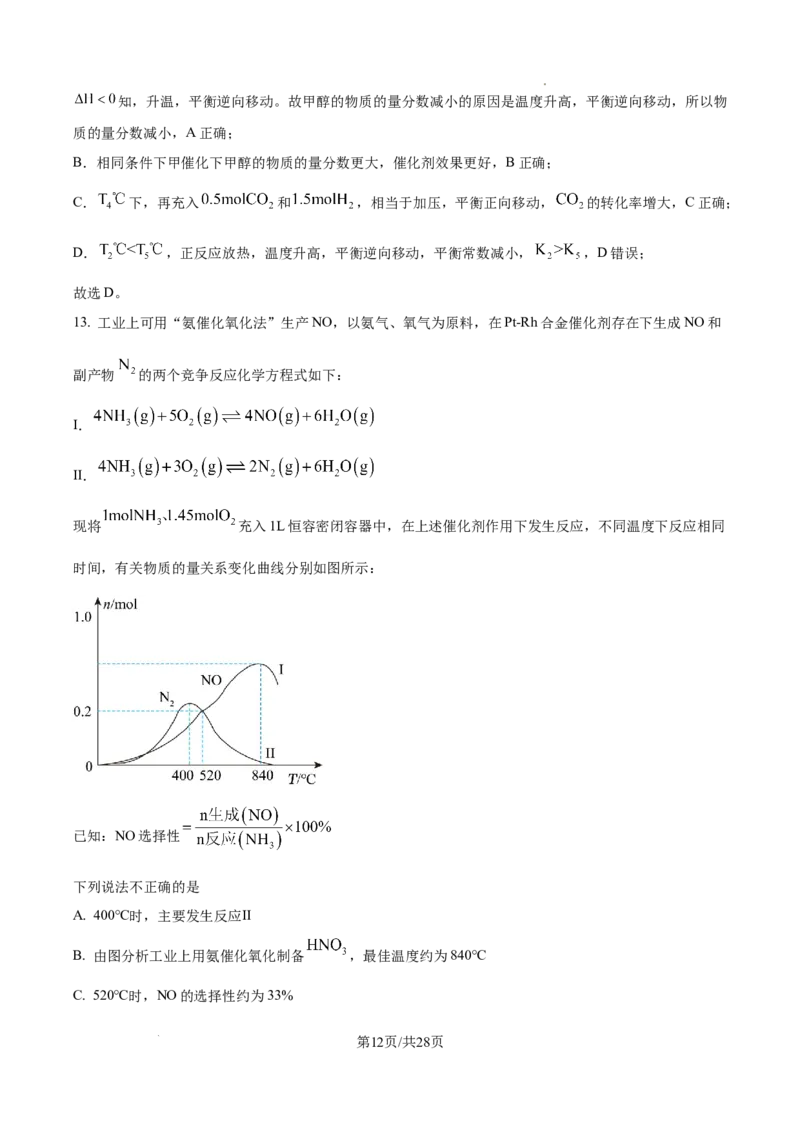
现将 充入1L恒容密闭容器中,在上述催化剂作用下发生反应,不同温度下反应相同
时间,有关物质的量关系变化曲线分别如图所示:
已知:NO选择性
下列说法不正确的是
A. 400℃时,主要发生反应Ⅱ
B. 由图分析工业上用氨催化氧化制备 ,最佳温度约为840℃
C. 520℃时,NO的选择性约为33%
第12页/共28页
学科网(北京)股份有限公司D. 840℃时,存在某一时刻:
【答案】D
【解析】
【详解】A.400℃时,根据图像可知N 的物质的量大于NO,说明副反应Ⅱ占主导,主要发生反应Ⅱ,A
2
正确;
B.工业制备HNO 需NO产率最高,840℃时NO的物质的量达到峰值,此时NO产率最大,为最佳温度,
3
B正确;
C.520℃时,图像中NO和N 的物质的量相等,设均为a mol。根据N守恒,反应的NH 为n(NO)
2 3
+2n(N )=a+2a=3a mol,NO选择性=生成NO的NH /反应的NH = ,C正确;
2 3 3
D.根据N守恒,n(剩余NH )+n(NO)+2n(N )=1 mol(初始N总量),则n(NO)+2n(N )=1 mol-n(剩余
3 2 2
为
NH )。由于反应 可逆反应,NH 不能完全转化,n(剩余NH )>0,故n(NO)+2n(N )<1 mol,不存在该时刻,
3 3 3 2
D错误;
故选D。
14. 常温下,用0.1000mol/LNaOH溶液分别滴定20.00mLbmol/L的盐酸和醋酸溶液,两个滴定过程中溶液
pH的变化曲线如图所示。下列说法不正确的是
A. 曲线I表示滴定醋酸
B. a点浓度最大的离子是Na+
C. V[NaOH(aq)]=20mL时,c(Cl-)>c(CH COO-)
3
D. 用酚酞作指示剂,达到滴定终点时,溶液从无色刚好变为粉红色,且半分钟内不褪色
【答案】B
【解析】
第13页/共28页
学科网(北京)股份有限公司【详解】A.相同条件下等浓度的酸,弱酸的pH大,因此Ⅰ代表的是醋酸,A正确;
B.a点溶质为等浓度的醋酸和醋酸钠,有电荷守恒: ,此时溶
液显酸性,则 ,B错误;
C.V[NaOH(aq)]=20 mL时,溶质分别恰好为等浓度氯化钠和醋酸钠,盐酸是强酸、醋酸为弱酸,醋酸钠
溶液中醋酸根离子发生水解,c(Cl−)>c(CHCOO−),C正确;
3
D.用碱滴定酸的时候,终点时溶液显弱碱性(滴定强酸过量的半滴碱或者滴定弱酸时弱酸强碱盐都使终
点显碱性),用酚酞作指示剂,达到滴定终点时,溶液从无色刚好变为粉红色,且半分钟内不变色,D正
确;
故选B。
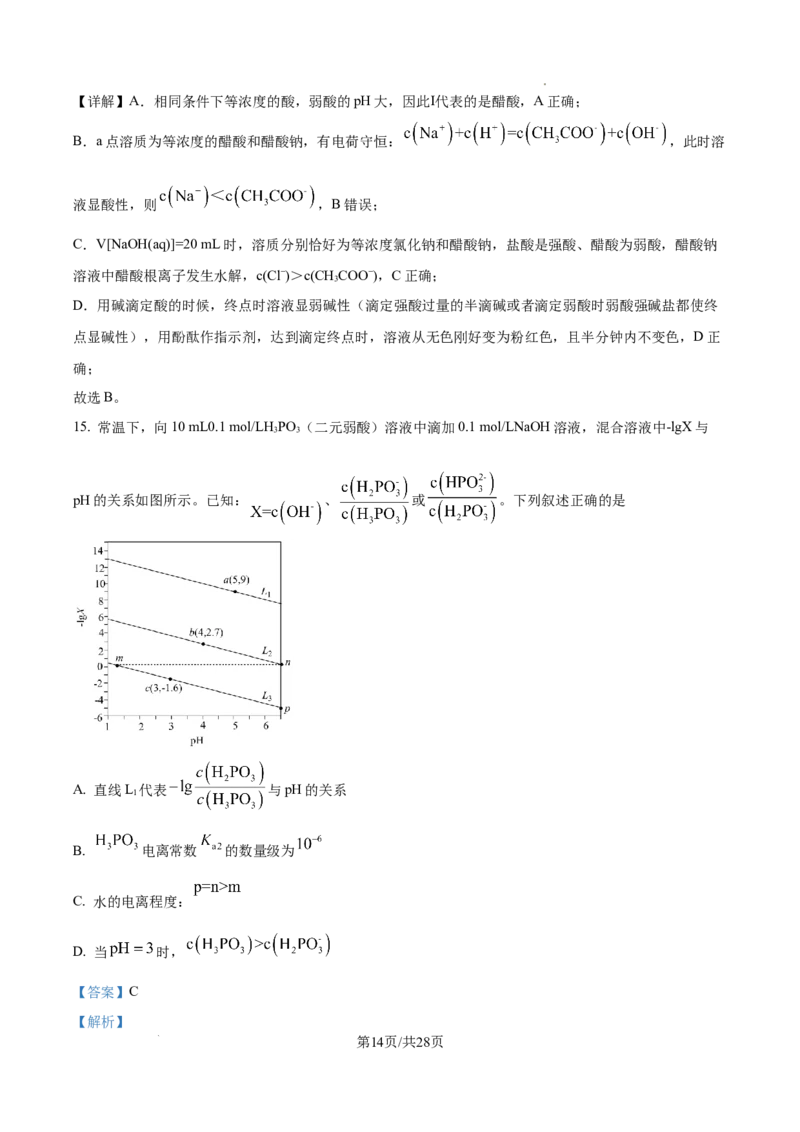
15. 常温下,向10 mL0.1 mol/LH PO (二元弱酸)溶液中滴加0.1 mol/LNaOH溶液,混合溶液中-lgX与
3 3
pH的关系如图所示。已知: 、 或 。下列叙述正确的是
A. 直线L 代表 与pH的关系
1
B. 电离常数 的数量级为
C. 水的电离程度:
D. 当 时,
【答案】C
【解析】
第14页/共28页
学科网(北京)股份有限公司【分析】分析直线代表的含义:直线代表-lgX与pH的关系,X可能是c(OH-)、 或 ,
对于X= c(OH-),-lgc(OH-)=14-pH。由于在常温下水的离子积K =c(H+)∙c(OH-)=10-14,pOH+pH=14,如a点
w
pH=5,-lgc(OH-)=14-pH=14-5=9,故L 代表X=c(OH-)与溶液pH的关系。对于二元弱酸HPO 在溶液中存
1 3 3
在两步电离平衡:HPO H++ ,K = ; H++ ,K =
3 3 a1 a2
,由于K >K ,在c(H+)相同时, ,
a1 a2
,故L 表示 与pH的关系,L 表示 与pH的
2 3
关系,然后根据问题分析解答。
【详解】A.根据上述分析可知:L 代表X=c(OH-)与溶液pH的关系,A错误;
1
B.HPO 为二元弱酸,其第二步电离 H++ ,电离平衡常数K = ,直线
3 3 a2
L 表示 与pH的关系。lgK =lgc(H+)+ ,当溶液pH=4时,根据直线L 上b点坐
2 a2 2
标可知 ,此时,-lgK =4+2.7=6.7,所以K =10-6.7,故K 的数量级为10⁻7,B错误;
a2 a2 a2
C.m点为L 上-lgX=0的点,此时 ,溶液为NaH PO 与HPO 等浓度的混合溶液,此时溶
3 2 3 3 3
液pH≈1.4,溶液显强酸性,HPO 的电离会抑制水的电离;n点为L 上-lgX=0的点, ,溶
3 3 2
液为NaH PO 与NaHPO 等浓度的混合溶液,此时溶液pH=6.5,溶液显弱酸性,以电离为主,抑制水的电
2 3 2 3
第15页/共28页
学科网(北京)股份有限公司离;p点为L 上lgX=-5, ,溶液pH=6.5,几乎完全电离为 ,溶液显弱酸性,抑制
3
水的电离,故水的电离程度p=n>m,C正确;
D.pH=3时,L 上c点(-lgX=-1.6),即 ,故微粒浓度:c( )>c(H PO ),D
3 3 3
错误;
故合理选项是C。
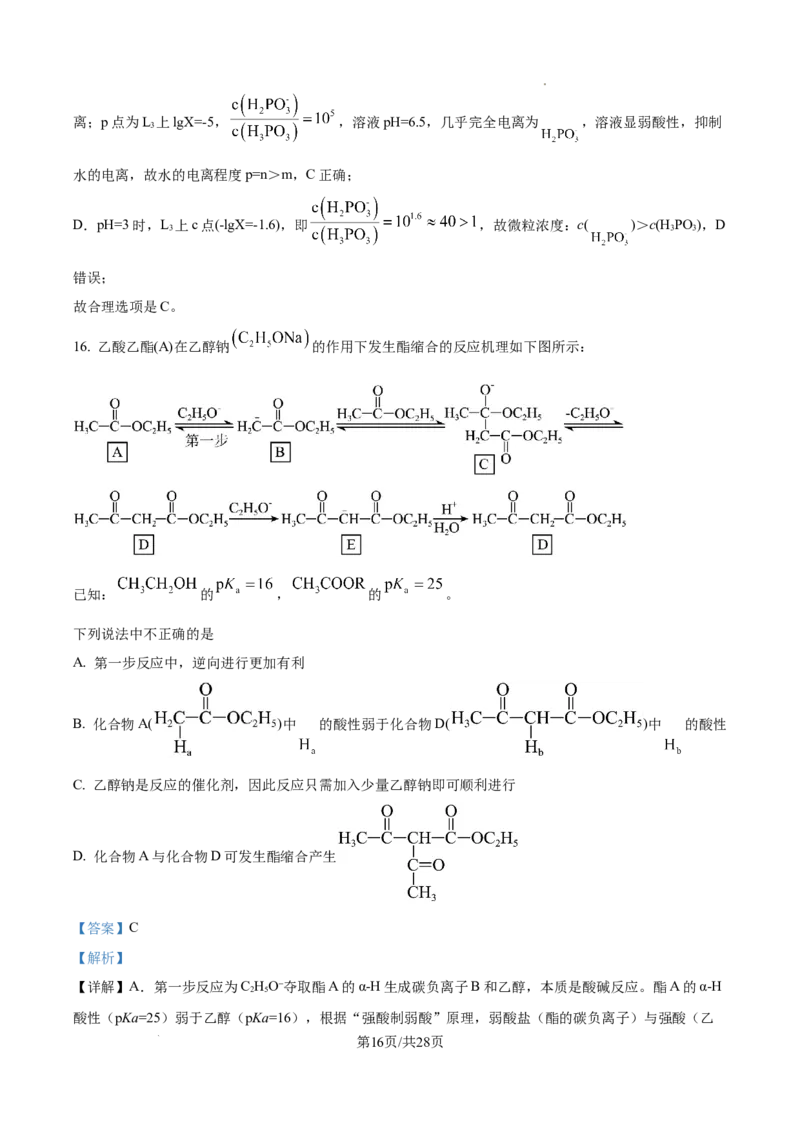
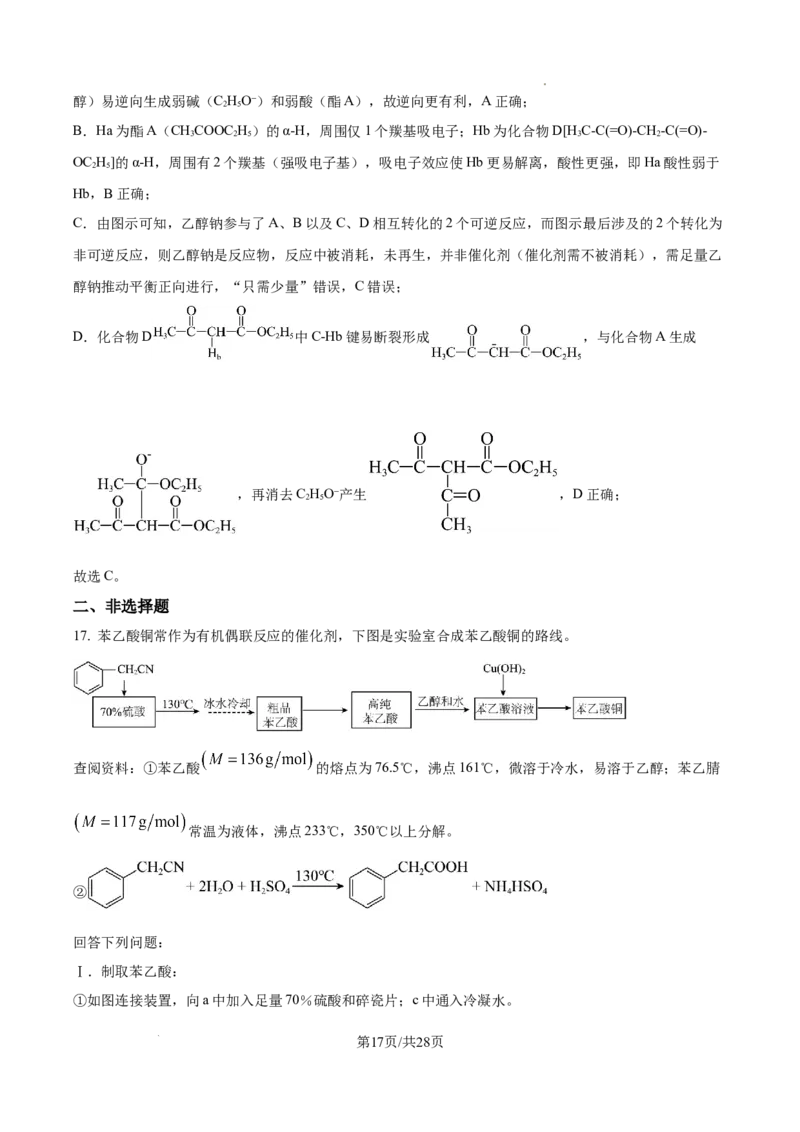
16. 乙酸乙酯(A)在乙醇钠 的作用下发生酯缩合的反应机理如下图所示:
已知: 的 , 的 。
下列说法中不正确的是
A. 第一步反应中,逆向进行更加有利
B. 化合物A( )中 的酸性弱于化合物D( )中 的酸性
C. 乙醇钠是反应的催化剂,因此反应只需加入少量乙醇钠即可顺利进行
D. 化合物A与化合物D可发生酯缩合产生
【答案】C
【解析】
【详解】A.第一步反应为C HO⁻夺取酯A的α-H生成碳负离子B和乙醇,本质是酸碱反应。酯A的α-H
2 5
酸性(pKa=25)弱于乙醇(pKa=16),根据“强酸制弱酸”原理,弱酸盐(酯的碳负离子)与强酸(乙
第16页/共28页
学科网(北京)股份有限公司醇)易逆向生成弱碱(C HO⁻)和弱酸(酯A),故逆向更有利,A正确;
2 5
B.Ha为酯A(CHCOOC H)的α-H,周围仅1个羰基吸电子;Hb为化合物D[H C-C(=O)-CH -C(=O)-
3 2 5 3 2
OC H]的α-H,周围有2个羰基(强吸电子基),吸电子效应使Hb更易解离,酸性更强,即Ha酸性弱于
2 5
Hb,B正确;
C.由图示可知,乙醇钠参与了A、B以及C、D相互转化的2个可逆反应,而图示最后涉及的2个转化为
非可逆反应,则乙醇钠是反应物,反应中被消耗,未再生,并非催化剂(催化剂需不被消耗),需足量乙
醇钠推动平衡正向进行,“只需少量”错误,C错误;
D.化合物D 中C-Hb键易断裂形成 ,与化合物A生成
,再消去C HO⁻产生 ,D正确;
2 5
故选C。
二、非选择题
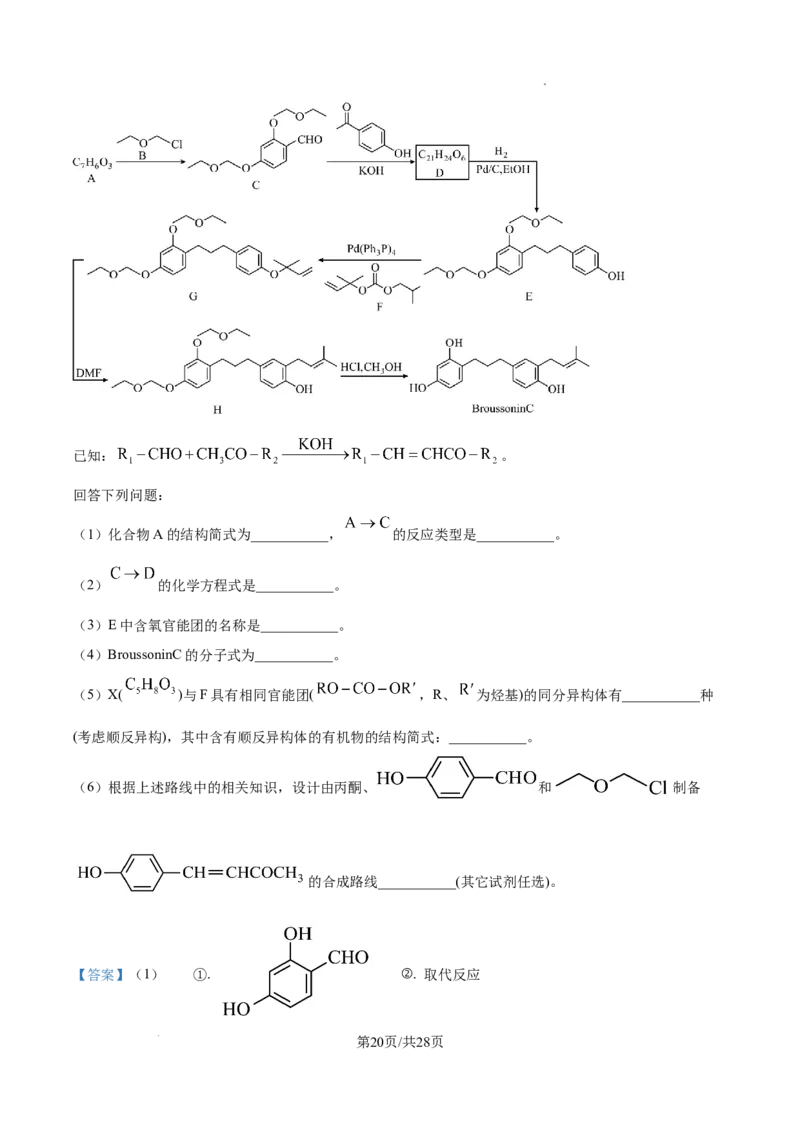
17. 苯乙酸铜常作为有机偶联反应的催化剂,下图是实验室合成苯乙酸铜的路线。
查阅资料:①苯乙酸 的熔点为76.5℃,沸点161℃,微溶于冷水,易溶于乙醇;苯乙腈
常温为液体,沸点233℃,350℃以上分解。
②
回答下列问题:
Ⅰ.制取苯乙酸:
①如图连接装置,向a中加入足量70%硫酸和碎瓷片;c中通入冷凝水。
第17页/共28页
学科网(北京)股份有限公司②用b缓缓滴加23.4 g苯乙腈到硫酸溶液中,然后升温到130℃,继续反应一段时间;
③反应结束后,将a中的产物转移到烧杯中;
④加适量冰水,静置,分离出苯乙酸粗品。
(1)仪器b的名称___________,仪器c作用是___________。
(2)制取苯乙酸的反应温度控制在130℃左右的原因___________。
(3)步骤④反应结束后加适量冰水,其目的是___________,再分离出苯乙酸粗品。下列仪器中可用于分
离苯乙酸粗品的是___________(填标号)。
A.分液漏斗 B.漏斗 C.烧杯 D.直形冷凝管 E.玻璃棒
(4)经重结晶后,得到24.48 g纯品苯乙酸,则苯乙酸的产率是___________%。
Ⅱ.制取苯乙酸铜:
(5)用 和NaOH溶液制备适量 沉淀,并多次用蒸馏水洗涤沉淀,可用于判断沉
淀是否洗净的试剂是___________。
(6)将苯乙酸加入到乙醇与水的混合溶剂中,充分溶解后,加入 搅拌30 min,过滤,滤液静置
一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是___________。
【答案】(1) ①. 恒压滴液漏斗 ②. 冷凝回流苯乙腈和硫酸,提高原料利用率
(2)温度过低,反应速率慢;温度过高,苯乙腈易分解
(3) ①. 降低苯乙酸溶解度,使其析出 ②. BCE
(4)
(5)稀硝酸和硝酸银溶液
(6)增大苯乙酸溶解度,使反应充分进行
【解析】
【分析】整个合成路线分为两个主要部分,一为苯乙酸的制备:苯乙腈在70%硫酸、130℃条件下反应,
经冰水冷却结晶、分离得到粗品苯乙酸,再提纯得到高纯苯乙酸;二为苯乙酸铜的合成:高纯苯乙酸溶解
第18页/共28页
学科网(北京)股份有限公司于乙醇和水的混合溶剂中,与 反应生成苯乙酸铜。据此进行综合分析。
【小问1详解】
仪器b为恒压滴液漏斗,仪器c为球形冷凝管,作用为冷凝回流苯乙腈和硫酸,提高原料利用率;
【小问2详解】
苯乙酸的熔点为76.5℃,沸点161℃,苯乙腈沸点233℃,350℃以上分解,温度控制在130℃左右,既能
保证反应速率又能防止苯乙腈受热分解或分解;
【小问3详解】
苯乙酸“微溶于冷水,易溶于乙醇”,加冰水可降低苯乙酸的溶解度,使其结晶析出;分离苯乙酸粗品的
操作是过滤,需要用到的仪器是漏斗(B)、烧杯(C)、玻璃棒(E);
【小问4详解】
苯乙腈的物质的量为 ,化学方程式表明苯乙腈与苯乙酸的物质的量之比为 ,故生成
苯乙酸,共 ,经重结晶后,得到 纯品苯乙酸,故苯乙酸的产率
;
【小问5详解】
用 和 溶液制备适量 沉淀, 沉淀中有 残留, 可用稀硝酸
和硝酸银溶液检验;
【小问6详解】
苯乙酸微溶于冷水,易溶于乙醇,故混合溶剂中乙醇的作用是增大苯乙酸溶解度,使反应充分进行。
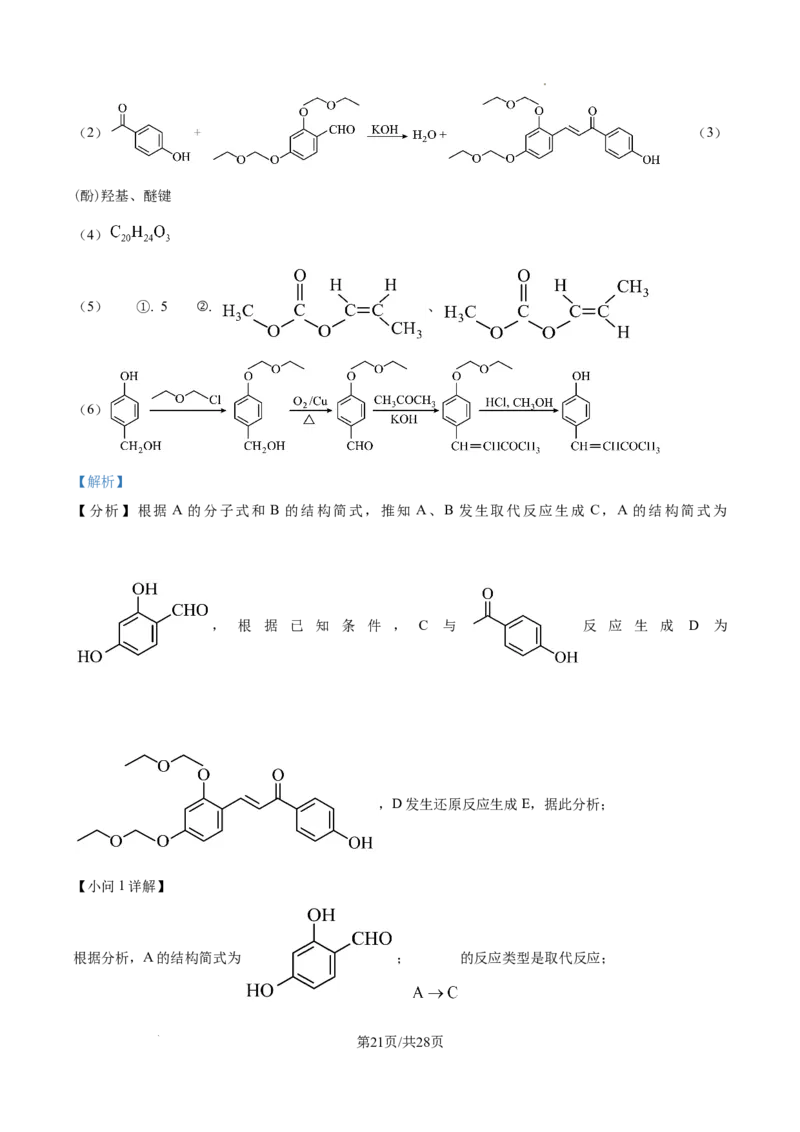
18. BroussoninC是很好的酪氨酸酶抑制剂,能克服黑色素过度产生带来的不利影响,昆明医科大学联合云
南中医药大学全合成BroussoninC,其合成路线如图所示。
第19页/共28页
学科网(北京)股份有限公司已知: 。
回答下列问题:
(1)化合物A的结构简式为___________, 的反应类型是___________。
(2) 的化学方程式是___________。
(3)E中含氧官能团的名称是___________。
(4)BroussoninC的分子式为___________。
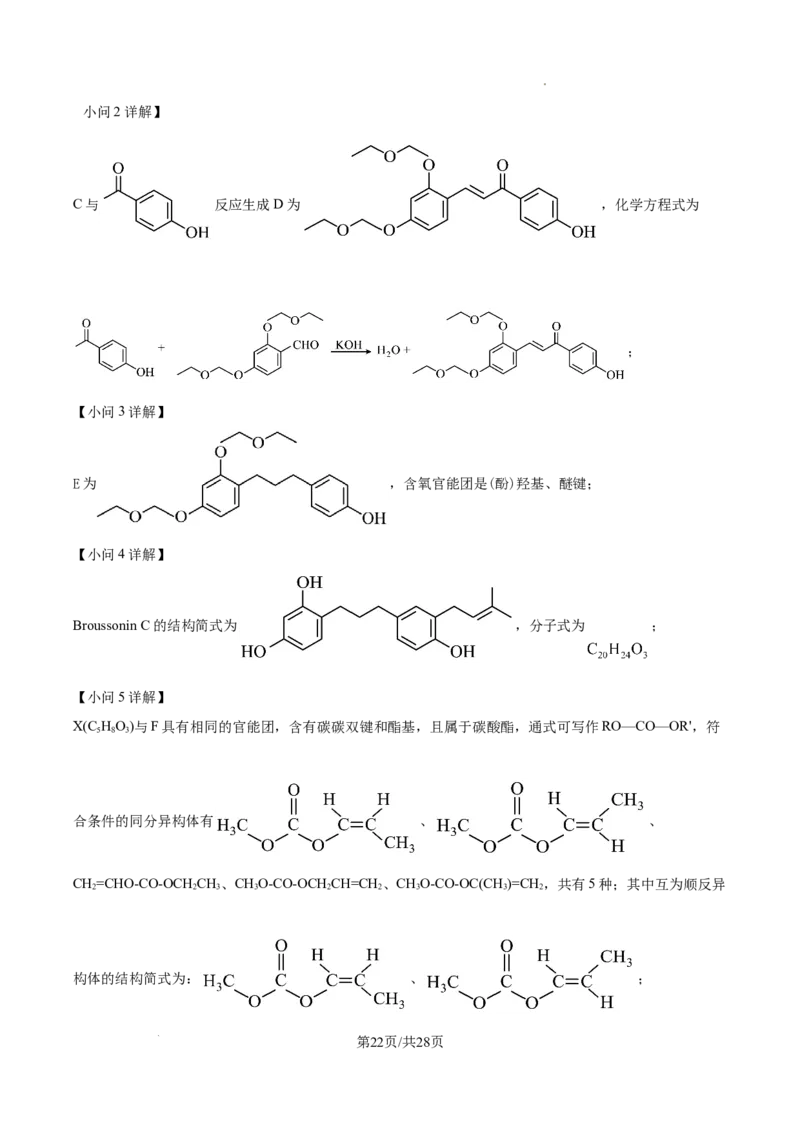
(5)X( )与F具有相同官能团( ,R、 为烃基)的同分异构体有___________种
(考虑顺反异构),其中含有顺反异构体的有机物的结构简式:___________。
(6)根据上述路线中的相关知识,设计由丙酮、 和 制备
的合成路线___________(其它试剂任选)。
【答案】(1) ①. ②. 取代反应
第20页/共28页
学科网(北京)股份有限公司(2) (3)
(酚)羟基、醚键
(4)
(5) ①. 5 ②. 、
(6)
【解析】
【分析】根据 A 的分子式和 B 的结构简式,推知 A、B 发生取代反应生成 C,A 的结构简式为
, 根 据 已 知 条 件 , C 与 反 应 生 成 D 为
,D发生还原反应生成E,据此分析;
【小问1详解】
根据分析,A的结构简式为 ; 的反应类型是取代反应;
第21页/共28页
学科网(北京)股份有限公司【
小问2详解】
C与 反应生成D为 ,化学方程式为
;
【小问3详解】
E为 ,含氧官能团是(酚)羟基、醚键;
【小问4详解】
Broussonin C的结构简式为 ,分子式为 ;
【小问5详解】
X(C HO)与F具有相同的官能团,含有碳碳双键和酯基,且属于碳酸酯,通式可写作RO—CO—OR',符
5 8 3
合条件的同分异构体有 、 、
CH=CHO-CO-OCH CH、CHO-CO-OCH CH=CH、CHO-CO-OC(CH )=CH ,共有5种;其中互为顺反异
2 2 3 3 2 2 3 3 2
构体的结构简式为: 、 ;
第22页/共28页
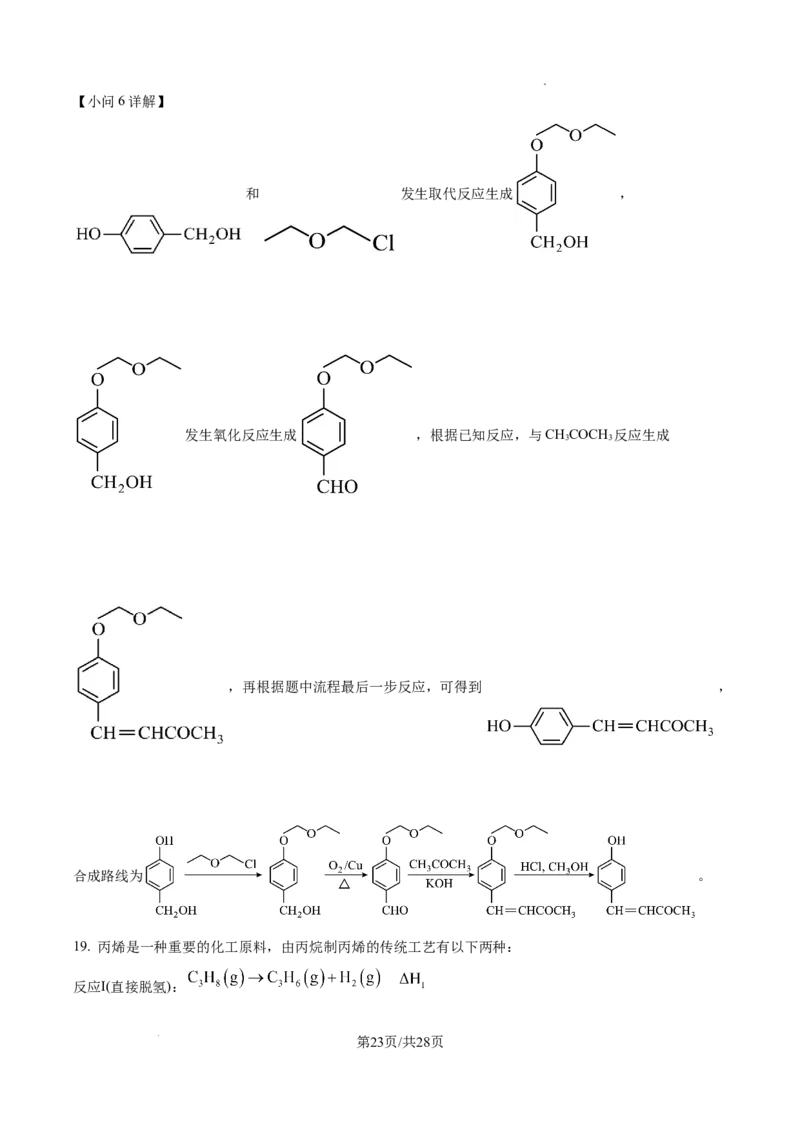
学科网(北京)股份有限公司【小问6详解】
和 发生取代反应生成 ,
发生氧化反应生成 ,根据已知反应,与CHCOCH 反应生成
3 3
,再根据题中流程最后一步反应,可得到 ,
合成路线为 。
19. 丙烯是一种重要的化工原料,由丙烷制丙烯的传统工艺有以下两种:
反应Ⅰ(直接脱氢):
第23页/共28页
学科网(北京)股份有限公司反应Ⅱ(氧化脱氢):
(1)25℃、101 kPa,丙烷、丙烯、氢气的摩尔燃烧焓分别为 、 、
,则 ___________ ,该反应在___________(填“高温”“低温”或“任
意温度”)条件下能自发进行。
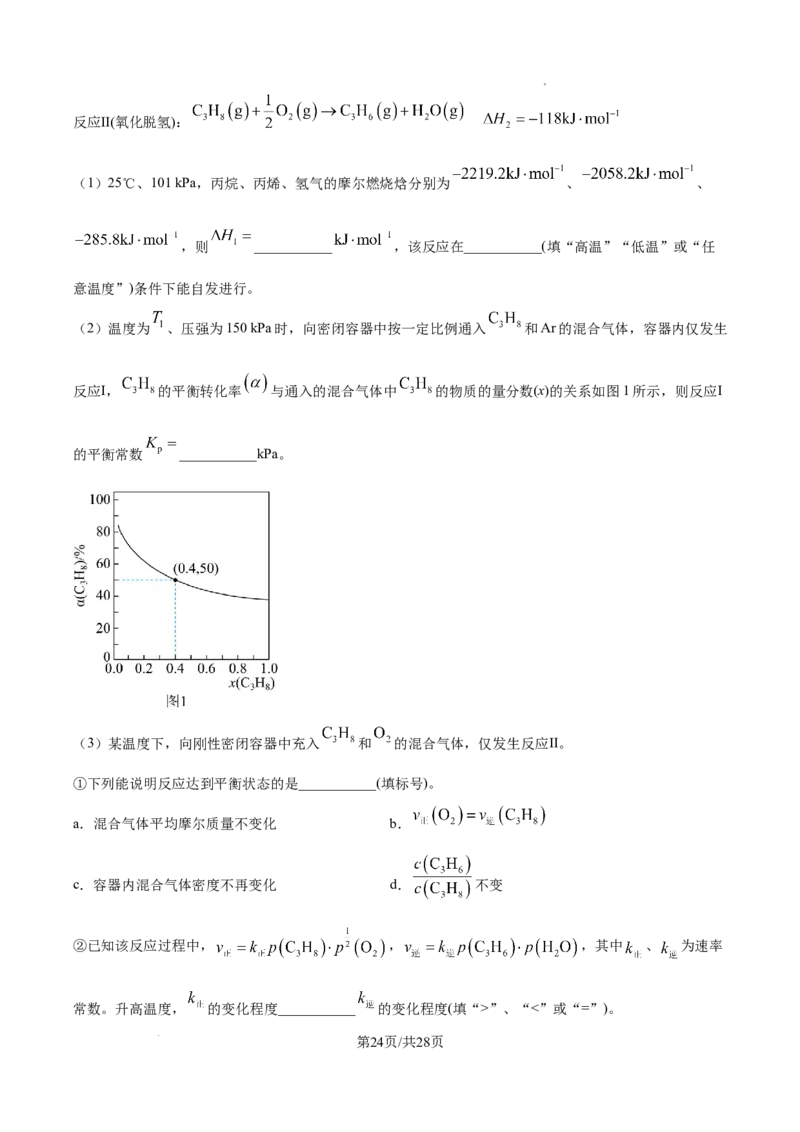
(2)温度为 、压强为150 kPa时,向密闭容器中按一定比例通入 和Ar的混合气体,容器内仅发生
反应Ⅰ, 的平衡转化率 与通入的混合气体中 的物质的量分数(x)的关系如图1所示,则反应Ⅰ
的平衡常数 ___________kPa。
(3)某温度下,向刚性密闭容器中充入 和 的混合气体,仅发生反应Ⅱ。
①下列能说明反应达到平衡状态的是___________(填标号)。
a.混合气体平均摩尔质量不变化 b.
c.容器内混合气体密度不再变化 d. 不变
②已知该反应过程中, , ,其中 、 为速率
常数。升高温度, 的变化程度___________ 的变化程度(填“>”、“<”或“=”)。
第24页/共28页
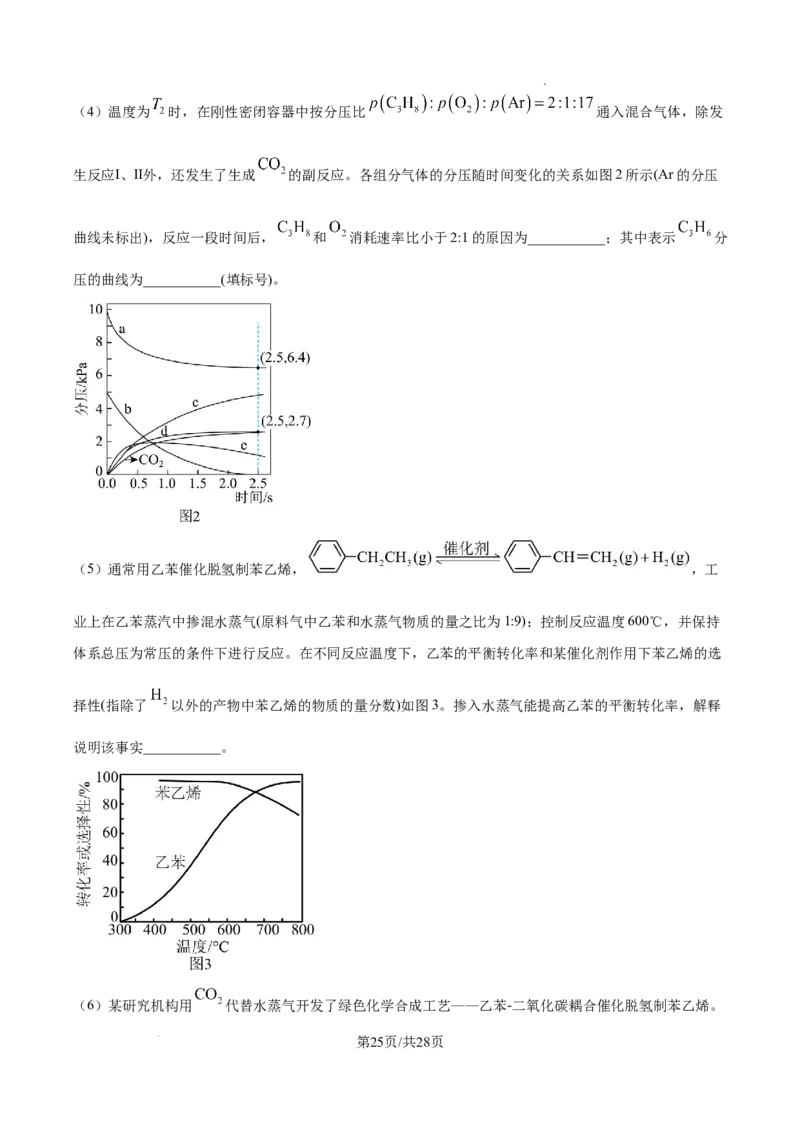
学科网(北京)股份有限公司(4)温度为 时,在刚性密闭容器中按分压比 通入混合气体,除发
生反应Ⅰ、Ⅱ外,还发生了生成 的副反应。各组分气体的分压随时间变化的关系如图2所示(Ar的分压
曲线未标出),反应一段时间后, 和 消耗速率比小于2:1的原因为___________;其中表示 分
压的曲线为___________(填标号)。
(5)通常用乙苯催化脱氢制苯乙烯, ,工
业上在乙苯蒸汽中掺混水蒸气(原料气中乙苯和水蒸气物质的量之比为1:9);控制反应温度600℃,并保持
体系总压为常压的条件下进行反应。在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选
择性(指除了 以外的产物中苯乙烯的物质的量分数)如图3。掺入水蒸气能提高乙苯的平衡转化率,解释
说明该事实___________。
(6)某研究机构用 代替水蒸气开发了绿色化学合成工艺——乙苯-二氧化碳耦合催化脱氢制苯乙烯。
第25页/共28页
学科网(北京)股份有限公司保持常压和原料气比例不变,与掺水蒸气工艺相比,在相同的生产效率下,可降低操作温度;该工艺中还
能够发生反应: , 。新工艺的特点有___________(填编号)。
① 与 反应,使乙苯脱氢反应的化学平衡右移
②有利于减少积炭
③不用高温水蒸气,可降低能量消耗
④有利于 资源利用
【答案】(1) ①. +124.8 ②. 高温
(2)25 (3) ①. ad ②. <
(4) ①. 和 消耗 ②. d
(5)正反应方向气体分子数增加,加入水蒸气起稀释作用,相当于起减压的效果
(6)①②③④
【解析】
【小问1详解】
摩尔燃烧焓是指1mol纯物质完全燃烧生成稳定氧化物时所放出的热量。
反应① (丙烷的摩尔燃烧焓);
反应② (丙烯的摩尔燃烧焓);
反应③ (氢气的摩尔燃烧焓)。
根据盖斯定律,用反应①减去反应②和反应③,可得反应 的 :
反应 的 >0,反应后气体物质的量增大,S>0。根据 ,当
T较大(高温)时, 的数值会大于 ,使得 ,反应能自发进行。所以该反应在高温条件下能
第26页/共28页
学科网(北京)股份有限公司自发进行。
【小问2详解】
设起始时C H 的物质的量为n,Ar的物质的量为m,则x = 。由图1可知,当x = 0.4时,C H 的平
3 8 3 8
衡转化率 = 50%。平衡时,n(C H)=n(1 - 50%) = 0.5n,n(C H)=n×50% = 0.5n,n(H )=n×50% = 0.5n,
3 8 3 6 2
n(Ar) = m。总物质的量n =0.5n + 0.5n + 0.5n + m = 1.5n + m,又因为x = 0.4= ,可得m = 1.5n,则n
总 总
=1.5n + 1.5n = 3n。
各物质的分压:
; ;
。反应Ⅰ的平衡常数 。
【小问3详解】
①a.反应Ⅱ ,反应前气体物质的量为1 + 0.5 = 1.5 mol,反应
后为1 + 1 = 2 mol,气体总质量不变。根据 ,n变化,M会变化,当混合气体平均摩尔质量不再变化时
说明反应达到平衡,a正确;
b.根据化学计量数, =1:2时,反应到达平衡状态,当 时,
正逆反应速率不相等,反应未达平衡,b错误;
c.容器为刚性密闭容器,体积不变,气体总质量不变,根据 ,密度始终不变,不能说明反应达到平
衡,c错误;
第27页/共28页
学科网(北京)股份有限公司d. 不变,说明各物质的浓度不再变化,反应达到平衡,d正确;
故选ad。
②反应Ⅱ ,为放热反应。升高温度,正、逆反应速率都增大,即k 、k 都增大,
正 逆
但平衡逆向移动,说明逆反应速率增大的程度更大,即k 的变化程度<k 的变化程度。
正 逆
【小问4详解】
温度为T 时,在刚性密闭容器中按分压比 ,则a为C H,b为O;
2 3 8 2
通入混合气体。由图可知有CO 生成,体系中还发生C H+ O=3CO +3H O、H+ O=H O,消耗O,
2 3 6 2 2 2 2 2 2 2
因此C H 和O 的消耗速率比小于2:1的原因是:H 和C H 消耗O;且p(H O)>p(CO),故c为HO;由
3 8 2 2 3 6 2 2 2 2
碳原子守恒可知,平衡时,∆n(C H)= n(CO)+n(C H),则∆p(C H)= p(CO)+p(C H),从而得出d为
3 8 2 3 6 3 8 2 3 6
C H,e为H。
3 6 2
【小问5详解】
加入水蒸气,体系的体积增大,各反应物和产物的分压减小,相当于起减压的效果,反应向压强增大的方
向移动,则平衡正向侈动,乙烯的平衡转化率增大,故答案为:正反应方向气体分子数增加,加入水蒸气
起稀释作用,相当于起减压的效果;
【小问6详解】
① 与 反应,减小H 浓度,使乙苯脱氢反应的化学平衡右移,正确;
2
② 可以与碳发生反应 ,有利于减少积炭,正确;
③不用高温水蒸气,可降低操作温度,降低能量消耗,正确;
④ ,得到有效利用,可减小 的排放并作为资源得到利用,正确;
故选①②③④。
第28页/共28页
学科网(北京)股份有限公司