文档内容
绝密★启用前 3.常温下,下列各组离子在水溶液中能大量共存的是
A.K+、OH-、HCO- B.Mg2+、Cl-、SO2-
3 4
江西省 2026届高三 10月一轮复习阶段检测
C.Na+、Al3+、[Al(OH)]- D.Na+、H+、SiO2-
4 3
4.实验室中模拟侯氏制碱法制备纯碱,下列操作错误或不能达到实验目的的是
化 学 试 卷
!"#
!"$%! !"
# #
$&’(")
*
试卷共8页,18小题,满分100分。考试用时75分钟。 $% &
$
%
注意事项:
&
饱和
食盐水
1.考查范围:化学物质及变化、化学计量在实验中的应用、元素及其化合物、物质结构与性质。 ’()#
*+,-
2.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡指定位置上。
A.制备氨气 B.制备CO C.制备NaHCO D.分离NaHCO 晶体
2 3 3
3.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改
5.在全面推进美丽中国建设中,化学知识发挥着巨大的作用。下列有关说法错误的是
动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷
A.酸雨对环境有巨大危害,酸雨的 pH小于5.6
上无效。
B.汽车尾气中的 CO对环境有害,CO属于酸性氧化物
4.考生必须保持答题卡的整洁。考试结束后,请将答题卡交回。
C.O 可以杀死河水中的有害细菌,该过程利用了 O 的强氧化性
3 3
D.光化学烟雾具有持久性危害,NO 是造成光化学烟雾的物质之一
可能用到的相对原子质量:C—12 O—16 Mg—24 Si—28 S—32 Cr—52 Cu—64 2
6.Fe的单质及其化合物存在如图所示的转化关系,X是一种淡黄色单质。下列说法正确的是
Zn—65 Se—79 Ce—140
A.X单质难溶于水,易溶于酒精和 CS # %
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项符合题目 2 !" !"$ & !"’
& (
! "
要求。 B.甲与 HO反应生成一种二元强酸 !
2
1.非物质文化遗产承载着民族的智慧和精神,是文化多样性的重要体现。下列非物质文化遗产中 C.反应②中,甲既是氧化产物又是还原产物
涉及物质的主要成分属于无机非金属材料的是 D.若反应①中 X过量,则生成的化合物中 Fe显+3价
A.分宜洋江赛龙舟的木质龙舟 B.莲花打锡的锡器 7.化学与生活息息相关,下列生产生活中的事实涉及的方程式错误的是
C.婺源砖雕的青砖 D.广昌孟戏的传统戏服 A.氢氟酸刻蚀玻璃:4HF+SiO SiF↑+2HO
2 4 2
点燃 电解
2.Na与少量的 CO 会发生反应:4Na+CO 2NaO+C,下列说法错误的是 B.工业制备金属钠:4Na++2HO4Na+O↑+4H+
2 2 2 2 2
高温
A.CO 的空间填充模型: C.工业用焦炭还原石英砂制粗硅:2C+SiO Si+2CO↑
2 2
D.漂白液中加入食醋用于短时间内增强漂白效果:CHCOOH+ClO-CHCOO-+HClO
·· 3 3
B.NaO的电子式:Na+[ · O · ]2-Na+
2 · ·· · 8.瑞昌市铜岭铜矿遗址对研究中国火法炼铜历史具有重要意义。火法炼铜时会发生反应:2CuFeS+
2
! " 高温
3O 2CuS+2FeO+2SO。设 N 为阿伏加德罗常数的值。下列说法正确的是
2 2 A
A.FeO含有的质子数为34N
C.基态 Na原子2p轨道的电子云轮廓图: ! A
!
B.生成1molCuS的同时会转移4N 个电子
A
!
#
C.25℃、101kPa下,6.72LO 含 σ键数目为0.3N
2 A
D.反应中涉及的元素均位于元素周期表的 p区
D.生成32gSO 的同时消耗 O 的分子数为0.75N
2 2 A
高三化学 第1页(共8页) 高三化学 第2页(共8页)
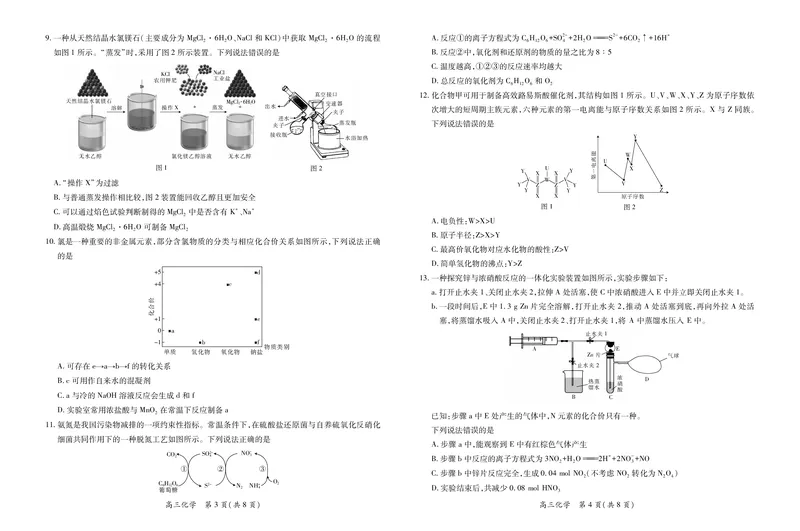
书书书9.一种从天然结晶水氯镁石(主要成分为 MgCl·6HO、NaCl和 KCl)中获取 MgCl·6HO的流程
2 2 2 2
如图1所示。“蒸发”时,采用了图2所示装置。下列说法错误的是
%#$ !"#$
农用钾肥 工业盐
真空接口
天然结晶水氯镁石 &’#$ ( !)* + , 变速器
溶解 操作- . 蒸发 . 出水
夹子
进水
蒸发瓶
夹子
接收瓶 水浴加热
无水乙醇 氯化镁乙醇溶液 无水乙醇
图1 图2
A.“操作 X”为过滤
B.与普通蒸发操作相比较,图2装置能回收乙醇且更加安全
C.可以通过焰色试验判断制得的 MgCl中是否含有 K+、Na+
2
D.高温煅烧 MgCl·6HO可制备 MgCl
2 2 2
10.氯是一种重要的非金属元素,部分含氯物质的分类与相应化合价关系如图所示,下列说法正确
的是
#
$
"
&
% !
物质类别
单质 氢化物 氧化物 钠盐
高三化学 第3页(共8页) 高三化学 第4页(共8页)
价合化
A.反应①的离子方程式为 CH O+SO2-+2HOS2-+6CO↑+16H+
6 12 6 4 2 2
B.反应②中,氧化剂和还原剂的物质的量之比为8∶5
C.温度越高,①②③的反应速率均越大
D.总反应的氧化剂为 CH O 和 O
6 12 6 2
12.化合物甲可用于制备高效路易斯酸催化剂,其结构如图 1所示。U、V、W、X、Y、Z为原子序数依
次增大的短周期主族元素,六种元素的第一电离能与原子序数关系如图 2所示。X与 Z同族。
下列说法错误的是
"
$
%
& #
% %
! !
$ # $
% " " % &
% % !
! ! !"#$
图1
’(
’)
’*
,
+*
A.可存在 e→a→b→f的转化关系
B.c可用作自来水的混凝剂
C.a与冷的 NaOH溶液反应会生成 d和 f
D.实验室常用浓盐酸与 MnO 在常温下反应制备 a
2
11.氨氮是我国污染物减排的一项约束性指标。常温条件下,在硫酸盐还原菌与自养硫氧化反硝化
细菌共同作用下的一种脱氮工艺如图所示。下列说法正确的是
!" # *"# ) % $"% &
! " #
! + ’ ,# " + *#% $ $’( " # 葡萄糖 # )
)(’&%
图2
A.电负性:W>X>U
B.原子半径:Z>X>Y
C.最高价氧化物对应水化物的酸性:Z>V
D.简单氢化物的沸点:Y>Z
13.一种探究锌与浓硝酸反应的一体化实验装置如图所示,实验步骤如下:
a.打开止水夹1、关闭止水夹2,拉伸 A处活塞,使 C中浓硝酸进入 E中并立即关闭止水夹1。
b.一段时间后,E中1.3gZn片完全溶解,打开止水夹 2,推动 A处活塞到底,再向外拉 A处活
塞,将蒸馏水吸入 A中,关闭止水夹2、打开止水夹1,将 A中蒸馏水压入 E中。
止水夹!
( ’
"# 片 气球
止水夹$
浓 ) 热蒸
硝
馏水
酸
% &
已知:步骤 a中 E处产生的气体中,N元素的化合价只有一种。
下列说法错误的是
A.步骤 a中,能观察到 E中有红棕色气体产生
B.步骤 b中反应的离子方程式为3NO+HO2H++2NO-+NO
2 2 3
C.步骤 b中锌片反应完全,生成0.04molNO(不考虑 NO 转化为 NO)
2 2 2 4
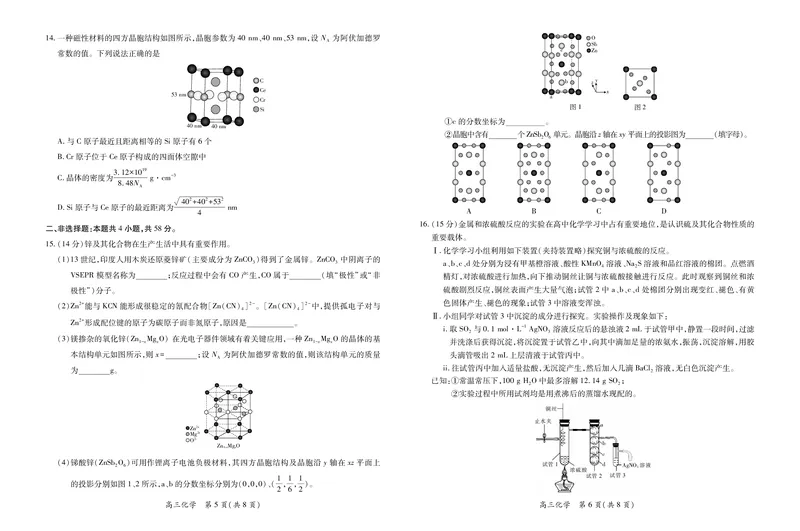
D.实验结束后,共减少0.08molHNO 314.一种磁性材料的四方晶胞结构如图所示,晶胞参数为 40nm、40nm、53nm,设 N 为阿伏加德罗 !
A
"#
常数的值。下列说法正确的是 & $%
% # # "
%& !
!"#$
’
%’
图1 图2
()
①c的分数坐标为 。
*+#$ ,+#$
②晶胞中含有 个ZnSbO单元。晶胞沿z轴在xy平面上的投影图为 (填字母)。
2 6
A.与 C原子最近且距离相等的 Si原子有6个
B.Cr原子位于 Ce原子构成的四面体空隙中
3.12×1019
C.晶体的密度为 g·cm-3
8.48N
A
槡402+402+532
D.Si原子与 Ce原子的最近距离为 nm
4 A B C D
16.(15分)金属和浓硫酸反应的实验在高中化学学习中占有重要地位,是认识硫及其化合物性质的
二、非选择题:本题共4小题,共58分。
重要载体。
15.(14分)锌及其化合物在生产生活中具有重要作用。
Ⅰ.化学学习小组利用如下装置(夹持装置略)探究铜与浓硫酸的反应。
(1)13世纪,印度人用木炭还原菱锌矿(主要成分为 ZnCO)得到了金属锌。ZnCO 中阴离子的
3 3 a、b、c、d处分别为浸有甲基橙溶液、酸性 KMnO 溶液、NaS溶液和品红溶液的棉团。点燃酒
4 2
VSEPR模型名称为 ;反应过程中会有 CO产生,CO属于 (填“极性”或“非 精灯,对浓硫酸进行加热,向下推动铜丝让铜与浓硫酸接触进行反应。此时观察到铜丝和浓
极性”)分子。 硫酸剧烈反应,铜丝表面产生大量气泡;试管 2中 a、b、c、d处棉团分别出现变红、褪色、有黄
(2)Zn2+能与 KCN能形成很稳定的氰配合物[Zn(CN)]2-。[Zn(CN)]2-中,提供孤电子对与 色固体产生、褪色的现象;试管3中溶液变浑浊。
4 4
Ⅱ.小组同学对试管3中沉淀的成分进行探究。实验操作及现象如下:
Zn2+形成配位键的原子为碳原子而非氮原子,原因是 。
i.取 SO 与0.1mol·L-1AgNO 溶液反应后的悬浊液2mL于试管甲中,静置一段时间,过滤
2 3
(3)镁掺杂的氧化锌(Zn MgO)在光电子器件领域有着关键应用,一种 Zn MgO的晶体的基
1-x x 1-x x 并洗涤后获得沉淀,将沉淀置于试管乙中,向其中滴加足量的浓氨水,振荡,沉淀溶解,用胶
本结构单元如图所示,则 x= ;设 N 为阿伏加德罗常数的值,则该结构单元的质量 头滴管吸出2mL上层清液于试管丙中。
A
ii.往试管丙中加入适量盐酸,无沉淀产生,然后加入几滴 BaCl溶液,无白色沉淀产生。
为 g。
2
已知:①常温常压下,100gHO中最多溶解12.14gSO;
2 2
②实验过程中所用试剂均是用煮沸后的蒸馏水现配的。
!"
#$%
(
!"#$
%&#$
’#(
)
!" %&’
)*! !
*
(4)锑酸锌(ZnSbO)可用作锂离子电池负极材料,其四方晶胞结构及晶胞沿 y轴在 xz平面上
2 6 &’! + $%&’ +,
"
()*
1 1 1 &’# &’"
的投影分别如图1、2所示,a、b的分数坐标分别为(0,0,0)、( , , )。
2 6 2
高三化学 第5页(共8页) 高三化学 第6页(共8页)请回答下列问题: 18.(15分)铜是人类最早发现和使用的金属之一,碘量法是测定黄铜中铜含量的常见方法之一,实
(1)组装好装置后,在加药品之前需要进行的操作为 ;实验过程中,需要取用 8.0mL浓 验步骤如下:
硫酸,则取用8.0mL浓硫酸所需要的实验室常见玻璃仪器有 。 i.称取1.25g黄铜试样(主要成分为Cu、Zn及微量的Fe)于烧杯中,加入 20.00mL8.00mol·L-1
(2)试管1中,铜丝与浓硫酸反应的化学方程式为 。 硝酸,盖上表面皿,低温加热,待试样完全溶解后冷却,用少量水冲洗杯壁和表面皿并将洗涤液
(3)试管2中 a处棉团现象说明有酸性物质生成;b处棉团褪去颜色时,发生反应的离子方程式 合并至烧杯中,继续加热蒸干溶液得到固体。将所得固体配制成500mL溶液 a。
为 ;c处棉团的现象说明 SO 具有 性(填化学性质)。 ii.吸取20.00mL溶液 a置于碘量瓶(如图)中,滴加乙酸—乙酸铵溶液调节 pH3~4;加入几滴
2
(4)请利用原实验装置,设计实验方案证明 SO 的漂白是可逆的: 指示剂 X后滴加 NHF饱和溶液至红色消失,得到溶液 b。
2 4
(写出必要的操作及实验现象)。 iii.向溶液 b中加1.00gKI(足量),塞紧瓶塞摇匀。用 0.10mol·L-1NaSO 标准液滴定至溶
2 2 3
(5)①忽略通入气体造成溶液体积的变化,常温常压下,饱和 SO 水溶液中,c(SO)+c(HSO)+ 液黄色几乎消失,滴加2滴淀粉溶液,继续滴定至终点,记录标准液消耗的体积为 VmL。
2 2 2 3
c(HSO-)+c(SO2-)≈ mol·L-1(保留小数点后1位数字)。 iv.重复实验三次,V的平均值为6.00。
3 3
②通过实验可知,试管3中的沉淀的成分为 (填化学式);加入浓氨水后,沉淀溶解
已知:①F-与 Fe3+能形成比[Fe(SCN)](n-3)-更稳定的[FeF]3-配合物;
n 6
时反应的离子方程式为 。 ②步骤 iii中会发生反应:I+2SO2-2I-+SO2-。
2 2 3 4 6
17.(14分)金属冶炼过程中产生的二次金粉具有重要的价值。一种从二次金粉(主要成分为 TeO、
2
Au、Zn、Cu、Pd和 Se)中回收金粉和硒的工艺流程如图所示。
6%!%&’(!
8% %&’($ 5% ’(4 #$
) "
!"
%& %&1 ’()* ’(2 +,! -. /0 .2 +," 3
#$ 碘量瓶
%&2 .1! 7#$ 请回答下列问题:
已知:①TeO(二氧化碲)能溶解在盐酸中:TeO+4HClTeCl+2HO;
2 2 4 2 (1)步骤 i中配制500mL溶液 a的过程中,下列操作示意图按先后排序为 (填字母),
②“氯化溶解”时,发生了反应:2Au+ClO-+6H++7Cl-2[AuCl]-+3HO、3Pd+2ClO-+
3 4 2 3 其中的仪器甲在使用之前需要进行的操作为 。
12H++16Cl-3[PdCl]2-+6HO。
6 2
请回答下列问题:
(1)基态 Cu原子价层电子排布式为 ;基态 Se原子的 M能层与 N能层的电子数之比为
!
"#$
(填最简整数比)。
% $ # " !
(2)写出一种能加快“酸浸”速率的措施: ;“酸浸液”中,存在的金属阳离子为
(2)步骤 ii中“指示剂 X”为 (填化学式)溶液;滴加 NHF饱和溶液的目的是
4
(填离子符号)。
。
(3)“氯化溶解”时,Se转化为 HSeO,反应过程中无气体产生。该反应的离子方程式为
2 3
(3)步骤 iii中,加入 KI溶液后会生成 CuI沉淀,反应的离子方程式为 ;判断滴定达
。
到终点的现象为 。
(4)“还原1”时,只有 HAuCl被还原,HAuCl转化为金粉的化学方程式为
4 4
(4)实验测得黄铜中铜的质量分数为 %;若用锥形瓶代替碘量瓶进行实验,则会导致实
。
验测定结果 (填“偏高”“偏低”或“无影响”)。
(5)“沉钯”时生成了(NH)[PdCl],1mol(NH)[PdCl]含有 mol配位键。
4 2 6 4 2 6
(6)“还原2”中,若消耗了400mol还原剂,则理论上能生成 kg硒。
高三化学 第7页(共8页) 高三化学 第8页(共8页)