文档内容
化学答案
1.C 2.B 3.C 4.B 5.B 6.D 7.D 8.C 9.C 10.B 11.C 12.C 13.D 14.D
15.(15分)(1)3d104s1(2分)
(2)4CuFeS +5O +20H+=4Cu2++4Fe3++10H O+8S(2分)PbSO (1分)
2 2 2 4
(3)85℃之后,氧气浓度随温度的升高而降低,浸出率下降。(2分)
(4)Cu2++S O2-+H O=CuS↓+SO2-+2H+(2分)
2 2 4
3
酸性环境下,Na S O 发生歧化反应造成Na S O 的损耗(或Fe3+在非酸性条件下也能氧化S O2-)
2 2 3 2 2 3 2
(2分) 3
(5)Cu2++HS-=CuS↓+H+,K=c(H+)/[c(Cu2+) c(HS-)]=K (H S)/K (CuS)=7.1×10-15÷6.3×10-36
a2 2 sp
=1.13×1021>>105,Cu2+可以完全沉淀(2分)
⋅
(6)Zn2+、Fe2+(2分)
16.(14分)
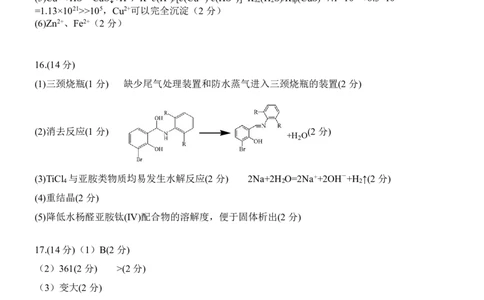
(1)三颈烧瓶(1 分) 缺少尾气处理装置和防水蒸气进入三颈烧瓶的装置(2 分)
(2)消去反应(1 分) (2 分)
+H O
2
(3)TiCl 与亚胺类物质均易发生水解反应(2 分) 2Na+2H O=2Na++2OH-+H ↑(2 分)
4 2 2
(4)重结晶(2 分)
(5)降低水杨醛亚胺钛(Ⅳ)配合物的溶解度,便于固体析出(2 分)
17.(14分)(1)B(2分)
(2)361(2 分) >(2分)
(3)变大(2 分)
(4)1:12(2分) 不变(2分)
(5)2.7(2分)
18.(15分)
(1)醚键、碳氯键(2 分) 间硝基苯甲醛(或3−硝基苯甲醛)(1 分)
1(2) (2 分) 酯化反应(或取代反应)(1分)
(3)弱(1 分) 化合物E 与H O形成的分子间氢键数目更多(1 分)
2
(4)AB(2 分)
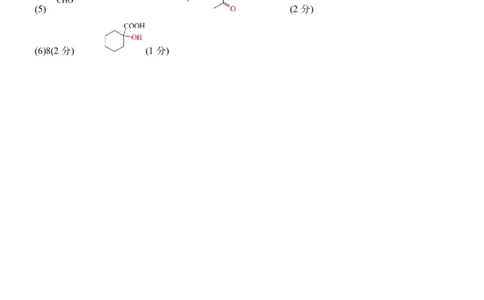
(5) (2 分)
(6)8(2 分) (1 分)
2