文档内容
相对原子质量:H-1 C-12 N-14 O-16 Na-23 Si一28 Cl-35.5 K-39 Cu-64 Se-79
一、选择题(本题共10分,每小题2分,每题只有一个正确选项)
1.今年3月修订的《环境空气质量标准》中新纳入的强制监测指标是( )
A.PM2.5 B.NOx C.SO D.可吸入颗粒物
2
2.下列关于化石燃料的加工说法正确的是( )
A.石油裂化主要得到乙烯
B.石油分馏是化学变化,可得到汽油、煤油
C.煤干馏主要得到焦炭、煤焦油、粗氨水和焦炉气
D.煤制煤气是物理变化,是高效、清洁地利用煤的重要途径
3.氮氧化铝(AlON)属原子晶体,是一种超强透明材料,下列描述错误的是( )
A.AlON和石英的化学键类型相同 B.AlON和石英晶体类型相同
C.AlON和Al O 的化学键类型不同 D.AlON和Al O 晶体类型相同
2 3 2 3
【答案】D
【解析】
第1页 | 共20页4.PH 一种无色剧毒气体,其分子结构和NH 相似,但P-H键键能比N-H键键能低。下列判断错误的是(
3 3
)
A.PH 分子呈三角锥形
3
B.PH 分子是极性分子
3
C.PH 沸点低于NH 沸点,因为P-H键键能低
3 3
D.PH 分子稳定性低于NH 分子,因为N-H键键能高
3 3
5.和氢硫酸反应不能产生沉淀的是( )
A.Pb(NO ) 溶液 B.NaS洛液 C.CuSO 溶液 D. H SO 溶液
3 2 2 4 2 4
二、选择题(本题共36分,每小题3分,每题只有一个正确选项)
6.元素周期表中铋元素的数据见右图,下列说法正确的是( )
A.Bi元素的质量数是209
第2页 | 共20页B.Bi元素的相对原子质量是209.0
C.Bi原子6p亚层有一个未成对电子
D.Bi原子最外层有5个能量相同的电子
7.水中加入下列溶液对水的电离平衡不产生影响的是( )
A.NaHSO 溶液 B.KF溶液 C.KAl(SO ) 溶液 D.NaI溶液
4 4 2
8.过量的下列溶液与水杨酸( )反应能得到化学式为C HONa的是( )
7 5 3
A.NaHCO 溶液 B.NaCO 溶液 C.NaOH溶液 D.NaCl溶液
3 2 3
第3页 | 共20页9.工业生产水煤气的反应为:C(s)+HO(g)→CO(g)+H (g)-131.4 kJ
2 2
下列判断正确的是( )
A.反应物能量总和大于生成物能量总和
B.CO(g)+H(g)→C(s)+H O(l)+131.4kJ
2 2
C.水煤气反应中生成1 mol H (g)吸收131.4 KJ热量
2
D.水煤气反应中生成1体积CO(g)吸收131.4 KJ热量
[来源:Zxxk.Com]
10.用滴定法测定NaCO(含NaCl杂质)的质量分数,下列操作会引起测定值偏高的是( )
2 3
A.试样中加入酚酞作指示剂,用标准酸液进行滴定
B.滴定管用蒸馏水洗涤后,直接注入标准酸液进行滴定
C.锥形瓶用蒸馏水洗涤后,壹接加入待测溶液进行滴定
D.滴定管用蒸馏水洗涤后,直接注入待测液,取20.00 mL进行滴定
11.工业上将氨气和空气的混合气体通过铂一铑合金网发生氨氧化反应,若有标准状况下 VL氨气完全反
应。并转移n个电子,则阿伏加德罗常数(N )可表示为( )
A
第4页 | 共20页12.下列有机化合物中均含有酸性杂质,除去这些杂质的方法中正确的是( )
A.苯中含苯酚杂质:加入溴水,过滤
B.乙醇中含乙酸杂质:加入碳酸钠溶液洗涤,分液
C.乙醛中含乙酸杂质:加入氢氧化钠溶液洗涤,分液
D.乙酸丁酯中含乙酸杂质:加入碳酸钠溶液洗涤,分液
13.下列关于硫酸工业生产过程的叙述错误的是( )
A.在接触室中使用铁粉作催化剂
B.在接触室中运用热交换技术可充分利用能源
C.把硫铁矿磨成细粉末,可以提高原料的利用率
D.该反应采用450℃~500℃主要是因为该温度下催化剂活性好
14.右图装置中发生反应的离子方程式为:Zn+2H+→Zn2++H ↑,下列说法错误的是( )
2
A.a、b不可能是同种材料的电极
第5页 | 共20页B.该装置可能是电解池,电解质溶液为稀盐酸
C.该装置可能是原电池,电解质溶液为稀盐酸
D.该装置可看作是铜-锌原电池,电解质溶液是稀硫酸
15.下图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO 晶体滴加一滴
4
浓盐酸后,立即用另一培养皿扣在上面。
已知:2KMnO +16HCl→2KCl+5Cl ↑+2MnCl +8H O
4 2 2 2
对实验现象的“解释或结论”正确的是( )
选项 实验现象 解释或结论
A a处变蓝,b处变红棕色 氧化性:Cl>Br >I
2 2 2
B c处先变红,后褪色 氯气与水生成了酸性物质
C d处立即褪色7 氯气与水生成了漂白性物质
D e处变红色 还原性:Fe2+>Cl-
【答案】D
【解析】
第6页 | 共20页16.实验室制取少量干燥的氨气涉及下列装置,其中正确的是( )
A.①是氨气发生装置 B.③是氨气发生装置
C.②是氨气吸收装置 D.④是氨气收集、检验装置
17.将l00ml 1mol/L 的NaHCO 溶液等分为两份,其中一份加入少许冰醋酸,另外一份加入少许Ba(OH)
3 2
固体,忽略溶液体积变化。两份溶液中c(CO2-)的变化分别是( )
3 [来源:学科网ZXXK]
A.减小、减小 B.减小、增大 C.增大、增大 D.增大、减小
第7页 | 共20页三、选择题(本题共20分,每小题4分,每小题有一个或两个正确选项。只有一个正确选项的,多选不给
分;有两个正确选项的,选对一个给2分,选错一个,该小题不给分)
18.为探究锌与稀硫酸的反应速率(以v(H )表示),向反应混合液中加入某些物质,下列判断正确的是(
2
)
A.加入NH HSO 固体,v(H )不变 B.加入少量水,v(H )减小
4 4 2 2
C.加入CHCOONa固体,v(H )减小 D.滴加少量CuSO 溶液,v(H )减小
3 2 4 2
19.含有下列各组离子的溶液中,通入过量SO 气体后仍能大量共存的是( )
2
A.H+、Ca2+、Fe3+、N0 - B.Ba2+、Cl-、Al3+、H+
3
C.Na+、NH +、I-、HS- D.Na+、Ca2+、K+、Cl-
4
第8页 | 共20页20.火法炼铜首先要焙烧黄铜矿,其反应为:2CuFeS+O →Cu S+2FeS+SO
2 2 2 2
下列说法正确的是( )
A.SO 既是氧化产物又是还原产物
2
B.CuFeS 仅作还原剂,硫元素被氧化
2
C.每生成1 molCu S,有4mol硫被氧化
2
D.每转移1.2 mol电子,有0.2 mol硫被氧化
【答案】AD
21.常温下a mol/L CH COOH稀溶液和b mol/L KOH稀溶液等体积混合,下列判断一定错误的是(
3
)
A.若c(OH-)>c(H+),a=b B.若c(K+)>c(CH COO-),a>b
3 [来源:学#科#网Z#X#X#K]
C.若c(OH-)=c(H+),a>b D.若c(K+)0)
4 2 2 3 4 2
完成下列填空:
31.在一定温度下进行上述反应,若反应容器的容积为2 L,3 min后达到平衡,测得固体的质量增
加了2.80 g,则H 的平均反应速率___ mol/(L·min);该反应的平衡常数表达式K=_____
2
32.上述反应达到平衡后,下列说法正确的是_。
a.其他条件不变,压强增大,平衡常数K减小
b.其他条件不变,温度升高,平衡常数K减小
c.其他条件不变,增大Si N 物质的量平衡向左移动
3 4
d.其他条件不变,增大HCl物质的量平衡向左移动
33.一定条件下,在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是__。
a.3v (N )=v (H ) b.v (HCl)=4v (SiCl )
逆 2 正 2 正 正 4
c.混合气体密度保持不变 d.c(N):c(H):c(HCl)=1:3:6
2 2
m
34.若平衡时H 和HCl的物质的量之比为n,保持其它条件不变,降低温度后达到新的平衡时,H
2 2
第12页 | 共20页m
和HCl的物质的量之比___n(填“>”、“=”或“<”)。
[来源:学科网]
七、(本题共12分)
碱式碳酸铜【Cu (OH) CO 】是一种用途广泛的化工原料,实验室以废铜屑为原料制取碱式碳酸
2 2 3
铜的步骤如下:
步骤一:废铜屑制硝酸铜
如图,用胶头滴管吸取浓HNO3缓慢加到锥形瓶内的废铜屑中(废铜屑过量),充分反应后过滤,得
到硝酸铜溶液。
步骤二:碱式碳酸铜的制备
向大试管中加入碳酸钠溶液和硝酸铜溶液,水浴加热至70℃左右,用0.4 mol/L的NaOH溶液
第13页 | 共20页调节pH至8.5,振荡,静置,过滤,用热水洗涤,烘干,得到碱式碳酸铜产品。
完成下列填空:
35.写出浓硝酸与铜反应的离子方程式。
36.上图装置中NaOH溶液的作用是__。反应结束后,广口瓶内的溶液中,除了含有NaOH外,还
有____(填写化学式)。
37.步骤二中,水浴加热所需仪器有____、__(加热、夹持仪器、石棉网除外);洗涤的目的是____。
38.步骤二的滤液中可能含有CO2-,写出检验CO2-的方法。
3 3
39.影响产品产量的主要因素有____。
40.若实验得到2.42 g样品(只含CuO杂质),取此样品加热至分解完全后,得到1.80 g固体,此样品
中碱式碳酸铜的质量分数是____。
八、(本题共12分)
碳酸氢铵是一种重要的铵盐。实验室中,将二氧化碳通入氨水可制得碳酸氢铵,用碳酸氢铵和氯
化钠可制得纯碱。
完成下列填空:
41.二氧化碳通入氨水的过程中,先有__晶体(填写化学式)析出,然后晶体溶解,最后析出
NH HCO 晶体。
4 3
第14页 | 共20页42.含0.800 mol NH3的水溶液质量为54.0 g,向该溶液通入二氧化碳至反应完全,过滤,得到滤液
31.2g,则NH HCO 的产率为____%。
4 3
43.粗盐(含Ca2+、Mg2+)经提纯后,加入碳酸氢铵可制得碳酸钠。实验步骤依次为:
①粗盐溶解;②加入试剂至沉淀完全,煮沸;③__;④加入盐酸调pH;⑤加入__;⑥过滤;⑦
灼烧,冷却,称重。
44.上述步骤②中所加入的试剂为_ _、_ _。
45.上述步骤④中加盐酸调pH的目的是__。
46.为探究NH HCO 和NaOH的反应,设计实验方案如下:
4 3
含0.1 mol NH HCO 的溶液中加入0.1 mol NaOH,反应完全后,滴加氯化钙稀溶液。
4 3
若有沉淀,则NH HCO 与NaOH的反应可能为_____(写离子方程式);
4 3
若无沉淀,则NH HCO 与NaOH的反应可能为______(写离子方程式)。
4 3
该实验方案有无不妥之处?若有,提出修正意见。
九、(本题共8分)
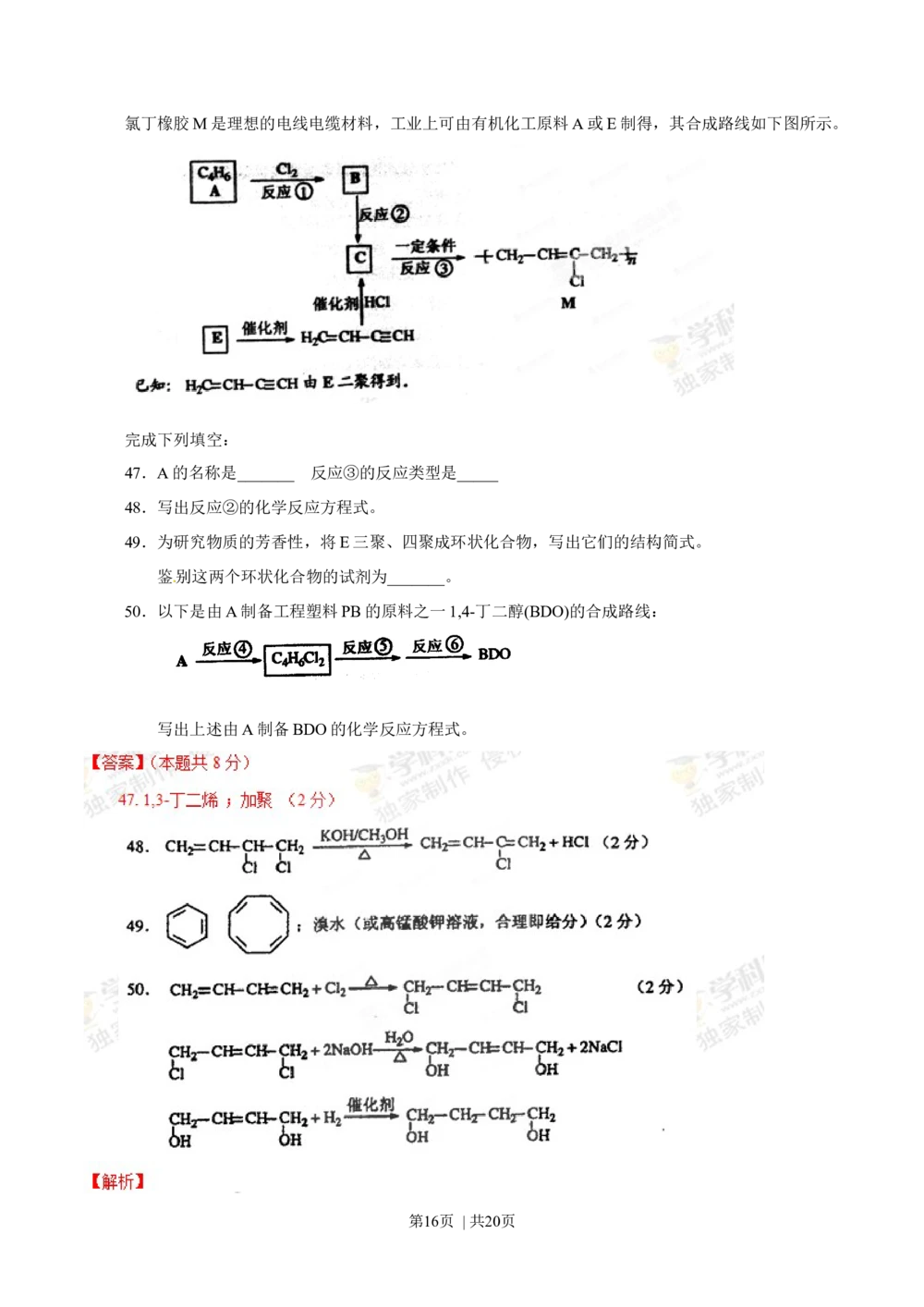
第15页 | 共20页氯丁橡胶M是理想的电线电缆材料,工业上可由有机化工原料A或E制得,其合成路线如下图所示。
完成下列填空:
47.A的名称是_______ 反应③的反应类型是_____
48.写出反应②的化学反应方程式。
49.为研究物质的芳香性,将E三聚、四聚成环状化合物,写出它们的结构简式。
鉴别这两个环状化合物的试剂为_______。
50.以下是由A制备工程塑料PB的原料之一1,4-丁二醇(BDO)的合成路线:
写出上述由A制备BDO的化学反应方程式。
第16页 | 共20页十、(本题共12分)
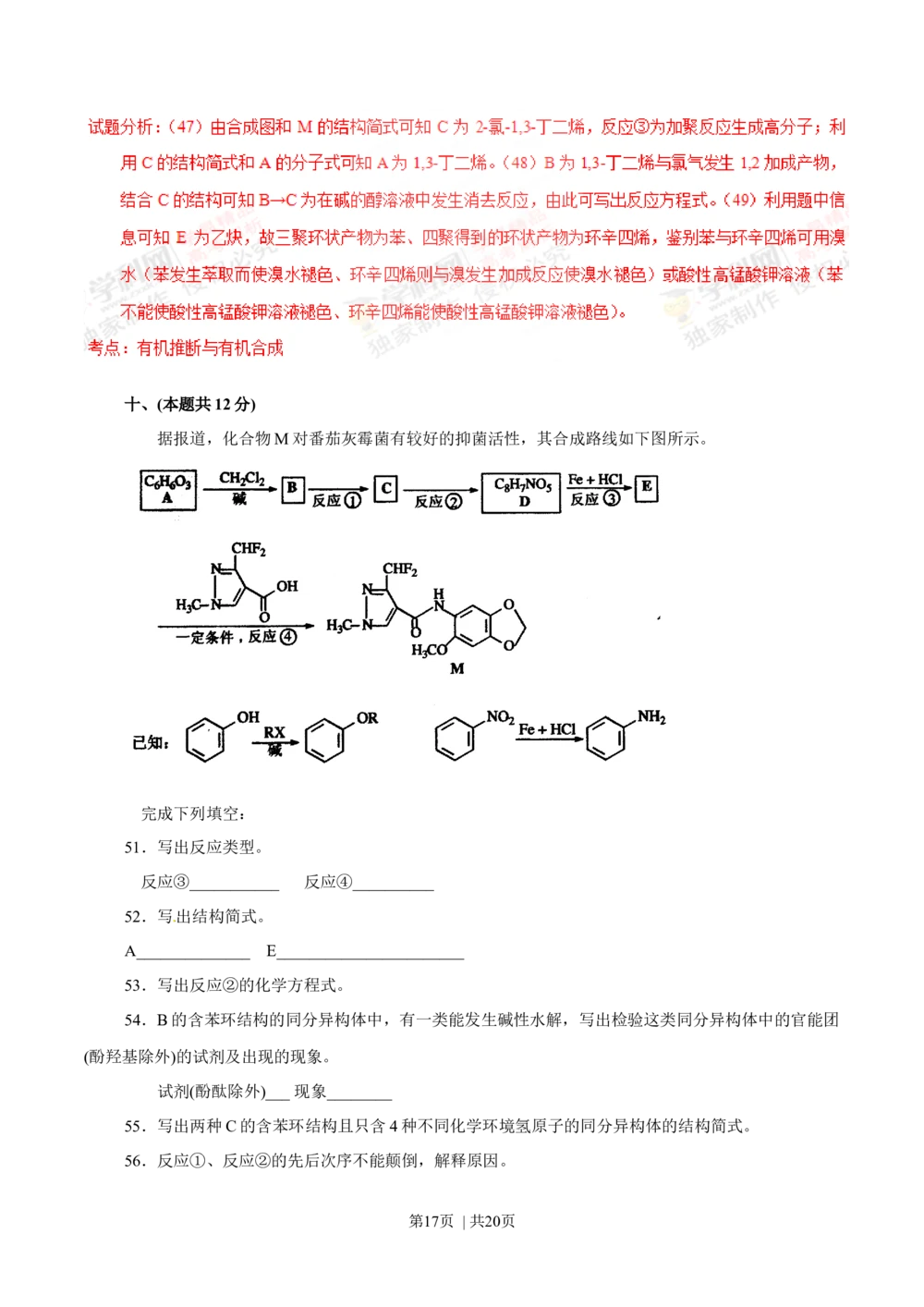
据报道,化合物M对番茄灰霉菌有较好的抑菌活性,其合成路线如下图所示。
完成下列填空:
51.写出反应类型。
反应③___________ 反应④__________
52.写出结构简式。
A______________ E_______________________
53.写出反应②的化学方程式。
54.B的含苯环结构的同分异构体中,有一类能发生碱性水解,写出检验这类同分异构体中的官能团
(酚羟基除外)的试剂及出现的现象。
试剂(酚酞除外)___ 现象________
55.写出两种C的含苯环结构且只含4种不同化学环境氢原子的同分异构体的结构简式。
56.反应①、反应②的先后次序不能颠倒,解释原因。
第17页 | 共20页十一、(本题共16分)
钠是活泼的碱金属元素,钠及其化合物在生产和生活中有广泛的应用。
第18页 | 共20页完成下列计算:
57.叠氮化钠(NaN )受撞击完全分解产生钠和氮气,故可应用于汽车安全气囊。若产生40.32 L(标准
3
状况下)氮气,至少需要叠氮化钠___g。
58.钠-钾合金可在核反应堆中用作热交换液。5.05 g钠-钾合金溶于200 mL水生成0.075 mol氢气。
(1)计算溶液中氢氧根离子的物质的量浓度(忽略溶液体积变化)。
(2)计算并确定该钠-钾合金的化学式。
59.氢氧化钠溶液处理铝土矿并过滤,得到含铝酸钠的溶液。向该溶液中通入二氧化碳,有下列反
应:
2NaAl(OH) +CO →2Al(OH) ↓ +Na CO+H O
4 2 3 2 3 2
己知通入二氧化碳336 L(标准状况下),生成24 mol Al(OH) 和15 mol Na CO ,若通入溶液的二氧
3 2 3
化碳为112L(标准状况下),计算生成的Al(OH) 和NaCO 的物质的量之比。
3 2 3
60.常温下,称取不同氢氧化钠样品溶于水,加盐酸中和至pH=7,然后将溶液蒸干得氯化钠晶体,
蒸干过程中产品无损失。
氢氧化钠质量(g) 氯化钠质量(g)
① 2.40 3.51
② 2.32 2.34
③ 3.48 3.51
上述实验①②③所用氢氧化钠均不含杂质,且实验数据可靠。通过计算,分析和比较上表3组数据,
给出结论。
第19页 | 共20页第20页 | 共20页