文档内容
【试卷总评】1.试题继续坚持考查学生的基础知识,考查的内容都是重点内容。如:化学与
生活(第6题)、阿伏加德罗常数(第7题)、元素周期表和元素周期律(第8题)、离子方程式
正误判断(第9题)、离子浓度大小的比较(第10题)、原电池(第11题)、化学反应速率和化学
平衡(第12题)、无机化合物的计算(第13题)、无机推断(第26题)、有机反应类型的判断、
有机分子中原子共面的判断、有机化学方程式的书写等 (第27题)、仪器的识别、气密性的
检查、实验误差解释、相关计算、实验评价及设计(第28题)、化学式的推断、方程式书写、
热化学方程式的书写、同分异构体的书写(第29题)。
2.紧扣教材。如第9题四个离子方程式均直接源自课本内容。它对教学中重视教材的使
用会起到不可估量的作用。
3.注重实验能力的考查。化学是以实验为基础的科学。《考试说明》明确指出“设计和完成
实验的能力”,可见高考对实验能力的要求是比较高的。试卷中28题以制取NH 和氨气中
3
N、H原子个数测定来考查化学实验基础知识,涉及到仪器的识别、气密性的检查、实验误差解
释、相关计算、实验评价及设计;
总之,2012年化学试题的质量是好的,能较好区分考生知识和能力水平的高低,同时它的
命题思想对今后的中学化学教学发挥了良好的指挥棒的作用。
2012 年全国高考(四川卷)理综综合化学部分
6.下列关于“化学与健康”的说法不正确的是
A.服用铬含量超标的药用胶囊会对人体健康造成危害
B.食用一定量的油脂能促进人体对某些维生素的吸收
C.“血液透析”利用了胶体的性质
D.光化学烟雾不会引起呼吸道疾病
7.设N 为阿伏加德罗常数的值,下列叙述正确的是
A
A.标准状况下,33.6L氟化氢中含有氟原子的数目为1.5N
A
B.常温常压下,7.0g乙烯与丙烯的混合物中含有氢原子的数目为N
A
C.50mL 18.4mol/L浓硫酸与足量铜微热反应,生成SO 分子数目为0.46N
2 A
D.某密闭容器盛有0.1molN 和0.3molH ,在一定条件下充分反应,转移电子的数目为0.6N
2 2 A
8.已知W、X、Y、Z为短周期元素,W、Z同主族,X、Y、Z同周期,W的气态氢化物的稳
定性大于Z的气态氢化物稳定性,X、Y为金属元素,X的阳离子的氧化性小于Y的阳离子的
第1页 | 共8页氧化性,下列说法正确的是
[来源:Z&xx&k.Com]
A.X、Y、Z、W的原子半径依次减小
B.W与X形成的化合物中只含离子键
C.W的气态氢化物的沸点一定高于Z的气态氢化物的沸点
D.若W与Y的原子序数相差5,则二者形成化合物的化学式一定为Y W
2 3
9.下列离子方程式正确的是
[来源:学&科&网]
A.钠与水反应:Na + 2H O = Na+ + 2OH- + H ↑
2 2
B.硅酸钠溶液与醋酸溶液混合:SiO 2- + 2H+ = H SiO ↓
3 2 3
C.0.01mol/LNH Al(SO ) 溶液与0.02mol/LBa(OH) 溶液等体积混合:
4 4 2 2
NH + +Al3+ + 2SO 2- + 2Ba2+ + 4OH- = 2BaSO ↓ + Al(OH) ↓ + NH ·H O
4 4 4 3 3 2
△
D.浓硝酸中加入过量铁粉并加热:Fe + 3NO - + 6H+ Fe3+ + 3NO ↑ + 3H O
3 2 2
【答案】:C
【解析】:Na + 2H O = Na+ + 2OH- + H ↑电荷不守恒,A不正确;醋酸是弱酸,要用分子式
2 2
表示,B不正确;浓硝酸中加入过量铁粉时,产物应为Fe2+,D不正确。
【考点定位】本题考查离子方程式的书写和正误判断。涉及到氧化还原反应和复分解反应离
子反应。
10.常温下,下列溶液中的微粒浓度关系正确的是
A.新制氯水中加入固体NaOH:c(Na+) = c(Cl-) + c(ClO-) + c(OH-)
B.pH = 8.3的NaHCO 溶液:c(Na+) > c(HCO -) > c(CO 2-) > c(H CO )
3 3 3 2 3
C.pH = 11的氨水与pH = 3的盐酸等体积混合:c(Cl-) = c(NH +) > c(OH-) = c(H+)
4
D.0.2mol/LCH COOH溶液与0.1mol/LNaOH溶液等体积混合:
3
2c(H+) – 2c(OH-) = c(CH COO-) – c(CH COOH)
3 3
11.一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为:CH CH OH – 4e- + H O =
3 2 2
CH COOH + 4H+。下列有关说法正确的是
3
第2页 | 共8页A.检测时,电解质溶液中的H+向负极移动
B.若有0.4mol电子转移,则在标准状况下消耗4.48L氧气
[来源:学科网]
C.电池反应的化学方程式为:CH CH OH + O = CH COOH + H O
3 2 2 3 2
D.正极上发生的反应为:O + 4e- + 2H O = 4OH-
2 2
12.在体积恒定的密闭容器中,一定量的SO 与1.100molO 在催化剂作用下加热到600℃发
2 2
催化剂
生反应:2SO + O 2SO ,ΔH<0。当气体的物质的量减少0.315mol时反应达到平
2 2 加热 3
衡,在相同温度下测得气体压强为反应前的82.5%。下列有关叙述正确的是
A.当SO 的生成速率与SO 的消耗速率相等时反应达到平衡
3 2
B.降低温度,正反应速率减小程度比逆反应速率减小程度大
C.将平衡混合气体通入过量BaCl 溶液中,得到沉淀的质量为161.980g
2
D.达到平衡时,SO 的转化率为90%
2
13.向27.2gCu和Cu O的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成NO
2
和Cu(NO ) ,在所得溶液中加入1.0mol/L的NaOH溶液1.0L,此时溶液呈中性。金属离子已
3 2
完全沉淀,沉淀质量为39.2g。下列有关说法不正确的是
A.Cu与Cu O的物质的量之比为2∶1 B.硝酸的物质的量浓度为2.6mol/L
2
C.产生的NO在标准状况下的体积为4.48L D.Cu、CuO与硝酸反应后剩余HNO 为0.2mol
2 3
【答案】:B
【解析】:设Cu和Cu O的物质的量分别为xmol、ymol,根据题意,则有
2
64x+144y=27.2 ……①
第3页 | 共8页由Cu Cu(OH) Cu O 2Cu(OH) 得34x+68y-16y=39.2-27.2……②,解①②得x=0.2
2 2 2
y=0.1
Cu与Cu O的物质的量之比为0.2∶0.1=2∶1,A正确;硝酸的物质的量为硝酸铜中NaOH和
2
NO的物质的量之和,1.0mol +(0.2 mol×2+0.1 mol×2)/3=1.2 mol,硝酸的物质的量浓度
为1.2 mol /0.5L =2.4 mol/L,B不正确;产生的NO在标准状况下的体积为22.4L/ mol×(0.2 mol
×2+0.1 mol×2)/3=4.48L,C正确;Cu、CuO与硝酸反应后剩余HNO为1.0mol-0.2 mol×
2 3
2-0.1 mol×2×2=0.2mol,D正确。
【考点定位】本题考查铜及其化合物知识和氧化还原反应的计算。
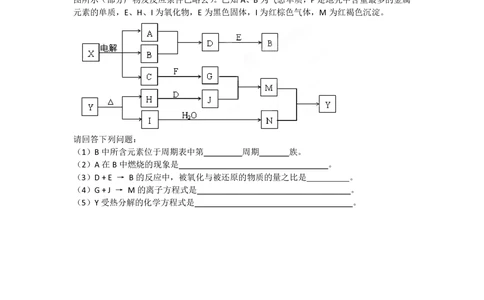
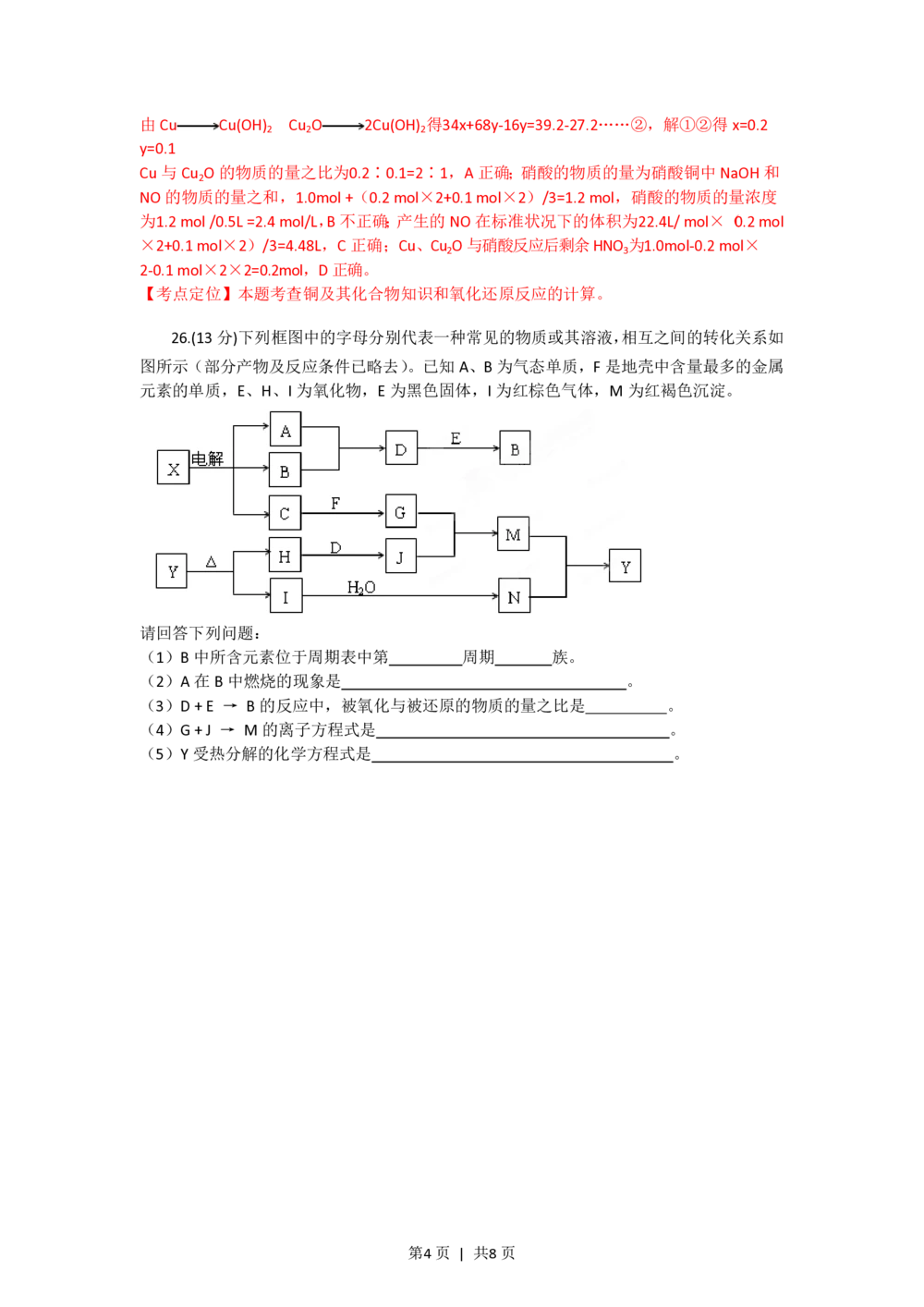
26.(13分)下列框图中的字母分别代表一种常见的物质或其溶液,相互之间的转化关系如
图所示(部分产物及反应条件已略去)。已知A、B为气态单质,F是地壳中含量最多的金属
元素的单质,E、H、I为氧化物,E为黑色固体,I为红棕色气体,M为红褐色沉淀。
请回答下列问题:
(1)B中所含元素位于周期表中第 周期 族。
(2)A在B中燃烧的现象是 。
(3)D + E → B的反应中,被氧化与被还原的物质的量之比是 。
(4)G + J → M的离子方程式是 。
(5)Y受热分解的化学方程式是 。
第4页 | 共8页27.(14分)已知:—CHO + (C H ) P=CH—R → —CH=CH—R + (C H ) P=O,R代表原子或原
6 5 3 6 5 3
子团。W是一种有机合成中间体,结构简式为:HOOC—CH=CH—CH=CH—COOH,其合成发
生如下:
其中,M、X、Y、Z分别代表一种有机物,合成过程中的其他产物和反应条件已略去。X与
W在一定条件下反应可以生成酯N,N的相对分子质量为168。
请回答下列问题:
(1)W能发生反应的类型有 (填写字母编号)
A.取代反应 B.水解反应 C.氧化反应 D.加成反应
(2)已知 为平面结构,则W分子中最多有 个原子在同一平面。
(3)写出X与W在一定条件下反应生成N的化学方程式 。
(4)写出含有3个碳原子且不含甲基的X的同系物的结构简式: 。
(5)写出第②步反应的化学方程式 。
第5页 | 共8页28.(17分)甲、乙两个研究性学习小组为测定氨分子中氮、氢原子个数比,设计如下实验流程:
实验中,先用制的的氨气排尽洗气瓶前所有装置中的空气,再连接洗气瓶和气体收集
装置,立即加热氧化铜。反应完毕后,黑色的氧化铜转化为红色的铜。
下图A、B、C为甲、乙两小组制取氨气时可能用到的装置,D为盛有浓硫酸的洗气瓶。
甲小组测得,反应前氧化铜的质量m g、氧化铜反应后剩余固体的质量m g、生成氮气在标
1 2
准状况下的体积V L。
1
乙小组测得,洗气前装置D的质量m g、洗气后装置D的质量m g、生成氨气在标准状况下
3 4
的体积V L。
2
请回答下列问题:
(1)写出仪器a的名称 。
(2)检查A装置气密性的操作是 。
(3)甲、乙两小组选择了不同的方法制取氨气,请将实验装置的字母编号和制备原理填写
在下表的空格中。
实验装置 实验药品 制备原理
甲小 A 氢氧化钙、硫酸、硫酸 反应的化学方程式为 ① 。
组 铵
[来源:学科网]
乙小 用化学平衡原理分析氢氧化钠的作用:
② 浓氨水、氢氧化钠
组 ③ 。
(4)甲小组用所测得数据计算出氨分子中氮、氢的原子个数之比为 。
第6页 | 共8页(5)乙小组用所测得数据计算出氨分子中氮、氢的原子个数比明显小于理论值,其原因是
。为此,乙小组在原有实验的基础上增加了一个
装有某药品的实验仪器,重新实验。根据实验前后该药品的质量变化及生成氨气的体积,得
出了合理的实验结果。该药品的名称是 。
29.(16分)直接排放煤燃烧产生的烟气会引起严重的环境问题,将 回收CO
2
烟气通过装有石灰石浆液的脱硫装置可以除去其中的二氧化硫,
分离
最终生成硫酸钙。硫酸钙可在右图所示的循环燃烧装置的燃料反
尾气 CO 、H O
2 2
应器中与甲烷反应,气体产物分离出水后得到几乎不含杂质的二氧
化碳,从而有利于二氧化碳的回收利用,达到减少碳排放的目的。空 气 CaSO 燃 料
4
请回答下列问题: 反应器 反应器
CaS
(1)煤燃烧产生的烟气直接排放到空气中,引发的主要环境问
题有 。(填写字母编号) 空气 甲烷
A.温室效应 B.酸雨 C.粉尘污染 D.水体富营养化
(2)在烟气脱硫的过程中,所用的石灰石浆液在进入脱硫装置前,需通一段时间二氧化碳
以增加其脱硫效率;脱硫时控制浆液的pH值,此时浆液含有的亚硫酸氢钙可以被氧气快速
氧化生成硫酸钙。
①二氧化碳与石灰石浆液反应得到的产物为 。
②亚硫酸氢钙被足量氧气氧化生成硫酸钙的化学方程式为 。
[来源:学.科.网]
(3)已知1mol CH 在燃料反应器中完全反应生成气态水时吸收 160.1kJ,1mol CH 在氧气中
4 4
完全燃烧生成气态水时放热802.3kJ。写出空气反应器中发生的热化学方程式:
第7页 | 共8页。
(4)回收的CO 与苯酚钠在一定条件反应生成有机物M,其化学式为C H O Na,M经稀硫
2 7 5 3
酸酸化后得到一种药物中间体N,N的结构简式为 。
①M的结构简式为 。
②分子中无—O—O—,醛基与苯环直接相连的N的同分异构体共有 种。
第8页 | 共8页