文档内容
石家庄市第一中学 2026 届高三年级统一摸底考试
化学试卷
注意事项:
1.本卷满分 100 分,考试时间 75 分钟。答题前,先将自己的姓名、准考证号填写在试题卷
和答题卡上,并将准考证号条形码粘贴在答题卡上的指定位置。2.选择题的作答:每小题选
出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑写在试题卷、草稿纸和答题卡上
的非答题区域均无效。3.非选择题的作答:用签字笔直接答在答题卡上对应的答题区域内。
写在试题卷、草稿纸和答题卡上的非答题区域均无效。
4.考试结束后,请将本试题卷和答题卡一并上交。
可能用到的相对原子质量: H 1 O 16 B 11 N 14 K 39 Fe56 Zn 65 Cu 64
一、选择题:本题共 14 小题,每小题3分,共 42分。每小题只有一个选项符合题目要求。
1.传统文化是中华文明的瑰宝。下列有关传统文化摘要的分析错误的是( )
选项 传统文化摘要 分析
A 日照香炉生紫烟 “紫烟”是碘升华导致的
B “泽中有火”“上火下泽”。泽,指湖泊池 “火”指CH 燃烧
4
沼
C 落汤螃蟹着红袍 发生了化学变化
D 《本草经集注》中记载“以火烧之,紫 “硝石”指KNO
3
青烟起,乃真硝石也”
2.化学用语是学习化学的重要工具,下列化学用语表述正确的是( )
A. 的电离方程式:
B.2-己烯的键线式:
C. 的VSEPR模型:
D.基态 的价层电子排布图:3.甲烷分子的球棍模型如下图所示。下列关于甲烷分子的说法中,不正确的是( )
A.分子式为CH B.属于烷烃 C.含有碳氢键 D.所有原子在同一平
4
面上
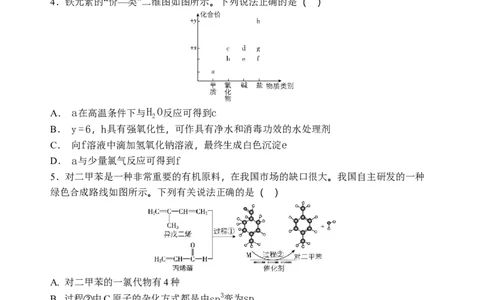
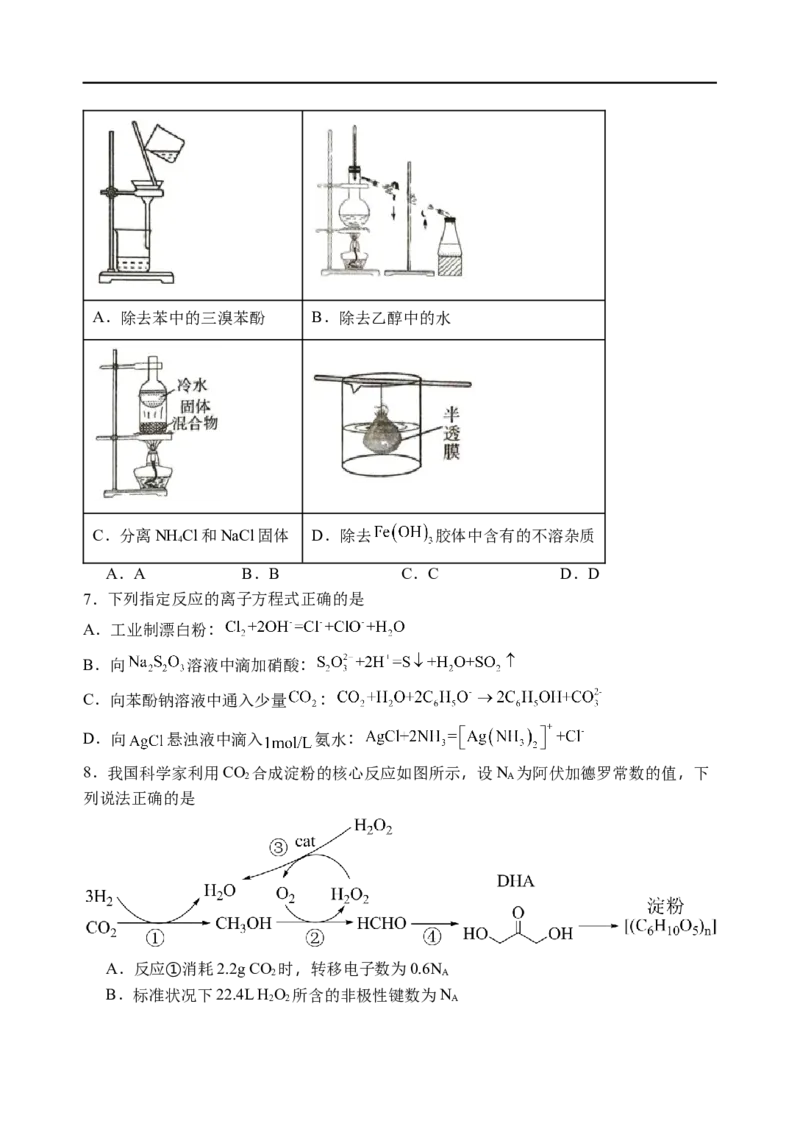
4.铁元素的“价—类”二维图如图所示。下列说法正确的是( )
A. a在高温条件下与H O反应可得到c
2
B. y=6,h具有强氧化性,可作具有净水和消毒功效的水处理剂
C. 向f溶液中滴加氢氧化钠溶液,最终生成白色沉淀e
D. a与少量氯气反应可得到f
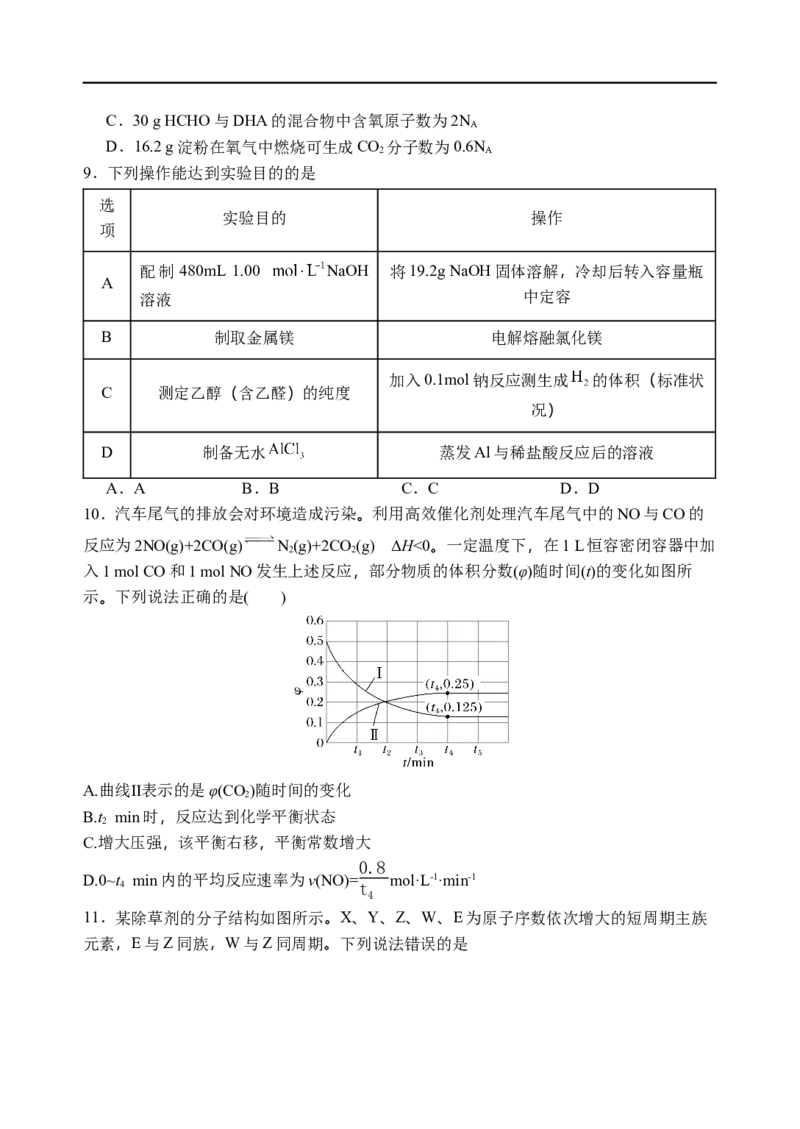
5.对二甲苯是一种非常重要的有机原料,在我国市场的缺口很大。我国自主研发的一种
绿色合成路线如图所示。下列有关说法正确的是( )
A. 对二甲苯的一氯代物有4种
B. 过程②中C原子的杂化方式都是由sp3变为sp
C. 该反应的副产物不可能有间二甲苯
M
D. 的结构简式为
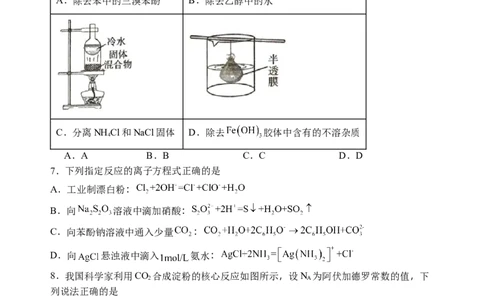
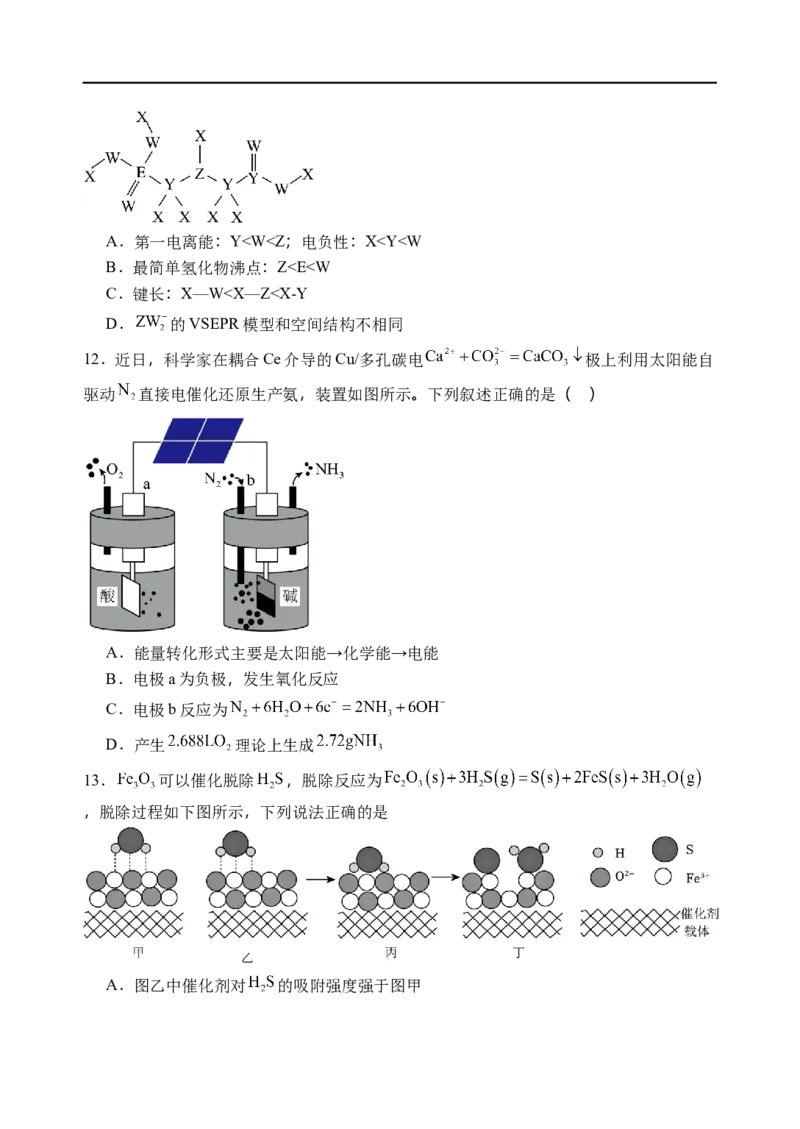
6.下列装置及操作能达到对应目的的是( )A.除去苯中的三溴苯酚 B.除去乙醇中的水
C.分离NH Cl和NaCl固体 D.除去 胶体中含有的不溶杂质
4
A.A B.B C.C D.D
7.下列指定反应的离子方程式正确的是
A.工业制漂白粉:
B.向 溶液中滴加硝酸:
C.向苯酚钠溶液中通入少量 :
D.向 悬浊液中滴入 氨水:
8.我国科学家利用CO 合成淀粉的核心反应如图所示,设N 为阿伏加德罗常数的值,下
2 A
列说法正确的是
A.反应①消耗2.2g CO 时,转移电子数为0.6N
2 A
B.标准状况下22.4L H O 所含的非极性键数为N
2 2 AC.30 g HCHO与DHA的混合物中含氧原子数为2N
A
D.16.2 g淀粉在氧气中燃烧可生成CO 分子数为0.6N
2 A
9.下列操作能达到实验目的的是
选
实验目的 操作
项
配制 480mL 1.00 NaOH 将19.2g NaOH固体溶解,冷却后转入容量瓶
A
溶液 中定容
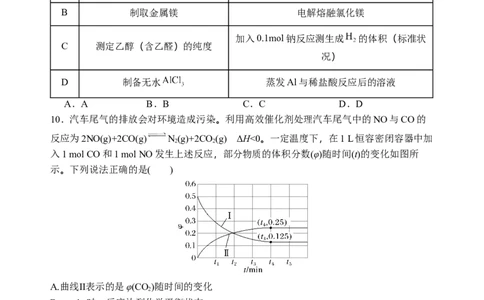
B 制取金属镁 电解熔融氯化镁
加入0.1mol钠反应测生成 的体积(标准状
C 测定乙醇(含乙醛)的纯度
况)
D 制备无水 蒸发Al与稀盐酸反应后的溶液
A.A B.B C.C D.D
10.汽车尾气的排放会对环境造成污染。利用高效催化剂处理汽车尾气中的NO与CO的
反应为2NO(g)+2CO(g) N(g)+2CO (g) ΔH<0。一定温度下,在1 L恒容密闭容器中加
2 2
入1 mol CO和1 mol NO发生上述反应,部分物质的体积分数(φ)随时间(t)的变化如图所
示。下列说法正确的是( )
A.曲线Ⅱ表示的是φ(CO)随时间的变化
2
B.t min时,反应达到化学平衡状态
2
C.增大压强,该平衡右移,平衡常数增大
0.8
D.0~t min内的平均反应速率为v(NO)= mol·L-1·min-1
4 t
4
11.某除草剂的分子结构如图所示。X、Y、Z、W、E为原子序数依次增大的短周期主族
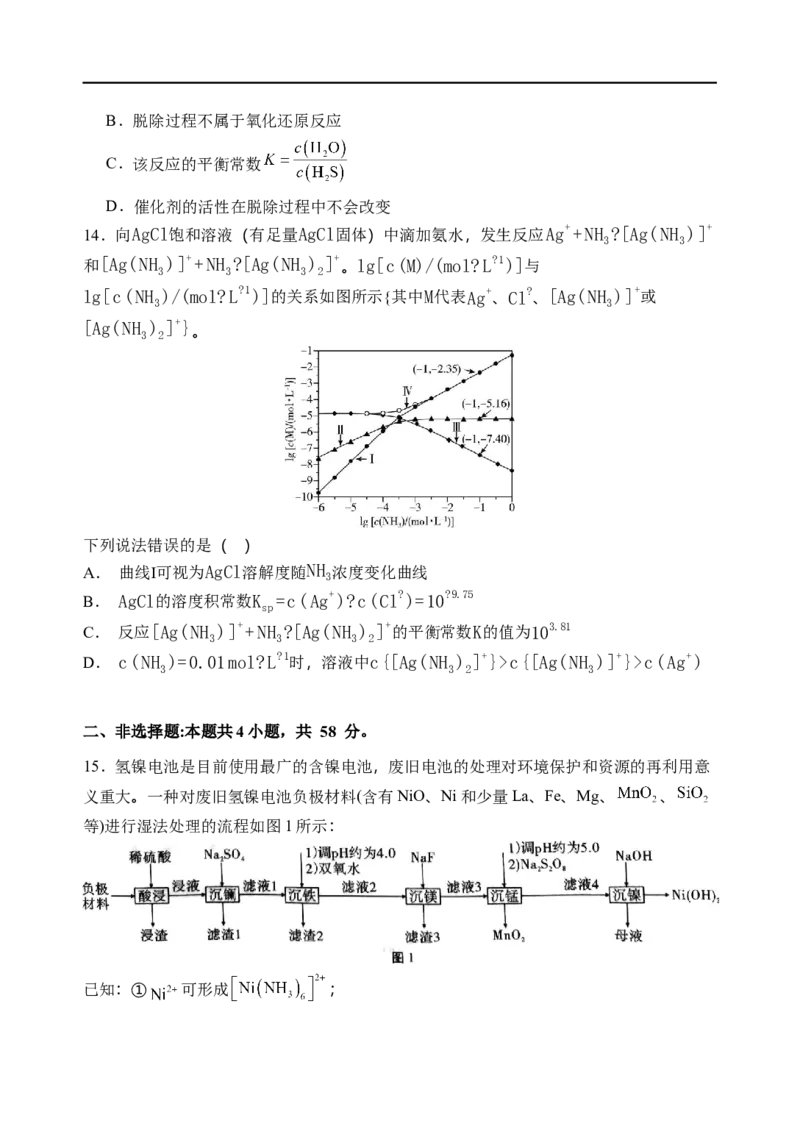
元素,E与Z同族,W与Z同周期。下列说法错误的是A.第一电离能:Yc{[Ag(NH )]+}>c(Ag+)
3 3 2 3
二、非选择题:本题共4小题,共 58 分。
15.氢镍电池是目前使用最广的含镍电池,废旧电池的处理对环境保护和资源的再利用意
义重大。一种对废旧氢镍电池负极材料(含有NiO、Ni和少量La、Fe、Mg、 、
等)进行湿法处理的流程如图1所示:
已知:① 可形成 ;② ;
③ 第一步完全电离, 。
回答下列问题:
(1)“酸浸”后浸渣的主要成分为 。
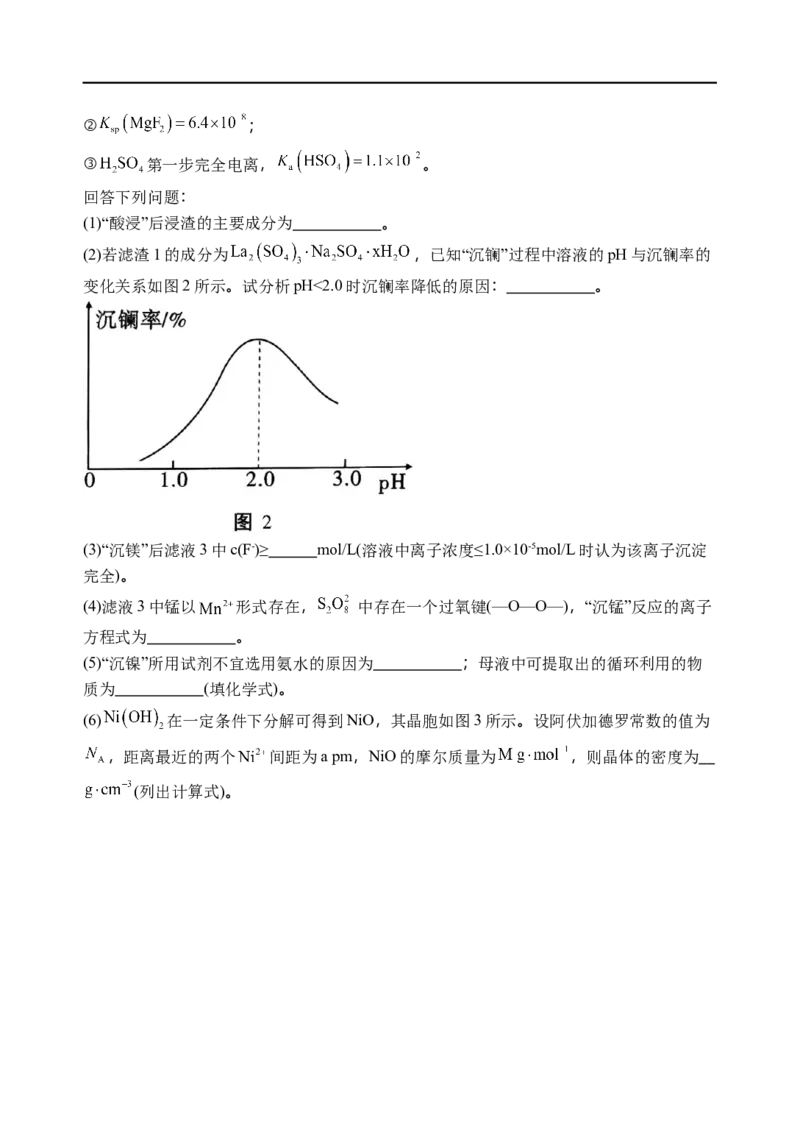
(2)若滤渣1的成分为 ,已知“沉镧”过程中溶液的pH与沉镧率的
变化关系如图2所示。试分析pH<2.0时沉镧率降低的原因: 。
(3)“沉镁”后滤液3中c(F-)≥ mol/L(溶液中离子浓度≤1.0×10-5mol/L时认为该离子沉淀
完全)。
(4)滤液3中锰以 形式存在, 中存在一个过氧键(—O—O—),“沉锰”反应的离子
方程式为 。
(5)“沉镍”所用试剂不宜选用氨水的原因为 ;母液中可提取出的循环利用的物
质为 (填化学式)。
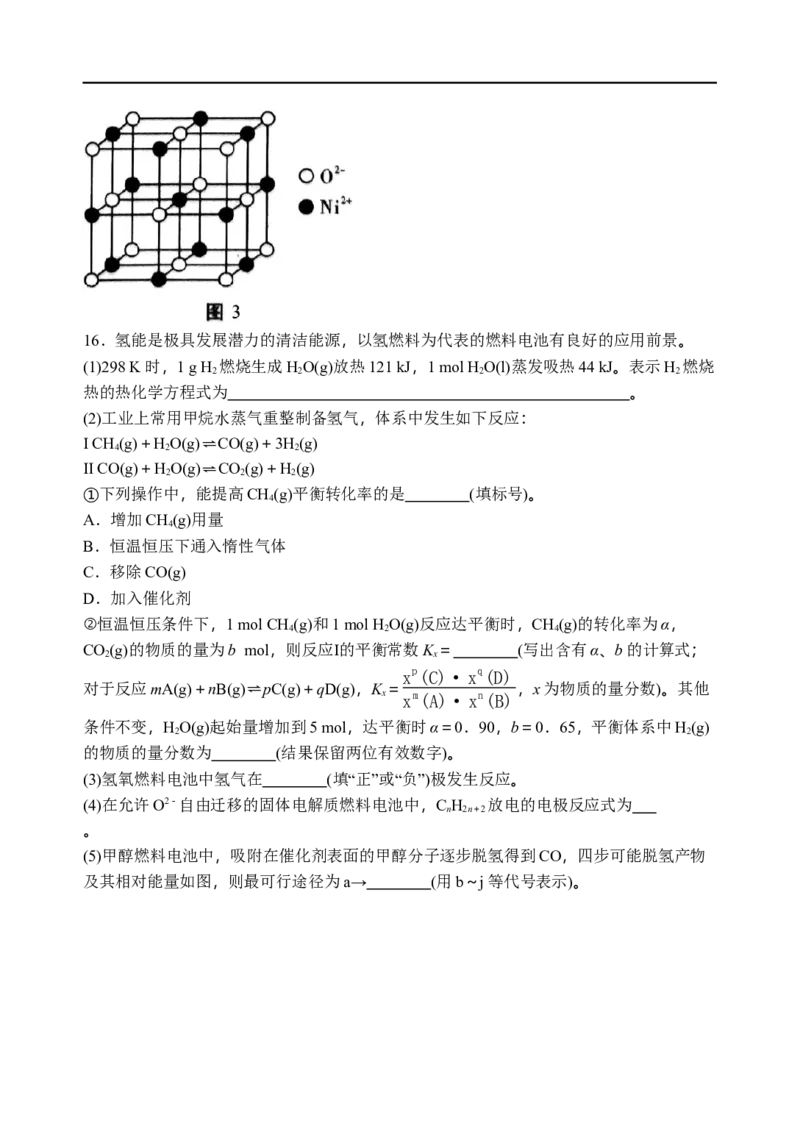
(6) 在一定条件下分解可得到NiO,其晶胞如图3所示。设阿伏加德罗常数的值为
,距离最近的两个 间距为a pm,NiO的摩尔质量为 ,则晶体的密度为
(列出计算式)。16.氢能是极具发展潜力的清洁能源,以氢燃料为代表的燃料电池有良好的应用前景。
(1)298 K时,1 g H 燃烧生成HO(g)放热121 kJ,1 mol H O(l)蒸发吸热44 kJ。表示H 燃烧
2 2 2 2
热的热化学方程式为 。
(2)工业上常用甲烷水蒸气重整制备氢气,体系中发生如下反应:
Ⅰ CH
4
(g)+H
2
O(g)⇌CO(g)+3H
2
(g)
Ⅱ CO(g)+H
2
O(g)⇌CO
2
(g)+H
2
(g)
①下列操作中,能提高CH(g)平衡转化率的是 (填标号)。
4
A.增加CH(g)用量
4
B.恒温恒压下通入惰性气体
C.移除CO(g)
D.加入催化剂
②恒温恒压条件下,1 mol CH (g)和1 mol H O(g)反应达平衡时,CH(g)的转化率为α,
4 2 4
CO(g)的物质的量为b mol,则反应Ⅰ的平衡常数K= (写出含有α、b的计算式;
2 x
xp(C)·xq(D)
对于反应mA(g)+nB(g)⇌pC(g)+qD(g),K
x
=
xm(A)·xn(B)
,x为物质的量分数)。其他
条件不变,HO(g)起始量增加到5 mol,达平衡时α=0.90,b=0.65,平衡体系中H(g)
2 2
的物质的量分数为 (结果保留两位有效数字)。
(3)氢氧燃料电池中氢气在 (填“正”或“负”)极发生反应。
(4)在允许O2-自由迁移的固体电解质燃料电池中,C H 放电的电极反应式为
n 2n+2
。
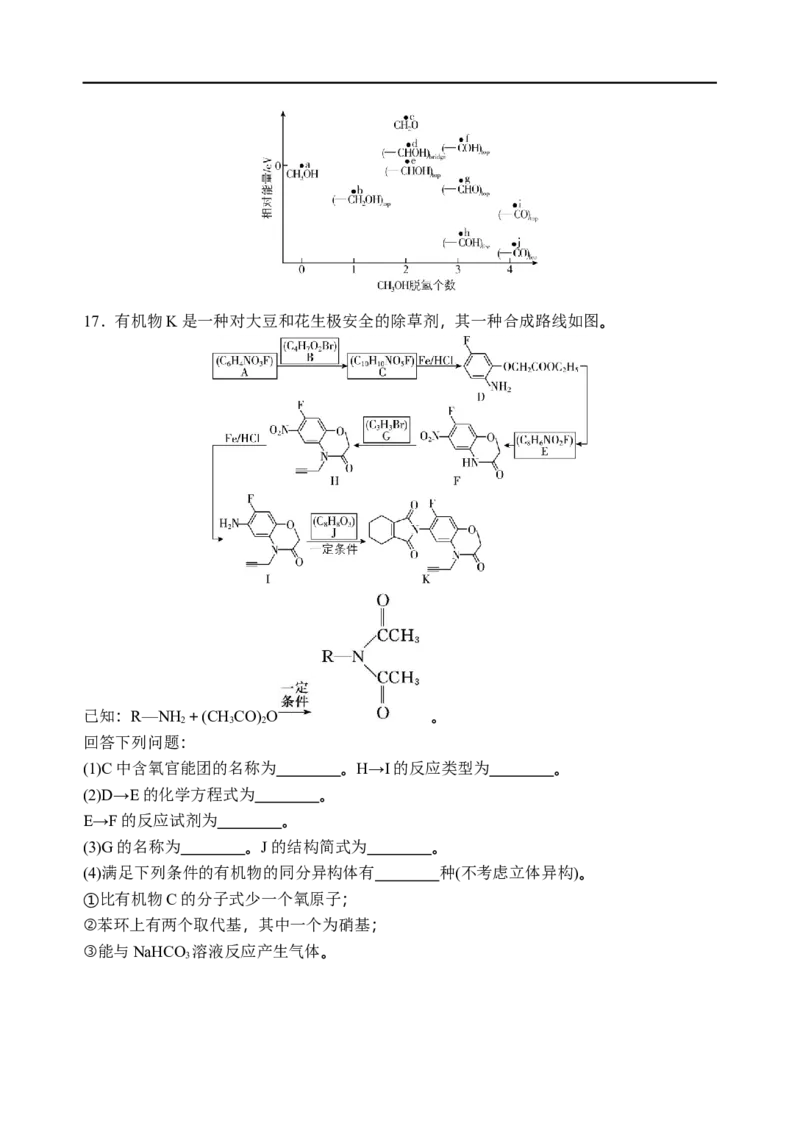
(5)甲醇燃料电池中,吸附在催化剂表面的甲醇分子逐步脱氢得到CO,四步可能脱氢产物
及其相对能量如图,则最可行途径为a→ (用b~j等代号表示)。17.有机物K是一种对大豆和花生极安全的除草剂,其一种合成路线如图。
已知:R—NH +(CHCO) O 。
2 3 2
回答下列问题:
(1)C中含氧官能团的名称为 。H→I的反应类型为 。
(2)D→E的化学方程式为 。
E→F的反应试剂为 。
(3)G的名称为 。J的结构简式为 。
(4)满足下列条件的有机物的同分异构体有 种(不考虑立体异构)。
①比有机物C的分子式少一个氧原子;
②苯环上有两个取代基,其中一个为硝基;
③能与NaHCO 溶液反应产生气体。
3(5)已知:2RCOOH (RCO) O。根据上述信息,写出以苯和 为原料合成
2
的路线。
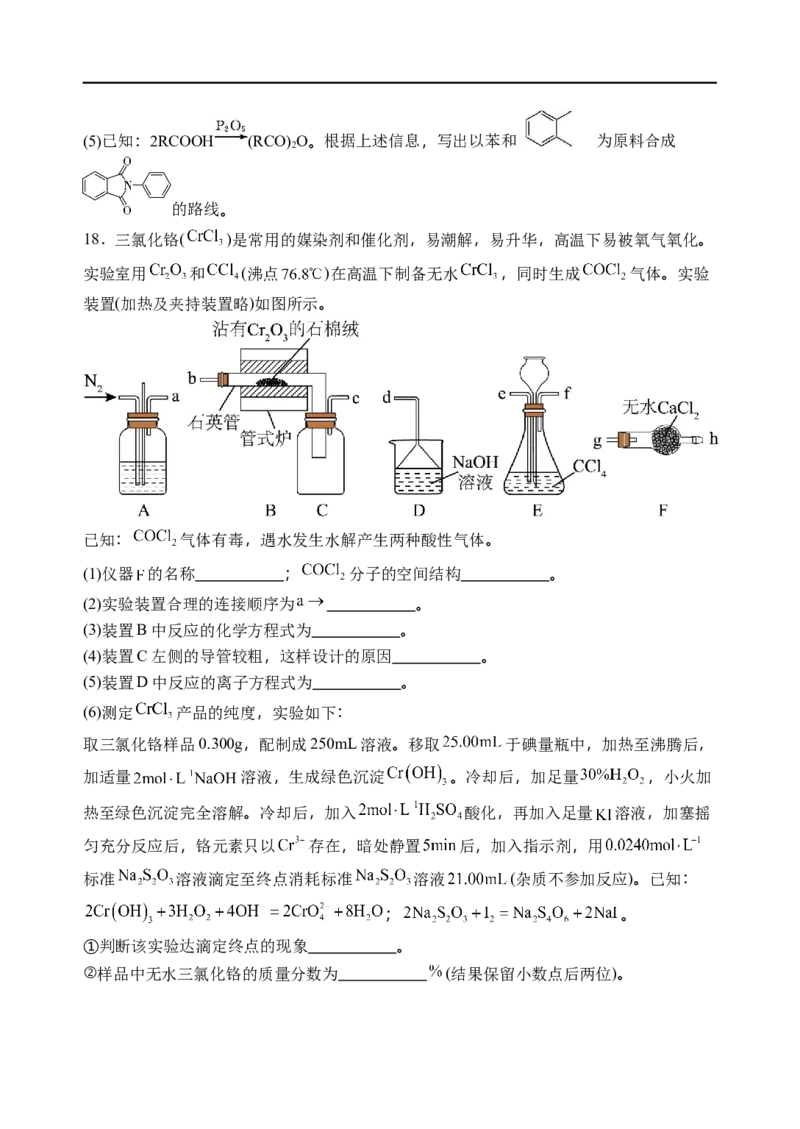
18.三氯化铬( )是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气氧化。
实验室用 和 (沸点 )在高温下制备无水 ,同时生成 气体。实验
装置(加热及夹持装置略)如图所示。
已知: 气体有毒,遇水发生水解产生两种酸性气体。
(1)仪器 的名称 ; 分子的空间结构 。
(2)实验装置合理的连接顺序为 。
(3)装置B中反应的化学方程式为 。
(4)装置C左侧的导管较粗,这样设计的原因 。
(5)装置D中反应的离子方程式为 。
(6)测定 产品的纯度,实验如下:
取三氯化铬样品0.300g,配制成250mL溶液。移取 于碘量瓶中,加热至沸腾后,
加适量 溶液,生成绿色沉淀 。冷却后,加足量 ,小火加
热至绿色沉淀完全溶解。冷却后,加入 酸化,再加入足量 溶液,加塞摇
匀充分反应后,铬元素只以 存在,暗处静置 后,加入指示剂,用
标准 溶液滴定至终点消耗标准 溶液 (杂质不参加反应)。已知:
; 。
①判断该实验达滴定终点的现象 。
②样品中无水三氯化铬的质量分数为 (结果保留小数点后两位)。