文档内容
专题45 原电池原理与应用
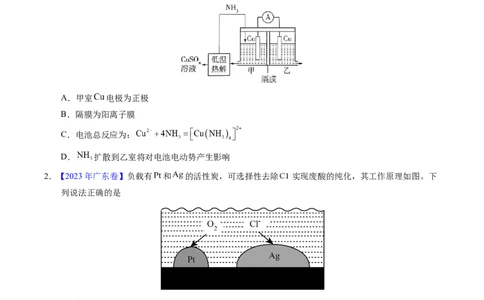
1.【2023年山东卷】利用热再生氨电池可实现 电镀废液的浓缩再生。电池装置如图所示,甲、乙
两室均预加相同的 电镀废液,向甲室加入足量氨水后电池开始工作。下列说法正确的是
A.甲室 电极为正极
B.隔膜为阳离子膜
C.电池总反应为:
D. 扩散到乙室将对电池电动势产生影响
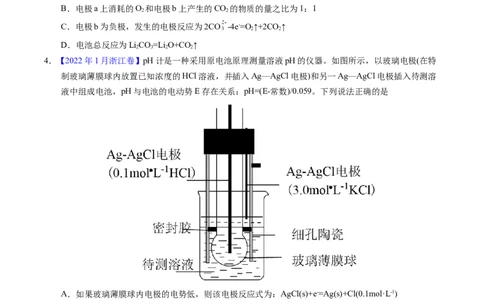
2.【2023年广东卷】负载有 和 的活性炭,可选择性去除 实现废酸的纯化,其工作原理如图。下
列说法正确的是
A. 作原电池正极
B.电子由 经活性炭流向
C. 表面发生的电极反应:
D.每消耗标准状况下 的 ,最多去除
3.【2021年重庆卷】CO 电化学传感器是将环境中CO 浓度转变为电信号的装置,工作原理如图所示,
2 2
其中YSZ是固体电解质,当传感器在一定温度下工作时,在熔融LiCO 和YSZ之间的界面X会生成
2 3
固体LiO。下列说法错说的是
2A.CO 迁移方向为界面X →电极b
B.电极a上消耗的O 和电极b上产生的CO 的物质的量之比为1:1
2 2
C.电极b为负极,发生的电极反应为2CO -4e-=O ↑+2CO ↑
2 2
D.电池总反应为LiCO=Li O+CO↑
2 3 2 2
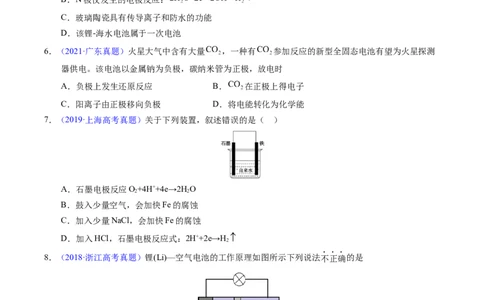
4.【2022年1月浙江卷】pH计是一种采用原电池原理测量溶液pH的仪器。如图所示,以玻璃电极(在特
制玻璃薄膜球内放置已知浓度的HCl溶液,并插入Ag—AgCl电极)和另一Ag—AgCl电极插入待测溶
液中组成电池,pH与电池的电动势E存在关系:pH=(E-常数)/0.059。下列说法正确的是
A.如果玻璃薄膜球内电极的电势低,则该电极反应式为:AgCl(s)+e-=Ag(s)+Cl(0.1mol·L-1)
B.玻璃膜内外氢离子浓度的差异不会引起电动势的变化
C.分别测定含已知pH的标准溶液和未知溶液的电池的电动势,可得出未知溶液的pH
D.pH计工作时,电能转化为化学能
5.【2022年湖南卷】海水电池在海洋能源领域备受关注,一种锂-海水电池构造示意图如下。下列说法错
误的是A.海水起电解质溶液作用
B.N极仅发生的电极反应:
C.玻璃陶瓷具有传导离子和防水的功能
D.该锂-海水电池属于一次电池
6.(2021·广东真题)火星大气中含有大量 ,一种有 参加反应的新型全固态电池有望为火星探测
器供电。该电池以金属钠为负极,碳纳米管为正极,放电时
A.负极上发生还原反应 B. 在正极上得电子
C.阳离子由正极移向负极 D.将电能转化为化学能
7.(2019·上海高考真题)关于下列装置,叙述错误的是( )
A.石墨电极反应O+4H++4e→2H O
2 2
B.鼓入少量空气,会加快Fe的腐蚀
C.加入少量NaCl,会加快Fe的腐蚀
D.加入HCl,石墨电极反应式:2H++2e→H
2
8.(2018·浙江高考真题)锂(Li)—空气电池的工作原理如图所示下列说法不正确的是
A.金属锂作负极,发生氧化反应
B.Li+通过有机电解质向水溶液处移动
C.正极的电极反应:O+4e—==2O2—
2
D.电池总反应:4Li+O+2H O==4LiOH
2 29.(2017·浙江高考真题)金属(M)-空气电池的工作原理如图所示。下列说法不正确的是
A.金属M作电池负极
B.电解质是熔融的MO
C.正极的电极反应
D.电池反应
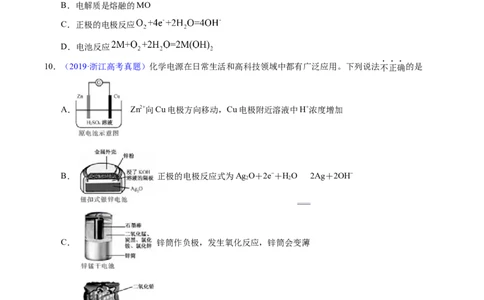
10.(2019·浙江高考真题)化学电源在日常生活和高科技领域中都有广泛应用。下列说法不正确的是
A. Zn2+向Cu电极方向移动,Cu电极附近溶液中H+浓度增加
B. 正极的电极反应式为Ag O+2e−+HO 2Ag+2OH−
2 2
C. 锌筒作负极,发生氧化反应,锌筒会变薄
D. 使用一段时间后,电解质溶液的酸性减弱,导电能力下降
11.(2015·天津高考真题)锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下
列有关叙述正确的是A.铜电极上发生氧化反应
B.电池工作一段时间后,甲池的c(SO 2-)减小
4
C.电池工作一段时间后,乙池溶液的总质量增加
D.阴阳离子离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡
12.(2016·上海高考真题)图1是铜锌原电池示意图。图2中,x轴表示实验时流入正极的电子的物质的
量,y轴表示( )
A.铜棒的质量 B.c(Zn2+) C.c(H+) D.c(SO 2-) -
4
13.(2012·全国高考真题)①②③④四种金属片两两相连浸入稀硫酸中都可组成原电池.①②相连时,外
电路电流从②流向①;①③相连时,③为正极;②④相连时,②上有气泡逸出;③④相连时,③的质
量减少.据此判断这四种金属活泼性由大到小的顺序是( )
A.①③②④ B.①③④② C.③④②① D.③①②④
14.(2015·全国高考真题)微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如
图所示。下列有关微生物电池的说法错误的是
A.正极反应中有CO 生成
2
B.微生物促进了反应中电子的转移
C.质子通过交换膜从负极区移向正极区
D.电池总反应为C H O+6O =6CO +6H O
6 12 6 2 2 2
15.(2013·上海高考真题)糕点包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与
钢铁的吸氧腐蚀相同。下列分析正确的是A.脱氧过程是吸热反应,可降低温度,延长糕点保质期
B.脱氧过程中铁作原电池正极,电极反应为:Fe-3e=Fe3+
C.脱氧过程中碳做原电池负极,电极反应为:2HO+O+4e=4OH-
2 2
D.含有1.12g铁粉的脱氧剂,理论上最多能吸收氧气336mL(标准状况)
16.(2016·全国高考真题)Mg-AgCl电池是一种以海水为电解质溶液的水激活电池。下列叙述错误的是
A.负极反应式为Mg-2e-=Mg2+
B.正极反应式为Ag++e-=Ag
C.电池放电时Cl-由正极向负极迁移
D.负极会发生副反应Mg+2HO=Mg(OH)+H ↑
2 2 2
17.(2007·全国高考真题)在盛有稀HSO 的烧杯中放入用导线连接锌片和铜片,下列叙述正确的是
2 4
A.正极附近的SO 2―离子浓度逐渐增大
4
B.电子通过导线由铜片流向锌片
C.正极有O 逸出
2
D.铜片上有H 逸出
2
18.(2010·湖南高考真题)根据下图,可判断出下列离子方程式中错误的是
A.2Ag(s)+Cd2+(aq)=2Ag+(aq)+Cd(s)
B.
C.2Ag+(aq)+Cd(s)= 2Ag(s)+Cd2+(aq)
D.
19.(2012·上海高考真题)右图装置中发生反应的离子方程式为:Zn+2H+=Zn2++H↑,下列说法错误的
2
是
A.a、b不可能是同种材料的电极
B.该装置可能是电解池,电解质溶液为稀盐酸
C.该装置可能是原电池,电解质溶液为稀盐酸
D.该装置可看作是铜-锌原电池,电解质溶液是稀硫酸
20.(2013·全国高考真题)银质器皿日久表面会逐渐变黑,这是生成了Ag S的缘故。根据电化学原理可
2进行如下处理:在铝质容器中加入食盐溶液,再将变黑的银器漫入该溶液中,一段时间后发现黑色会
褪去。下列说法正确的是
A.处理过程中银器一直保持恒重
B.银器为正极,Ag S被还原生成单质银
2
C.该过程中总反应为2Al+3Ag S=6Ag+Al S
2 2 3
D.黑色褪去的原因是黑色Ag S转化为白色AgCl
2
21.(2008·广东高考真题)用铜片、银片、Cu (NO) 溶液、AgNO 溶液、导线和盐桥(装有琼脂-KNO
3 2 3 3
的U型管)构成一个原电池 。以下有关该原电池的叙述正确的是( )
①在外电路中,电流由铜电极流向银电极
②正极反应为:Ag++e-=Ag
③实验过程中取出盐桥,原电池仍继续工作
④将铜片浸入AgNO 溶液中发生的化学反应与该原电池反应相同
3
A.①② B.②③ C.②④ D.③④
22.(2013·全国高考真题)“ZEBRA”蓄电池的结构如图所示,电极材料多孔Ni/NiCl 和金属钠之间由钠
2
离子导体制作的陶瓷管相隔。下列关于该电池的叙述错误的是( )
A.电池反应中有NaCl生成
B.电池的总反应是金属钠还原三价铝离子
C.正极反应为:NiCl +2e-=Ni+2Cl-
2
D.钠离子通过钠离子导体在两电极间移动
23.(2009·上海高考真题)茫茫黑夜中,航标灯为航海员指明了方向。航标灯的电源必须长效、稳定。我
国科技工作者研制出以铝合金、Pt-Fe合金网为电极材料的海水电池。在这种电池中
①铝合金是阳极 ②铝合金是负极 ③海水是电解液 ④铝合金电极发生还原反应
A.②③ B.②④ C.①② D.①④
24.(2016·浙江高考真题)如图所示进行实验,下列说法不正确的是A.装置甲的锌片上和装置乙的铜片上均可观察到有气泡产生
B.甲、乙装置中的能量变化均为化学能转化为电能
C.装置乙中的锌、铜之间用导线连接电流计,可观察到电流计指针发生偏转
D.装置乙中负极的电极反应式:Zn-2e-===Zn2+
25.(2016·海南高考真题)某电池以KFeO 和Zn为电极材料,KOH溶液为电解溶质溶液。下列说法正
2 4
确的是
A.Zn为电池的负极
B.正极反应式为2FeO2−+10H++6e-=Fe O+5H O
4 2 3 2
C.该电池放电过程中电解质溶液浓度不变
D.电池工作时OH−向负极迁移
26.(2012·福建高考真题)将下图所示实验装置的 K 闭合,下列判断正确的是
A.Cu 电极上发生还原反应
B.电子沿 Zn→a→b→Cu 路径流动
C.片刻后甲池中c(SO 2-)增大
4
D.片刻后可观察到滤纸b点变红色
27.(2013·海南高考真题)Mg-AgCl电池是一种能被海水激活的一次性贮备电池,电池反应方程式为:
2AgCl+ Mg = Mg2++ 2Ag +2Cl-。有关该电池的说法正确的是
A.Mg为电池的正极
B.负极反应为AgCl+e-=Ag+Cl-
C.不能被KCl 溶液激活
D.可用于海上应急照明供电
28.(2014·海南高考真题)锂锰电池的体积小、性能优良,是常用的一次电池。该电池反应原理如图所示,
其中电解质LiClO,溶于混合有机溶剂中,Li+通过电解质迁移入MnO 晶格中,生成LiMnO 。 回答
4 2 2
下列问题:(1)外电路的电流方向是由________极流向________极(填字母)。
(2)电池正极反应式为___________________________________。
(3)是否可用水代替电池中的混合有机溶剂?________(填“是”或“否”),原因是
________________________________________________________________。
(4)MnO 可与KOH和KClO 在高温下反应,生成KMnO ,反应的化学方程式为
2 3 2 4
_______________________________________________。KMnO 在酸性溶液中歧化,生成KMnO 和
2 4 4
MnO 的物质的量之比为___________。
2
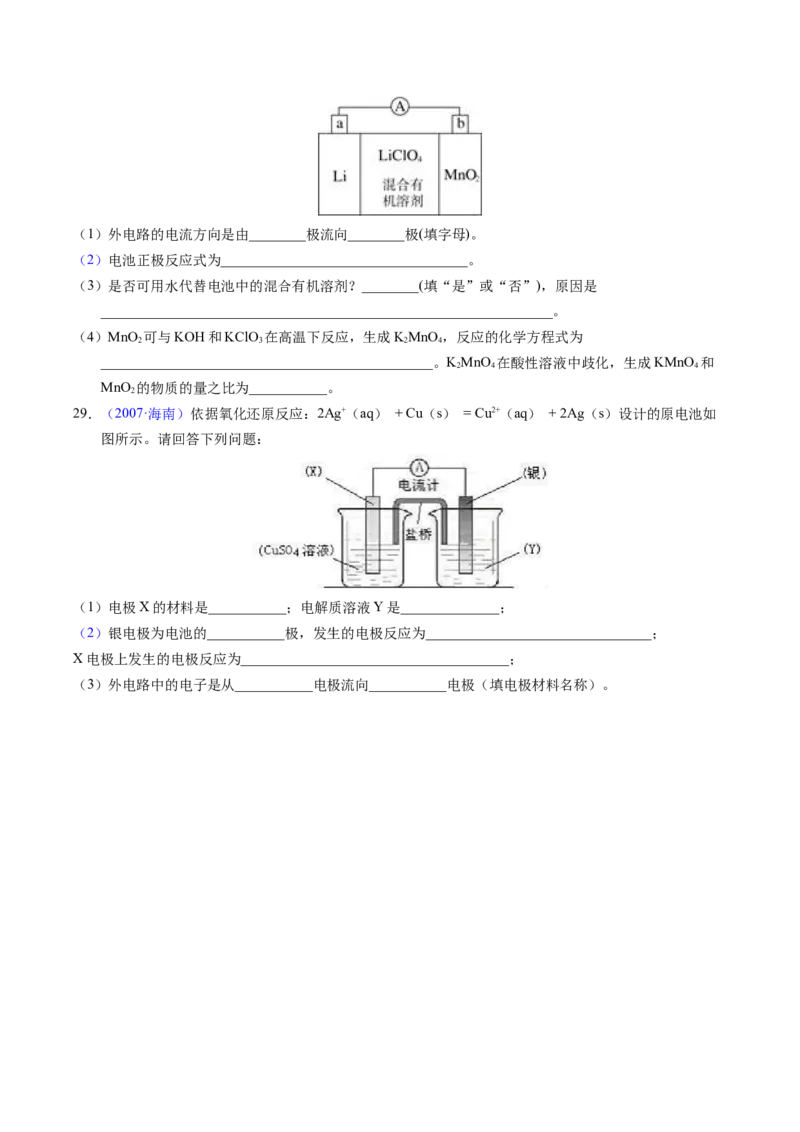
29.(2007·海南)依据氧化还原反应:2Ag+(aq) + Cu(s) = Cu2+(aq) + 2Ag(s)设计的原电池如
图所示。请回答下列问题:
(1)电极X的材料是___________;电解质溶液Y是______________;
(2)银电极为电池的___________极,发生的电极反应为________________________________;
X电极上发生的电极反应为______________________________________;
(3)外电路中的电子是从___________电极流向___________电极(填电极材料名称)。